Экспериментальное исследование распределения молекул О2 по колебательным уровням в O2 (А1G)-I среде
Автор: Азязов В.Н., Антонов И.О., Свистун М.И., Уфимцев Н.И.
Журнал: Известия Самарского научного центра Российской академии наук @izvestiya-ssc
Рубрика: Лазерная техника и технология
Статья в выпуске: 1 т.5, 2003 года.
Бесплатный доступ
Впервые экспериментально обнаружен колебательно-возбужденный кислород в активной среде химического кислородно-йодного лазера (ХКЛ). Показано, что в ходе быстрого EE-обмена энергией колебательное возбуждение практически равномерно распределяется между молекулами кислорода, находящимися в электронных состояниях..g 3 X, g a. 1 и +.g 1 b. Экспериментально показано, что средний запас колебательных квантов молекул кислорода в активной среде ХКЛ превышает 30%. Изучены зависимости пороговой доли синглетного кислорода и коэффициента усиления от доли колебательно-возбужденного кислорода в среде.
Короткий адрес: https://sciup.org/148197733
IDR: 148197733 | УДК: 621.373
Experimental investigation of O2 molecules distribution over vibrational levels in O2 (А1.G)-I medium
Vibrationally excited oxygen in active medium of chemical oxygen-iodine laser (COIL) using emission method was detected for the first time. It is shown that because of fast EE-exchange of energy the mean number of vibrational quanta per one molecule in each of a component O2(. g 3У X ), O2( g 1Д a ) and O2( +.g b1 ) is approximately equal and exceeds 30 % in active medium of COIL. Dependencies of the threshold singlet oxygen yield and gain coefficient on the relative population of vibrationally excited oxygen are studied.
Текст научной статьи Экспериментальное исследование распределения молекул О2 по колебательным уровням в O2 (А1G)-I среде
Создание химического кислородно-йодного лазера (ХКЛ) явилось важным достижением лазерной физики. Длина волны его излучения 1=1,315 мкм попадает в область малых потерь кварцевых волоконных световодов. Возможность транспортирования излучения позволяет использовать его в безлюдных гибких технологических процессах. ХКЛ может быть использован в автоматическом лазерно-технологическом комплексе в промышленности, при ремонте и демонтаже отслуживших свой срок атомных реакторов, при проведении спасательных работ в зоне стихийных бедствий и т.д.
Дезактивация электронной энергии в активной среде химического кислородно-йод-ного лазера (ХКЛ) приводит к образованию колебательно-возбужденных молекул O2, H 2 O, I2 в следующих процессах:
O2( a )+O2( a HO2( b ,v)+O2(X,v‘),(1)
O2( a )+F^O2( b ,v)+I,(2)
O2( b )+H2O^O2( a ,v)+H2O(v‘).(3)
Здесь и далее O2(X), O2( a ), O2( b ) - молекула кислорода в электронных состояниях X3L - , a 1 Д b 1^; I, I * - атом иода в состояниях 2? 3/2 и 2 P 1/2 ; ОД, ОД), I 2 2 (B) -молекула иода в состояниях X12 + , А’3 П 2u,
А3П 1u, B3 П + . В реакции пулинга (1) обра-
0u зуется колебательно-возбуждённый кислород O2(b,v) с вероятностями выхода 0,32 для v=0; 0,04 для v=1; 0,64 для v=2 [1]. Распределение дефекта энергии между продуктами реакции пулинга (2) неизвестно. Вероятность образования колебательно-возбужденной H2O(001) в реакции (3) равна 0,1 [2]. Расчеты показывают, что большая часть выделяющейся энергии в реакциях (1-3) поступает в колебательные степени свободы продуктов [3].
Колебательно-возбужденный кислород может играть важную роль в процессах формирования активной среды ХКЛ, особенно при диссоциации I2. В [4, 5] было выдвинуто предположение, что электронно-возбужденные состояния иода I2(A) и I2(A‘) являются промежуточными в процессе диссоциации иода. Они заселяются при столкновениях с колебательно-возбужденным синглетным кислородом в процессах:
О 2 ( a ,v=1) + I2(X)^O2(X) + I , (A'), (4)
О 2 ( a ,v=2) + I2(X)«O , (X) + I , (A). (5)
Колебательно-возбужденный O2(a) может также напрямую влиять на величину пороговой доли синглетного кислорода и коэффициента усиления активной среды лазера, участвуя в реакции инвертирования лазерного перехода атома иода I^I*. Принятая величина пороговой доли рассчитывалась без учета влияния колебательно-возбужденного кислорода и может быть существенно уточнена. Это позволит внести коррективы в теоретическую модель ХКЛ.
Регистрация колебательно-возбужденного кислорода представляет собой сложную проблему из-за отсутствия у молекулы O2 собственного дипольного момента [6]. В активной среде ХКЛ происходит возбуждение электронных и колебательных состояний частиц. Их эмиссионные спектры несут богатую информацию о скоростях протекающих процессов и о количественном содержании возбужденных частиц. В [7] эмиссионным методом измерена доля колебательно-возбужденного кислорода на выходе химического генератора синглетного кислорода. Сравнение интенсивностей полос излучения димоля кислорода на длинах волн 1=579 и 634 нм показало, что доля кислорода на первом колебательном уровне существенно неравновесна и составляет 2%. Методика, использованная в [7], неприменима для регистрации колебательновозбужденного O2 в активной среде ХКЛ, так как люминесценция иода на переходе I 2 (B)^I 2 (X) перекрывает полосы излучения димоля кислорода.
Расчеты показывают, что средний запас колебательных квантов в активной среде ХКЛ может достигать нескольких десятков процентов [7]. Экспериментального подтверждения этому факту получено не было. В данной работе исследуются спектры люминесценции кислорода на переходах
O2( b ,v=0)^O2(X,v=0)+h v6(6)
O2( b ,v=1)^O2(X,v=1)+h v7(7)
O2( b ,v=2)^O2(X,v=2)+h v8
с целью обнаружения и количественного определения колебательно-возбужденного кислорода в активной среде ХКЛ.
Эксперимент
Регистрация спектров люминесценции полос излучения (6-8) проводилась на экспериментальной установке, схема которой приведена на рис.1. Наработка электронно-возбужденных молекул O2(а) осуществлялась в химическом струйном генераторе синглетного кислорода, который подробно описан в работе [7], хлорированием щелочного раствора H2O2. Щелочной раствор перекиси водорода приготовлялся в баке 2 из 1,2 л H2O2 (37% вес.) и 0,8 л раствора KOH (14,5 моль/ л). Температура раствора поддерживалась равной -15°C. Скорость струй в реакторе составляла 5 м/с. Скорость газа в реакционной зоне регулировалась щелевым краном 5, установленным на выходе генератора.
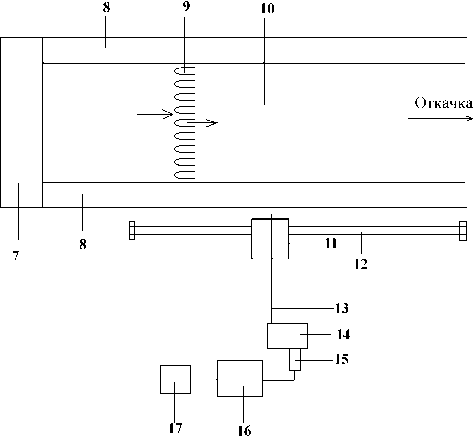
Непосредственно к блоку генератора пристыковывалась измерительная ячейка (рис.1 б), изготовленная из органического стекла. Ширина газового тракта 10 измерительной ячейки 5 см, высота 1,5 см. На расстоянии 16 см от щелевого крана 5 располагались сопла 9 для ввода иодного потока. Высота каждого сопла 1,5 см, ширина 2,5 мм, длина по потоку 1.0 см, толщина медных стенок сопла 0,15 мм. Внешние поверхности сопел покрывались тонким слоем ПММА, растворенного в хлороформе. Всего сопел было девять, расстояние между боковыми поверхностями соседних сопел равнялось 2,5 мм. Расстояние от среза соплового блока до щелевого крана 6, регулирующего скорость газа в измерительной ячейке составляло 24 см.
Сечение газового тракта, не занятое соплами, служило для формирования плоских параллельных кислородных струй. Таким образом, за сопловым блоком формировались чередующиеся иодные и кислородные струи c одинаковыми поперечными сечениями 2,5x15 мм. Во избежание конденсации йода на стенках соплового блока его температура поддерживалась равной 40°С.
Излучение газовой среды проходило через стенку измерительной ячейки 8, попадало на конец световода 13 и транспортировалось по нему к входной щели монохроматора 14. Световой поток на выходе монохроматора регистрировался фотоумножителем 15. Электрический сигнал с выхода фотоумножителя усиливался с помощью прецизионного усилителя 16, полоса пропускания которого устанавливалась равной 0-10 Гц.
В качестве несущего газа для паров иода
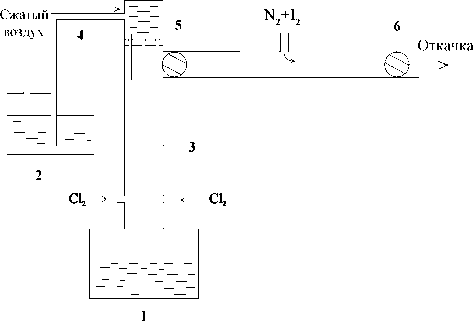
а)
б)
Рис.1. Схема экспериментальной установки. а) ě общий вид, б) ě вид сверху. 1 ě приемный бак, 2 ě питающий бак, 3 ě реакционная зона генератора, 4 инжектор раствора, 5, 6 ě щелевые краны, 7 ě генератор синглетного кислорода, 8 ě стенки измерительной ячейки, 9 ě сопла для ввода иодного потока, 10 ě газовый тракт измерительной ячейки, 11 ě подвижная платформа, 12 ě направляющая подвижной платформы, 13 ě световолокно, 14 ě монохроматор, 15 ě фотоумножитель ФЭУ-69б, 16 ě усилитель У7-1, 17 ě PC со встроенной платой АЦП
использовался азот. Парогенератор газообразного иода и система измерения его расхода аналогичны описанным в работе [8]. Для сбора и обработки информации использовался персональный компьютер 17 со встроенной платой аналого-цифрового преобразователя. Система сканирования монохроматора вырабатывала электрические импульсы, которые также поступали в компьютер и служили реперами при калибровке спектров по длинам волн. Скорость сканирования спектров 80 нм/ мин. Длительность пусков определялась запасом раствора в питающем баке 2 и составляла примерно 40 сек.
Во всех проведенных экспериментах расходы хлора GCl 2 и несущего пары I2 буферного газа были одинаковыми: G = G =2,5 Cl2 N2
ммоль/с. В связи с этим скорости кислородных и иодных газовых струй за сопловой решеткой можно считать приблизительно равными. Средняя расчетная скорость газа в измерительной ячейке за сопловой решеткой равнялась примерно 40 м/с. Доля O2(a) на выходе генератора синглетного кислорода составляла ηа=[Na ]/[NO2 ] ≈ 60±10 %, а сте- пень утилизации Cl2 в генераторе превышала 95 %. (Na ,NO2 - концентрации O2(a) и кислорода во всех электронных состояниях).
Результаты и их обсуждение
Исследовалась газовая смесь, близкая по составу к активной среде ХКЛ. Измерения показали, что спектр её излучения в области длин волн λ=480÷820 нм представлен в основном широкополосным излучением молекулярного йода с максимумом интенсивности при λ≈580 нм. Его излучение перекрывает ряд полос люминесценции кислорода. В области длин волн λ=750÷800 нм интенсивность излучения йода слабее интенсивности излучения кислорода на переходах (6-8). На рис.2 представлены значения интенсивности сигналов I регистрирующей аппаратуры в интервале значений длин волн λ = 757÷785 нм для двух значений начальной доли молекулярного иода Q I2 = G I 2 / G Cl2 : для верхней кривой Q I2 = 0,83 %, для нижней кривой Q I2 = 0,31 % ( G I 2 ‒ расход I2) при давлениях газа в генераторе синглетного кислорода Рг ≈ 35 мм
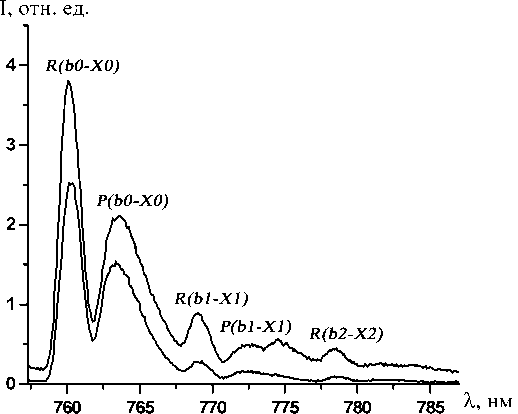
Рис.2. Интенсивность излучения I в относительных единицах в зависимости от длины волны X при следующих условиях: N2:O2:H2O=100:100:4,
Р г - 35 мм рт. ст., Р я =3 мм рт. ст., L c = 5 см, доля йода n I 2 = 0,83 % для верхней кривой и n I 2 = 0,31 % для нижней кривой.
R(bi-Xi), P(bi-Xi) - контуры R и P полос излучения молекулы кислорода О2(b, v=i)^O2(X, v'=i)+ hv, где i - номер колебательного уровня рт. ст., в измерительной ячейке Р - 3 мм рт. ст., на расстоянии Lc =5 см от среза соплового блока вдоль по потоку. На рисунке символами R(bi-Xi) и P(bi-Xi) обозначены контуры R и P вращательных ветвей для трех электронно-колебательно-вращательных переходов (6-8) молекулы О2 (i - номер колебательного уровня). Регистрация спектров излучения производилась с разрешением по длинам волн 0,5 нм.
Полоса излучения с центром при X=762 нм принадлежит переходу (6), и ее интенсивность намного превосходит интенсивность переходов с центрами при X=771 нм (процесс (7)) и X=780 нм (процесс (8)). Для перехода (8) интенсивность излучения в P-ветви сравнима с шумами регистрирующей аппаратуры. На контур перехода P(b1-X1) накладывается дополнительная полоса излучения с центром при X- 774 нм. Интенсивность этой полосы возрастает с увеличением начальной доли молекулярного иода QI2 . Полосы излучения переходов (6-8) в R-ветвях отчетливо видны и не перекрываются другими полосами излучения.
Интенсивность излучения bi-Xi-ой поло- сы Ibi-Xi пропорциональна произведению σm3qiiNbi [1], где σm‒ волновое число m-го , перехода, Nbi ‒ концентрация кислорода O2(b,v=i), qii ‒ фактор Франка-Кондона. Найдем отношение концентраций колебательновозбужденных молекул на первом Nb1 и втором Nb2 колебательных уровнях к концентрации на нулевом уровне Nb0 :
N b 1 ° 6 I R ( b 1 - X1 ) q 0,0
nbi = ы = ”737 ;
N b0 ° 7 I R ( b0 _ X0 ) q ii ’
N b2 ° 6 I R ( b 2 - X 2 ) q 0 0 nb2 = ” = ~ ~,
Nb0 °8IR(b0-X0)q22 ’ где IR(bi-Xi) - значение интенсивности сигнала R-ветви для v=i. Значения ° 3q00 =2,103 - 1012, °37qI,1 =1,729 • 1012 и °7q22 =1,373-1012 взяты из [9].
На рис.3 представлены экспериментальные зависимости относительной населенно сти O2(b) на 1-ом Qb1 и на 2-ом колебатель ном уровне gb2 от начального относительно го содержания молекулярного иода QI2 на расстоянии 5 см от среза соплового блока вдоль по потоку при давлениях газа в генераторе синглетного кислорода Рг - 35 мм рт. ст., в измерительной ячейке Ря - 3 мм рт. ст. Результаты наших экспериментов показывают, что максимальная доля колебательно-возбужденных молекул O2(b) составила 22 % и 10 % соответственно для первого и второго колебательных уровней при содержании иода в кислородном потоке около 1 %. Дальней шее увеличение ηI2 приводит к незначитель ному падению Qb1 и Qb2.
Скорость реакции (2) намного выше скорости реакции (1). Поэтому заселение колебательных уровней O2( b ) происходит в основном в реакции (2). Разница в энергиях элект-
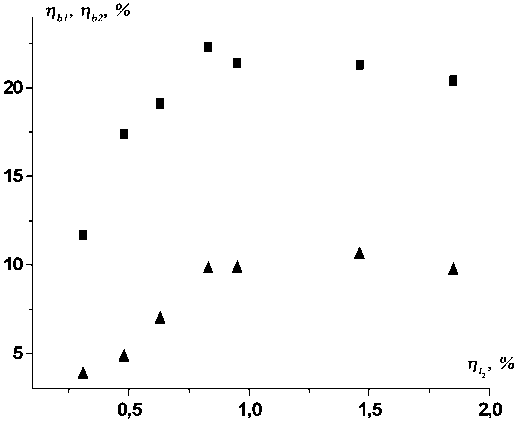
Рис.3. Относительная населенность электронновозбужденного кислорода О2( b ) на первом n b1 (■) и на втором n b2 (▲) колебательных уровнях в зависимости от относительного начального содержания I2 в кислороде при Р г = 35 мм рт. ст., Р я =3 мм рт. ст., L c =5 см
ронного возбуждения между начальным и конечным продуктами процесса (2) составляет 2364 см-1. Распределение выделяющейся энергии по продуктам реакции неизвестно. Будем предполагать, что вероятности образования O2( b ) с v=0, 1 и 2 равны a b0 , a b1 и a b2 соответственно. Перераспределение колебательных квантов энергии между молекулами кислорода O2( а ), O2( b ) и O2(X) наиболее эффективно осуществляется в ходе следующих ЕЕ-энергообменных процессов:
O2( b ,v=1)+O2( а ,v"=0)^O2( а ,v=1)+O2( b ,v"=0) - 79 см-1(9)
O2(b,v=1)+O2(X,v"=O)^O2(X,v=1)+O2(b ,v"=0) - 151 см-1(10)
O2( b ,v=2)+O2( a ,v"=0)^O2( a ,v=2)+O2( b ,v"=0)
-159 см-1(11)
O2(b,v=2)+O2(X,v"=0)^O2(X,v=2)+O2(b ,v"=0) - 307 см-1(12)
O2(a,v=1)+O2(X,v"=0)^O2(X,v=1)+O2(a ,v"=0) - 72 см-1(13)
O2(a,v=2)+O2(X,v"=0)^O2(X,v=2)+O2(a ,v"=0) -148 см-1(14)
В [10,11] измерены константы скорости EE-обмена O2( b , v=1,2) с молекулами O2(X)
(процессы (10) и (12)). Они нашли, что Кх 0=1,52-10-11> К 12=2,7-10-12 см3/с и связывают это с более высоким значением дефекта энергии в процессе (12).
Отличительной особенностью кислородной среды является низкая скорость VV и VT-релаксации на компонентах активной среды ХКЛ - O2, N2, H 2 O. Убыль колебательных кв антов энергии из колебательного резервуар а кислорода осуществляется преимущественно в ходе VV-обмена с молекулами воды H 2 O [7]:
O2(v)+H2O(000)^O2(v-1)+H2O(010).
В эксперименте были обнаружены высокие концентрации колебательно-возбужденного кислорода O2( b , v=1 и 2). Заселение этих состояний осуществляется по двум каналам. Первый канал - это возбуждение данных состояний в реакции пулинга (2). Второй канал - обмен колебательными квантами энергии в ходе EE-процессов (9-12). Вклад второго канала тем выше, чем выше средний запас колебательных квантов у молекул кислорода.
Квазистационарные концентрации колебательно-возбужденных молекул кислорода O2( а ), O2( b ) и O2(X) определяются в основном протеканием быстрых ЕЕ энергообменных процессов (9-12). В этих условиях доли колебательно - возбужденного O2( b ) с v=1 П ь1 = N bl/ N bO и с v=2 П ь2 = NtolN bO могут быть определены с хорошей точностью из следующих уравнений:
Y bl K 3 n w
Qh =+ b1 K9 П ао(1 + в 1R
+ exp ( 114T ) [ 1 + в i RexP (- 104T )
i + в i R
Y b2 K 3 4 w +
K + l П ao (1 + в 2 R)
+ exp V 229T ) [ 1 + в 2 Reeqp ( - 213/t ) "
Q al (15)
Q a2 (16)
l + в 2 R
где n w = N wl NO2 ; П а0 = N aol N02
-
n XO N XO [N O2 ; na1 N a1 1N aO ;
-
Па2 = N a2 I N aO ; R = N XO I N aO ;
-
в , = kJk;- ^. K ;
-
в2 = Kl i^ Kh = Kn,Ku •
Первые слагаемые в уравнениях (15) и (16) определяют долю колебательно-возбужденного O2( b ), обусловленную возбуждением в реакции пулинга (2). Вторые слагаемые определяют долю O2( b , v=1,2), обусловленную перераспределением колебательных квантов энергии между молекулами O2( a ), O2( b ) и O2(X) в ходе быстрых EE-обменных процессов (9-14). Константы скоростей EE-обмена между молекулами O2( b ) и O2( a ) в процессах (9) и (11) не известны. Но дефект энергии в процессе (9) меньше, чем в аналогичном процессе (10). То же справедливо для процессов (11) и (12). Тенденция к увеличению скорости с уменьшением дефекта энергии реакции EE-обмена, отмеченная в [10,11], указывает, что K 10 K 9 <1 и K 12 /K 11 <1. Дефект энергии в процессах (10) и (11) практически одинаков: 151 и 159 см-1. Можно предположить, что K+ = K ,+0 .
Проанализируем полученные уравнения (15) и (16). В условиях проведенных экспериментов Q b, = 0,22; q,2 = 0,1; Q w = 0,04; Q a0 =0,5; R =1; Т =400 К. В этих условиях вклад первых слагаемых < 0,01, даже при Y b1 = Y b2 =1. Значения выражений в квадратных скобках во вторых слагаемых в (15) и (16) близки к единице. С учетом вышесказанного можно написать следующие приближенные соотношения:
Q b1 = Q a1 exp ( 114lT ) и Q b2 = Q a2 exP ( 229/T )
Отсюда доли колебательно-возбужденного синглетного кислорода со ставляют Qa1=17 % и па2 =6 %. Средний запас колебательных квантов в исследуемой нами кисло-родно-йодной среде Пv = У пПп ^ 30 % (Пп -n доля колебательно-возбужденного О2 на n-ом колебательном уровне, n =1, 2, 3 ...).
Расчеты
С целью определения влияния колебательно-возбужденного синглетного кислорода на работу ХКЛ был проведен расчет пороговой доли рА ; “ , т.е. доли молекул синглетного кислорода O2( a ), при которой коэффициент усиления равен нулю. Общепринятое значение этой величины около15% при T=300 K. На практике это означает, что активная среда ХКЛ начнет усиливать, когда доля молекул сиглетного кислорода превысит 15%.
Колебательно-возбужденные молекулы синглетного кислорода O2( a ,v=1) и O2( a ,v=2) наряду с O2( a ,v=0) будут участвовать в инвертировании лазерного перехода в ХКЛ в процессах
O2(a,v=0)+I^ O2(X,v=0)+I* +279 см-1, (17) O2(a,v=1) +I^ O2(X,v=1)+I* +207 см-1, (18) O2(a,v=2) +I^ O2(X,v=2)+I* +131 см-1. (19)
Константы скорости реакций (18) и (19) неизвестны. С ростом номера колебательного уровня уменьшаются значения дефектов энергии и констант равновесия в процессах (17-19). Спин-орбитальный переход атома иода будет инвертирован в каждом из процессов (17-19), если соответствующие пороговые доли синглетного кислорода будут: для (17) - 15 %; для (18) - 20 %; для (19) - 26 %. В данной работе показано, что концентрация молекул колебательно-возбужденного O2( а ) на первом и втором уровнях существенна. Суммарная пороговая доля O2( a ) должна быть выше общепринятого значения.
Коэффициент усиления активной среды ХКЛ g рассчитывается по формуле
-
—о | N * - — Nr |= 7oN ( зп . - 1 ) g 12 ( I 2 1 J 24 Io I h где о - поперечное сечение индуцированного излучения N * , N I - концентрация атомарного йода I * , I соответственно, N Io - суммарная концентрация атомов йода, П * = N * [N I o • Для квазистационарных условий при условии g =0 были получены
формулы для расчета пороговой доли синглет ного кислорода на нулевом, первом и втором ко лебательных уровнях:
a1 K p13 (η 0
η 1 η a0
-
η a0 ) + η a0
η a2 =
K p14 (η 0
η 2 η a0
-
η a0 ) + η a0
th η 0 - 2 γ 1 K p18 η a1
ηΔ 0 = 2K p17 +1 +
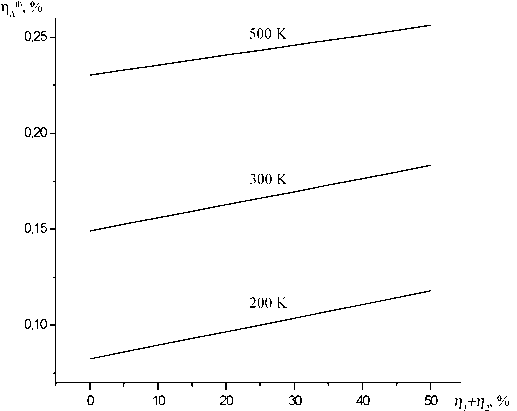
Рис.4. Суммарная пороговая доля синглетного кислорода в зависимости от относительного содержания колебательно-возбужденного кислорода в смеси для трех значений температуры среды при η 1 : η 2 =7:3
γ 1 (η 1 -η a1 )-2 γ 2 K p19 + γ 2 (η 2 -η a2 )
+ 2Kp17 + 1 . (22
В этом выражении γ 1 = K 1 - 8 K 1 - 7 ,
γ 2 = K 1 - 9 K 1 - 7 , Kpi ‒ константа равновесия i -ого процесса, η t Δ h 0 - пороговая доля синглетного кислорода на нулевом колебательном уровне .
На рис.4 представлены рассчитанные из уравнений (20-22) суммарные пороговые доли синглетного кислорода в зависимости от концентрации колебательно-возбужденного кислорода. Отношение η 1 к η 2 приняли равным 7/3. Как видно из рисунка, значения пороговой доли увеличиваются с ростом доли колебательно-возбужденных молекул О2. От значений γ 1 и γ 2 , т.е. отношений неизвестных констант K18 и K19 к известной K17 , пороговая доля зависит очень слабо. На рис.5 представлены зависимости коэффициента усиления от доли колебательно бужденного кислорода во всех электронны стояниях. Содержание колебательно-возбу ного кислорода в активной среде ХКЛ слаб яет на значение коэффициента усиления ср
Заключение
Эмиссионная методика позволяет обнар вать колебательно-возбужденный кислород и делять его количественное содержание в акт среде ХКЛ. Полосы излучения электронно-ко тельно-вращательных переходов молекулы к рода (6-8) попадают в область длин волн вид диапазона, где интенсивность излучения молекулярного иода на переходе I2(B)→I2(X) минимальна. В области реакционной зоны за сопловым блоком на расстоянии по потоку несколько сантиметров, где еще высока концентрация I2, интенсивность излучения на переходе I2(B)→I2(X) одного порядка с интенсивностью излучения полос (7-8). Это обстоятельство не позволило провести измерения в области диссоциации I2. В O2(a)-I среде, близкой по составу к активной среде ХКЛ, относительное содержание колебательно-возбужденных молекул O2(b) достигало в экспериментах ηb1 ≈22 % для первого колебательного уровня и ηb2 ≈10 % для второго. Максимальное содержание O2(b,v) было зафиксировано при относительном начальном содержании I2 в кислороде около1 %. Относительное содержание колебательно-возбужденного кислорода слабо падает вдоль координаты по потоку.
Возбуждение колебательных уровней O2 осуществляется в процессах (2) и (3). Из-за быстрого
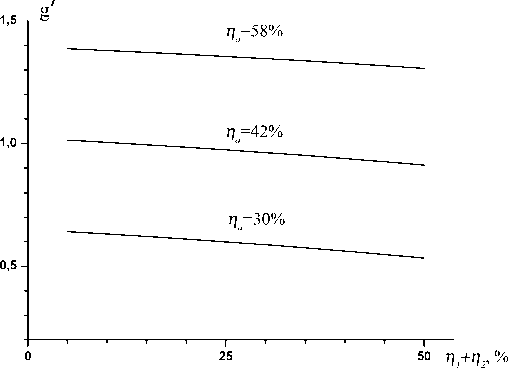
Рис.5. Расчетные значения отнормированного коэффициента усиления g' = 24gI(7 σ N I o ) в зависимости от относительного содержания колебательно-возбужденного кислорода в смеси для трех значений η a при η 1 : η 2 = 7:3
EE-обмена энергией в процессах (9-14) степень колебательного возбуждения молекул кислорода O2(X), O2( a ) и O2( b ) практически одинакова. Используя измеренные экспериментально относительные населенности O2( b ) ‒ η b1 и η b2 из уравнений (15) и (16) можно найти относительные населенности синглетного кислорода на v=1 и v=2. Для состава среды N2:O2:I2:H2O=100:100:1:4, парциального давления кислорода около 1,5 мм рт. ст. и Т≈400К максимальные относительные населенности синглетного кислорода составили для первого уровня примерно 17%, а для второго примерно 6%.
Таким образом, впервые на основе эмиссионной методики экспериментально показано, что средний запас колебательных квантов молекул кислорода в активной среде ХКЛ достигает 30 %. Этот факт является еще одним аргументом в пользу модели диссоциации I2, в которой колебательно-возбужденный кислород участвует в заселении промежуточных электронновозбужденных состояний иода I2(A′) и I2(A).
В теоретические модели ХКЛ необходимо включать процессы с участием колебательно-возбужденных молекул O2. Реакции (4) и (5) могут играть важную роль в процессе диссоциации I2. Расчеты показывают, что пороговая доля синглетного кислорода оказывается на несколько процентов выше общепринятого значения, если учитывать влияние колебательновозбужденного кислорода. Коэффициент усиления активной среды ХКЛ слабо уменьшается с ростом концентрации O2( a , v). К сожалению, в процессах (2) и (3) неизвестно распределение выделяющейся энергии между продуктами реакции. Неизвестны и значения констант скоростей процессов (4, 5, 9, 11, 18 и 19). Эти причины усложняют теоретическое моделирование кинетических процессов в ХКЛ.


