Экспериментальное обоснование и выбор способа радиочастотной аблации при солитарных опухолях
Автор: Кошель А.П., Зуева Е.П., Клоков С.С., Севастьянова Н.В., Мартынюк А.К., Толстых А.С., Списивцев С.А., Разина Т.Г., Крылова С.Г., Амосова Е.Н., Ефимова Л.А., Лопатина К.А., Сафонова Е.А., Гомбоев Т.д
Журнал: Сибирский онкологический журнал @siboncoj
Рубрика: Лабораторные и экспериментальные исследования
Статья в выпуске: 5 (41), 2010 года.
Бесплатный доступ
С целью изучения противоопухолевого и противометастатического действия радиочастотных токов с различным време- нем экспозиции выполнено экспериментальное исследование на 45 мышах с карциномой легких Льюис. На 10-е сут после перевивки животные были распределены на 3 группы: контроль - животные с опухолями без воздействий (n=15); группа № 1 - одномоментное, однократное воздействие 2 электродами (n=15); группа № 2 - одномоментное, однократное воздей- ствие 4 электродами (n=15). Продолжительность эксперимента составила 21 сут. По результатам эксперимента показано, что воздействие на первичную опухоль радиочастотными токами с использованием 4 электродов одновременно приводит к достоверному (p
Радиочастотная аблация, экспериментальная опухоль
Короткий адрес: https://sciup.org/14055678
IDR: 14055678
Experimental verification and choice of the method of radio-frequency ablation of solitary tumors
Experimental study on 45 mice with Lewiss lung carcinoma was carried out to investigate antitumor and antimetastatic activities of radiofrequency currents with different exposition times. On day 10 after inoculation, animals were divided into 3 groups: the control group (n=15): animals with tumors having no any exposure to radiofrequency; group 1 (n=15): single exposure to radiofrequency currents using 2 electrodes, group 2 (n=15): single exposure using 4 electrodes. Duration of the experiment was 21 days. The results of the experiment showed that the exposure of the primary tumor to radiofrequency current using 4 electrodes simultaneously resulted in significant inhibition of primary tumor growth (p
Текст научной статьи Экспериментальное обоснование и выбор способа радиочастотной аблации при солитарных опухолях
Возможность выполнения оперативных вмешательств у пациентов с первичными и метастатическими опухолями печени до настоящего времени не превышает 10 % [7, 10]. При этом среди причин низкой резектабельности не последнее место занимает необходимость значительного расширения объема операции, особенно при наличии 2 и более очагов, что при сомнительной радикальности вмешательства сопряжено со значительным увеличением степени операционного риска у ослабленных онкологических больных. Использование же малоинвазивных методов деструкции опухоли (радиочастотная термоаблация) в комплексном лечении данных пациентов позволяет рассчитывать на увеличение пятилетней продолжительности жизни до 35,4 % [3]. В настоящее время методы локальной деструкции получили широкую распространённость, несмотря на сравнительно короткую историю их клинического применения. Область их применения в онкологии – лечение пациентов с опухолевым поражением печени, почек, лёгких и костей [14].
Все известные в настоящее время методы локальной деструкции можно разделить на химические и физические. К первым относят алкоголизацию очагов, введение в опухоль гипертонического раствора или цитостатиков, ко вторым – различные методики холодовой и тепловой деструкции [18]. На практике чаще применяется методы теплового разрушения опухолевых тканей, из них радиочастотная термоаблация (РЧА) является одним из наиболее перспективных [2, 12,]. Его можно использовать как в самостоятельном виде, так и в комбинации с другими деструктивными, лекарственными и традиционными хирургическими методами лечения опухолевых поражений печени [6, 8, 9]. В хирургии печени РЧА впервые была применена J. P. McGahan et al. d 1990 г. [16]. Основное ее назначение – чрескожная, лапароскопическая или «открытая» термодеструкция опухолей. В России клиническое использование технологии РЧА только начинается, и пока не существует единого взгляда на возможности данной методики [5].
Цель исследования – изучение противоопухолевого и противометастатического действия радиочастотных токов с различным временем экспозиции в эксперименте на мышах с карциномой легких Льюис.
Материал и методы
Эксперименты выполнены на половозрелых животных: 45 мышах-самках линии С57ВL/6 массой 19–21 г, конвенциональных, 1 категории, полученных из отдела экспериментального биомоделирования НИИ фармакологии СО РАМН (г. Томск). Содержание животных осуществлялось в соответствии с правилами, принятыми Европейской Конвенцией по защите позвоночных животных, используемых для экспериментальных и иных научных целей [11]. Экспериментальные исследования проведены в соответствии с правилами лабораторной практики (GLP), приказом МЗ РФ № 267 от 19.06.03. «Об утверждении правил лабораторной практики», Федеральном законом «О лекарственных средствах» (статья 36), «Руководством по экспериментальному (доклиническому) изучению новых фармакологических веществ» (Москва, 2005).
В качестве экспериментальной модели взята карцинома легких Льюис [15], которая перевивается на 12–14-е сут роста, средняя продолжительность жизни животных – 24 дня. После выдерживания животных в карантине в течение 10 дней с целью адаптации к условиям вивария мыши взвешены и равномерно распределены на группы. Карцинома легких перевита подкожно по 5–6×10 6 клеток в 0,1 мл физиологического раствора [4]. На 10-е сут после перевивки животных равномерно распределили на следующие группы:
Контроль – животные с опухолями без воздействий (n=15).
Группа № 1 – одномоментное, однократное воздействие 2 электродами на 10-е сут развития опухоли (n=15).
Группа № 2 – одномоментное, однократное воздействие 4 электродами на 10-е сут развития опухоли (n=15).
Продолжительность эксперимента составила 21 сут. Для радиочастотной термоаблации использовали опытный образец деструктора онкологического (ДО-01). Аппарат состоит из генератора (мощность 80 Вт, частота колебаний 440 кГц) и дополнительных опций (контроль импеданса и температуры), а также перисталь-тирующего насоса, подающего охлаждающую жидкость (стерильный физиологический раствор) и набора охлаждаемых электродов длиной 15 см с рабочей частью 1 см. Контроль температуры в зоне воздействия осуществляли с помощью термодатчика. Время работы определялось автоматически по достижении заданного импеданса – 350 Ом.
После обработки операционного поля рабочие электроды вводили в опухоль, на всю длину его рабочей части, отступая от края опухоли 3–5 мм. В группе № 1 воздействие радиочастотными токами проводилось однократно с помощью 2 электродов (рис. 1). В группе № 2 однократное воздействие на опухоль осуществляли с помощью 4 электродов одновременно (рис. 2). Воздействие проводилось мощностью 2 Вт при сопротивлении 350 Ом. В ходе манипуляции контролировалась температура тканей, которая составляла 80–100°С. Эффективность
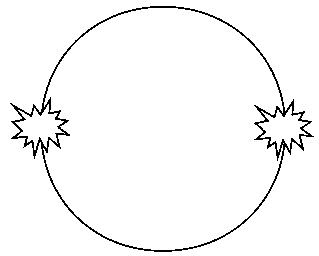
Рис. 1. Схема расположения электродов по отношению к опухоли в группе экспериментальных животных № 1
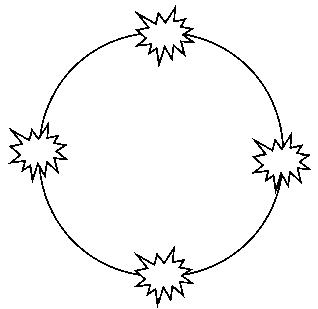
Рис. 2. Схема расположения электродов по отношению к опухоли в группе экспериментальных животных № 2
лечебных воздействий оценивали на 21-е сут опыта, измеряя массу новообразования и подсчитывая процент торможения роста опухоли (ТРО) по формуле
А- В tpo =--100%,
А где А – средняя масса опухоли в контрольной группе; В – средняя масса опухоли в опытной группе.
Для определения интенсивности процесса метастазирования использовано несколько показателей: количество метастазов в легких (для каждого животного в группе и среднее значение); площадь метастатического поражения, которую рассчитывают по формуле πr 2 , определяя при этом диаметр метастазов.
Частоту метастазирования опухоли вычисляли в процентах по отношению числа животных с метастазами к общему количеству мышей в группе. Индекс ингибирования метастазирова- ния (ИИМ), который позволяет оценить степень метастатического поражения, рассчитывали по формуле [1]
ИИМ = Лк х Вк × 100 %, где А к и А – частота метастазирования в лёгкие у мышей контрольной и опытной групп; В к и В – среднее число метастазов в лёгких в контрольной и опытной группах.
В случае значительного поражения легочной ткани, когда регистрировалось большое количество метастатических узлов, оценивали степень метастатического поражения по шкале, предложенной D. Tarin, J.E. Price (1979) и позволяющей дифференцировать тяжесть поражения в зависимости от количества метастазов и их размеров. Выделяли низкую (LCP – low colonization potential: 1 степень – <10 узлов и 2 степень – от 10 до 30) и высокую (HCP – high colonization potential: 3 степень – >30 узлов, отсутствуют сливные узлы; 4 – <100, есть сливные и 5 – >100 узлов) степень поражения легких. По окончании экспериментов мышей умерщвляли, соблюдая «Правила проведения работ с использованием экспериментальных животных», утвержденные Министерством здравоохранения РФ.
Результаты и обсуждение
У мышей контрольной группы (без воздействий) объём опухоли закономерно повышался на протяжении всего эксперимента. В основной группе № 1 обнаружена тенденция к уменьшению массы опухолевого узла в 1,5 раза по сравнению с контролем. Процент торможения роста опухоли составил 33 %. Частота метастазирования, количество и площадь метастазов в данной группе достоверно не отличались от таковых в контроле, при этом 37,5 % мышей имели более высокую – 3 степень поражения, тогда как в контроле этот показатель составил 8,3 % (табл. 1, 2).
В группе № 2 применение деструктора вызвало достоверное торможение опухолевого роста (65 %), а масса опухоли уменьшилась в 2,9 раза. Кроме того, в данной группе отмечалось снижение количества метастазов в легкие – в 1,6 раза по сравнению с аналогичными значениями в контроле, в 2,6 раза уменьшилась площадь
Влияние режимов РЧА на развитие карциномы легких Льюис (Х ± m)
Таблица 1
|
Группы сравнения |
Масса опухоли, г |
Торможение роста опухоли, % |
Частота метастазирования, % |
Кол-во метастазов на 1 мышь |
Площадь метастазов на 1 мышь, мм2 |
ИИМ, % |
|
Контроль |
2,36 ± 0,35 |
- |
100 |
22,58 ± 3,55 |
17,99 ± 5,46 |
- |
|
РЧА, режим № 1 |
1,57 ± 0,25 |
33 |
100 |
24,38 ± 2,96 |
21,61 ± 7,74 |
-8 |
|
РЧА, режим № 2 |
0,82 ± 0,13* |
65 |
100 |
14,00 ± 2,62** |
7,02 ± 1,99 |
38 |
Примечание: * – различия статистически значимы по сравнению с группой контроля (p<0,01); ** – различия статистически значимы по сравнению с группой контроля (p<0,05).
Влияние режимов РЧА на тяжесть метастатического поражения легких у экспериментальных животных
Таблица 2
|
Группа сравнения |
Степень поражения легких метастазами, % |
|||||
|
Нет метастазов |
LCP |
HCP |
||||
|
1 |
2 |
3 |
4 |
5 |
||
|
Контроль |
- |
16,7 |
75 |
8,3 |
- |
- |
|
РЧА, режим № 1 |
- |
25 |
37,5* |
37,5* |
- |
- |
|
РЧА, режим № 2 |
- |
33,3 |
66,7 |
- |
- |
- |
Примечание: * – различия статистически значимы по сравнению с группой контроля (p<0,05).
метастазов. Все животные имели 1-ю и 2-ю степень метастатического поражения, индекс ингибирования метастазирования составил 38 % (табл. 1, 2).
Объём опухоли у животных в обеих основных группах на 7-е сут имел выраженную
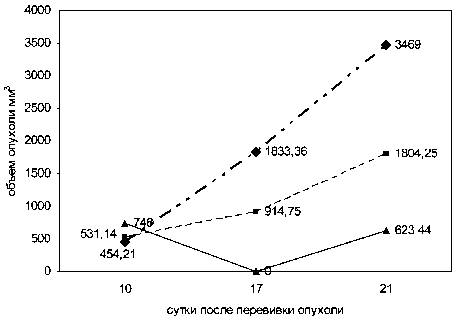
—ф. - группа контроля —■—деструкция, №1 —*—деструкция, №2
Рис. 3. Динамика роста объема перевиваемой опухоли в сравниваемых группах экспериментальных животных тенденцию к уменьшению. При этом наиболее существенно он уменьшился в группе № 2, в которой отмечались лишь некротические участки на месте расположения опухоли. Несмотря на то, что на 21-е сут после трансплантации опухоли её объём в обеих экспериментальных группах вновь стал увеличиваться, он всё ещё статистически значимо отличался от группы контроля (рис. 3).
Заключение. Таким образом, в эксперименте на мышах-самках линии С57Вl/6 с карциномой лёгких Льюис показано, что воздействие на первичную опухоль радиочастотными токами с использованием 4 электродов одновременно приводит к достоверному торможению роста первичного опухолевого узла и снижению количества отдаленных метастазов. Полученные данные позволяют говорить о перспективности применения РЧА у пациентов с первичными и метастатическими опухолями печени как в плане лечения опухоли, так и в плане предупре- ждения отдаленного метастазирования. Вместе с тем небольшое количество наблюдений требует проведения дальнейших экспериментальных и клинических исследований.


