Экспериментальное обоснование этиопатогенетического подхода в хирургии патологии периартикулярных тканей
Автор: Кокорин В.В.
Журнал: Вестник Национального медико-хирургического центра им. Н.И. Пирогова @vestnik-pirogov-center
Рубрика: Оригинальные статьи
Статья в выпуске: 2 т.17, 2022 года.
Бесплатный доступ
В статье представлены результаты экспериментального исследования прочности структур периартикулярных тканей на примере трупного материала костно-сухожильного комплекса дистального сухожилия бицепса и лучевой кости. Исследование проведено на трупном материале, взятом у мужчин в возрасте 35-45 лет, не позднее 48 суток со дня смерти, не имеющих, согласно медицинской документации, патологии костно-мышечной системы и системных заболеваний, оказывающих влияние на прочность исследуемых тканей. 30 препаратов сухожилия дистального бицепса и 30 препаратов костно-сухожильного комплекса были стандартизированы для проведения испытаний. В исследовании использована сервогидравлическая многоцелевая динамическая испытательная машина (для биомедицинских материалов). Оснащение соответствовало возможности проведения сложных двухосевых испытаний на растяжение/сжатие и вращение с синхронизацией управления по обеим осям нагружения. Целью исследования являлось изучение наиболее подверженных повреждению структур периартикулярных тканей, а также сравнение их характеристик в экспериментальном исследовании. Результаты исследования показали закономерность первичного повреждения места перехода дистального сухожилия двуглавой мышцы плеча в бугристость лучевой кости, которое является физиологической переходной структурой - фиброзно-хрящевым энтезисом. В критической точке приложения силы, растяжение костно-сухожильного комплекса приводит к отрыву энтезальной части, при сохранении целостности фасции. При исследовании сухожилия на растяжение, в первую очередь, происходит разрыв фасциальной ткани, покрывающей сухожилие, а только потом сухожильных волокон. Выполненное экспериментальное исследование позволяет утверждать о важной роли физиологических свойств фасциально-мышечной структуры в комплексе периартикулярных тканей, таких как эластичность, упругость, сократимость, выполняющих демпферную функцию в связке костно-сухожильного комплекса и играющей важную роль в предотвращении повреждений периартикулярных тканей, в частности энтезисов, при воздействии механических факторов.
Энтез, энтезопатия, регенерация, эксперимент, периартикулярные ткани
Короткий адрес: https://sciup.org/140295059
IDR: 140295059 | DOI: 10.25881/20728255_2022_17_2_43
Experimental substantiation of the etiopathogenetic approach in surgery of periarticular tissue pathology
The article presents the results of an experimental study of the strength of the structures of periarticular tissues on the example of cadaveric material of the bone-tendon complex of the distal biceps tendon and radius. The study was conducted on cadaveric material taken from men aged 35-45 years, no later than 48 days from the date of death, who, according to medical documentation, do not have pathology of the musculoskeletal system and systemic diseases that affect the strength of the studied tissues. 30 preparations of the distal biceps tendon and 30 preparations of the bone-tendon complex were standardized for testing. In the study used a servo-hydraulic multipurpose dynamic testing machine (for biomedical materials). The equipment corresponded to the possibility of conducting complex two-axis tensile/compression and rotation tests with control synchronization on both loading axes. The aim of the study was to study the structures of periarticular tissues most susceptible to damage, as well as to compare their characteristics in an experimental study. The results of the study showed the regularity of the primary damage to the transition site of the distal tendon of the biceps muscle of the shoulder into the tuberosity of the radius, which is a physiological transitional structure - fibrous-cartilaginous enthesis. At the critical point of application of force, stretching of the bone-tendon complex leads to the separation of the enthesal part, while maintaining the integrity of the fascia. When examining a tendon for stretching, first of all, there is a rupture of the fascial tissue covering the tendon, and only then the tendon fibers. The performed experimental study allows us to assert the important role of the physiological properties of the fascial-muscular structure in the complex of paraarticular tissues, such as elasticity, elasticity, contractility, performing a damping function in the ligament of the bone-tendon complex and playing an important role in preventing damage to periarticular tissues, in particular entheses, under the influence of mechanical factors.
Текст научной статьи Экспериментальное обоснование этиопатогенетического подхода в хирургии патологии периартикулярных тканей
Актуальность: на сегодняшний день в мире самые часто встречаемые жалобы взрослого населения во многом связаны с заболеваниями опорно-двигательного аппарата. При этом большая доля из них приходится на патологию периартикулярных тканей (ПАТ), что закономерно обусловлено постоянной двигательной активностью человека, в которой эти ткани играют огромную роль и задействованы во всех локомоторных паттернах. Обращения по поводу патологии ПАТ составляют до 60% всех первичных обращений к врачам-специалистам, а по некоторым данным превышают эту цифру, так как в статистику не попадают случаи обращения к непрофильным специалистам.
Периариткулярные или околосуставные ткани — объединяющее понятие, которое включает не только суставные образования (хрящ, капсула, связка, синовиальная оболочка, надкостница, кость и т. д.), но и отдаленные структуры, участвующие в формировании движений сустава — мышцы, фасции, связки, сухожильные влагалища, суставные сумки, апоневрозы, нервнососудистые образования и даже подкожно-жировая клетчатка [1].
Как частный вид скелетно-мышечных болезней, независимо от этиологии, во многом патология ПАТ обусловлена едиными патогенетическими закономерностями, определяющими их появление и переход в хроническое состояние [2].
Патология ПАТ не ограничивается анатомической областью сустава и, согласно МКБ10, имеет довольно широкий диапазон: теносиновит, тендинит, тендиноз, бурсит,

Кокорин В.В.
энтезит, энтезопатия, капсулит, фасциит, апоневрозит, миофасциальный болевой синдром и т. д.
По данным ряда авторов генез патологии ПАТ основан как на травматическом и дегенеративно-дистрофическом, так и инфекционно-воспалительном механизмах, а по нашим представлениям имеет место их комбинация и чередование в определенной последовательности, в зависимости от ряда условий и причин.
Малая изученность этиологических факторов, сложность патоморфологических, нейротрофических и иммуновоспалительных нарушений определяет не только трудность в выборе лечебной тактики и лекарственных препаратов, но и оказывает влияние на сроки выздоровления [3].
Более 40% оперативных вмешательств в практике хирурга и травматолога при патологии ПАТ занимают вмешательства, связанные с болевым синдромом и хронизацией процесса, при этом частота рецидивов дегенеративно-воспалительных изменений за последнее десятилетие существенно не изменилась и достигает более 50% [4–6].
В связи с увеличением продолжительности жизни населения планеты, по данным скринингового исследования, увеличивается не только абсолютное количество заболеваний костно-мышечной системы и, соответственно, ПАТ, но и степень дегенеративных изменений костной, сухожильной, фасциальной и др. околосуставных тканей [7].
У большинства пациентов в возрасте более 60 лет, по данным ультразвукового и магнитно-резонансного исследований, наблюдаются более выраженные дегенеративно-дистрофические нарушения комплекса ПАТ, и замедление сроков их репарации, что требует более тщательного подхода в диагностике, а также правильного выбора лечебной тактики [8–10].
Клинические наблюдения свидетельствуют, что перспективы улучшения результатов восстановительного лечения пациентов с патологией ПАТ за счет оптимизации консервативных и физиотерапевтических методов лечения, применение новых групп фармакологических препаратов, без учета этиопатоморфологических особенностей заболеваний, в основном себя исчерпали [11–13], а хирургические методы, по нашему мнению, анатомически необоснованы и представлены довольно радикальными нефизиологическими операциями.
Анализ причин ограниченной эффективности стандартных подходов в лечении больных патологией ПАТ свидетельствует о необходимости подробного изучения этиопатогенетических механизмов с целью совершенствования методов консервативного лечения и хирургических вмешательств с учетом изученных факторов, анатомо-физиологических особенностей, а также с использованием современных достижений регенеративной медицинской биологии [14; 15].
Для обоснования такого подхода к формированию лечебной тактики, был использован богатый опыт экспериментальной хирургии [16–18].
Цель: определить структурные элементы ПАТ, изучить упругость и прочность тканей, а также определить наиболее подверженные повреждению структуры КСК, путем моделирования воздействия механического агента, оценки морфологических изменений, проведения сравнительного анализа полученных данных.
Материалы и методы
Комплекс ПАТ включает в себя множество структур, из которых наиболее подверженным изменениям — в силу различных этиологических и филогенетических причин — оказываются переходные ткани. Обстоятельства их повреждения разнообразны. Для наглядности демонстрации мы выбрали механическую теорию их возникновения и рассмотрели на примере костно-сухожильного комплекса (КСК), состоящего из дистального сухожилия бицепса и лучевой кости.
Исследование проведено на трупном материале, взятом у мужчин в возрасте 35–45 лет, не позднее 48 суток со дня смерти, не имеющих, согласно медицинской документации, патологии костно-мышечной системы и системных заболеваний, оказывающих влияние на прочность исследуемых тканей. Взятие материала и исследование проводилось с согласия родственников и одобрено локальным этическим комитетом.
30 препаратов сухожилия дистального бицепса и 30 препаратов КСК были стандартизированы для проведения испытаний. В исследовании использована cервогидравлическая многоцелевая динамическая испытательная машина (для биомедицинских материалов) — LFV-10-T50II (Рис. 1). Оснащение соответствовало возможности проведения сложных двухосевых испытаний на растяжение/сжатие и вращение с синхронизацией

Рис. 1. Сервогидравлическая многоцелевая динамическая испытательная машина для испытания биомедицинских материалов, LFV-10-T50II.
Кокорин В.В.
управления по обеим осям нагружения. Выполнялся механический анализ величины возможной нагрузки на сегмент, от момента появления начальных повреждений до полного прекращения приложения силы воздействия. Параметры исследования включали характеристики — растяжение и деформации с постепенным увеличением силы приложения.
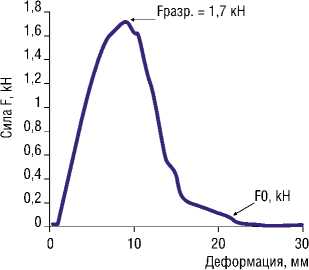
Эксперимент проводили в два этапа. На первом — 30 стандартизированных препаратов сухожилия дистального бицепса — исследовали на растяжение и деформацию. Деформация определяла максимальную способность ткани сохранять целостность и упругость до появления первых признаков повреждения ткани при максимальных критических нагрузках — критическая сила разрыва (Fразр., кН) — после которой сила сопротивления ткани уменьшалась и при полном разрыве и при расхождении краев ткани относительно друг о друга, равнялась нулю (F0, кН) (Рис. 2, 3).
Определена средняя сила приложения необходимая для разрыва сухожилия при постепенном увеличении нагрузки — Fсух. ср. = 1,2 кН, при этом медиана составила Ме сух. = 1,2кН (0,8–1,7), средняя величина деформации сухожилия в момент пикового приложения силы, составила Д пик. сух. ср. = 6,1 мм, а в нулевой точке Д F0. сух. ср. = 13,5 мм.
Второй этап эксперимента включал исследование 30 стандартизированных препаратов КСК, закрепленных в испытательной машине по отработанной методике таким образом, чтобы результаты исследования были максимально сопоставимы и исключали разницу точек приложения силы. В исследуемые параметры так же были включены параметры растяжения и деформации. Среднее значение силы приложения необходимой для разрыва КСК при постепенном увеличении нагрузки составило Fкск. ср. = 0,35 кН, медиана Ме кск. = 0,4 кН (0,2–0,6) (Рис. 4).
Отдельной задачей второго этапа исследования, явилось определение первичной точки возникновения повреждения КСК при приложении механической силы, направленной на разрыв.
Во всех исследуемых стандартизированных КСК препаратах (n = 30), при равных условиях (точка фиксации, постепенно увеличивающейся одинаковой скоростью приложения силы) первичной точкой повреждения, за-
А
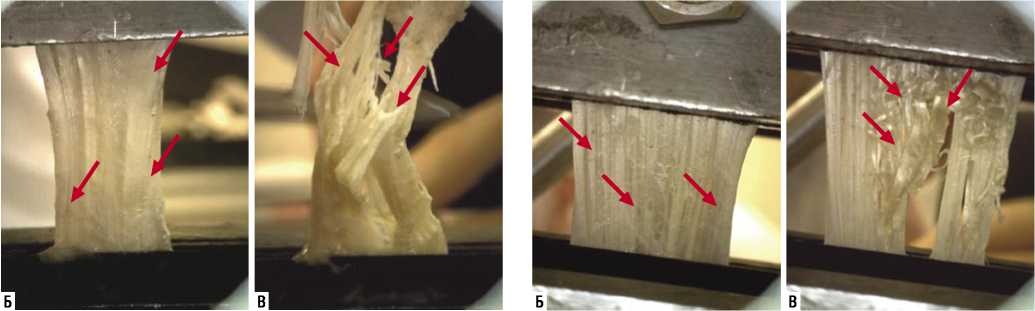
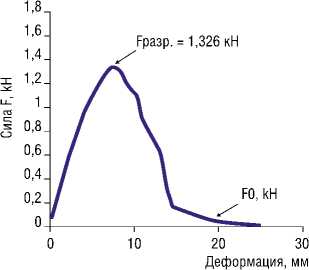
Рис. 3. Исследование прочности сухожилия (I этап). А — график соотношения приложенной силы к величине деформации при растяжении сухожилия, пиковая точка Fразр. = 0,6 кН, соответствует началу разрыва волокон. Б — состояние равновесия сил сопротивления и разрыва сухожильных волокн, участки разрыва фасции (указаны стрелками). В — сухожильные волокна разорваны частично, сопротивление ткани сохраняется, сила приложения уменьшается и стремится к нулю, деформация в нулевой точке приложения силы (F = 0 кН) составила 20 мм.
Рис. 2. Исследование прочности сухожилия (I этап). А — график соотношения приложенной силы к величине деформации при растяжении сухожилия, пиковая точка Fразр. = 1,7 кН, соответствует началу разрыва волокон. Б — сухожильные волокна предельно натянуты, сила сопротивления и разрыва находятся в состоянии равновесия, стрелками указаны участки разрыва фасции. В — волокна сухожилия деформированы, сопротивление ткани отсутствует, сила приложения равна 0 (F = 0 кН), деформация составила 22 мм.
Кокорин В.В.
фиксированной скоростной камерой исследовательского комплекса, стало место перехода дистального сухожилия двуглавой мышцы плеча в бугристость лучевой кости, которое является физиологической переходной структурой и описывается в литературе как фиброзно-хрящевой энтезис.
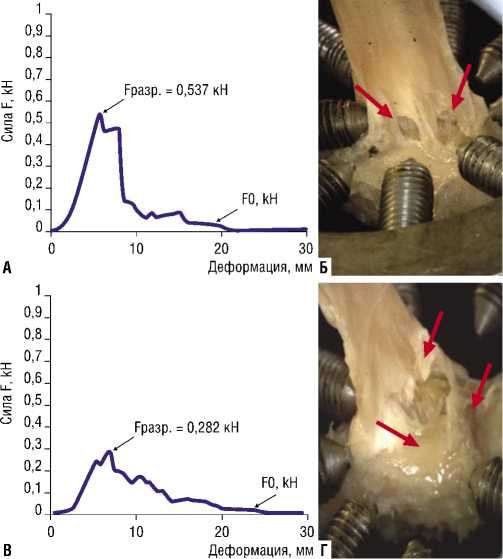
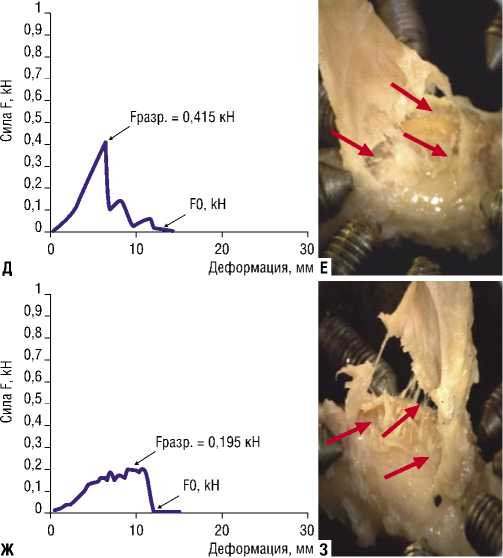
Рис. 4. График зависимости растяжения КСК от силы воздействия F, kH (А, В, Д, Ж); разрыв энтезальной части КСК (указан стрелками) (Б, Г, Е, З).
Выводы
Выполненное экспериментальное исследование позволяет утверждать о важной роли физиологических свойств фасциально-мышечной структуры в комплексе периартикулярных тканей, таких как эластичность, упругость, сократимость, выполняющих демпферную функцию в связке КСК комплекса и играющей важную роль в предотвращении повреждений ПАТ, в частности энтезисов, при воздействии механических факторов. Так как при регидности мышц и фасций, соответственно, мы получаем близкую к экспериментальной модели фиксацию структур КСК, то, соответственно, с большей долей вероятности можем утверждать о начальных признаках возникновения и распространения патологического процесса ПАТ именно из области энтезиса — переходных тканевых структур.
При исследовании сухожильной ткани на прочность отмечена следующая закономерность — при критических показателях воздействия силы, когда сила сопротивления и разрыва находятся в состоянии равновесия (Fсопр. = Fразр.), а целостность сухожильных волокон сохранена, в первую очередь происходит разрыв фасциальной ткани, покрывающей сухожилие. В отличие от КСК, при растяжении которого в критической точке приложения силы происходит, отрыв энтезальной части при сохранении целостности фасции (Рис. 5).
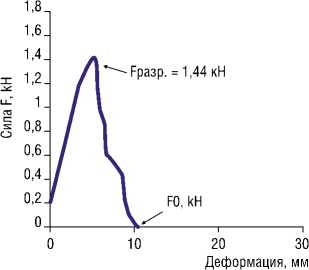

Рис. 5. Растяжение дистального сухожилия бицепса плеча. А — график соотношения приложенной силы к величине деформации при растяжении сухожилия, пиковая точка Fразр.=1,44 кН, соответствует началу разрыва волокон. Б — фиксированное сухожилие, волокна не натянуты, фасция интактна. В — разрыв фасции (указан стрелками), сухожильные волокна напряжены, целостность сохранена.
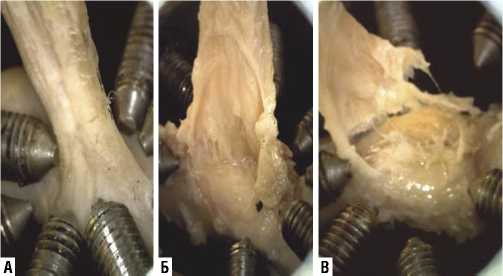
Рис. 6 Растяжение КСК. А — пиковая точка Fразр. = 0,44 кН, соответствует началу разрыва энтезальной части (Б), фасция покрывающая сухожилие интактна; В — полный отрыв энтезальной части, F0.

Кокорин В.В.
Вместе с тем установлено что при прочих равных условиях, сила приложения необходимая для разрыва сухожилия при постепенном увеличении нагрузки (Fсух. ср.) составила 1,2 кН, а медиана (Ме сух.) 1,2 кН (0,8–1,7), в то время как для отрыва энтезальной части комплекса требуется (Fкск. ср.) 0,35 кН, при медиане (Ме кск.) 0,4 кН (0,2–0,6), что трехкратно меньше силы воздействия на сухожилие и объясняет частое повреждение в первую очередь этой структуры при механических перегрузках (Рис. 6).
Обсуждение
В структуре ПАТ энтезис является наиболее молодым филогенетическим комплексом с точки зрения эволюции, поэтому молодая и еще несовершенная структура является такой уязвимой для воздействия повреждающих факторов.
Непонятна роль аваскулярной переходной зоны энтеза, преимущественно повреждающейся при патологии ПАТ. Неясность структуры заставляет задуматься о характере эволюционных изменений — прогрессивное совершенствование, незаконченное развитие или деструктивный регресс?
Рассматривая с разных позиций, мы отмечаем, что при патологии ПАТ чаще повреждается энтезокомплекс, который защищен от васкулярных/ геморрагических/ экссудативных процессов/повреждений сосудов — их отсутствием, а ткани структуры энтеза изначально адаптирована к работе в бессосудситых, гипотрофических условиях.
С другой стороны, именно по этой же причине возникает регенераторный дефицит, хронизация процесса и длительное течение болезни [19; 20].
Является ли отсутствие сосудов в энтезе филогенетическим прогрессом или остается незавершенным развитием, а может имеет признаки локомоторной дегенерации, требует дальнейшего изучения.
Заключение
Выполненный эксперимент демонстрирует принципиальную важность при устранении патологии энтеза, независимо от ее генеза, обеспечить васкуляризацию поврежденных тканей, без которой невозможно добиться эффективной репаративной регенерации. В качестве наиболее перспективного метода следует рассматривать индуцированный ангиогенез с помощью клеточных и генных технологий [15; 19; 21].
Автор заявляет об отсутствии конфликта интересов (The author declare no conflict of interest).
Список литературы Экспериментальное обоснование этиопатогенетического подхода в хирургии патологии периартикулярных тканей
- Speed CA. Fortnightly review: Corticosteroid injections in tendon lesions. BMJ. 2001; 323(7309): 382-6. doi: 10.1136/bmj.323.7309.382.
- Каратеев А.Е., Мисиюк А.С. Нестероидные противовоспалительные препараты как первая ступень при лечении скелетно-мышечной боли // Современная ревматология. — 2015. — №9(3). — С.61-69. doi:10.14412/1996-7012-2015-3-61-69.
- Хитров Н.А. Параартикулярные ткани: варианты поражения и их лечение // РМЖ. — 2017. — №3. — С.177-184.
- Сёмкин В.А., Зарецкая А.С. Амбулаторное лечение пациентов с обширными кистами челюстных костей // Стоматология. — 2010. — Т.89. — №3. — С. 34-36.
- Щипский А.В., Годунова И.В. Причины рецидива кистозных образований челюстей // Стоматология. — 2016. — Т.95. — №2. — С.84-88.
- Morgan TA, Burton CC, Qian F. A retrospective review of treatment of the odontogenic keratocyst. J. Oral. Maxillofac. Surg. 2005; 63(5): 635-639.
- Бондаренко Н.А., Лосев Ф.Ф., Бондаренко А.Н. Потребность в дентальной имплантации и частота ее применения // Кубанский научный медицинский вестник. — 2010. — №3-4 (117-118). — С.29-32.
- Иванов С.Ю., Мураев А.А., Ямуркова Н.Ф. Реконструктивная хирургия альвеолярной кости. — М.: ГЭОТАР-Медиа, 2016. — 360 с.
- Кулаков А.А., Гветадзе Р.Ш., Брайловская Т.В., Харькова А.А., Дзиковицкая Л.С. Современные подходы к применению метода дентальной имплантации при атрофии и дефектах костной ткани челюстей // Стоматология. — 2017. — Т.96. — №1. — С.43-45.
- De Groot RJ, Oomens MAEM, Forouzanfar T, Schulten EAJM. Bone augmentation followed by implant surgery in the edentulous mandible: A systematic review. J. Oral Rehabil. 2018; 45(4): 334-343.
- Алиев С.Э., Назарян Д.Н., Мельников Д.А. Интраоперационные осложнения при заборе свободного расщепленного аутотрансплантата теменной области и пути их решения // Анналы пласт., реконструктив. и эстет. хирургии. — 2013. — №4. — С.22-25.
- Калакуцкий Н.В., Якунин С.И., Авраменко В.В., Веселова К.А. Оценка функции нижней конечности после пересадки васкуляризированного аутотрансплантата из малоберцовой кости у детей при устранении дефектов нижней челюсти // Анналы пласт., реконструктив. и эстет. хирургии. — 2016. — №3. — С.27-34.
- Mertens C, Decker C, Engel M, et al. Early bone resorption of free microvascular reanastomized bone grafts for mandibular reconstruction — a comparison of iliac crest and fibula grafts. J. Craniomaxillofac. Surg. 2014; 42(5): 217-223.
- Шевченко Ю.Л., Матвеев С.А., Пинаев Г.П. и др. Экспериментальное обоснование возможности имплантации эмбриональных кардиомиоцитов в комплексной терапии миокардиальной слабости // Физиология человека. — 1999. — Т.25. — №4. — С. 109-117.
- Шевченко Ю.Л. Медико-биологические и физиологические основы клеточных технологий в сердечно-сосудистой хирургии. — СПб.: Наука, 2006. — 263 с.
- Кованов В.В. Эксперимент в хирургии. — М.: Мол. Гвардия, 1989. — 237с.
- Шалимов С.А., Радзиховский А.П., Кейсевич Л.В. Руководство по экспериментальной хирургии. — М.: Медицина, 1989. — 270 с.
- Экспериментальная хирургия / Под. ред. Шевченко Ю.Л. — изд. 2-е, доп. — М.: Династия, 2011. —583 с.
- Шевченко Ю.Л., Борщев Г.Г. Стимуляция ангиогенеза эндогенными факторами роста // Вестник национального медико-хирургического Центра им. Н.И. Пирогова. — 2018. — Т13. —№3. — С.96-102.
- Шевченко Ю.Л., Матвеев С.А., Соловьев И.А. Роль ангиогенеза в норме и патологии // Вестник Российской Военно-медицинской академии. — 2001. — Т.5. — №1. — С 92-98.
- Шевченко Ю.Л., Борщев Г.Г. Экстракардиальная реваскуляризация миокарда у больных ИБС с диффузным поражением коронарного русла. — М.: Изд-во «Национального медико-хирургического Центра им. Н.И. Пирогова», 2022. — 292 с.


