Экспериментальное обоснование введения кеналога в стекловидную камеру глаза после витрэктомии
Автор: Шишкин М.М., Перова Н.В., Гильманшин Т.Р., Довжик И.А.
Журнал: Вестник Национального медико-хирургического центра им. Н.И. Пирогова @vestnik-pirogov-center
Рубрика: Оригинальные статьи
Статья в выпуске: 1 т.3, 2008 года.
Бесплатный доступ
Данное исследование посвящено обоснованию интравитреального введения Кеналога в офтальмохирургической практике. В эксперименте были исследованы безопасность и эффективность интравитреального введения препарата, в том числе - после субтотальной витрэктомии. Отрицательного воздействия препарата, приводящего к патологическим изменениям внутренних структур авитреального и витреального глаза, нами выявлено не было. Зарегистрированные изменения функциональной активности сетчатки витреального глаза в виде увеличения амплитуды волны В ЭРГ носили обратимый характер и нормализовалось к 21 суткам исследования. Интравитреальное введение Кеналога по сравнению с субтеноновым наиболее эффективно подавляет локальный воспалительный ответ на операционную травму и предупреждает развитие патологической пролиферативной реакции.
Короткий адрес: https://sciup.org/140188713
IDR: 140188713 | УДК: 617.747
Текст научной статьи Экспериментальное обоснование введения кеналога в стекловидную камеру глаза после витрэктомии
Стремительное развитие современной витреорети-нальной хирургии (ВРХ) характеризуется внедрением усовершенствованных хирургических приемов, многие из которых являются по своей сути излишне радикальными. В итоге конечная благая цель достигается за счет дополнительных повреждений внутренних структур глаза [11, 15]. Вследствие этого развивается патологический воспалительный ответ, который в ряде случаев стимулирует развитие пролиферативной витреоретинопатии. В настоящее время все больше исследователей приходит к выводу, что для профилактики развития выраженного воспалительного ответа после операционной травмы необходимо применение фармакологических препаратов [7].
Наиболее широкое клиническое применение в офтальмологии в последнее время нашли глюкокортикостероиды (ГКС) [4, 5, 7]. Как известно, ГКС оказывают угнетающее воздействие на все фазы воспалительного процесса [6, 7]. Для лечения патологии заднего отдела глаза ГКС применяются в виде местных периокулярных (парабульбарных, ретробульбарных и субтеноновых) инъекций [2].
В начале 80-х годов прошлого столетия Machemer R. с соавторами впервые исследовали в эксперименте возможность интравитреального введения ГКС. Данный способ имеет ряд преимуществ: в витреальной полости создается высокая внутриглазная концентрация препарата, увеличивается время его воздействия непосредственно на очаг поражения, значительно уменьшается системное побочное действие [22].
В настоящее время, в офтальмологии наиболее часто применяется препарат группы ГКС – триамцинолона ацетонид (ТА) – твердая кристаллическая структура которого и медленная растворимость в водной среде определяет длительное воздействие. Несмотря на то, что Кеналог (коммерческая форма триамцинолона) не предназначен для интравитреального введения, в современной литературе появляется все большее количество публикаций об эффективности данного пути введения при лечении рефрактерного макулярного отека и неоваскуляризации сетчатки и хороидеи [17, 20, 21, 23, 25]. В то же время имеются сообщения об отсутствии преимущества данного пути введения препарата по сравнению с более безопасным – субтеноновым [12, 16, 18]. Данные литературных источников указывают наиболее часто используемую для интравитреального введения дозу Кеналога в 0,1 мл, однако, мнения о побочном действии указанной дозы на морфологию и функцию сетчатки расходятся [17, 19, 20, 21, 24, 26]. Также в доступной литературе нами не найдено данных о безопасности введения Кеналога в авитреальный глаз. Вышеизложенные факты обозначили актуальность проблемы и послужили предметом настоящего исследования.
Целью работы явилось экспериментальное обоснование профилактического введения Кеналога в полость глаза после витрэктомии.
Задачи исследования
-
1. Изучение в эксперименте биологического действия Кеналога при его введении в авитреальный и витреаль-ный глаз.
-
2. Сравнение эффективности интравитреального и субтенонового введения препарата кеналог на экспериментальной модели операционной травмы.
Материалы и методы
Предметом исследования явился препарат с торговым названием Кеналог (Kenalog) (Bristol-Myers Squibb S.r.L., Италия). Для решения поставленных задач было выполнено 2 части экспериментального исследования. В первой части было изучено биологическое действие Кеналога на интраокулярные структуры и функцию сетчатки при его интравитреальном введении, во второй – его эффективность при данном способе введения.
Эксперимент был выполнен на кроликах породы Шиншилла весом от 2 до 2,5 кг, одинаковой окраски.
В первой части эксперимента биологическое действие препарата исследовали как при наличии стекловидного тела (СТ), так и после субтотальной витрэктомии (ВЭ).
Эту часть исследования выполняли на 4-х экспериментальных группах по 5 животных (10 глаз) в каждой: 1 группа (контроль) – после инъекции раствора BSS в СТ; 2 группа (контроль) – после ВЭ без введения Кеналога; 3 группа – после инъекции Кеналога в СТ; 4 группа – после ВЭ и введения Кеналога в СК (рис. 1, 2, 3 А и Б). Вводимая интравитреально доза препарата составяла 0,1 мл (4 мг активного вещества).
Прижизненные исследования включали в себя офтальмобиомикроскопию на 1, 7, 14, 21 и 30 сутки после операции; электроретинографию (ЭРГ) и тонометрию на 7, 14, 21 и 30 сутки. Для изучения динамики показателей ЭРГ учитывали процент сохранности амплитуды волны В по отношению к усредненным данным интактных глаз принятых за 100%. Амплитуда волны В характеризует биоэлектрическую активность внутренних слоев сетчатки и наиболее широко используется в клинической практике [1]. Уровень внутриглазного давления (ВГД) также выражали в процентах относительно нормальных показателей интактных глаз, принятых нами за 100%.
Конфокальную и световую микроскопию тканей глаза выполняли после энуклеации на 30 послеоперационные сутки. Для гистологического исследования энуклеированные глаза обрабатывали по общепринятой методике, гистологические срезы окрашивали гематок-силин-эозином.
Вторая часть эксперимента включала в себя исследование эффективности Кеналога вводимого в СК после ВРХ с целью профилактики воспалительно-пролиферативного ответа на операционную травму. Для этого выполняли ВЭ по стандартной методике. Для моделирования стандартной воспалительной реакции глаза на операционную травму по завершении ВЭ в полость глаза вводили 0,2 мл аутокрови. За основу взяли модель, описанную Сleary P. и Ryan S. (1979). Эффективность интравитреального введения Кеналога сравнивали с его субтеноновым введением. Эту часть исследования выполнили на 3-х экспериментальных группах, по 15 животных (30 глаз) в каждой: 1-ая группа (контроль) – после ВЭ и введения аутокрови в СК; 2-ая группа – после ВЭ с введением аутокрови и Кеналога в СК; 3-я группа – после ВЭ с введением аутокрови в СК и Кеналога субтеноново в дозе 0,5 мл. Методами исследования служили: офтальмобиомикроскопия, ЭРГ и световая микроскопия сетчатки. Сроки прижизненного наблюдения данной части эксперимента составили 1, 4, 7, 15 и 30 сутки. Микропрепараты для световой микроскопии готовили на 30 сутки.
Витрэктомию выполняли по стандартной методике с использованием офтальмохирургической системы «Oert-ly» (Швейцария), 2-х портовым доступом под контролем операционного микроскопа «Takagi OM-5», при увеличе-ниии 10,0х(Takagi, Seiko Co., Ltd, Япония) и скошенной (25 град.) контактной роговичной линзы (рис. 1, 2).
Животных выводили из эксперимента на 30 сутки после операции. Работу с экспериментальными животными выполняли в соответствии с требованиями нормативного документа Министерства Здравоохранения «Правила проведения работ с использованием экспериментальных животных» (Приказ МЗ СССР № 755 от 12.08.77).
Результаты и обсуждение
Полученные в 1-ой экспериментальной части результаты выявили отсутствие побочного влияния на орган зрения интравитреально введенного 0,1 мл Кеналога. На протяжении всего периода наблюдения (7–30 сутки) нами не отмечено каких-либо заметных изменений со стороны внутренних структур глазного яблока у животных всех групп: роговица и глубжележащие оптические среды оставались прозрачными; сохранялась живая реакция зрачка на свет; цвет и структура радужной оболочки оставались без перемен; каких-либо очаговых изменений со стороны сетчатки и зрительного нерва, которые можно было бы трактовать как результат побочного действия Кеналога, мы также не наблюдали. При этом, во 2-ой контрольной группе (ВЭ без введения препарата) офтальмобиомикроскопически отмечали признаки воспаления, связанного с хирургическим витреоретинальным вмешательством. Воспалительная реакция выражалась в хемозе, гиперемии конъюнктивы (100%) и опалесценции влаги передней камеры (30,0%), в подавляющем большинстве случаев эти признаки полностью купировались на 7 сутки послеоперационного наблюдения. Отсутствие каких-либо клинически заметных признаков воспаления со стороны прооперированных глаз у животных 4-ой группы (ВЭ с введением Кеналога) мы связываем с противовоспалительным действием препарата. Признаков воспалитель-
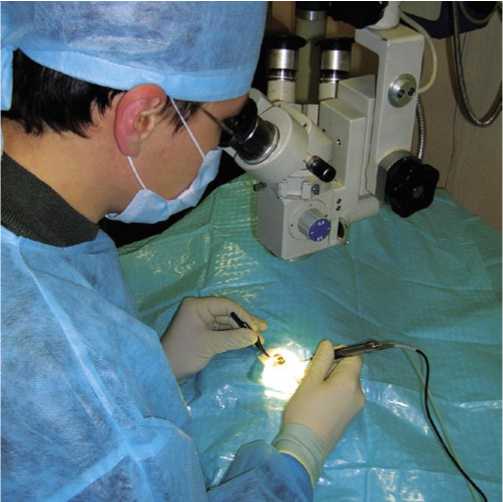
Рис. 1. Интравитреальная инъекция Кеналога
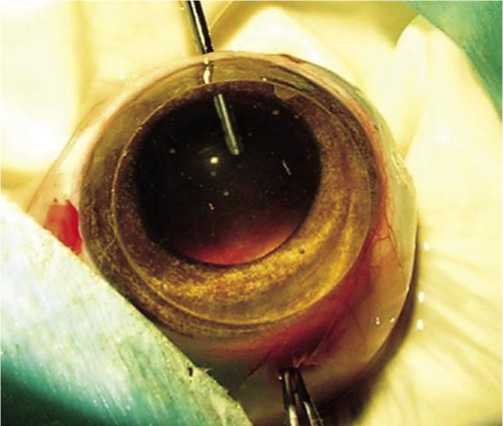
Рис. 2. Операция субтотальная витрэктомия
Табл. 1. Относительные показатели средней амплитуды волны В (%) электроретинограммы животных обеих групп в разные сроки первой части эксперимента
|
Группа |
Период исследования |
|||
|
7 сутки |
15 сутки |
21 сутки |
30 сутки |
|
|
Группа 1 |
86,1+4,3* |
106,6+5,4 |
108,4+3,1 |
96,1+4,9 |
|
Группа 2 |
82,3+5,7* |
88,3+3,9 |
105,3+4,2 |
112,8+5,1 |
|
Группа 3 |
122,6+5,2* |
125,5+5,8* |
115,1+3,8 |
107,5+4,3 |
|
Группа 4 |
108,7+3,7 |
97,5+4,3 |
106,4+5,4 |
109,3+3,9 |
|
Интактный глаз (норма) |
100+5,6 |
100+5,6 |
100+5,6 |
100+5,6 |
* достоверная разница (р<0,05) между данным значением и значением интактного глаза ной реакции на 1-ые и последующие сутки в 1 и 3 группах, после интравитеральной инъекции, нами не отмечено.
Результаты нашего исследования соответствуют результатам наблюдений других авторов, которые отмечали повреждающее воздействие ВРХ на интраокулярные структуры с развитием изменений на тканевом уровне. По их данным витрэктомия без дополнительного медикаментозного лечения может вызвать соответствующий воспалительный ответ, а в ряде случаев – пролиферативную реакцию с формированием патологических мембран в стекловидной камере глаза [3, 10, 13]. Однако, по данным тех же авторов, в большинстве случаев изменения сетчатки после экспериментальной ВРХ носят обратимый характер и продолжительность активной воспалительной реакции ограничена. Уже на 30 послеоперационные сутки изменения в тканях оперированного глаза, отмеченные в течение первых двух недель после ВРХ, полностью разрешаются.
Достоверной разницы в уровне ВГД между контрольными и опытными группами нами отмечено не было. У всех животных оно сохранялось в пределах нормы. Это свидетельствует об отсутствии влияния данной дозы препарата на гидродинамику исследуемых глаз при введении его в СК.
Об отсутствии токсического влияния вводимой дозы Кеналога на ткани глаза свидетельствовали результаты гистологических исследований. Заметной разницы между препаратами тканей глаза опытных и контрольных групп нами выявлено не было (рис. 3А–Г).
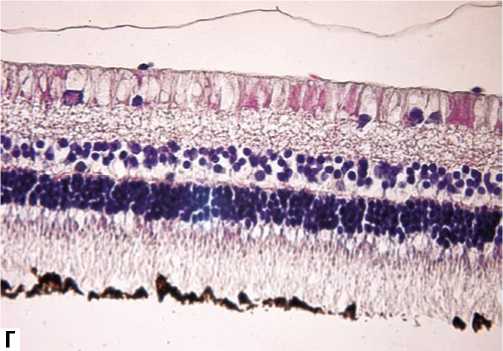
На микропрепаратах всех групп видна правильная структура цилиарного тела с обычным клеточным составом, нормальным калибром сосудов, равномерной толщиной пигментного эпителия. Угол передней камеры открыт. Сетчатая оболочка имеет правильное строение с четкой дифференциацией всех составляющих ее слоев (рис. 4 А–Г). Наружный, внутренний зернистые слои и слой фоторецепторов хорошо выражены. Ретинальный пигментный эпителий сохраняет обычное строение. Ганглиозные клетки не изменены. Признаков патологических (дистрофических или/и воспалительных) изменений в слоях сетчатки, которые можно было бы связать с действием интравитреально введенного Кеналога, нами не отмечено.
Результаты конфокальной микроскопии эндотелиального пласта роговицы животных свидетельствуют об отсутствии качественных и количественных изменений эндотелиальных клеток и об идентичности микроскопической картины на опытных и контрольных глазах кроликов. Статистически достоверной разницы между средним количеством эндотелиальных клеток у интактных животных (2612+127 кл/мм2) и у животных каждой из опытных групп нами выявлено не было. На основании этого можно говорить об отсутствии повреждающего влияния Кеналога на структуры передней камеры глаза.
В отличие от данных приведенных выше результаты электрофизиологического исследования сетчатки
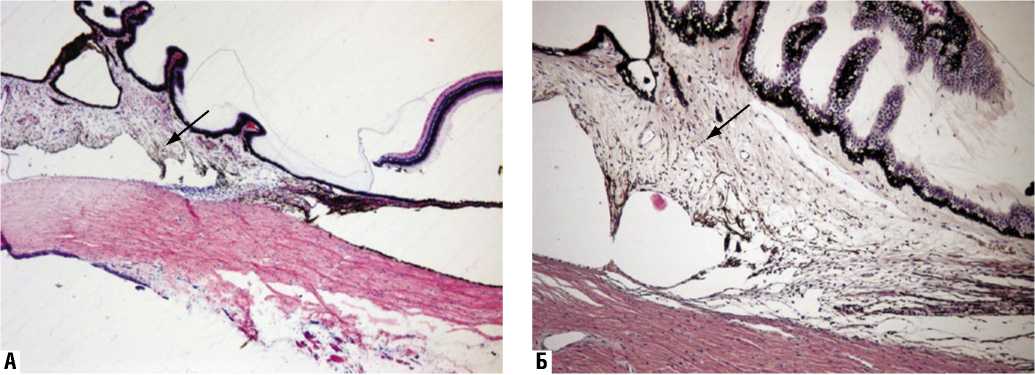
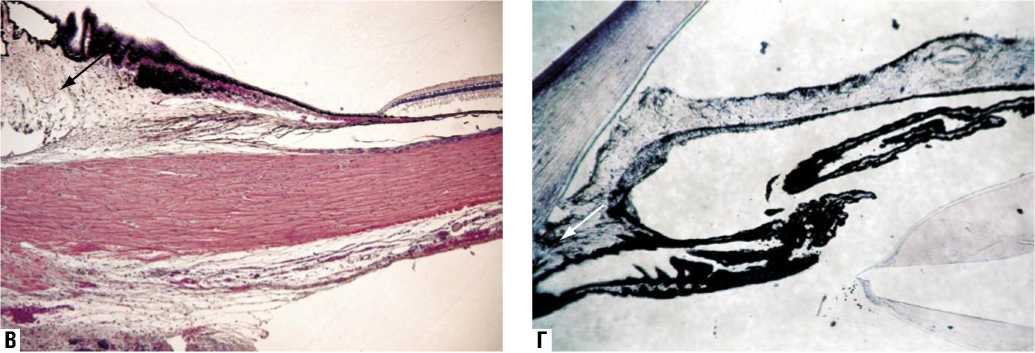
Рис. 3. Гистологическая картина тканей цилиарного тела (указано стрелкой) при изучении биологического действия препарата на 30 послеоперационные сутки. А – в 1-ой экспериментальной группе, Б – во 2-ой экспериментальной группе, В – в 3-ей экспериментальной группе, Г – в 4-ой экспериментальной группе. А, В, Г - увеличение х 50. Б - увеличение х 100
у животных экспериментальных групп отличались и меняли свое значение в течение периода наблюдения (табл. 1). Наиболее значительные функциональные изменения сетчатки зарегистрированы в первой половине послеоперационного периода у животных 1–3 групп по сравнению с нормой и 4-ой группой. Так, на 7-ые сутки в первых двух группах отмечали депрессию амплитуды волны В: в 1-ой – до 86,1+4,3% от среднего уровня нормы, во 2-ой – до 82,3+5,7%. Показатели биоэлектрической активности сетчатки у животных 3-ей опытной группы на 7–14 сутки, наоборот, характеризовались максимумом (в среднем до 122,6+5,2 – 125,5+5,8% от уровня интактного глаза). Проведенный нами статистический анализ показал достоверную разницу (р<0,05) между значениями амплитуды В волны ЭРГ животных каждой из 1–3 групп и интактными глазами в указанный период. Показатели ЭРГ в более поздние сроки у животных этих групп нормализовались. Заметных изменений электрогенеза сетчатки у животных 4-ой группы мы не наблюдали в течение всего периода наблюдения. Угнетение биоэлектрической активности сетчатки в 1-ой и 2-ой группах в первой поло- вине периода исследования можно объяснить влиянием операционной травмы, что соответствует наблюдениям других авторов [3, 8].
Отсутствие депрессии «b» – волны ЭРГ в 3-ей и 4-ой группах мы связываем с влиянием Кеналога, оказывающего угнетающее воздействие на все фазы воспалительного процесса с одновременным повышением устойчивости клеток к внешним воздействиям [5, 6]. Значительное возрастание амплитуды В волны в 3-ей группе на 7–14 сутки исследования мы связываем с более длительным нахождением препарата в витреальном глазу (по сравнению с авитреальным) и возможным его раздражающим действием на сетчатку [9]. Последующая нормализация ЭРГ свидетельствует о том, что отмеченные выше функциональные изменения носят обратимый характер. Отсутствие достоверной разницы амплитуды В волны ЭРГ между контрольными и опытными группами на 30 послеоперационные сутки свидетельствует о безопасности указанной дозы препарата при интравитреальном его введении, в т.ч. и в авитреальный глаз.
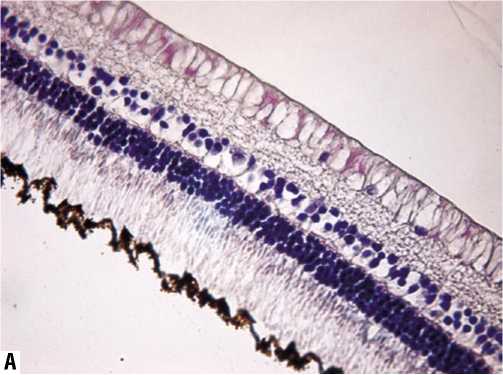
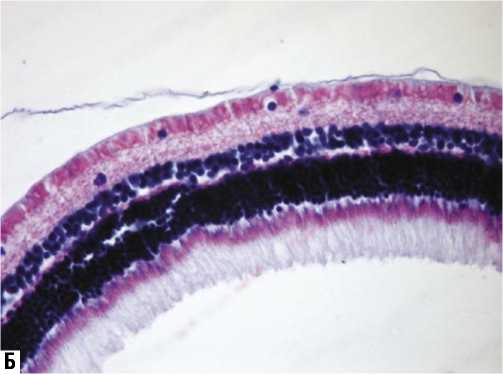
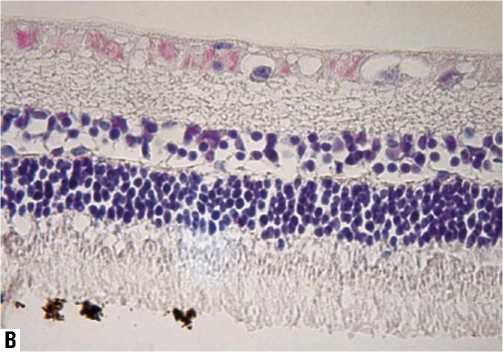
Рис. 4. Гистологическая картина тканей сетчатки глаза при изучении биологического действия препарата на 30 послеоперационные сутки. А – в 1-ой экспериментальной группе, Б – во 2-ой экспериментальной группе, В – в 3-ей экспериментальной группе, Г – в 4-ой экспериментальной группе. Увеличение х 400
Таким образом, нами не было выявлено каких-либо необратимых изменений со стороны внутренних структур витреальных и авитреальных глаз животных после введения Кеналога в СК.
Во 2-ой части эксперимента проводили изучение эффективности противовоспалительного и антипроли-феративного действия Кеналога после ВРХ в зависимости от методики введения препарата.
Регистрируемая нами воспалительная реакция со стороны переднего отрезка глаза в данной экспериментальной части носила значительно более выраженный характер по сравнению с наблюдениями в 1-ой части исследования и осложнялась ПВР. Это связано с провос-палительным действием введенной в СК аутокрови.
При офтальмобиомикроскопии на 1-ые послеоперационные сутки, в 1-ой группе (без введения Кеналога) мы наблюдали отек конъюнктивы и инъекцию поверхностных сосудов глаза в 100%. Во всех случаях в конъюнктивальной полости присутствовало слизисто-гнойное отделяемое. Опалесценцию влаги передней камеры отмечали в 60% наблюдений, серозный экссудат в передней камере
– в 30% (рис. 5А). Интраокулярную фибриноидную реакцию в передней трети стекловидной камеры отмечали в 53,3% наблюдений. Диффузное помутнение влаги СК, вызванное введением аутокрови, не позволяло оценить состояние сетчатки и зрительного нерва в течение первых 15 послеоперационных суток ни в одной из групп.
У животных 2 группы (введение Кеналога в СК авитреального глаза) на первые сутки в мы наблюдали лишь локальные хемоз и гиперемию конъюнктивы в области операционного разреза в 33,3% наблюдений (1-ая группа – 100,0%), опалесценцию влаги передней камеры – в 16,7% (1-ая группа – 60,0%) (рис. 5Б). Фибриноидную реакцию в передней трети стекловидной камеры регистрировали в 10,0 % наблюдений (1-ая группа – 53,3%). Экссудата в передней камере не наблюдали, в то время как у животных 1-ой группы подобную реакцию отмечали в 30,0%.
В 3-ей группе (введение Кеналога в субтеноновое пространство) хемоз и гиперемия конъюнктивы с незначительным слизистым отделяемым также носили локальный характер и визуализировались в 70,0% (во 2-
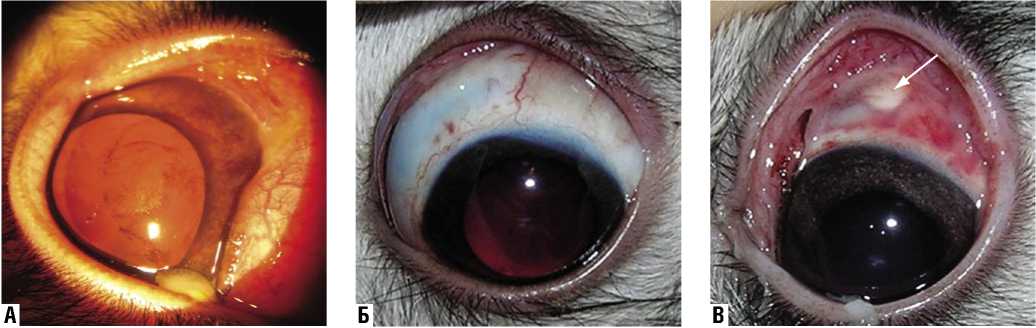
Рис. 5. Передний отрезок глазного яблока на 1-ые сутки после ВЭ и введения 0,2 мл аутокрови в СК (А), дополнительного введения 0,1 мл Кеналога в СК (Б), дополнительного субтенонового введения 0,5 мл Кеналога (В) (стрелкой указана смещенная в передний сегмент масса субтеноново введенного триамцинолона)
ой группе – 33,3% соответственно). Опалесценция влаги передней камеры у животных этой группы была отмечена нами в 36,7 % наблюдений (во 2-ой – 16,7%), экссудата в передней камере не было (рис. 5В). Фибриноидную реакцию стекловидной камеры отмечали в 23,3 % наблюдений (во 2-ой – 10,0%).
У животных 1-ой группы к концу 2-ой недели послеоперационного периода отмечали полное разрешение признаков воспаления переднего отрезка глаза, в то время как у животных 2-ой и 3-ей групп – данные признаки не регистрировались нами уже на 4-ые сутки. Более выраженный и длительный воспалительный процесс у животных 1-ой группы сопровождался более выраженной пролиферативной реакцией в полости глаза. Так, на 30-ые сутки, у животных 1-ой группы в СК визуализировали пролиферативные мембраны в 50 % наблюдений. Мембраны простирались от области скле-ростом в контралатеральном направлении или к диску зрительного нерва. При этом отмечали выраженную их плотность и ригидность (рис. 6А). Подобную реакцию у животных 2-ой группы не отмечали ни в одном случае (рис. 6Б), в 3-ей группе – только в 16,7 % наблюдений, но сформированные мембраны были менее плотными, сохраняли подвижность и располагались только в передней трети СК (рис. 6В). Гистологические исследования выявили значительную разницу состояния тканей глаза между экспериментальными группами. У животных 1-ой группы нами отмечены выраженные воспалительные изменения хороидеи и сетчатки в виде их диффузного отека и присутствия в них (и в остатках пристеночно расположенной крови) большого количества клеток воспалительного ряда (рис. 7А).
В большинстве случаев при микроскопии тканей глаза животных 2-ой группы отмечена лишь незначительная инфильтрация цилиарного тела, сетчатки и хоро-идеи единичными лимфоцитами, что можно объяснить противовоспалительным действием интравитреально веденного Кеналога (рис. 7Б).
В тканях глаз животных 3-ей группы в отличие от 2-ой наблюдали несколько более выраженную инфильтрацию лимфоцитами хороидеи (рис. 7В).
Результаты световой микроскопии второй части эксперимента свидетельствуют о том, что интравитре-альное введение Кеналога оказывает более благоприятное действие на весь воспалительный процесс по сравнению с субтеноновым его введением.
Результаты анализа ЭРГ (табл. 2) на 1-ые и 4-ые сутки после операции выявили достоверное снижение средней амплитуды В волны у животных всех 3-х экспериментальных групп: в пределах от 63,0+4,4 до 78,7+4,1% (р<0,05). В дальнейшем, во всех группах мы регистрировали нормализацию биоэлектрической активности сетчатки, но наиболее быстро восстанавливалось значение В волны во 2-ой опытной группе (после интравитреального введения Ке-налога): уже к 7 суткам после витрэктомии оно достигало исходной нормы. При этом, в 3-ей группе (субтеноновое введение препарата) исходных значений этот показатель достигал только к 15 суткам. У животных 1-ой группы (контроль) регистрировали наиболее значительное и длительное угнетение волны В, которое возвращалось к исходным данным только к 30 суткам наблюдения.
Полученные нами результаты электроретинографии коррелируют с результатами клинического и гистоло-
Табл. 2. Относительные показатели средней амплитуды волны В электро-ретинограммы (%) у животных опытных и контрольных групп в разные сроки второй части эксперимента
|
Группа |
Период исследования |
||||
|
1 сутки |
4 сутки |
7 сутки |
15 сутки |
30 сутки |
|
|
Группа 1 |
66,7+7,4* |
56,9+4,8* |
69,3+4,4* |
78,6+6,4* |
93,7+4,9 |
|
Группа 2 |
73,7+5,8 * |
78,7+4,1* |
96,8+4,9 |
94,2+6,7 |
108,8+3,5 |
|
Группа 3 |
63,0+4,4* |
65,7+3,2* |
86,7+2,7* |
108,4+4,1 |
105,6+6,7 |
|
Интактный глаз |
100+5,6 |
100+5,6 |
100+5,6 |
100+5,6 |
100+5,6 |
* достоверная разница (р<0,05) между данным значением и значением интактного глаза
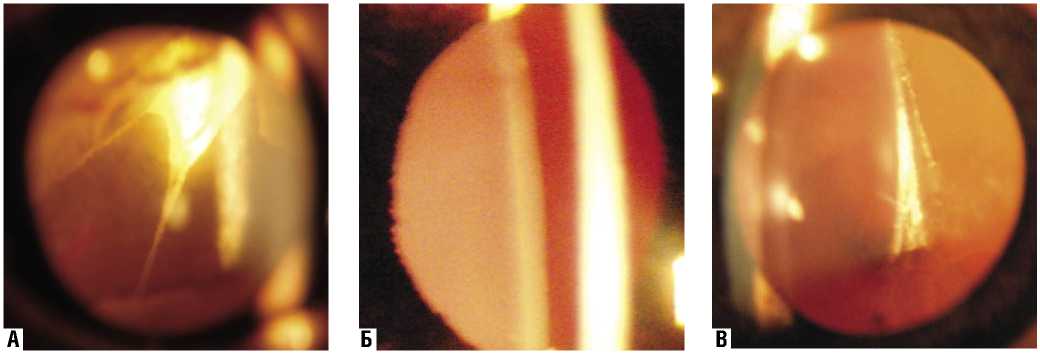
Рис. 6. Передняя треть СК на 30 сутки после ВЭ и введения 0,2 мл аутокрови в СК (А), дополнительного введения 0,1 мл Кеналога в СК (Б), дополнительного субтенонового введения 0,5 мл Кеналога (В)


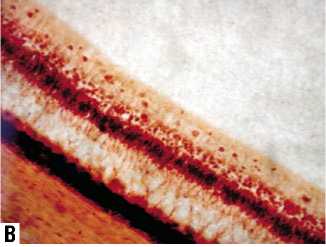
Рис. 7. Гистологическая картина тканей заднего сегмента глаза при изучении эффективности на 30 сутки. А и Б – в 1-ой экспериментальной группе, В - во 2-ой экспериментальной группе, Г - в 3-ей экспериментальной группе. Увеличение х 400.
гического исследования: угнетение биоэлектрической активности сетчатки соответствовало выраженности воспалительного процесса. Так, максимальное угнетение функции сетчатки и медленное ее восстановление, отмеченное нами у животных 1-ой контрольной группы, регистрировали на фоне наиболее выраженной воспалительной реакции. Менее выраженная депрессия В волны ЭРГ у животных 2 и 3 групп соответствовала менее выраженной реакции глаза на операционную травму.
Таким образом, различные методы исследования, примененные нами во 2-ой части эксперимента, показали, что введение Кеналога в СК авитреального глаза более эффективно (по сравнению с субтеноновой его инъекцией) ингибирует воспалительно-пролиферативный ответ на операционную травму. Наряду с этим, результаты нашего исследования свидетельствуют о том, что введение Кенало-га непосредственно в СК является не только эффективным, но и безопасным методом профилактики воспалительнопролиферативного ответа после витрэктомии.
Выводы
-
1. Кеналог дозой 0,1 мл, при введении в стекловидную камеру, не оказывает побочного действия на
-
2. Интравитреальный путь введения Кеналога, по сравнению с субтеноновым, наиболее эффективно купирует послеоперационную воспалительно-пролиферативную реакцию.
внутриглазные структуры и функцию витреального и авитреального глаза.
38–41.
Список литературы Экспериментальное обоснование введения кеналога в стекловидную камеру глаза после витрэктомии
- Бызов А.Л. Физиология сетчатки: нейромедиаторы и электрогенез Клиническая физиология зрения. -М., 1993. -С. 12-26.
- Егоров Е.А., Астахов Ю.С., Ставицкая Т.В. Офтальмофармакология. Руководство для врачей. -М., 2004. -С. 171-179.
- Куликов А.Н. Экспериментальное изучение высокочистых жидких перфторорганических соединений при интравитреальном введении. -Дисс. канд. мед. наук -СПб., 1997. -С. 165.
- Пасечникова Н.В., Зборовская А.В., Яковенко Т.А. Инфекционные задние увеиты.-Киев: 2005. -С. 38-40.
- Сафонова А.Ф., Лининов В.В., Михайлов К.В. Поиск фармакологических средств для профилактики и ранней терапии нарушений, вызванных экстремальными факторами//Сб. науч. тр.-Ленинград., 1986.-С. 38-41.
- Серов В.В., Пауков B.C. Воспаление. -М., Медицина, 1995. -С. 39-170.
- Тринус Ф.П., Клебанов Б.М., Ганджа И.М. Фармакологическая регуляция воспаления. -Киев, 1987. -С. 5-59.
- Чурашов С.В. Экспериментальное обоснование возможности интравитреального применения высокочистых перфторполиэфиров, перфторпропана и их сочетания.-Дисс. канд. мед. наук-СПб., 1998.-С. 170.
- Шамшинова A.M., Волков В.В. Функциональные методы исследования в офтальмологии. -М., Медицина, 1999. -С 415.
- Шишкин М.М. Передняя пролиферативная витреоретинопатия (патогенез, лечение, профилактика). -Дисс. докт.мед. наук. -СПб., 2000 -С. 375.
- Alfaro F, Liggett РЕ. Vitreoretinal surgery of the injured eye. -1999 -P. 225-238.
- Bonini-Filho MA, Jorge R, Barbosa JS. Intravitreal injection versus sub-tenons infusion of triamcinolone acetonide for refractory diabetic macular edema: a randomized clinical trial//Invest. Ophthalmol. Vis. Sci. -2005. -Vol. 46. -P. 3845-3849.
- Campochiaro PA, Bryan JA, Conway BP, Jaccoma EH. Intravitreal chemotactic and mitigenic activity: implication of blood-retinal barrier breakdown//Arch. Ophthalmol. -1986. -Vol. 104. -P. 1685-1687.
- Challa JK, Gilies MC, Penfold PL, et al. Exudative macular degeneration and triamcinolone. 18 month follow up//Aust. NZ J. Ophthalmol. -1998. -№ 26. -P. 277-288.
- Charles S, Katz A, Wood B. Vitreous microsurgery. -2002. -P. 150-243.
- Choi YJ, Oh IK, Oh JR, Huh K. Intravitreal versus posterior subtenon injection of triancinolone acetonide for diabetic macular edema//Korean J. Ophthlmol. -2006. -Vol.20, №4.-P.205-209.
- Danis RP, Ciulla ТА, Pratt LM, et al. Intravitreal triamcinolone acetonide in exuda tive age-related macular degeneration//Retina. -2000. -№ 20. -P. 244-250.
- Inoue M, Takeda K, Morita K, Yamada M, Tanigawara Y. Vitreous concentrations of triamcinolone accetonide in human eyes after intravitreal or subtenon injection//Am. J. Ophthalmol. -2004. -Vol. 138, № 6. -P. 1046-1048.
- Jager RD, Aiello LP, Patel SC, et al. Riscs of intravitreous injection: a comprehensive review//Retina. -2004. -№ 24. -P. 676-698.
- Jonas JB, Kreissig I, Degenring RF. Intravitreal triamcinolone acetonide for pseudophakic cystoid macular edema//Am. J. Ophthalmol. -2003. -№. 136. -P. 384-386.
- Jonas JB, Kreissig I, Hugger P, et al. Intravitreal triamcinolone acetonide for exudative age related macular degeneration//Br. J. Ophthalmol. -2003. -№ 87. -P. 462-468.
- Machemer R. Treatment of intraocular proliferarions with intravitreal steroids//Trans. Am. Ophthalmol. Soc. -1979. -Vol. 77. -P. 171-180.
- Martidis A, Duker LS, Greenberg PB, et al. Intravitreal triamcinilone for refracrory diabetic macular edema//Ophthalmology. -2002 -№. 109. -P. 920-927.
- McCuen BW, Bessler M, Tano Y. The lask of toxicity of intravitreally administrated triamcinolone acetonide//Am. J. Ophthalmol. -1981. -Vol. 91, №6. -P. 785-788.
- Tano Y, Chandler D, Machemer R. Treatment of intraocular proliferation with intravitreal injection of triamcinolone acetonide//Am. J. Ophthalmol. -1980. -№.90. -P. 810-816.
- Yeung CK, Kwok PC, Chiang WY, Pang CP. The Toxic and Stress Responses of Cultured Human Retinal Pigment Epithelium (ARPE19) and Human Glial Cells (SVG) in the Presence of Triamcinolone//Invest. Ophthalmol. Vis. Sci. -2003. -Vol. 44. -P. 5293-5300.


