Экспрессия активной формы каспазы-3 не является достоверным показателем индукции апоптоза в стимулированных CD4+ Т-лимфоцитах
Автор: Сайдакова Евгения Владимировна, Власова Виолетта Викторовна
Журнал: Вестник Пермского университета. Серия: Биология @vestnik-psu-bio
Рубрика: Иммунология
Статья в выпуске: 3, 2019 года.
Бесплатный доступ
Цель настоящей работы - анализ экспрессии активной формы каспазы-3 в стимулированных CD4+ Т-лимфоцитах и сопоставление ее с другими широко используемыми маркерами апоптоза и активности CD4+ Т-клеток. В процессе исследований мононуклеарные клетки периферической крови человека стимулировали анти-CD3/анти-CD28 антителами в течение 48 ч. и определяли экспрессию активной формы каспазы-3, маркеров активации (CD25), пролиферации (Ki-67) и апоптоза (PO-PRO/PI и AnnexinV/PI) методом проточной цитометрии. Было установлено, что под влиянием стимулятора доля каспаза-3-позитивных лимфоцитов среди CD4+CD45RA- Т-клеток увеличилась в 5.7 раз (P 0.05). Относительное количество клеток, экспрессирующих активную форму каспазы-3, было связано с параметрами активации (R = 0.878; P 0.05). Исходя из полученных данных можно заключить, что использование активной формы каспазы-3 в качестве единственного маркера при исследовании апоптоза стимулированных CD4+ Т-лимфоцитов приводит к ложноположительным результатам, во многом отражающим активацию клеток. Для получения достоверных данных требуется введение дополнительных параметров, учитывающих как индукцию программируемой клеточной гибели, так и активность лимфоцитов.
Cd4+ т-лимфоциты, апоптоз, каспаза-3, проницаемость цитоплазматической мембраны, асимметрия цитоплазматической мембраны, активация, проточная цитометрия
Короткий адрес: https://sciup.org/147227098
IDR: 147227098 | УДК: 612.086 | DOI: 10.17072/1994-9952-2019-3-353-358
Expression of active caspase-3 is not a reliable apoptosis marker in stimulated CD4+ T-cells
One of the common methods for flow cytometry apoptosis detection is the intracellular active caspase-3 analysis. Still, in stimulated CD4+ T-cells this molecule expression may not be a sign of the guaranteed cell death. The aim of the present work was to analyze the active caspase-3 expression in stimulated CD4+ T-lymphocytes and to compare it with other widely used apoptosis and activity markers of CD4+ T-cells. We stimulated human peripheral blood mononuclear cells with anti-CD3/anti-CD28 antibodies for 48 hours and studied the expression of active caspase-3, activation (CD25), proliferation (Ki-67), and apoptosis (PO-PRO/PI and AnnexinV/PI) markers with flow cytometry. We found that under stimulation, the proportion of caspase-3-positive lymphocytes among CD4+CD45RA- T-cells increased by 5.7 times (P0.05). The relative number of cells expressing active caspase-3 was associated with activation (R=0.878; P0.05). Based on the data obtained, we conclude that the use of active caspase3 as the only marker to study apoptosis of stimulated CD4+ T-lymphocytes leads to false-positive results that mainly reflect cell activation. Reliable data requires the introduction of additional parameters that take into account both the induction of programmed cell death and lymphocyte activity.
Текст научной статьи Экспрессия активной формы каспазы-3 не является достоверным показателем индукции апоптоза в стимулированных CD4+ Т-лимфоцитах
кологических заболеваний [Carson, Ribeiro, 1993; O'Reilly, Strasser, 1999; Lowe, Lin, 2000]. Важная роль в регуляции апоптоза принадлежит ферменту «каспаза-3», который расщепляет ядерную ламину, зоны фокальных и межклеточных контактов, участвует во фрагментации ДНК [Brancolini et al., 1997; Janicke et al., 1998; Kook et al., 2003]. Появление в клетке активной формы каспазы-3 принято считать «точкой невозврата» в индукции апоптоза [Fan et al . , 2017]. Эта молекула используется как маркер для определения умирающих клеток в работах, направленных на изучение лейкемии, радиочувствительности, безопасности медицинских процедур и т.д. [Belloc et al., 2000; Carracedo et al., 2002; Santos et al., 2017]. Однако вопрос о том, является ли экспрессия активной формы каспазы-3 предвестником верной гибели стимулированных CD4+ Т-лимфоцитов, остается открытым.
Цель настоящей работы – проанализировать экспрессию активной формы касазы-3 в стимулированных CD4+ Т-лимфоцитах и сопоставить ее с другими широко используемыми маркерами апоптоза и активности CD4+ Т-клеток.
Материалы и методы исследований
Получение биологического материала
План работы был утвержден локальным этическим комитетом Пермского краевого центра по профилактике и борьбе со СПИД и инфекционными заболеваниями. Каждый участник исследования подписал информированное согласие.
Забор крови осуществляли натощак из локтевой вены в пробирки, содержащие этилендиаминтет-рауксусную кислоту. Мононуклеарные клетки периферической крови изолировали путем центрифугирования (400 g, 40 мин.) в градиенте плотности Диаколла ρ=1.077 (Диа-М, Россия). Полученные образцы подвергали контролируемому замораживанию до -80 ° С в течение суток в среде, содержащей 90% инактивированной теплом эмбриональной телячьей сыворотки (Gibco, США) и 10% диметилсульфоксида (MP Biochemicals, США), после чего клетки переносили в жидкий азот для длительного хранения.
Постановка культур
Мононуклеарные клетки периферической крови размораживали и использовали для постановки культур. В образец клеток в соотношении 2:1 вносили ан-ти-CD3 и анти-CD28 антитела, конъюгированные с магнитными бусами (Gibco, США). В качестве контроля были использованы мононуклеарные клетки без добавления митогена. Образцы культивировали в иммунологических 96-луночных круглодонных планшетах (МиниМед, Россия) в полной питательной среде при +37 ° С в течение 48 ч.
Цитометрический анализ
Разделение мононуклеарных клеток периферической крови на субпопуляции выполняли с помощью коммерческих антител к поверхностным антигенам CD4 и CD45RA (BioLegend, США). Т-лимфоциты с фенотипом CD4+CD45RA– оценивали в качестве клеток памяти [Akbar et al . , 1988].
При исследовании апоптоза Т-лимфоцитов выявляли ряд параметров:
-
1) активацию сигнальных путей апоптоза устанавливали по связыванию моноклональных антител, специфичных к активной форме каспазы-3 (BD Bioscience, США);
-
2) проницаемость клеточной мембраны детектировали, окрашивая клетки PO-PRO (Thermo Fisher Scientific, США) и йодистым пропидием (Thermo Fisher Scientific, США);
-
3) нарушение асимметрии клеточной мембраны исследовали, добавляя к лимфоцитам AnnexinV, конъюгированный с флуоресцентным красителем (Beckman Coulter, США).
В качестве умирающих путем апоптоза рассматривали клетки с фенотипами: Caspase-3+, PO-PRO+PI+ или AnnexinV+PI+. Делящиеся клетки оценивали при помощи анти-Ki-67 антител (BD Pharmingen, США). Активированные Т-лимфоциты определяли по связыванию анти-CD25 антител (BioLegend, США). Также к активированным причисляли клетки с фенотипами PO-PRO+PI– или AnnexinV+PI–.
Цитометрический анализ проводили на приборе CytoFLEX S (Beckman Coulter, США). Для визуализации и обработки результатов использовали программу CytExpert (Beckman Coulter, США).
Статистическая обработка данных
Статистическая обработка результатов выполнялась методами непараметрического анализа. Рассчитывали медиану и интерквартильный размах (25–75%). Сравнение величин проводили с использованием U-критерия Манна-Уитни. Корреляционный анализ выполняли по методу Спирмена. Вычисления и построение графиков проводили с использованием пакета компьютерных программ Stata 11.1.
Результаты и их обсуждение
В исследование были включены 10 относительно здоровых добровольных доноров крови; в основном женщины (70%). Средний возраст обследованных составил 33.6 года.
Двое суток инкубации мононуклеарных клеток со стимулирующим агентом привели к увеличению доли CD4+CD45RA– Т-лимфоцитов, экспрессирующих активную форму каспазы-3 (рис. 1).
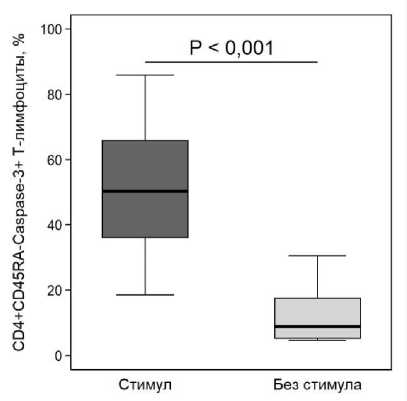
Рис. 1 . Процентное содержание каспаза-3+ клеток.
Мононуклеарные клетки выделяли из периферии-ческой крови здоровых людей (n = 10) и инкубировали 48 ч. с добавлением анти-CD3/анти-CD28 антител (стимул) или без них (без стимула). Различия между группами устанавливали с использованием U-критерия Манна-Уитни ражающих увеличенную проницаемость и нарушенную асимметрию клеточной мембраны, были статистически значимо связаны между собой (рис. 2).
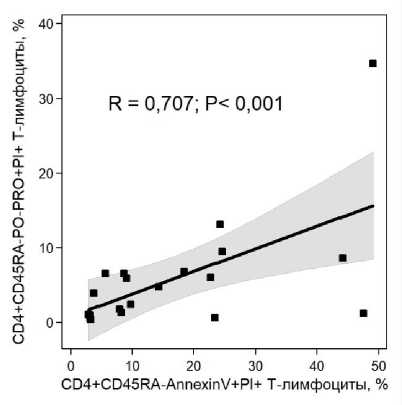
Рис. 2 . Различные подходы к определению апоптоза дают схожие результаты.
R – коэффициент ранговой корреляции Спирмена
Параллельно с анализом экспрессии активной формы каспазы-3 нами были определены другие маркеры апоптоза CD4+ Т-лимфоцитов: увеличение проницаемости и нарушение асимметрии клеточной мембраны. При их использовании было установлено, что 48 ч. инкубации со стимулирующим агентом не приводят к увеличению количества CD4+ Т-клеток памяти, умирающих путем апоптоза (таблица).
Относительное количествоCD4+ Т-клеток памяти, умирающих путем апоптоза
|
Показатели |
Стимул |
Без стимула |
|
PO-PRO+PI+, % |
9.0 (1.3–24.8) P > 0.05 |
6.4 (2.1–11.7) |
|
AnnexinV+PI+, % |
20.6 (6.7–24.4) P > 0.05 |
8.7 (3.6–21.8) |
Примечание. Указаны медианы и интерквартильные размахи. Мононуклеарные клетки выделяли из периферической крови здоровых людей и инкубировали 48 ч. с добавлением анти-CD3/анти-CD28 антител (стимул) или без них (без стимула). Лимфоциты с фенотипом CD4 + CD45RA – окрашивали наборами красителей, отражающих индукцию апоптоза. Статистический анализ – U-критерий Манна-Уитни.
Корреляционный анализ продемонстрировал отсутствие статистически значимых связей между процентным содержанием CD4+CD45RA–Caspase-3+ и CD4+CD45RA–PO-PRO+PI+ Т-клеток ( P> 0.05). Корреляции между относительными количествами CD4+CD45RA–Caspase-3+ и CD4+CD45RA– AnnexinV+PI+ Т-лимфоцитов также выявлено не было (P > 0.05). Вместе с тем, доли умирающих клеток, определенные при помощи красителей, от-
В отсутствие связей с показателями апоптоза, экспрессия каспазы-3 оказалась ассоциирована с индексами активности стимулированных CD4+ Т-клеток. Так, процентное содержание Т-клеток памяти, несущих активную форму каспазы-3, коррелировало с долей активированных (CD25+) Т-лимфоцитов (рис. 3). Важно отметить, что другие показатели апоптоза не имели статистически значимых корреляционных зависимостей с содержанием CD4+CD25+ Т-клеток памяти.
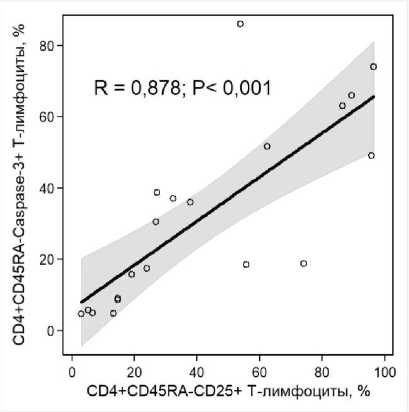
Рис. 3 . Связь процентного содержания каспаза-3+ и активированных CD4+ Т-клеток памяти.
R – коэффициент ранговой корреляции Спирмена
Также относительное количество каспаза-3-поззитивных CD4+ Т-клеток памяти было статистически значимо связано с долей делящихся (Ki-67+) CD4+ Т-лимфоцитов (рис. 4). При использова- нии других маркеров программируемой гибели клеток схожих корреляционных зависимостей обнаружено не было (P > 0.05).
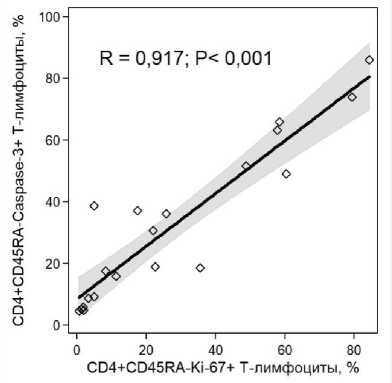
Рис. 4 . Связь экспрессии активной формы каспазы-3 и пролиферации CD4+ Т-клеток памяти.
R – коэффициент ранговой корреляции Спирмена
В свою очередь, число каспаза-3-содержащих Т-клеток памяти было ассоциировано с долей CD4+CD45RA–AnnexinV+PI– Т-клеток (рис. 5) и процентным содержанием CD4+CD45RA–PO-PRO+PI– Т-лимфоцитов (рис. 6). Важно отметить, что относительное количество активированных (CD25+) Т-клеток памяти также было статистически значимо связано как с долей PO-PRO+PI– Т-лимфоцитов (R = 0.684; P < 0.001), так и с процентным содержанием AnnexinV+PI– Т-клеток (R = 0.893; P < 0.001).
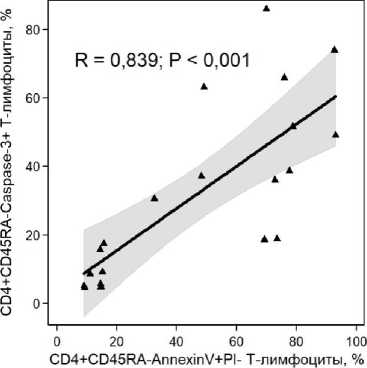
Рис. 5 . Связь экспрессии активной формы каспазы-3 и нарушения асимметрии мембраны жизнеспособных CD4+ Т-клеток памяти.
R – коэффициент ранговой корреляции Спирмена
Таким образом, в результате проведенных исследований нами было установлено, что при стимуляции клеток через Т-клеточный рецептор в жизнеспособных CD4+ Т-лимфоцитах памяти пе- риферической крови человека индуцируется экспрессия активной формы каспазы-3. Число каспа-за-3-позитивных CD4+CD45RA– Т-клеток ассоциировано с показателями активации (CD25+, PO-PRO+PI–, AnnexinV+PI–) и пролиферации (Ki-67+) Т-лимфоцитов, но не коррелирует с показателями апоптоза (PO-PRO+PI+, AnnexinV+PI+) этих клеток.
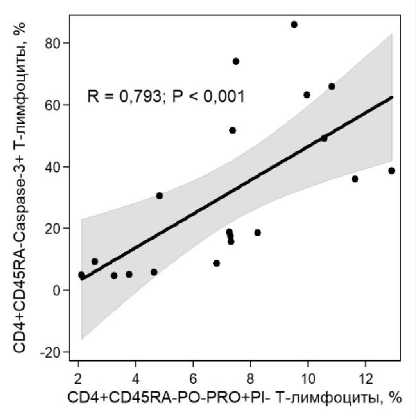
Рис. 6 . Связь экспрессии активной формы каспазы-3 и проницаемости мембраны жизнеспособных CD4+ Т-клеток памяти.
R – коэффициент ранговой корреляции Спирмена
Каспаза-3 относится к числу эффекторных цистеиновых протеаз. Её функции напрямую связаны с развитием характерной для апоптоза морфологии клетки [Alnemri, 1997], но не ограничиваются индукцией программируемой гибели. Так, она вовлечена в дифференцировку скелетной мускулатуры [Fernando et al., 2002], деление В-лимфоцитов [Woo et al., 2003] и созревание эритроцитов [Lamkanfi et al . , 2007]. В Т-лимфоцитах каспаза-3 необходима для запуска активных фаз клеточного цикла [Alam et al., 1999; Kennedy et al . , 1999], а ее ингибирование приводит к дефекту пролиферации стимулированных наивных Т-клеток [Alam et al . , 1999]. Также известно, что в жизнеспособных активированных Т-клетках каспаза-3 сохраняет способность расщеплять свои физиологические субстраты (PARP, ядерная ламина), хотя в присутствие интерлейкина-2 наличие активной формы каспазы-3 не приводит к расщеплению ДНК [Wilhelm, Wagner, Hacker, 1998]. Вероятно, в сигнальном пути апоптоза существуют контрольные точки, предотвращающие гибель клетки вопреки действию каспазы-3. Механизмы регуляции активности каспазы-3 в жизнеспособных клетках на сегодняшний день остаются неизвестными.
Заключение
Согласно полученным нами данным, экспрессия активной формы каспазы-3 плотно связана с активацией и пролиферацией CD4+CD45RA– Т-клеток. Поэтому ее использование в качестве единственного маркера при исследовании апоптоза стимулированных CD4+ Т-лимфоцитов может приводить к получению ложноположительных результатов. Комбинирование с другими параметрами, отражающими индукцию программируемой клеточной гибели и активность лимфоцитов, может облегчить интерпретацию получаемых данных и увеличить достоверность выводов.
Список литературы Экспрессия активной формы каспазы-3 не является достоверным показателем индукции апоптоза в стимулированных CD4+ Т-лимфоцитах
- Akbar A.N. et al. Loss of CD45R and gain of UCHL1 reactivity is a feature of primed T cells // J. Immunol. 1988. Vol. 140. P. 2171-2178.
- Alam A. et al. Early activation of caspases during T lymphocyte stimulation results in selective substrate cleavage in nonapoptotic cells // J. Exp. Med. 1999. Vol. 190. P. 1879-1890.
- Alnemri E.S. Mammalian cell death proteases: a family of highly conserved aspartate specific cysteine proteases // J. Cell Biochem. 1997. Vol. 64. P. 33-42.
- Belloc F. et al. Flow Cytometry detection of caspase 3 activation in preapoptotic leukemic cells // Cytometry. 2000. Vol. 40. P. 151-160.
- Brancolini C. et al. Dismantling cell-cell contacts during apoptosis is coupled to a caspase-dependent proteolytic cleavage of beta-catenin // J. Cell Biol. 1997. Vol. 139. P. 759-771.
- Carracedo J. et al. Caspase-3-dependent pathway mediates apoptosis of human mononuclear cells induced by cellulosic haemodialysis membranes // Nephrol. Dial. Transplant. 2002. Vol. 17. P. 1971-1977.
- Carson D.A., Ribeiro J.M. Apoptosis and disease // The Lancet. 1993. Vol. 341. P. 1251-1254.
- Fan J. et al. Circulating Peptidome and Tumor-Resident Proteolysis // Enzymes. 2017. Vol. 42. P. 1-25.
- Fernando P. et al. Caspase 3 activity is required for skeletal muscle differentiation // Proc. Natl. Acad. Sci. USA. 2002. Vol. 99. P. 11025-11030.
- Janicke R.U. et al. Caspase-3 is required for DNA fragmentation and morphological changes associated with apoptosis // J. Biol. Chem. 1998. Vol. 273. P. 9357-9360.
- Kennedy N.J. et al. Caspase activation is required for T cell proliferation // J. Exp. Med. 1999. Vol. 190. P. 1891-1896.
- Kook S. et al. Caspase-dependent cleavage of tensin induces disruption of actin cytoskeleton during apoptosis // Biochemical and Biophysical Research Communications. 2003. Vol. 303. P. 37-45.
- Lamkanfi M. et al. Caspases in cell survival, proliferation and differentiation // Cell Death. Differ. 2007. Vol. 14. P. 44-55.
- Lowe S.W., Lin A.W. Apoptosis in cancer // Carcinogenesis. 2000. Vol. 21. P. 485-495.
- O'Reilly L.A., Strasser A. Apoptosis and autoimmune disease // Inflamm. Res. 1999. Vol. 48. P. 5-21.
- Santos N.F.G.D. et al. Active caspase-3 expression levels as bioindicator of individual radiosensitivity // An. Acad. Bras. Cienc. 2017. Vol. 89. P. 649-659.
- Vaux D.L., Strasser A. The molecular biology of apoptosis // Proc. Natl. Acad. Sci. USA. 1996. Vol. 93. P. 2239-2244.
- Wilhelm S., Wagner H., Hacker G. Activation of caspase-3-like enzymes in non-apoptotic T cells // Eur. J. Immunol. 1998. Vol. 28. P. 891-900.
- Woo M. et al. Caspase-3 regulates cell cycle in B cells: a consequence of substrate specificity // Nat. Immunol. 2003. Vol. 4. P. 1016-1022.


