Экспрессия гена BRCA1 при нейроэндокринных опухолях желудочно-кишечного тракта
Автор: Гафтон И.Г., Имянитов Е.Н., Семиглазов В.В., Мацко Д.Е., Гафтон Г.И., Семилетова Ю.В., Иевлева А.Г., Михнин А.Е., Лемехов В.Г.
Журнал: Сибирский онкологический журнал @siboncoj
Рубрика: Клинические исследования
Статья в выпуске: 4 (64), 2014 года.
Бесплатный доступ
Представлены результаты молекулярно-генетического исследования экспрессии гена BRCA1 у больных нейроэндокринными опухолями желудочно-кишечного тракта. Исходя из анализа результатов выживаемости больных НЭО в зависимости от уровня экспрессии BRCA1, можно предположить о возможности использования данного показателя как в качестве прогностического критерия, так и в качестве фактора, определяющего целесообразность назначения препаратов платины. Чем агрессивнее нейроэндокринные опухоли, тем ниже экспрессия гена BRCA1, тем менее целесообразно назначение платиносодержащих схем химиотерапии.
Нейроэндокринные опухоли, экспрессия brca1, лечение
Короткий адрес: https://sciup.org/14056441
IDR: 14056441 | УДК: 616.33/34-006-08:575.113:577.21
BRCA1 gene expression in endocrine tumors of the gastrointestinal tract
Results of molecular genetic study of BRCA1gene expression in patients with endocrine tumors of the gastrointestinal tract were presented. Based on the analysis of survival rates in patients with endocrine tumors of the gastrointestinal tract, the BRCA1expression level was suggested can be used as a prognostic criterion and as a factor determining the advisability of administration of platinum-based drugs. It was found that the more aggressive neuroendocrine tumors had the lower BRCA1expression. Therefore, administration of platinum-containing chemotherapy is unlikely to offer any benefit for these patients.
Текст научной статьи Экспрессия гена BRCA1 при нейроэндокринных опухолях желудочно-кишечного тракта
Нейроэндокринные опухоли (НЭО) представляют собой гетерогенную группу новообразований, исходящих из нейроэндокринных клеток, которые локализуются в различных органах и тканях человека. Развитие новых лабораторных технологий значительно упростило идентификацию нейроэндокринных клеток. Решающее значение в диагностике НЭО имеет иммуногистохимическое исследование. Одним из наиболее характерных маркеров нейроэндокринных компонентов является маркер специфических эндокринных гранул – хромогранин А [2, 3, 6, 9]. Другим универсальным антигеном опухолей данной группы является маркер молекул нейроадгезии – рецептор CD56
-
[4] . Патогенез нейроэндокринных опухолей, как и других карцином, сопряжён с накоплением соматических мутаций в онкогенах и антионкогенах. Многие характерные для карцином нарушения, в частности делеции участков хромосом («потери гетерозиготности»), метилирование регуляторных областей генома, аномалии экспрессии генов, обнаруживаются и в новообразованиях нейроэндокринного происхождения, однако в последнем случае подавляющая часть известных на сегодняшний день геномных дефектов не проявляет какой-либо специфичности [7].
Определение мутации и уровня экспрессии гена BRCA1 активно используется при лечении рака молочной железы (РМЖ) и рака яичников (РЯ), определяя прогноз заболевания и эффективность терапии. При наличии генетического дефекта в одном из генов наследственного рака BRCA1, BRCA2 или PALB2 опухоли обычно демонстрируют высокую чувствительность к BRCA-специфическим препаратам производным платины, ингибиторам PARP, митомицину и т.д. [8]. Высокая прогностическая значимость наличия мутации BRCA1 при РМЖ и РЯ заставляет многих ученых искать новые мишени в широком спектре онкологических нозологий.
В лечении НЭО хирургический подход продолжает занимать ведущие позиции даже при генерализованных формах заболевания. Отдаленные показатели общей выживаемости при системной терапии этой группы больных остаются неудовлетворительными. Современные подходы к молекулярной диагностике и таргетной терапии позволяют обнаружить потенциально уязвимые мутации и подобрать эффективное лечение хотя бы для небольшой части онкологических пациентов с НЭО. Кроме того, открывшиеся возможности таргетной терапии дали новую ветвь в клинических исследованиях. Её превалирующее значение состоит в селективном воздействии на опухоль без повреждения здоровых клеток.
Возможно, что новые препараты окажутся эффективными для терапии нейроэндокринных опухолей за счет использования их биологических особенностей (выраженная васкуляризация, наличие рецепторов соматостатина и других пептидов, рецепторы тирозинкиназы). Целесообразно проведение клинических исследований для оценки как новых, так и уже известных мутаций и показателей экспрессии генов с целью определения прогноза заболевания и улучшения показателей эффективности лекарственной терапии.
Целью исследования являются выявление прогностически значимых мутаций у больных нейроэндокринными опухолями желудочно-кишечного тракта и оптимизация лечения данной группы пациентов.
Материал и методы
В исследование включено 58 больных с гистологически верифицированным нейроэндокринным раком желудочно-кишечного тракта рТ 1–4 N 0–3 M 0 стадии, радикально оперированных с января 1994 г. по декабрь 2013 г. в клинике ФГБУ «НИИ онкологии им. Н.Н. Петрова». Сведения о пациентах были получены из историй болезни, амбулаторных карт, гистологических заключений, стандартных протоколов исследования операционного материала. Минимальный период наблюдения составил 5 мес, максимальный – 18 лет. Отдаленные результаты наблюдения собраны по всем пациентам. При их анализе удалось установить, что 18 (31,0 %) больных умерли от основного заболевания. У 34 (58,6 %) пациентов выявлен рецидив заболевания в различные сроки наблюдения. При скрининге гистологического материала, полученного от 33 пациентов, на предмет наличия в опухоли уязвимых мутаций были выявлены следующие особенности: транслокаций EML4-ALK и делеций в 19 экзоне гена EGFR выявлено не было. Однако при последующем анализе была выявлена низкая экспрессия BRCA1 у 2 (6,1 %) из 33 (100,0 %) пациентов (таблица).
Делеции в 19 экзоне гена EGFR детектировали путем ПЦР-амплификации всей последовательности экзона при помощи прямого 5’-CTGTCATAGGGACTCTGGAT-3’ и обратного 5’-CAGCAAAGCAGAAACTCACAT-3’праймеров. Детекция транслокаций EML4-ALK осуществлялась путем ПЦР-амплификации 5 наиболее частых типов транслокаций ((EML4ex13/ALKex20, V.1; EML4ex20/ALKex20, V.2; EML4ex6/ALKex20, V.3; EML4ex18/ALKex20; EML4ex2/ALKex20) с помощью специфических праймеров. Последовательности кДНК гена-мишени BRCA1 и гена-рефери (SDHA) амплифицировали при помощи специфических праймеров в присутствии TaqMan-зондов.
Таблица
|
Экспрессия гена BRCA |
Женщины (n=20) |
Мужчины (n=13) |
|
До 0 |
3 (15,0 %) |
5 (38,5 %) |
|
0–2 |
8 (40,0 %) |
4 (30,8 %) |
|
2–4 |
8 (40,0 %) |
3 (23,1 %) |
|
4–7,4 |
1 (5,0 %) |
1 (7,7 %) |
Показатели экспрессии гена BRCA1 в зависимости от пола больных
Статистическая обработка полученных результатов проводилась с использованием принятых методов параметрической и непараметрической статистики. Вычисляли средние показатели и стандартные ошибки относительных величин. Статистическая значимость различий сравниваемых групп оценивалась с помощью критериев Пирсона и точных методов Фишера [1].
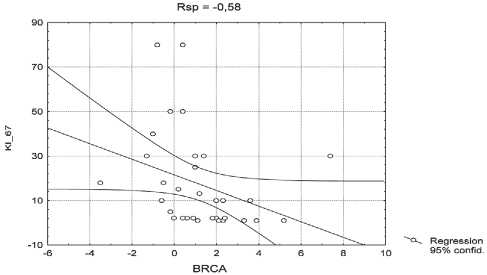
Рис. 1. Взаимосвязь показателей экспрессии BRCA1 с Ki67
Результаты и обсуждение
Для выявления взаимосвязей уровня экспрессии гена BRCA1 с исследуемыми показателями мы использовали коэффициент корреляции Спирмена (Rsp), который может принимать значения от –1 до +1. При этом отрицательный коэффициент корреляции позволяет принять гипотезу о наличии монотонной отрицательной связи, т.е. увеличение значения одной переменной ведет к уменьшению значения коррелирующей с ней переменной. Как следует из рис. 1, при исследовании взаимосвязи критерия Кi67 и уровня экспрессии BRCA 1 выявлена отрицательная монотонная связь, т.е. чем меньше показатель Ki67, тем выше экспрессия BRCA1 (Rsp –0,58), что также является статистически значимым показателем р=0,000362.
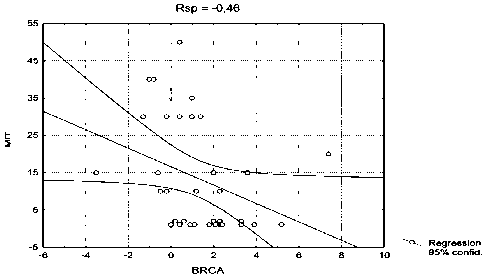
Рис. 2. Взаимосвязь показателей экспрессии BRCA1 с митотической активностью нейроэндокринных опухолей
Аналогичная картина наблюдается при исследовании митотической активности в нейроэндокринных опухолях в зависимости от показателей экспрессии BRCA1 (рис. 2), чем меньше показатель митотической активности, тем выше экспрессия BRCA1 (Rsp – 0,46), что также является статистически значимым показателем (р=0,006764). Диапазон показателей экспрессии BRCA1 статистически значимо (p=0,039) коррелирует со степенью дифференцировки НЭО, в среднем составляя при G1 – 2,1, тогда как при G2 и G3 – 0,4 (рис. 3). Таким образом, обобщая вышеописанные данные, можно утверждать, что чем агрессивнее нейроэндокринные опухоли, тем ниже экспрессия гена BRCA1 .
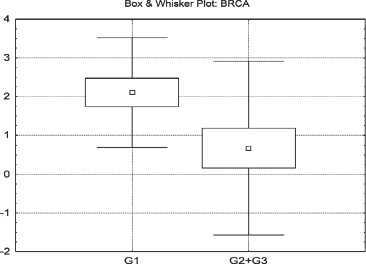
Степень дифференцировки
Рис. 3. Взаимосвязь показателей экспрессии BRCA1 со степенью дифференцировки нейроэндокринных опухолей
Так как BRCA-ассоциированные опухоли развиваются за счет дефекта системы репарации двухцепочечных разрывов и межнитевых сшивок ДНК, то терапия агентами, вызывающими подобные повреждения генома (препараты платины, митомицин С), может оказаться высокоэффективной. Положительный эффект такого лечения был показан в основном для наследственного РМЖ и РЯ [5]. В нашем случае у 6,1 % пациентов можно предположить эффективность назначения данной группы препаратов. При дополнительном анализе показателей экспрессии в зависимости от пола пациента статистически значимых изменений не выявлено, р=0,12 (рис. 4).
Для выявления взаимосвязей показателей экс-
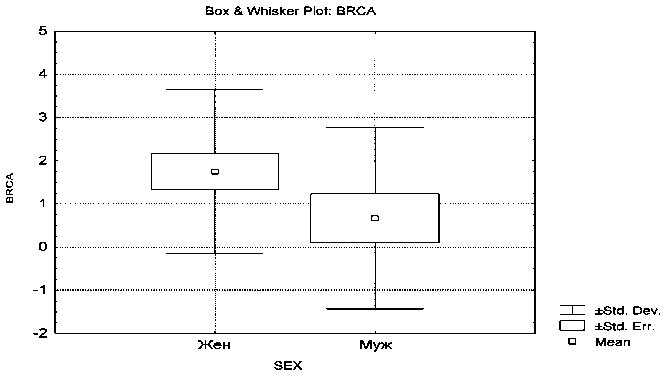
Рис. 4. Зависимость показателей экспрессии BRCA1 от пола пациентов с нейроэндокринными опухолями желудочно-кишечного тракта
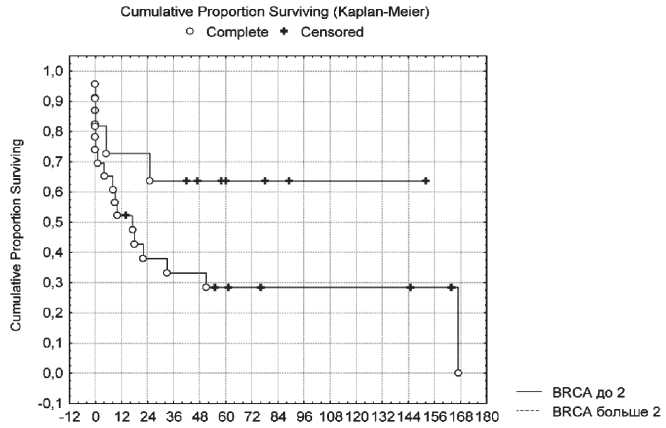
Безрецидивный период (мес.)
Рис. 5. Показатели безрецидивной выживаемости больных с нейроэндокринными опухолями желудочно-кишечного тракта в зависимости от уровня экспрессии BRCA1 (p<0,05)
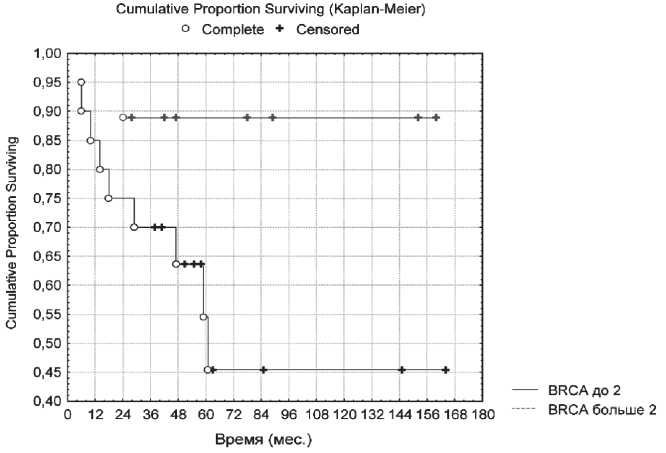
Рис. 6. Показатели общей выживаемости больных с нейроэндокринными опухолями желудочно-кишечного тракта в зависимости от уровня экспрессии BRCA1 (р=0,12)
прессии BRCA1 с исследуемыми критериями мы не могли применить традиционное значение BRCA1=4, так как с такими значениями наблюдали всего 2 пациентов. По этой причине мы воспользовались статистическими характеристиками нашей выборки по уровню экспрессии BRCA1 и реализовали 2 варианта анализа:
-
1) делением показателей BRCA1 по медиане;
-
2) делением показателей BRCA1 по тертилям.
Взаимосвязи уровня экспрессии BRCA1 удалось выявить при выделении подгруппы по верхней тер-тили, равной 2. Наблюдается статистически значимое (р<0,05) увеличение показателей безрецидивной выживаемости при уровне экспрессии BRCA1 выше значения 2,0 по сравнению со значением BRCA1 менее 2,0 (рис. 5). Медиана одногодичной безре-цидивной выживаемости при уровне экспрессии BRCA1 выше 2,0 составляет 52 %, пятилетней – 28 %, тогда как при экспрессии BRCA1 менее 2,0 медиана одногодичной безрецидивной выживаемости пациентов с НЭО составила 72 %, пятилетней – 62 %. При анализе показателей общей выживаемости (ОВ) установлено, что у больных с экспрессией BRCA1 выше 2,0 наблюдается тенденция (р=0,12) к увеличению уровня ОВ по сравнению с пациентами с экспрессией BRCA1 менее 2,0 (рис. 6). Исходя из результатов анализа выживаемости больных НЭО в зависимости от уровня экспрессии BRCA1 , можно предположить возможность использования данного показателя как в качестве прогностического критерия, так и в качестве фактора, определяющего целесообразность назначения препаратов платины.
Заключение
На основании полученных данных можно утверждать, что чем агрессивнее нейроэндокринные опухоли, тем ниже экспрессия гена BRCA1 . Целесообразно дальнейшее изучение эффективности препаратов платины у больных с низкой экспрессией BRCA1 .
Данная работа поддержана грантом РНФ № 14–15–00528


