Экспрессия генов CCR5 и RANTES при взаимодействии in vitro мононуклеаров периферической крови больных несовершенным остеогенезом с композитными материалами
Автор: Литвяков Николай Васильевич, Нечаев Кирилл Андреевич, Саприна Татьяна Владимировна, Дворниченко Марина Владимировна, Больбасов Евгений Николаевич, Каменчук Яна Александровна, Хлусов Игорь Альбертович
Журнал: Гений ортопедии @geniy-ortopedii
Рубрика: Оригинальные статьи
Статья в выпуске: 3, 2011 года.
Бесплатный доступ
Определение уровней экспрессии системы RANTES-CCR5 на мононуклеарах крови in vitro может, на наш взгляд, приме- няться для индивидуальной оценки перспективности материала имплантата в качестве триггера воспалительной/остео- индуктивной реакции у пациентов с несовершенным остеогенезом (НО). При этом экспрессия гена RANTES на монону- клеарах крови может оказаться эффективной в развитии методов прогнозирования степени воспалительного (остеолити- ческого) ответа, тогда как экспрессия гена CCR5 - репаративного ремоделирования костной ткани в ответ на применение различных имплантатов.
Хемокины, лейкоциты, имплантаты, композитные покрытия
Короткий адрес: https://sciup.org/142134584
IDR: 142134584 | УДК: 575.117.2:615.462:616.71-007.235-089.843
CCR5 and RANTES gene expression for interaction of peripheral blood mononuclear leukocytes in vitro and composite materials in patients with osteogenesis imperfecta
In our opinion, determination of the levels of RANTES-CCR5 system expression on blood mononuclear leucocytes in vitro can be used for individual evaluation of the perspective of implant material as inflammatory/osteoinductive reaction trigger in patients with osteogenesis imperfecta (OI). Besides, RANTES gene expression on blood mononuclear leucocytes may be effective in the development of the methods to predict the degree of inflammatory (osteolytic) response, while CCR5 gene expression - in the development of the methods to predict the process of reparative bone tissue remodeling in response to using different implants.
Текст научной статьи Экспрессия генов CCR5 и RANTES при взаимодействии in vitro мононуклеаров периферической крови больных несовершенным остеогенезом с композитными материалами
Исходами использования имплантируемых материалов являются их способности вызывать как негативную реакцию в виде гиперчувствительности, так и позитивную в виде стимуляции репаративных процессов в костной ткани.
В настоящее время достоверно установлено, что в основе негативного влияния материала лежит каскад событий, характерных для воспаления [1, 14, 20, 24], развитие которых сопровождается продукцией медиаторов, вовлечённых в патологическую резорбцию костной ткани. Показано, что эти события приводят к развитию гранулематозной реакции со стороны окружающих тканей и активации клеток к секреции цитокинов и протеолитических ферментов, выраженность и длительность выделения которых, согласно Rollins B. J. [20], является определяющей для развития патологического состояния.
Знание и понимание механизмов, приводящих к возникновению состояний, сопровождаемых пери-протезным остеолизом, позволит не только совершенствовать имплантируемые устройства, материалы и оперативную технику, но и прогнозировать индивидуальный ответ на введение того или иного материала.
Ведущая роль в этих событиях принадлежит таким полифункциональным медиаторам как простагландин Е2, интерлейкины-1α и-1β (IL-1α и IL-1β), интерлейкин-6 (IL-6), а также фактор некроза опухоли (TNF) [1, 23], обладающим полимодальными эффектами [1]. Повышение их концентрации в сыворотке крови может быть свидетельством любого специфического иммунного ответа. Индикатором специфичной реактивности к веществу имплантата [1] считают концентрацию растворимого рецептора интерлейкина-2. В связи с этим, попытки выделить наиболее специфичный маркер иммунореактивности к веществу имплантата продолжаются до настоящего времени.
Исследования in vitro показывают, что ответ культур мононуклеаров периферической крови на введение частиц вещества различается в зависимости от состава материала имплантата [6, 9, 10, 13, 23, 26]. При этом устанавливаются различные профили секреции цитокинов [26].
Ряд авторов [8, 18, 22, 26] выявил чёткую взаимосвязь между уровнями цитокинов и хемокинов (в частности, RANTES), которые, по-видимому, организованы в единую функциональную сеть.
RANTES — хемокин CC подкласса, который продуцируется эпителиальными клетками, лимфоцитами и тромбоцитами и является мощным хемоаттрактантом для моноцитов и лимфоцитов [15, 17, 18], эозинофилов [17, 18] и базофилов [17, 18], играет большую роль при различных видах иммунного ответа [19, 8].
Биологические эффекты RANTES реализуются через несколько типов рецепторов, наибольшее значение из которых имеют CCR1, CCR3, CCR4 [18] и CCR5 [19], экспрессирующиеся на клетках лимфоидного ряда, эозинофилах [11], тромбоцитах [28], тучных клетках и моноцитах, остеобластах и клетках мезенхимной линии [27].
Экспрессия рецепторов и их лиганда, как показывают исследования, может быть не только признаком определённых заболеваний, но и маркером хронизации и прогрессии воспалительного процесса [2, 4, 5, 7, 16, 20, 21]. С другой стороны, RANTES способен привлекать мезенхимные стволовые клетки в раневой очаг и способствовать репарации костной ткани, стимулировать миграцию предостеобластовк участку резорбции кости и их дифференцировку в остеобласты [27].
Специалистами в области медицинского материаловедения постоянно создаются материалы для репаративной регенерации костной ткани. Тем не менее, исследования свидетельствуют, что негативной стороной использования многих имплантируемых материалов может быть воспалительная реакция, приводящая к перипротезному остеолизу.
Главная проблема заключается в том, что в основе как негативного, так и позитивного влияния биоматериалов лежат сходные процессы, запускающие воспалительную реакцию. Актуальной, на наш взгляд, представляется попытка разграничить остеолити-ческие/остеоиндуктивные механизмы и предикторы посредством моделирования in vitro до клинического применения материала.
Целью данного исследования явилось изучение in vitro экспрессии генов RANTES и CCR5 мононуклеара-ми периферической крови у больных несовершенным остеогенезом (НО), как возможных маркеров реакции клеток на искусственные материалы.
МАТЕРИАЛЫ И МЕТОДЫ ИССЛЕДОВАНИЯ
В работе в качестве подложек для культивирования клеток применялись титановые диски диаметром 10 мм с двусторонними биоактивными покрытиями, являющимися композитом гидроксилапатита (ГАП) с природным биодеградируемым хитозаном (№ 1–2) или искусственным нерастворимым сополимером (№ 3–4). Нумерация дисков возрастала с увеличением содержания соответствующих полимеров в композитном покрытии.
Композитные покрытия ГАП с хитозаном получали электрохимическим осаждением. Хитозан (степень деацетилирования 85 %) добавлялся в концентрации 1,25 и 5 г/л в электролит, содержащий фосфаты кальция и ортофосфорную кислоту.
Композитные поверхности в соотношении компонентов 30 и 70 масс. % ГАП с сополимером поливинилиденфторида и тетрафторэтилена готовили шликерным способом. В каждой из 4-х групп исследуемых in vitro изделий тестировали по 3 диска.
Реагенты для культивирования клеток — среда RPMI-1640, L-глутамин получены от Биолот (Новосибирск, Россия), эмбриональная телячья сыворотка — от Sigma (США). Использовали реактивы, необходимые для выделения, анализа РНК и получения кДНК — сахароза, Трис-HCl, MgCl2, Тритон Х-100, агароза (Sigma, США), ДНК-аза I, коммерческие наборы для обратной транскрипции (Fermentas, Канада). Все использованные индивидуальные реагенты были категории «для молекулярной или клеточной биологии».
Периферическую кровь получали от пациента В., страдающего НО, путём пункции локтевой вены и сбора в пробирки типа «Vacuette» для выделения монону-клеаров (BD Diagnostics, США).
Мальчик В., 8 лет, с тяжелой формой заболевания, переломы появились после первого года жизни и про- исходят с периодичностью 3–4 раза в год. Клинически: отстает в росте от сверстников на 4,1 стандартных отклонения не только за счет деформаций скелета, но и в результате выявленной в 2007 году соматотропной недостаточности (стимулированная секреция СТГ в двух пробах менее 7,5 нг/мл). Получал терапию рекомбинантным гормоном роста (нордитропин). Имеются голубые склеры, dentinogenesis imperfecta, гиперметропия слабой степени, нормохромная анемия 1 степени смешанной этиологии. По классификации Sillence определили III тип НО. После серии оперативных вмешательств пациент способен передвигаться в специальных «ходунках», конечности опороспособны, исправлены грубые деформации нижних конечностей.
После центрифугирования на градиенте плотности Ficoll-Paque («Pharmacia», Швеция) (ρ = 1,077 г/см3) при 500 g в течение 10 минут клеточная масса троекратно отмывалась средой и осаждалась. Отмытые и осаждённые мононуклеары ресуспендировали в среде. Клеточность материала и его жизнеспособность определяли по стандартным методикам с использованием 0,4 % раствора трипанового синего.
Посев производили в 24-луночные планшеты (Orange scientific, Бельгия) при плотности 3∙106 клеток на лунку в среду: 85 % питательной среды RPMI-1640, 15 % эмбриональной телячьей сыворотки, L-глутамин (146 мг/100 мл). Культивирование производили в течение 52 часов как в отсутствие (контроль), так и в присутствии образцов композитных материалов. Использование крови от одного пациента позволило провести сравнительное тестирование реакции моно-нуклеаров на материалы с различными свойствами поверхности.
Далее клеточную массу собирали, лизировали буфером, содержащим 0,32 М сахарозы; 10 мМ Трис-HCl, рН 7,5; 5 мМ MgCl2; 1 % Тритон Х-100, для по- лучения цитоплазматического лизата, из которого выделяли РНК в соответствии с рекомендациями (25). Полученные препараты РНК обрабатывали ДНК-азой I. Качество выделенной РНК оценивали электрофоретически в 2,5 % агарозном геле по наличию выраженных бендов 28S и 18S рибосомальной РНК (рис. 1).
Rantes
GAPDH
CCR5
Рис. 1. Электрофореграмма препарата РНК. Видны бенды 28S и 18S и 5S рибосомальной РНК. М — маркер молекулярной массы
Дальнейшие манипуляции по получению кДНК осуществляли в соответствии с рекомендациями производителей коммерческих комплектов.
Последовательности праймеров и зондов [FAM-BHQ] (табл. 1) подбирали при помощи программы Oligo Analysis Vector NTI с использованием генетического банка данных с сайта www. ncbi. nlm. nih. gov.
Экспрессию генов CCR5 и RANTES в мононукле-арах крови оценивали с помощью метода обратнотранскриптазной ПЦР в режиме реального времени на амплификаторе RotorGene 6000 (Corbett Research, Австралия). Экспрессию CCR5 и RANTES выражали в процентах по отношению к непрерывно экспрессируемому гену фермента глицеральдегид 3-фосфат дегидрогеназы (GAPDH). Проверку чистоты ПЦР-продуктов проводили с использованием электрофореза в 2,5 % агарозном геле с бромистым этидием (рис. 2).
Маркер массы
Ьр 100
Рис. 2. Электрофореграмма продуктов ПЦР в режиме РВ генов GAPDH (91 bp) , RANTES (178 bp) и CCR5 (128 bp). М — маркер молекулярной массы
Костеобразующую способность искусственных материалов оценивали in vivo на 20 самцах мышей линии BALB/c массой 18-21 г в тесте эктопического остеогенеза. Животным подкожно вводили диски тестируемых образцов. Предварительно на диски с композитным покрытием наносили столбик костного мозга, который извлекали из бедренной кости сингенных животных. Через 1,5 месяца животных выводили из эксперимента посредством наркотизации эфиром, диски извлекали, фиксировали в формалине, декальцинировали. Парафиновые срезы тканевых пластинок, выросших на поверхности дисков, окрашивали по стандартной методике гематоксилином и эозином и подвергали гистологическому анализу. Эффективность костеобразования определяли как процент имплантатов, на которых выросла костная ткань, от общего числа тестируемых изделий данной группы.
В ходе эксперимента эктопического остеогенеза было использовано 40 дисков с покрытиями. Из этого числа впоследствии осуществлялся расчёт процента дисков с тканевыми пластинками, гистологический состав которых соответствовал грубоволокнистой костной ткани.
Для каждой выборки вычисляли среднее арифметическое, среднее квадратичное отклонение и среднюю квадратичную ошибку. Статистические различия оценивали с использованием критерия Манна-Уитни в программе Statistica 6. 0.
Таблица 1
Последовательности праймеров и зондов для ПЦР
|
Ген |
NM_ |
Праймеры и зонды |
Масса ампликона |
|
GAPDH |
NM_002046 |
F: GGAAGGTGAAGGTCGGAGT R: GCAACAATATCCACTTTACCAGA FAM CCAGGCGCCCAATACGACCA BHQ1 |
91 bp |
|
CCR5 |
NM_000579 |
F: GGGTGGAACAAGATGGATTA R: AGTGAGTAGAGCGGAGGCA FAM ATTATACATCGGAGCCCTGCCA BHQ1 |
128 bp |
|
RANTES |
NM_002985 |
F: CCCTCGCTGTCATCCTC R: TGACAAAGACGACTGCTGGGT FAM CGGACACCACACCCTGCTGCTT BHQ1 |
178 bp |
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Результаты оценки способности композитных материалов индуцировать экспрессию генов CCR5 и RANTES в мононуклеарах периферической крови у больных НО представлены на рисунке 3. Как следует из рисунка 3, все композитные материалы в значительной степени (в 2,5–7 раз) активировали экспрессию мононуклеарами гена RANTES. В целом, реакция клеток in vitro на образцы (№ 3-4) с искусственным нерастворимым сополимером выражена в большей степени по сравнению с композитным покрытием, несущим биодеградируемый хитозан (№ 1–2). Таким образом, можно предполагать, что экспрессия гена RANTES может быть маркером индивидуальной реакции клеток крови на контакт с разнообразными искусственными материалами. Это может быть использовано для прогнозирования характера и степени выраженности индуцированного воспалительного/остеолитического процесса для конкретного пациента в ответ на введение того или иного имплантата.
С другой стороны, согласно полученным данным, появляется возможность прогнозировать развитие остеоиндуктивного процесса в ответ на имплантацию искусственных материалов.
Так, схематически проиллюстрирована и показана функция RANTES в ремоделировании костной ткани. Цитокины TNF α, IL -1ß, и MIP -1α, продуцируемые клетками костного мозга или клетками предшественниками остеокластов, вызывают секрецию RANTES остеобластами. Повышенный уровень Ca2+, вышедшего из костного матрикса в период резорбции кости, способствует секреции RANTES и остеобластами, и остеокластами. RANTES стимулирует экспрессию CCR5 в остеобластах и их хемотаксис в участок резорбции кости, увеличивает их жизнеспособность [27], что может быть молекулярной основой репаративного ремоделирования костной ткани.
Повышенная экспрессия гена рецептора CCR5 в мононуклеарах периферической крови у больных
НО (см. рис. 3) отмечалась только в случае их взаимодействия in vitro с образцами № 3–4. В случаях тестирования образцов (№№ 1-2), несущих композитное покрытие ГАП с природным биодеградируемым хитозаном, показатели, напротив, уменьшались по сравнению со спонтанной экспрессией рецептора.
При дополнительном проведении теста эктопического остеогенеза на здоровых мышах было выявлено, что эффективность роста костной ткани для композитных покрытий с хитозаном (изделия № 1-2) составляла в среднем 38 % (диапазон 0-50 %, n = 16), для имплантатов, несущих композит ГАП и нерастворимого искусственного сополимера (№ 3–4) — 68 % (n = 24). При этом различия в остеоиндуктивной реакции между сравниваемыми группами покрытий достигали статистических величин.
Таким образом, результаты экспрессии in vitro гена CCR5 на мононуклеарах крови у больного НО (см. рис. 3) в ответ на введение имплантатов во многом согласуются с данными, полученными in situ при выращивании костной ткани из костного мозга мышей.
Исследование выполнено при поддержке гранта РФФИ № 09-04-99105-р_офи «Создание и внедрение экспериментальной модели на основе смешанной культуры мононуклеаров периферической крови человека со стромальными стволовыми клетками для исследования механизмов, диагностики и терапии метаболических остеопатий человека»; Федеральной целевой программы «Исследования и разработки по приоритетным направлениям развития научнотехнологического комплекса России на 2007–2013 годы» (государственный контракт № 16.512.11.2087), Аналитической ведомственной целевой программы (АВЦП) «Развитие научного потенциала высшей школы на 2009-2011 годы» (регистрационный номер проекта 2. 1. 1/14204) и гранта РФФИ № 09–04– 00287а.
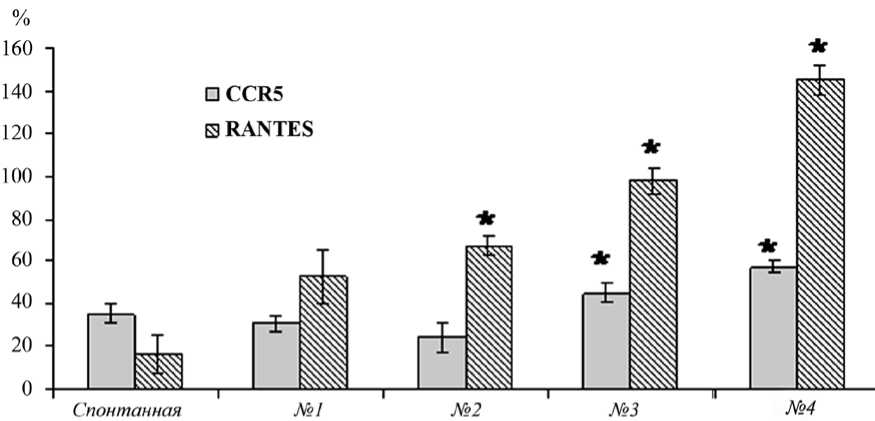
Рис. 3. Экспрессия генов CCR5 и RANTES в мононуклеарах периферической крови у больных несовершенным остеогенезом через 52 часа после инкубации с композитными материалами: по оси абсцисс — экспрессия генов CCR5 и RANTES, % по отношению к экспрессии GAPDH; по оси ординат — тестируемые образцы композитных материалов
ВЫВОДЫ
Определение уровней экспрессии системы RANTES-CCR5 на мононуклеарах крови in vitro может, на наш взгляд, применяться для индивидуальной оценки перспективности материала имплантата в качестве триггера воспалительной/остеоиндуктивной реакции у пациентов с НО.
Экспрессия гена RANTES на мононуклеарах крови может оказаться эффективной в развитии методов прогнозирования степени воспалительного (остеолитического) ответа, тогда как экспрессия гена CCR5 — репаративного ремоделирования костной ткани в ответ на применение различных имплантатов.


