Электрохимическое определение фуралтодона гидрохлорида иерархически структурированным фосфатом титана
Автор: Антон Дмитриевич Абрамян, Данил Андреевич Манько, Олег Игоревич Большаков, Вячеслав Викторович Авдин
Журнал: Вестник Южно-Уральского государственного университета. Серия: Химия @vestnik-susu-chemistry
Рубрика: Физическая химия
Статья в выпуске: 4 т.17, 2025 года.
Бесплатный доступ
В данной работе представлен синтез и исследование электрохимических свойств микросферического фосфата титана (TiP) сложного состава и иерархической структуры. Материал представляет собой микросферы фосфата титана. Он был применен в качестве высокоэффективной электроактивной добавки к угольной пасте для создания модифицированного электрода. Ключевым результатом является демонстрация превосходных электрохимических характеристик микросферического образца TiP 1/6 со средним размером ~8 мкм. Данный образец показал минимальное сопротивление переносу заряда (Rct = 12 Ом) и максимальный ток отклика (I = 1,37 мА) по сравнению с микросферами иных размеров. Это превосходство объясняется достижением оптимального баланса между двумя критически важными параметрами: составом поверхности, обеспечивающим низкое сопротивление переносу заряда, и структурой агрегированных микрочешуек, способствующей эффективной диффузии реагентов к активным центрам. Более мелкодисперсные сферы (~4 мкм), хотя и обладают минимальным диффузионным барьером (Rct = 41 Ом), уступают по сопротивлению переноса заряда. Крупные микросферы (~15 мкм, Rct = 15 Ом) имеют оптимальный состав поверхности, но их размер ограничивает диффузию. Сенсор на основе TiP 1/6 продемонстрировал выдающиеся аналитические параметры, включая низкий предел обнаружения широко применяемого антибиотика, широкий линейный рабочий диапазон и высокую селективность. Успешное тестирование сенсора на реальных образцах подтверждает его практическую применимость. Полученные результаты свидетельствуют о высоком потенциале синтезированного иерархического микросферического фосфата титана TiP 1/6 для разработки высокочувствительных и селективных электрохимических сенсоров, перспективных как для исследовательских задач, так и для коммерческого применения.
Фуралтодон гидрохлорид, электрохимическое определение, иерархически структурированный фосфат титана
Короткий адрес: https://sciup.org/147252527
IDR: 147252527 | УДК: 544.653 | DOI: 10.14529/chem250415
Electrochemical determination of furaltadone hydrochloride by hierarchically structured titanium phosphate
This work presents the synthesis and investigation of electrochemical properties of micro-spherical titanium phosphate (TiP) with complex composition and hierarchical structure. The material comprises centrically aggregated micro-sized flakes, employed as a highly efficient electroactive modifier in carbon paste electrodes. The key finding is the superior electrochemical performance of the TiP 1/6 sample (average microsphere size: ~8 μm), which exhibited the lowest charge transfer resistance (Rct = 12 Ω) and highest response current (I = 1.37 mA) among all tested microspheres. This enhancement is attributed to an optimal balance between two critical parameters: (i) surface composition ensuring low charge-transfer resis-tance, and (ii) hierarchical structure of aggregated micro-scales, facilitating efficient reagent diffusion to ac-tive sites. Smaller microspheres (~4 μm, Rct = 41 Ω) demonstrated minimal diffusion barriers, while larger ones (~15 μm, Rct = 15 Ω) displayed favorable surface composition, making TiP 1/6 sample optimized with both characteristics. The TiP 1/6-based sensor has delivered exceptional analytical performance, including a low detection limit of a widespread antibiotic, wide linear working range, and high selectivity. Successful real-sample analysis confirms its practical utility. These results highlight the significant potential of hierar-chical TiP 1/6 microspheres for developing highly sensitive and selective electrochemical sensors, suitable for both research and commercial applications.
Текст научной статьи Электрохимическое определение фуралтодона гидрохлорида иерархически структурированным фосфатом титана
Фуралтодон (ФТД) – антипротозойное антисептическое средство, относится к классу нитрофуранов [1, 2]. Он обладает антимикробным действием широкого спектра, благодаря свойствам 5-нитрофуранового кольца, используется, как кормовая добавка для стимуляции роста, а также для лечения протозойных и бактериальных инфекций [3]. Загрязнение пищевых продуктов ФТД приводит к его трансформации в химические соединения: 3-амино-5-морфолиноэтил-2-оксазолидон (АМОЗ), семикарбазид или 1-аминогидантоин. Метаболизм этих соединений крайне вреден для здоровья человека [4].
ФТД производится и используется в нескольких странах благодаря своей эффективности и низкой стоимости. Однако необходимость определения количества ФТД в пищевых продуктах на рынке крайне важна, поскольку его остатки в пище или воде обладают канцерогенными свойствами и вызывают заболевания у людей [5]. Традиционные методы анализа ФТД, такие как высокоэффективная жидкостная хроматография (ВЭЖХ), жидкостная хроматография-масс-спектрометрия (ЖХ-МС) и иммуноферментный анализ (ИФА), обладают существенными недостатками. Для определения ФТД при помощи этих методов анализа требуется: дорогостоящее оборудование, сложная пробоподготов-ка, высокая квалификация специалистов и значительные временные затраты. В связи с этим особый интерес представляют электрохимические методы анализа, сочетающие в себе: высокую чувствительность, скорость анализа, доступность и низкую стоимость [6, 7].
Электрохимические методы обладают рядом преимуществ: экономичность, стабильность, высокая чувствительность к аналитам, простота в использовании и универсальность. Поэтому электрохимические методы исследования обрели популярность в фармацевтической и экологической сферах [8]. Ключевым компонентом электрохимической аналитической системы является электроактивная добавка, которая при наложении потенциала способна селективно и эффективно преобразовывать анализируемое вещество на поверхности с отъемом электрона (анодное окисление) или с передачей электрона (катодное восстановление). Основные требования к таким материалам включают химическую стабильность, кристалличность, разветвлённую поверхность и наличие электроактивных центров участвующих в редокс-процессах.
В последнее время особый интерес вызывают так называемые иерарахически структурированные материалы, которые демонстрируют более одного уровня структурной организации. Данные материалы в отличие от регулярно-структурированных демонстрируют более высокую удельную площадь поверхности и мультимодальную пористость и, часто анизотропию свойств: электропроводящих, сорбционных и механических. Более того, строго организованные или повторяющиеся мотивы в иерархически структурированных материалах способствуют улучшению передачи электронов в продольном направлении [9, 10].
Диоксид титана с иерархической структурой может быть адаптирован для создания нового электрохимически активного материала. Чтобы проверить эту гипотезу, мы провели гидротермальную обработку прекурсоров оксида титана в присутствии различных анионов с целью анионного темплатирования, ранее успешно примененного в синтезе иерархически структурированных материалов [11, 12]. В результате были получены новые иерархические структуры, на основе фосфата титана, демонстрирующие широкую вариативность морфологии. Ранее в нашей группе была показана принципиальная возможность использования иерархически структурированного фосфата титана для электрохимического определения сулькотриона [13]. Мы решили более подробно исследовать влияние размеров иерархически структурированных микросфер фосфата титана на их электроактивность.
С целью разработки высокоэффективных сенсоров для мониторинга ФТД, исследование было направлено на создание электрохимически активных материалов на основе фосфата титана (TiP). Решаемые задачи включали: (1) контроль морфологии формируемых материалов, (2) изучение связи их морфологии синтезируемого с электрохимическими свойствами, и (3) их апробацию в виде электроактивной добавки в составе угольно-пастового электрода (УПЭ) в электрохимическом определении ФТД.
Экспериментальная частьРеагенты
DL-миндальная кислота (100 %, Bingospa), K 3 [Fe(CN) 6 ] (НеваРеактив), K 4 [Fe(CN) 6 ] (НеваРе-актив), KCl (НеваРеактив), NH 4 OH (25 %, НеваРеактив), H 2 O 2 (40 %, БиохимРеагент), порошок титана ПТМ–1, H 3 PO 4 (98 %, Вектон), угольный порошок (< 45 µм) (Sigma Aldrich), парафиновое масло, (Sigma Aldrich), использовались без предварительной очистки.
Элементный анализ и морфология поверхности образцов изучались с помощью электронного микроскопа Jeol JSM 7001F.
Фазовый состав и структура образцов изучались на порошковом дифрактометре Rigaku Optima IV. Съемка проводилась в диапазоне углов 2θ от 5 до 90° со скоростью съемки 5°/мин. В исследовании использовалось излучение медной трубки CuKα (λ = 1,541 Å) при ускоряющем напряжении 40 кВ.
Регистрацию ИК-спектров пропускания проводили на ИК-Фурье-спектрометре Shimadzu IRAffinity S1 в диапазоне от 400 до 4000 см–1 с разрешением 4 см–1 и числом повторений 40.
Элементный состав образцов анализировали методом оптико-эмиссионной спектроскопии с индуктивно-связанной плазмой (ИСП-ОЭС) с использованием спектрометра Perkin Elmer ORAS OPTIMA 7300 DV для определения концентрации титана и фосфора с использованием спектральных линий 336,121 нм (Ti) и 213,617 нм (P). Калибровочные кривые для элементов показали большую линейность (R2 = 0,9999). Перед анализом твердые образцы растворяли в 5 мл 35 % перекиси водорода (H2O2) при постепенном нагревании от 100 до 180 °С, избегая бурного кипения. После полного растворения добавляли 5 мл концентрированной серной кислоты (H 2 SO 4 ) и нагревали смесь при 150–250 °С до обесцвечивания. Затем температуру повышали до 350 °C и раствор выпаривали до появления густых паров H2SO4. После охлаждения остаток растворяли и доводили объем до метки в мерной колбе емкостью 50 мл.
Электрохимические исследования проводились на бипотенциостате CH Instruments (CHIn-strumetns, Остин, Техас, США), модель 760 b. Программное обеспечение для вольтамперометрии CHI (версия 2.03, CHInstrumetns). Использовалась трехэлектродная ячейка (общий объем 10 мл), где в качестве рабочего электрода использовался немодифицированный или модифицированный УПЭ, Ag/AgCl в качестве электрода сравнения и платиновая проволока в качестве вспомогательного электрода. Для характеристики электрода в качестве тестового раствора использовалась 5 ммоль/л смесь K 3 [Fe(CN) 6 ]/K 4 [Fe(CN) 6 ] (1:1) в 0,1 М KCl. В качестве фонового раствора использовался универсальный буферный раствор Бриттона-Робинсона (БР). Электрохимическая импедансная спектроскопия (ЭИС) регистрировалась в диапазоне частот от 10 мГц до 10 кГц. Циклическая вольтамперометрия (ЦВА) регистрировалась в диапазоне потенциалов от -0,5 В до 1,0 В со скоростью развертки 50 мВ/с. Для разработки аналитических процедур использовалась квадратно-волновая вольтамперометрия [31].
Немодифицированный угольно-пастовый электрод (УПЭ) готовили путем смешивания 80 % по весу углеродного порошка и 20 % парафинового масла в растворе. Через 30 мин смешивания образовывалась однородная углеродная паста (УП). Модифицированные электроды готовили путем добавления определенного количества синтезированных материалов к немодифици-рованной углеродной пасте. Проценты были рассчитаны как часть только графитового порошка, в то время как процент масла всегда был постоянным и составлял 20 %. После гомогенизации смеси тефлоновый корпус был заполнен углеродной пастой, а поверхность электрода была очищена бумагой и использовалась без дополнительной очистки [31,32].
Раствор искусственной мочи для исследования реальных образцов был приготовлен из смеси мочевины 8 г/л, NaCl 7,5 г/л, KCl 4,5 г/л и Na 3 PO 4 4,5 г/л.
Синтез Ti-комплекса с DL-миндальной кислотой
Согласно ранее опубликованной методике [14]. 0,41 г (8,5 ммоль) порошка титана диспергировали в 5 мл NH 4 OH (25 %), затем добавляли 40 мл перекиси водорода (37 %) для растворения металла, контролируя температуру смеси в диапазоне 5–10 °C. Полученный светло-желтый раствор пероксокомплекса затем смешивали с раствором DL-миндальной кислоты (2,6 г, 17 ммоль) в 5 мл воды. Полученный водный раствор затем выпаривали при пониженном давлении на роторном испарителе при 30–40 °C, получая титановый комплекс в виде светло-желтого порошка.
Синтез микроструктурированного фосфата титана гидротермальным методом
Раствор комплекса титана с миндальной кислотой (0,69 г, 1,66 ммоль) в 20 мл воды помещали в тефлоновый вкладыш автоклава, затем добавляли фосфорную кислоту (98 %) в количестве, соответствующем исходному мольному соотношению элементов Ti:P, который варьировался от 1/8 до 1/4. Приготовленные водные растворы герметично закрывали в автоклаве из нержавеющей стали и нагревали. Полученные осадки декантировали и промывали дистиллированной водой с последующим центрифугированием. Наконец, осадки сушили в вакууме при 90 °C в течение ночи. В табл. 1 приведены данные получения, состава, размера и шифры образцов, полученных при различных условиях.
Таблица 1 Характеристики полученных образцов
|
№ |
T, °С |
Время, ч |
Начальное соотношение Ti:P |
Выход, мг |
Соотношение элементов Ti:P в осадке |
Шифр |
Размер микросфер, µм |
|
1 |
140 |
24 |
1/4 |
262 |
0,86 |
TiP 1/4 |
15,2±1,6 |
|
2 |
140 |
24 |
1/5 |
304 |
0,88 |
TiP 1/5 |
11,0±0,8 |
|
3 |
140 |
24 |
1/6 |
262 |
0,85 |
TiP 1/6 |
7,2±1,2 |
|
4 |
140 |
24 |
1/7 |
260 |
0,88 |
TiP 1/7 |
4,9±1,3 |
|
5 |
140 |
24 |
1/8 |
281 |
0,85 |
TiP 1/8 |
3,6±0,4 |
|
Тип I |
120 |
4 |
1/5 |
105 |
0,85 |
– |
– |
|
Тип II |
140 |
24 |
1/5 |
280 |
0,86 |
– |
– |
|
Тип III |
120 |
72 |
1/4 |
258 |
0,86 |
– |
– |
Обсуждение результатов
Продукты гидротермального синтеза фосфата титана как потенциального электрокатализатора демонстрируют три типа морфологии в зависимости от продолжительности времени синтеза, температуры и исходного соотношения реагентов: водорастворимого комплекса и фосфорной кислоты. При малом времени выдержки, относительно низком содержании фосфорной кислоты и низкой температуре формируется аморфный осадок (тип I). СЭМ-микрофотография продукта TiP не показала отчетливых структурных особенностей и представляет собой изображение набора бесформенных агрегатов (рис. 1а). Рентгенограмма продукта показывает аморфное гало, без видимых рефлексов (рис. 1б). Важно отметить, что при более низких концентрациях фосфорной кислоты (ФК) осадка не образуется.
Микросферический фосфат титана (тип II), который формируется в широком диапазоне параметров, и при строгом контроле условий приобретают правильную форму с узким распределением по размерам. Их структура представляет собой сферически упорядоченные агрегаты микрочешуек. Продолжительный синтез (≥ 48 ч) приводит к рекристаллизации микросфер в термодинамически стабильные гексагональные стержни тип III.

а)
б)
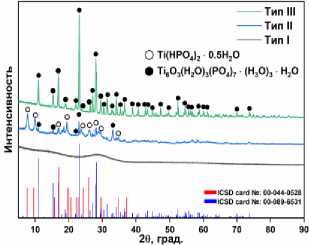
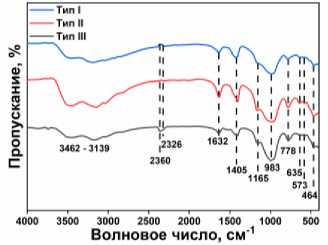
Рис. 1. а) СЭМ-изображения различных типов мифологий фосфата титана: тип I (без морфологии), тип II (микросферы), тип III (микростержни) и EDS-анализ микросфер; б) рентгенофазовый анализ различных типов фосфатов титана; в) ИК-спектры различных типов мифологий фосфата титана тип I–III
в)
EDS-анализ образца тип II подтверждает равномерное распределение элементов Ti, P и O (рис. 1а). Рентгенофазовый анализ (рис. 1б) выявил эволюцию состава от аморфного TiP (4 ч) через двухфазную систему Ti(HPO 4 ) 2 ·0.5H 2 O/Ti 6 O 3 (H 2 O) 3 (PO 4 ) 7 ·(H 3 O) 3 ·H 2 O (12 ч) до монокристаллической фазы Ti 6 O 3 (H 2 O) 3 (PO 4 ) 7 ·(H 3 O) 3 ·H 2 O (≥ 48 ч) (рис. 1а) [15–17]. Очевидно также нарастание степени кристалличности фосфата титана при более длительном времени гидротермального синтеза.
Анализируя ИК-спектры на рис. 1в, можно сказать следующее: наличие широкой полосы поглощения в районе 3462–3139 см–1 указывает на валентные колебания связей O-H в гидроксильных группах (-Ti-OH, -P-OH) и/или молекулах адсорбированной воды [18–20]. Различия в форме и интенсивности этой полосы между типами говорят о разной степени гидратации или количестве поверхностных OH-групп. Полосы при ~1165 см–1 (валентные колебания P-O в P-O-P или связи P=O) и особенно интенсивный пик при ~983 см–1 (характерное валентное колебание связи P=O в фосфатных группах) однозначно подтверждают доминирующее присутствие фосфатных анионов (PO43– или их конденсированных форм). Полосы в области 635–464 см–1 (валентные колебания Ti-O-Ti в оксидной сетке TiO 6 и/или Ti-O-P связей, а также деформационные колебания O-P-O) характерны для структур, содержащих титан-кислородные октаэдры, связанные с фосфатными тетраэдрами [21–23].

а)
б)
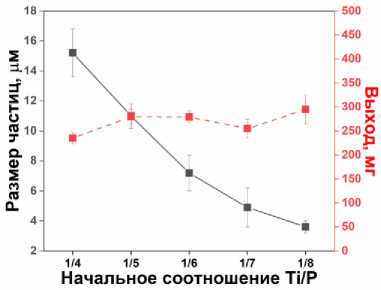
Рис. 2. а) СЭМ-микрофотографии образцов TiP, синтезированных при различных начальных соотношениях Ti:P, б) соответствующий средний размер и выход TiP образцов (24 ч, 140 °C)
Исследования показали выраженную зависимость размера микросферических частиц от концентрации фосфорной кислоты (ФК) (рис. 2а, б). При изменении начального соотношения Ti:P от 1/8 до 1/4 наблюдалось значительное увеличение их среднего размера с ~3–4 мкм до ~15 мкм (рис. 2б). Данный эффект объясняется тем, что более высокие концентрации ФК приводят к увеличению числа центров кристаллизации, что способствует образованию более мелких микросфер. С другой стороны, высокие концентрации фосфат-анионов препятствуют механизму пере-растворения-осаждения, блокируя рост микросфер по механизму Оствальдовского созревания.
Электрокаталитические свойства материалов
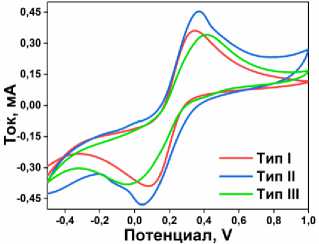
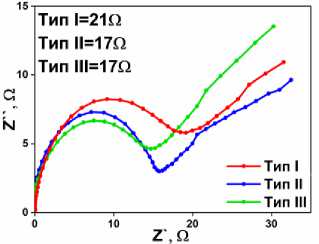
Электрохимическое исследование материалов с различной морфологией (типы I–III) методами циклической вольт-амперометрии (ЦВА) и электрохимической импедансной спектроскопии (ЭИС) в системе [Fe(CN) 6 ]3–/4– показало, что микросферические структуры (тип II) демонстрируют наилучшие характеристики: минимальное сопротивление переносу заряда (Rct = 17 Ом против 21 Ом для типа I) (рис. 3б) и повышенную эффективность, обусловленную их иерархической чешуйчатой структурой (рис. 3а). Подобная структура, во-первых, создаёт предпосылки для более высокой площади поверхности, а, во-вторых, разветвлённая структура пор улучшает массо-перенос. Это в совокупности делает микросферические микросферы (тип II) перспективными кандидатами для электрохимического анализа.
а)
б)
в)
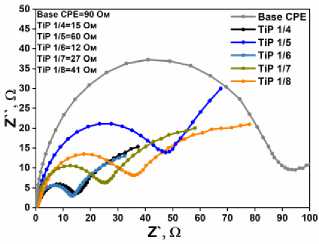
Рис. 3. а) ЦВА окислительно-восстановительной пары Fe 2+/3+ для УПЭ модифицированных TiP образцами с морфологиями типов I–III; б) ЭИС для УПЭ модифицированных TiP образцами с морфологиями типов I–III; в) ЦВА окислительно-восстановительной пары Fe 2+/3+ + для УПЭ модифицированных TiP 1/8–1/4;
г) ЭИС для УПЭ модифицированных TiP 1/8–1/4
г)
Электрохимическое исследование микросфер с размером микросфер от 4 до 15 мкм (табл. 1, № 1–5) методами ЦВА и ЭИС в системе [Fe(CN) 6 ]3–/4–, представленное на рис. 3в, г, выявило нетривиальную зависимость функциональных характеристик от размера сферических частиц. Микросферы с наибольшим средним размером демонстрируют наименьшее сопротивление переносу заряда. Скорее всего, высокоразвитая структура упорядоченных чешуек обеспечивает состав поверхности с лучшей адгезией ионов. Для мелких микросфер (~4 мкм) характерны редкие и изолированные чешуйки, с меньшей площадью контакта с электролитом.
Вместе с тем, развитая система пор в больших микросферах неизбежно повышает диффузионный барьер для ионов, в отличие от микросфер малого размера. Таким образом, оптимальная комбинация диффузионного и поверхностного факторов в микросферах TiP 1/6 предопределило оптимальный ток для микросфер, находящихся посредине размерного диапазона. Данный компромисс между поверхностной доступностью и иерархический сложностью делает материалы со средним размером микросфер наиболее перспективными для практического применения в электрохимических сенсорах.
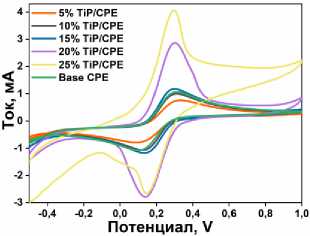
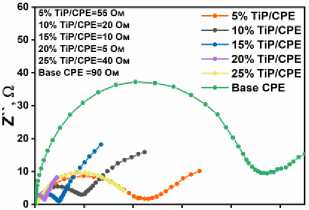
Для оптимизации количества модификатора в угольной пасте мы использовали дополнительные измерения ЭИС в паре [Fe(CN) 6 ]3–/4– для УПЭ с различным содержанием TiP 1/6: 5, 10, 15, 20 и 25 %. Из результатов, представленных на рис. 4а–в, электрод УПЭ с 20 % TiP 1/6 показал наименьшее значение R ct = 5 Ом, что означает, что это количество является наиболее подходящим для приготовления УПЭ модифицированного TiP 1/6.
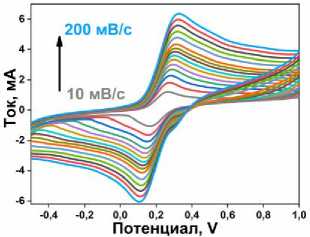
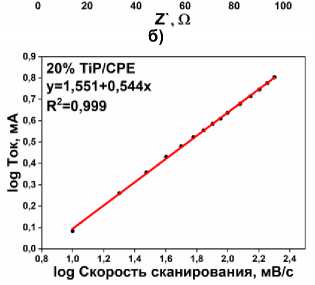
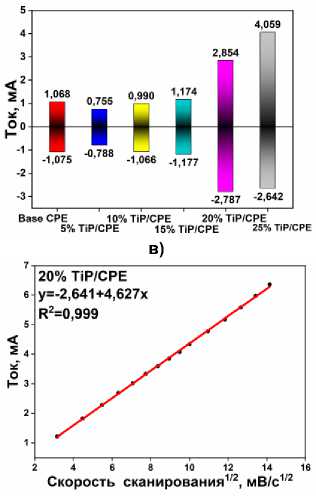
Электрод с оптимальным содержанием электроактивной добавки был испытан при различных скоростях развертки (от 10 до 200 мВ/с) в растворе [Fe(CN) 6 ]3–/4– (рис. 4г). Увеличение логарифма скорости сканирования сопровождается линейным увеличением значений логарифма токов окисления в окислительно-восстановительной системе, с коэффициентом линейной регрессии ≈ 0,5 (рис. 4д). Это характерное поведение процессов с диффузионным контролем, что является дополнительным подтверждением ранее высказанной гипотезы о влиянии на процесс разветвленной иерархии пор. Диффузионный контроль процесса подтверждается линейной зависимостью катодного тока от квадратного корня скорости сканирования (рис. 4е). Таким образом, образец фосфата титана с морфологией II типа, полученного при исходном соотношении Ti:P равном 1/6, был выбран для применения в электрохимической сенсорике и дальнейшего анализа реальных образцов.
д)
е)
Рис. 4. а) ЦВА-кривые в окислительно-восстановительной паре Fe 2+/3+ для УПЭ с различным содержанием TiP 1/6: 5, 10, 15, 20 и 25 %; б) спектры ЭИС для УПЭ с различным содержания TiP 1/6 (5, 7, 10 и 15 %); в) токи окисления-восстановления для УПЭ с различным содержания TiP 1/6; г) ЦВА в окислительно-восстановительной паре Fe 2+/3+ для УПЭ с 20 % TiP 1/6 при различных скоростях сканирования (10–200 мВ/с); д) зависимость log(I a ) от log(v) для УПЭ с 20 % TiP 1/6; е) зависимость от I a для УПЭ с 20 % TiP 1/6 от v 1/2
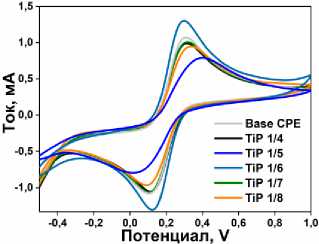
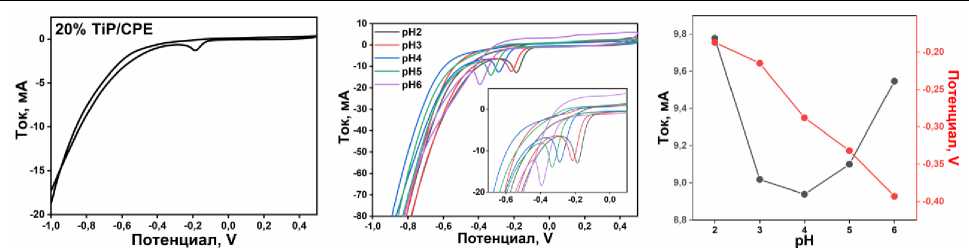
Для оценки электроаналитических свойств синтезированных материалов проведено исследование их активности в отношении восстановления ФТД методом циклической вольтамперометрии. На рис. 5а представлены вольтамперограммы электродов 20 % TiP/УПЭ в 1 ммоль/л растворе ФТД (БР, pH = 2) при скорости сканирования 50 мВ/с и 20 % содержания катализатора. Электрод демонстрируют четко выраженный пик восстановления при –0,2 В, отсутствующий при обратном сканировании, что свидетельствует о необратимом характере электрохимического процесса.
а) б) в)
Рис. 5. а) Электрохимический профиль 1 ммоль/л ФТД для 20 % TiP/УПЭ при скорости сканирования 50 мВ/с, поддерживающий электролит БР pH=2; б) ЦВА при 50 мВ/с для 1 ммоль/л ФТД при 20 % TiP/УПЭ в диапазоне 2-6;
в) зависимость I и E от pH
Для оптимизации условий электрохимического определения ФТД методом ЦВА исследовали влияние pH (2–6) в 1 ммоль/л растворе аналита при скорости сканирования 50 мВ/с. Результаты представлены на рис. 5б, в. Наблюдалось уменьшение тока восстановления при повышении pH от 2 до 4 с одновременным смещением потенциала в менее положительную область. Максимальный отклик получен при pH = 2, тогда как при pH < 2 наблюдалось снижение сигнала и деградация аналитического пика. Данное значение определяется специфическими электрохимическими свойствами нитрофурановых производных, определенными ранее, согласно которым нитрогруппа претерпевает анодное восстановление с активным участием протонов среды [24].
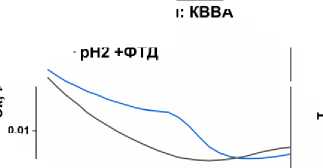
Для разработки электроаналитической методики определения ФТД проведено сравнительное исследование импульсных методов: дифференциальной импульсной вольтамперометрии (ДИВА) и квадратно-волновой вольтамперометрии (КВВА). Из опробованных методов только КВВА продемонстрировало восстановление аналита на 20 % TiP/УПЭ в БР при pH=2 (рис. 6a, б), что обусловило его выбор для дальнейших исследований.
|
■0,03 ------------------------------------------------------ Метод измерения: ДИВА ----рН2 ---рН2 + ФТД ■°02' г О н -0,01 ■ |
-0,030 -0,025 -0,020 ■ < ^-0,015 А М о н-0,010- -0,005- |
|
0,00--1t1t------------- |
0,000 - |
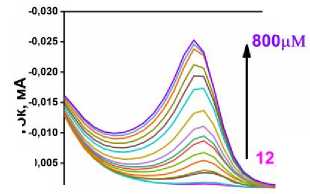
Последовательно были оптимизированы амплитуда импульса (в диапазоне от 10 до 100 мВ), частота (в диапазоне от 10 до 100 Гц) и приращение потенциала (в диапазоне от 2 до 16 мВ). Во время оптимизации одного параметра другие оставались постоянными. В результате, мы получили следующие оптимальные значения: амплитуда импульса – 10 мВ, приращение импульса – 10 мВ и частота – 10 Гц, которые были использованы для разработки электроаналитического метода.
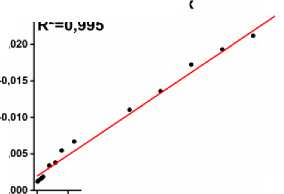
Исследование электрохимического отклика электрода 20 % TiP/УПЭ на различные концентрации ФТД методом КВВА в оптимизированных условиях выявило линейную зависимость тока восстановления от концентрации: I(µА) = 1,975Е–3+2,844Е–5×С(мкМ) (R²=0,99) (рис. 6в, г). Параметры калибровочной кривой δ – стандартное отклонение и b – угловой коэффициент, были использованы для расчета нижнего предела обнаружения (НПО, 3δ/b), и предела количественного определения (ПКО, 10δ/b). Рассчитанные НПО 0,035 мкМ и ПКО 0,105 мкМ, сопоставимы с аналитическими характеристиками ранее опубликованных электрохимических методов определения ФТД [25, 26].
Селективность разработанного сенсора 20 % TiP/УПЭ была тщательно исследована путем тестирования потенциальных мешающих агентов, включая распространенные ионы и органические соединения (рис. 6д). Результаты демонстрируют отличную избирательность датчика: все протестированные вещества (включая обычные ионы) не оказывают значительного влияния. Полученные данные подтверждают, что разработанный электрохимический сенсор обладает достаточной селективностью для практического применения в мониторинге ФТД в водных системах.
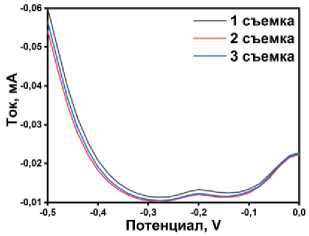
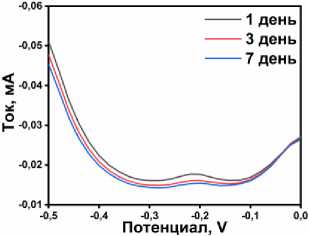
Проверка воспроизводимости для трех последовательных измерений для концентрации 60 мкМ показала стандартное отклонение (СО) = 7,7 % (рис. 7а), а исследования стабильности в течение недели (1 день, 3 день и 7 день) для 60 мкМ раствора подтвердили сохранение отклика электрода (СО = 10,1 %) (рис. 7б). Полученные результаты свидетельствуют о надежности разработанного метода для количественного определения ФТД, что обусловлено оптимальной структурой материала и его электрокаталитическими свойствами.
а)
б)
в)
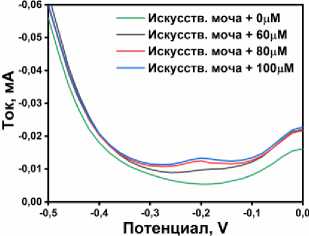
Рис. 7. а) Исследования повторяемости; б) исследования стабильности; обнаружения и степени извлечения ФТД в пробах в) искусственной мочи и г) водопроводной воды
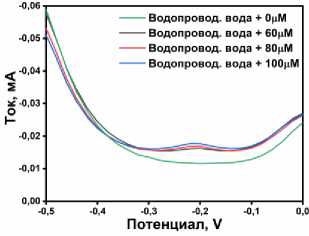
г)
Практическая применимость была проверена с использованием датчика на основе 20 % TiP/УПЭ для определения концентрации ФТД. Было выбрано два типа проб: водопроводная вода и раствор искусственной мочи. Образцы были проанализированы в соответствии с разработанной нами методикой электрохимического анализа. Образцы разбавлялись буфером БР при pH = 2 в соотношении 1:1 и тестировались напрямую. Важнейшей характеристикой аналитического метода является также степень извлечения, которая для исследуемого электрода проводи- лась добавлением стандартного раствора ФТД до концентраций 60, 80 и 100 мкМ. Полученные вольтамперограммы приведены на рис. 7в, г, а результаты измерения реальных образцов приведены в табл. 2. Степени извлечения реальных образцов были сопоставимы с добавленным количеством ФТД, при этом результаты колебались от 97 до 109 %, и эти результаты доказывают, что предлагаемый датчик может успешно применяться для мониторинга ФТД.
Таблица 2 Результаты определения ФТД и исследования степени его извлечения в образцах в режиме реального времени
|
Реальный образец |
60 мкМ |
Степень извлечения, % |
80 мкМ |
Степень извлечения, % |
100 мкМ |
Степень извлечения, % |
|
Калибровочная кривая |
–0,0074 |
– |
–0,0132 |
– |
–0,0144 |
– |
|
Водопроводная вода |
–0,0075 |
101 |
–0,0136 |
103 |
–0,0140 |
97 |
|
Искусственная моча |
–0,0076 |
103 |
–0,0131 |
99 |
–0,0157 |
109 |
Заключение
В этой работе был синтезирован микросферический фосфат титана сложного состава и иерархической структуры, представляющий собой центрически агрегированные микрочешуйки. Данный материал служит превосходной электроактивной добавкой для электрода из угольной пасты. Наилучшие электрохимические характеристики продемонстрировал образец TiP 1/6 со средним размером микросфер (~8 мкм), обладающий минимальным сопротивлением переносу заряда (R ct = 12 Ом) и максимальным током окисления (I = 1,37 мА) в растворе [Fe(CN) 6 ]3–/4–. Этот результат объясняется оптимальным сочетанием состава поверхности, обеспечивающим низкое сопротивление переноса заряда и эффективную диффузию реагентов к поверхности. Для мелкодисперсных микросфер (~4 мкм, Rct = 41 Ом), характерны редкие чешуйки малого размера, в то время как для крупных микросфер (~15 мкм, Rct = 15 Ом), характерна разветвленная структура чешуек. Малые размеры снижают контакт поверхности с электролитом, а развитая иерархическая структура больших микросфер увеличивает диффузионный барьер аналита к поверхности. Срединный размер TiP 1/6 достигает баланса между этими двумя тенденциями, обеспечивая максимальный ток и минимальное сопротивление переносу заряда. Это делает его наиболее перспективным материалом для разработки высокочувствительных электрохимических сенсоров. Был предложен аналитический метод определения фуралтодона с превосходными аналитическими параметрами: НПО = 0,035 мкМ, линейным рабочим диапазоном 12–800 мкМ и высокой селективностью. Измерения реальных образцов показали, что этот материал обладает большим потенциалом применения как электрохимический сенсор в исследовательских, так и в коммерческих целях.


