Электролитические свойства растворов угольной кислоты и инновационные методы оперативного контроля качества вод типа конденсата на ТЭС
Автор: Щербаков Владимир николаевиЧ.
Журнал: Advanced Engineering Research (Rostov-on-Don) @vestnik-donstu
Рубрика: Машиностроение и машиноведение
Статья в выпуске: 4 (83) т.15, 2015 года.
Бесплатный доступ
Целью работы является совершенствование оперативного кондуктометрического контроля качества пара на ТЭС. Для этого разработана методика определения концентраций СО 2 в паре при нейтральном водно-химическом режиме без дозирования аммиака. Использован метод измерений электропроводности конденсата пара при рабочих давлениях парогенераторов и различных температурах. Реализация данного метода с помощью специального устройства обеспечила значительное снижение инерционности контроля и дифференцирование примесей. Проанализированы экспериментальные данные о первых кажущихся константах диссоциации и предельной эквивалентной электропроводности угольной кислоты, константах диссоциации и предельной эквивалентной электропроводности NaCl в жидкой фазе на линии насыщения. На основании данного анализа оценена погрешность определения предложенным методом концентраций СО 2 и примесей в паре в виде NaCl. Рассчитана погрешность аппроксимации для зависимостей, описывающих поведение констант диссоциации и предельной эквивалентной электропроводности угольной кислоты, которые могут быть использованы при расчете концентраций по предложенной методике, а также при организации и ведении водно-химических режимов.
Оперативный контроль, качество пара, кондуктометрические методы, угольная кислота, электролитические свойства
Короткий адрес: https://sciup.org/14250168
IDR: 14250168 | УДК: 621.182.12 | DOI: 10.12737/16069
Electrolytic properties of carbonic acid solutions and innovative methods of operational control of water quality such as condensation at TPP
The work objective is to improve the operational conductometric vapor quality control at the thermal power plants. To this end, methods identifying СО 2 concentrations in the vapor under the neutral aqueous-chemical mode without ammonia addition are developed. The technique of measuring the steam condensate conductivity at the operating pressures of steam generators and at different temperatures is used. The implementation of this method with the use of a special device significantly reduces the control response rate and differentiation of impurities. The experimental data on the first apparent dissociation constants and the limiting equivalent conductance of the carbonic acid, dissociation constants, and the limiting equivalent conductance of NaCl in the liquid phase on the saturation line are analyzed. On the basis of this analysis, an error in determining СО 2 concentration and the impurities in vapor in the form of NaCl by the proposed method is estimated. The approximation error for the dependencies describing the dissociation constants behavior, and the limiting equivalent conductance of the carbonic acid, which can be used in the calculation of the concentrations by the proposed methodology, as well as during the organization and management of water chemistry, is estimated.
Текст научной статьи Электролитические свойства растворов угольной кислоты и инновационные методы оперативного контроля качества вод типа конденсата на ТЭС
Введение. При организации и ведении водно-химического режима (ВХР) на ТЭС основными задачами являются замедление процессов коррозии конструкционных материалов и образования отложений в пароводяном тракте энергетических установок [1]. Снижение рН растворов и усиление коррозионных процессов определяются наличием в питательной воде и паре котельных установок угольной кислоты, следовательно, ее содержание необходимо свести к минимуму [1, 2].
Причинами нарушения норм ВХР могут быть:
-
— присосы охлаждающей воды в конденсаторах турбин;
-
— растворение в конденсате CO 2 , содержащегося в воздухе;
-
— попадание в конденсатно-питательный тракт потенциально кислых веществ, разлагающихся при высоких температурах Т с образованием СО2 [3 ,4].
В настоящее время на станциях оперативный контроль качества вод типа конденсата осуществляется путем анализа охлажденных до Т = 298,15К проб, отобранных из контрольных точек.
Авторы [3, 5] предложили новый метод оперативного контроля примесей в конденсатах, позволяющий упростить существующую методику контроля. Суть метода заключается в следующем. Определяется концентрация примесей С путем измерения рН, Т и удельной электропроводности χ охлажденных проб до и после катионообменного фильтра и решаются уравнения, соответствующие математическим моделям ионных равновесий в водных растворах. Значения концентраций примесей в виде ионов Cl –, Na + , HCO 3 – и свободной углекислоты получаются на основании анализа уравнений электронейтральности, электрической проводимости, баланса углекислоты до и после H-фильтра, диссоциации углекислоты по первой ступени.
Но анализ охлажденных проб предполагает наличие устройств отбора, транспортирования, снижения давления и охлаждения пробы. Такая методика связана со значительным транспортным запаздыванием пробы. Это негативно влияет на достоверность полученных результатов и возможность быстрого реагирования в случае внезапного резкого изменения контролируемых параметров в потоке пара.
Значительно уменьшить инерционность процесса измерения и исключить необходимость в пробоотборных линиях и устройствах подготовки пробы позволяет метод контроля, заключающийся в измерении χ конденсата контролируемого пара в кондуктометрической ячейке охлаждаемого датчика, размещенного в потоке пара [6–9]. При этом С примесей в паре определяют из зависимости С = f (χ) [6, 10]. Однако в работах [6, 10] отсутствует подробный анализ возможностей метода для условий, когда в паре энергоблоков с нейтральным ВХР без дозирования аммиака присутствуют примеси в виде диоксида углерода и NaCl. Не была детально разработана и методика определения С на основании данных о χ водных растворов СО 2 с учетом наблюдаемых на станциях реальных значений С и особенностей изменения χ с температурой.
Целью настоящей работы является совершенствование метода определения концентрации примесей в паре, основанного на измерении χ конденсата пара охлаждаемым датчиком [8], и оценка погрешности определения С примесей в конденсате пара, содержащем только СО 2 и NaCl в количестве, характерном для ТЭС при нейтральном ВХР без дозирования аммиака.
Для достижения поставленной цели:
-
— решены задачи, связанные с анализом изменения первых кажущихся констант диссоциации K d1 и предельной эквивалентной электропроводности Λо угольной кислоты и Λо NaCl в жидкой фазе на линии насыщения;
Машиностроение и машиноведение
-
— разработаны методики определения χ на основании данных о K d1 и Λ о для угольной кислоты и определения С на основании данных о χ;
-
— выполнена оценка погрешности аппроксимации для данных о K d1 и Λ о угольной кислоты.
Анализ экспериментальных данных. Для решения поставленных задач были использованы экспериментальные данные авторов [6, 11–16] о K d1 и Λ о для угольной кислоты и данные о Λ о для NaCl [11]. Анализ зависимости K d1 от Т на линии насыщения в жидкой фазе, представленной на рис. 1, показывает, что в диапазоне изменения Т от 298 до 323К Kd1 возрастает от 4,45∙10–7 до 5,19∙10–7 [11], а затем уменьшается до 3,6∙10–7 при 373К и до 1,81∙10–9 при 593К [6]. Причем с увеличением Т K d1 уменьшается все сильнее. Если при увеличении Т от 373 до 473К K d1 уменьшается в 2,46 раза [6], то при увеличении Т от 473 до 573 и до 593К — уже в 14,4 и в 36 раз соответственно. Следует отметить, что на рис. 1 представлены далеко не все экспериментальные данные о K d1 , известные из литературных источников. Это объясняется тем, что разные авторы рассматривают близко расположенные показатели, и графически изобразить такие данные сложно.
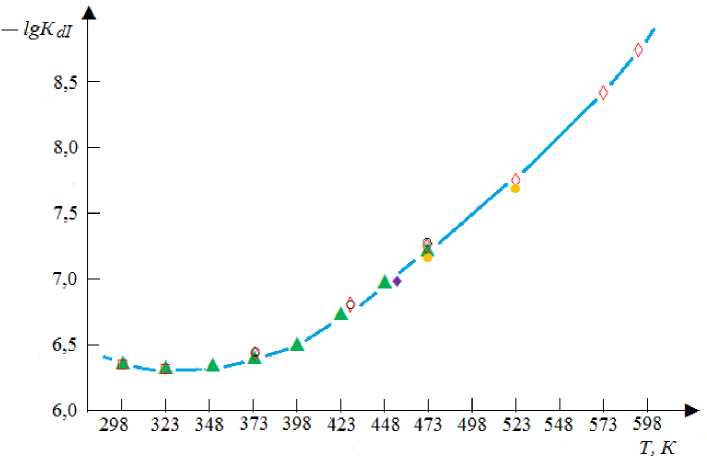
Рис. 1. Зависимость первых констант диссоциации угольной кислоты от температуры: ◊ — [6]; □ — [11]; ▲ — [14]; ○ — [15]; • — [16]; ♦ — [21]
В качестве примеров могут быть приведены работы Диксона и Миллеро [17] ( Т = 273–308К), Шедловского и Маккейна [18] (273–311К), Харнеда и Боннера [19] (273–323К), Накаямы [20] (273–323К), Пака, Кима и Ли [21] (298– 448К), Миллеро, Хуанга, Грэхэма и Пиеррота [22] (273–323К), Петтерсона, Слокума, Бассэя и Месмера [23], Ли и Ду-ана [24]. Данные авторов [23, 24] представлены в виде математической модели для зависимости К dI от Т .
Методика определения χ и С. Значения χ высокоразбавленных растворов NaCl и СО 2 определялись путем расчета с использованием данных о К dI и Λ о [6, 11–13]. На основании анализа данных о К d , Λ о и степеней диссоциации α для NaCl в рассматриваемой области изменения Р, Т, С при выполнении оценочных расчетов полагали, что
Λ NaCl = Λ о NaCl и χ NaCl = Λ о NaCl ∙ С ∙ρ/ρ ну ∙ 10–3, где С — концентрация раствора в кг-экв/м 3 ; ρ — плотность раствора при Т опыта; ρну — плотность раствора при нормальных условиях.
Для нахождения χ растворов Н 2 СО 3 значения α определяли из уравнения
К d1 = α2 ∙ С ∙ f 2/(1 – α), где f — средний коэффициент активности.
Величину f рассчитывали по уравнению Дебая [12]. Значения эквивалентной электропроводности Λ находили из соотношения
α = Λ /Λ i .
Здесь Λ i — эквивалентная электропроводность гипотетически полностью диссоциированного раствора при концентрации α 1 ∙ С , где α 1 = Λ/Λо. Величину Λ i определяли по уравнению Робинсона — Стокса [25], а χ для растворов Н 2 СО 3 — из соотношения между χ и Λ: χ = Λ ∙ С ∙ ρ/ρну ∙10– 3 .
При оценке вклада χ NaCl и вклада χ Н 2 СО 3 в суммарную удельную электропроводность раствора χсум. учитывался характер изменения χ NaCl и χ Н 2 СО 3 при изменении температуры. Результаты расчетов для температур 323,15 и 373,15К и С СО 2 , равных 50, 500 и 5000 мкг/кг при С Na = 5 мкг/кг, представлены в табл. 1.
Таблица 1
Вклад NaCl в суммарную удельную электропроводность конденсата пара, содержащего NaCl и СО 2 , и отношение χ NaCl / χ СО 2
|
Т , К |
С Na = 5 мкг/кг |
|||||
|
С СО 2 = 50 мкг/кг |
С СО 2 = 500 мкг/кг |
С СО 2 = 5000 мкг/кг |
||||
|
323,15 |
0,120* |
0,138** |
0,0336* |
0,0347** |
0,0101* |
0,0102** |
|
373,15 |
0,166* |
0,199** |
0,0495* |
0,0520** |
0,0152* |
0,0154** |
|
*δ 1 = χ NaCl / χ сум ; **δ 2 = χ NaCl / χ СО 2 |
||||||
Значение С Na = 5 мкг/кг выбрано исходя из допустимых максимальных предельных величин, соответствующих правилам технической эксплуатации котельных агрегатов [2]. Как видно из табл. 1, δ2 = χ NaCl / χ СО2 намного меньше единицы. Основной вклад в χсум. с учетом поправки на χ растворителя вносит растворенная СО2. С увеличени- ем С СО2 от 50 до 5000 мкг/кг δ2 уменьшается от 0,138 до 0,0102 при Т = 323,15К и от 0,199 до 0,0154 при Т = 373,15К. С увеличением Т от 323,15 до 373,15К δ2 возрастает в 1,44; 1,50 и 1,51раза при С СО2, равной 50, 500 и 5000 мкг/кг. Величина δ1 с ростом С СО2 от 50 до 500 и 5000 мкг/кг уменьшается в 3,57 и в 11,9 раз при Т = 323,15К и в 10,9 раз при Т = 373,15К. Величина δ1 с ростом С СО2 от 50 до 500 и 5000 мкг/кг уменьшается в 3,57 и в 11,9 раз при T = 323,15К и в 3,35; 10,9 раз при Т = 373,15К.
С ростом Т от 323,15 до 373,15К δ 1 увеличивается в 1,38; 1,47 и в 1,50 раза при С СО 2 , равной 50, 500 и 5000 мкг/кг. Так как δ 1 = χ NaCl / χсум., то из табл. 1 следует, что присутствие NaCl в конденсате пара при С СО 2 = 50 мкг/кг влияет на 12 % на χ сум. при Т = 323,15К и на 16,6% при Т = 373,15К. Однако при увеличении С СО 2 до 500 и 5000 мкг/кг это влияние снижается до 3,36; 4,95 и 1,01 и 1,52 % соответственно.
Современные прецизионные приборы обеспечивают измерение проводимости разбавленных водных растворов электролитов с погрешностью не более 0,05–0,15 % [26]. При С СО 2 , равной 50 и 500 мкг/кг, относительное увеличение χ сум за счет NaCl, равное δ 1 , составляет 0,12; 0,166 и 0,0336; 0,0495 (для Т = 323,15 и 373,15К). При этом относительная погрешность определения χ сум в таких измерениях будет не более 0,5% [6], что приемлемо для оценочных расчетов. При С СО 2 , равной 5000 мкг/кг, δ 1 уменьшается до 0,0101 и 0,0152. В этом случае погрешность определения χсум . , всего в два и в три раза меньше определяемой величины δ 2 , и поэтому достоверная оценка δ 1 затруднена.
С СО 2 и С NaCl по данным о χсум. определяется по разработанной нами методике. Она основана на определении χсум. при Т , равных 323,15 и 373,15К. При Т = 323,15К
χ сум. = χ сум.1 = χ 1 СО 2 + χ 1 NaCl, где χ 1 СО 2 и χ 1 NaCl — вклады в удельную электропроводность χ сум. , обусловленные присутствием в конденсате СО 2 и NaCl.
С изменением Т изменятся χ сум. , χ 1 СО 2 и χ 1 NaCl.
Пусть χ 1 СО 2 при Т = 373,15К изменится в a раз, а χ 1 NaCl — в b раз. Тогда для Т = 373,15К
χ сум = χ сум.2 = a ∙ χ 1 СО 2 + b ∙ χ 1 NaCl.
Значения коэффициентов a и b находятся путем расчета χ по изложенной выше методике для монорастворов СО 2 и NaCl при Т , равных 323,15 и 373,15К.
Решением системы двух представленных линейных уравнений для χсум.1 и χсум.2 находятся неизвестные χ 1 СО 2 и χ 1 NaCl при Т = 323,15К. Затем определяются значения С СО 2 и С NaCl при этой Т на основании ранее полученных для водных монорастворов СО 2 и NaCl градуировочных зависимостей вида χ 1 = f ( C ). Результаты вычислительного эксперимента, выполненного в соответствии с предложенной методикой в рассматриваемом диапазоне изменения С и Т, подтвердили корректность предложенной математической модели.
Оценка погрешности аппроксимации данных о К d1 и Λ о . Для выполнения расчетов с целью определения С СО 2 необходимы данные о К d1 и Λ о угольной кислоты. На основании выполненных нами ранее экспериментальных исследований путем измерения электропроводности водных растворов СО 2 при Т от 373,15 до 593,15К [6] были получены зависимости К d1 и Λо от Т. Нами предложены уравнения, описывающие эти зависимости [27]:
– lgК d1 = 2,49762 ∙ 10–5 ∙ Т 2 – 0,013909088 ∙ Т + 8,167523085; Λ о = 2,960 ∙ 10–5 ∙ Т 3 – 0,054 ∙Т 2 + 33,156 ∙ Т – 5557,36.
Данные о рК d1 = – lgК d1 , Λо и значения относительной погрешности аппроксимации δ представлены в табл. 2.
Таблица 2
Зависимости первых кажущихся констант диссоциации К dI и предельной эквивалентной электропроводности Λ о угольной кислотыот температуры на линии насыщения и относительные погрешности их аппроксимации (δ рК dI и δ Λ о )
|
Т, К |
рК d1 = –lg К d1 , кмоль/м 3 |
δ рК d1 , % |
Λо·10, См∙м2 ∙кг-экв–1 |
δ Λ о , % |
|
373,15 |
6,453 |
0,031 |
793 |
0,260 |
|
429,15 |
6,796 |
0,034 |
1000 |
0,934 |
|
473,15 |
7,186 |
0,110 |
1120 |
1,058 |
|
523,15 |
7,740 |
0,173 |
1160 |
0,306 |
|
573,15 |
8,346 |
0,647 |
1175 |
0,406 |
|
593,15 |
8,742 |
0,424 |
1184 |
0,317 |
Машиностроение и машиноведение
Наименьшие значения δ для К d1 — при Т не более 523,15К. В этом случае δ рК d1 не превышает 0,173 %. С увеличением Т от 523,15 до 573,15К δ возрастает до 0,647 %. Наименьшее значение δ для Λо равно 0,26 % при Т = 373,15К, наибольшее — 1,058 % при Т = 473,15К.
Такую погрешность аппроксимации данных о К d1 и Λ о можно считать приемлемой при выполнении расчетов с использованием указанных величин, учитывая значения погрешности полученных экспериментальных данных [6].
Следует отметить, что мы определяли С СО 2 и С NaCl на основании измерения χ сум. при Т = 323,15 и Т = 373,15К. Аналогичные измерения можно выполнять и при более высоких Т . При этом с уменьшением К d1 уменьшается χ растворов СО 2 и изменятся значения δ 1 и δ 2 , представленные в табл. 1. Такая работа может быть выполнена в рамках отдельного исследования.
Заключение . Разработан метод оперативного кондуктометрического контроля концентраций СО 2 и NaCl в конденсате пара на ТЭС при нейтральном ВХР без дозирования аммиака. Предложено устройство для его реализации, обеспечивающее дифференцирование примесей и значительное снижение инерционности контроля. Выполнена оценка погрешности определения концентраций предложенным методом. Рассчитана погрешность аппроксимации для зависимостей, описывающих поведение первых кажущихся констант диссоциации и предельной эквивалентной электропроводности угольной кислоты при Т от 373,15 до 593,15К, которые можно использовать при расчете концентраций предложенным методом, а также при организации и ведении ВХР.
Информация о концентрации примесей для одних и тех же объектов, полученная одновременно от устройств контроля, реализующих предложенный метод, и от устройств, работающих с охлажденной пробой [4, 5], может быть использована для создания нового контроля, сочетающего в себе преимущества обоих методов и расширяющего возможности совершенствования существующих систем химико-технологического мониторинга ВХР на ТЭС и АЭС [28].
Список литературы Электролитические свойства растворов угольной кислоты и инновационные методы оперативного контроля качества вод типа конденсата на ТЭС
- Воронов, В. Н. Водно-химические режимы ТЭС и АЭС/В. Н. Воронов, Т. И. Петрова. -Москва: Издательский дом МЭИ, 2009. -238 с.
- Правила технической эксплуатации электрических станций и сетей РФ СО 153-34.20.501-2003/Министерство энергетики Российской Федерации. -Москва: Энергосервис, 2003. -145 с.
- Ларин, Б. М. Основы математического моделирования химико-технологических процессов обработки теплоносителя на ТЭС и АЭС/Б. М. Ларин, Е. Н. Бушуев. -Москва: Издательский дом МЭИ, 2009. -306 с.
- Мартынова, О. И. Поведение органики и растворенной углекислоты в пароводяном тракте электростанций/О. И. Мартынова//Теплоэнергетика. -2002. -№ 7. -С. 67-70.
- Бушуев, Е. Н. Исследование и математическое моделирование химико-технологических процессов водообработки на ТЭС: дис. … д-ра техн. наук/Е. Н. Бушуев. -Иваново, 2010. -359 с.
- Щербаков, В. Н. Исследование электрофизических свойств водных теплоносителей при высоких параметрах: дис. … канд. техн. наук/В. Н. Щербаков. -Москва, 1980. -204 с.
- Кондуктометрический датчик: а. с. 958943 СССР: МКИ4 G01N 27/02/Д. Л. Тимрот . -№ 3248961; заявл. 16.02.81; опубл. 15.09.82, Бюл. № 34. -3 с.
- Щербаков, В. Н. Совершенствование кондуктометрического контроля качества конденсата пара при термической очистке вод/В. Н. Щербаков//Вестник Дон. гос. техн. ун-та. -2013. -Т. 13, № 3/4 (72/73). -С. 117-124.
- Экспериментальное и теоретическое обоснование нового метода контроля качества рабочего тела в контурах ТЭС и АЭС/Н. Н. Ефимов //Изв. вузов. Северо-Кавк. регион. Техн. науки. -2012. -№ 3 (166). -С. 28-32.
- Лукашов, Ю. М. Экспериментально-теоретическое обоснование новых методов контроля качества пара и воды современных теплоэнергетических установок: дис. … д-ра техн. наук/Ю. М. Лукашов. -Москва, 1981. -412 с.
- Новый справочник химика и технолога: в 12 т. Т. 7. Химическое равновесие. Свойства растворов/под ред. А. М. Симановой. -Санкт-Петербург: Профессионал, 2004. -998 с.
- Дамаскин, Б. Б. Электрохимия/Б. Б. Дамаскин, О. А. Петрий, Г. А. Цирлина. -Москва: Химия; Колос С, 2006. -672 с.
- Добош, Д. Электрохимические константы. Справочник для электрохимиков/Д. Добош. -Москва: Мир, 1980. -365 с.
- Stefansson, A. Carbonic acid ionization and the stability of sodium bicarbonate and carbonate ion pairs to 200oC -A potentiometric and spectrophotometric study/A. Stefansson, P. Benezeth, J. Schott//Geochimica et Cosmochimica Acta. -2013. -Vol. 120. -P. 600-611.
- Рыженко, Б. Н. Определение констант диссоциации угольной кислоты и расчет степеней гидролиза СО32-и НСО3-ионов в растворах карбонатов и бикарбонатов при повышенных температурах/Б. Н. Рыженко//Геохимия. -1963. -№ 2. -С. 137-148.
- Read, A.-J. The First Ionization Constant of Carbonic Acid from 25 to 250o C and to 2000 bar/A.-J. Read//Journal of Solution Chemistry. -1975. -Vol. 4, № 1. -P. 53-70.
- Dickson, A.-G. A comparison of the equilibrium constants for the dissociation of carbonic acid in seawater media/A. G. Dickson, F. J. Millero//Deep-Sea Research. -1987. -Vol. 34. -P. 1733-1743.
- Shedlovsky, T. The first ionization constant of carbonic acid, 0 to 38 from conductance measurements/T. Shedlovsky, D.-A. MacInnes//Journal of the American Chemical Society. -1935. -Vol. 57. -P. 1705-1710.
- Harned, H.-S. The first ionization of carbonic acid in aqueous solution of sodium chloride/H.-S. Harned, F.-T. Bonner//Journal of the American Chemical Society. -1945. -Vol. 67. -P. 1026-1031.
- Nakayama, F.-S. Thermodynamic functions for the dissociation of NaHCO3, NaCO3-, H2CO3, and HCO3-/F.-S. Nakayama//Journal of Inorganic and Nuclear Chemistry. -1971. -Vol. 33. -P. 1287-1291.
- Spectrophotometric measurement of the first dissociation constants of carbonic acid at elevated temperatures/S.-N. Park //Journal of the Chemical Society Faraday Transactions. -1998. -Vol. 94. -P. 1421-1425.
- The dissociation of carbonic acid in NaCl solutions as a function of concentration and temperature/F.-J. Millero //Geochimica et Cosmochimica Acta. -2007. -Vol. 71. -P. 46-55.
- Carbonate equilibrium in hydrothermal systems -first ionization of carbonic acid in NaCl media to 300o C/C.S. Patterson //Geochimica et Cosmochimica Acta. -1982. -Vol. 46. -P. 1653-1663.
- Li, D. The speciation equilibrium coupling with phase equilibriumin the H2O-CO2-NaCl system from 0 to 250o C, from 0 to 1000 bar, and from 0 to 5 molality of NaCl/D. Li, Z. Duan//Chemical Geology. -2007. -Vol. 244. -P. 730-751.
- Робинсон, Р. Растворы электролитов/Р. Робинсон, Р. Стокс. -Москва: Иностранная литература, 1963. -425 с.
- Первухин, Б. С. Развитие научно-методических основ проектирования кондуктометрических приборов контроля жидкостей и разработка технических средств их метрологического обеспечения: автореф. дис. … д-ра техн. наук/Б. С. Первухин. -Барнаул, 2012. -39 с.
- Щербаков, В. Н. Инновационные электрофизические методы оперативного контроля качества вод типа конденсата на ТЭС/В. Н. Щербаков, Г. А. Власков//Обозрение прикладной и промышленной математики. -2014. -Т. 21, вып. 5. -С. 764-765.
- Егошина, О. В. Современное состояние систем химико-технологиче-ского мониторинга на тепловых станциях на основе опыта МЭИ и НПЦ «Элемент»/О. В. Егошина, В. Н. Воронов, М. П. Назаренко//Теплоэнергетика. -2014. -№ 3. -С. 39-45.


