Электролиты на основе калиевого криолита для низкотемпературного получения алюминия
Автор: Ткачева О.Ю., Редькин А.А., Дедюхин А.А., Аписаров А.П., Тиньгаев П.Е., Зайков Ю.П.
Журнал: Журнал Сибирского федерального университета. Серия: Техника и технологии @technologies-sfu
Статья в выпуске: 5 т.7, 2014 года.
Бесплатный доступ
Исследованы и описаны общими регрессионными уравнениями основные физико-химические свойства (температура ликвидуса, электропроводность, растворимость оксида алюминия) смешанных калий-натриевых криолитовых расплавов с криолитовым отношением 1,3-1,5 с добавками LiF и CaF2. На основании выявленных закономерностей определены составы электролитов, перспективные для низкотемпературного электролитического получения алюминия: KF-AlF3 и KF-NaF-AlF3, содержащие 12-15 мас. % NaF, с криолитовым отношением 1,3-1,5 и температурой ликвидуса ниже 800 °С. Растворимость глинозема в таких электролитах составляет не менее 4,5 мас. % в интервале температур 700-800 °С. Для повышения электропроводности рекомендуются добавки LiF в количестве не более 3 мас. %. Присутствие CaF2 в электролите нежелательно.
Калиевый криолит, калий-натриевый криолит, электропроводность, температура ликвидуса, растворимость оксида алюминия, фторид кальция, низкотемпературный электролиз
Короткий адрес: https://sciup.org/146114874
IDR: 146114874 | УДК: 532:537.311.32;
Electrolytes based on the potassium kriolit for low-temperature obtaining of aluminium
The general regression equations basic physical and chemical properties (liquidus temperature, conductivity, solubility of alumina) mixed potassium-sodium cryolite melts with cryolite ratio 1,31,5 with additives LiF and CaF2 are investigated and described. Based on the identified patterns the electrolyte composition, promising for low-temperature aluminum electrowinning are defi ned: KFAlF3 and KF-NaF-AlF3, containing 12-15 wt.% NaF, with cryolite ratio of 1,3-1,5 and the liquidus temperature below 800 C. The solubility of alumina in electrolytes such is not less than 4.5 wt.% in the temperature range of 700-800 C. In order to increase the electrical conductivity supplements LiF in an amount of not more than 3 wt.% are recommended. CaF2 in the presence of the electrolyte is not desirable.
Текст научной статьи Электролиты на основе калиевого криолита для низкотемпературного получения алюминия
В настоящее время практически весь первичный алюминий получают методом Эру-Холла, который более чем за 100 лет не претерпел принципиальных изменений. Метод заключается в электролитическом разложении глинозема, растворенного в натриевом криолитовом расплаве (Na3AlF6 с добавками AlF3, CaF2 и др.), при температуре около 950 °С. Процесс сопровождается расходом угольных анодов и выбросом в атмосферу значительного количества вредных газов (СО, СО2 и фреонов), создающих парниковый эффект. Кардинальная модификация процесса Эру-Холла возможна при замене расходуемых угольных анодов на нерасходуемые инертные аноды, которые не взаимодействуют с электролитом и выделяющимся на них кислородом. Использование таких анодов (металлических, керамических, керметных) в сочетании со смачиваемыми алюминием катодами (например, на основе диборида титана) дает возможность существенно уменьшить межполюсное расстояние в алюминиевых электролизерах и снизить расход электроэнергии. Отсутствие необходимости в частой замене анодов и регулировании межполюсного расстояния позволит конструировать электролизеры с улучшенными экологическими показателями.
Однако на текущий момент нет информации об успешном применении инертных анодов в условиях традиционной технологии. Основной причиной этого является агрессивность криолит-глиноземного расплава при высоких температурах электролиза. Для предотвращения быстрого коррозионного разрушения конструкционных материалов требуется уменьшить рабочую температуру процесса. В этой связи возникает необходимость создания и развития новой технологии – технологии низкотемпературного электролиза. Основные ее достоинства – энергосбережение, значительное снижение выбросов парниковых газов и увеличение срока службы электролизера.
Попытки разработать низкотемпературный процесс получения алюминия были сконцентрированы на модификации традиционного электролита на основе натриевого криолита: понижения температуры добивались главным образом за счет увеличения содержания фторида алюминия. Однако из-за низкой растворимости глинозёма в таких расплавах они не нашли применения в промышленности.
Другим путем решения вопроса выступает поиск новых электролитов на основе калиевого криолита. Смеси KF-AlF3 с мольным (криолитовым) отношением NKF/NAlF3 от 1,3 до 1,5 плавятся при температуре ниже 800 оС, а растворимость глинозема в них выше, чем в натриевой системе [1]. Однако в электролизной ванне могут накапливаться вносимые вместе с глиноземом фториды натрия и кальция, что существенно влияет на свойства электролита. До недавнего времени физико-химические свойства смешанных криолитовых расплавов с низким криолитовым отношением (КО) практически не изучались. Это, по-видимому, и послужило причиной неудач большинства попыток провести электролиз растворов глинозема в электролитах на основе калиевого криолита, в лабораторных ячейках с инертными анодами при температуре 700 °С [2-4]. Основные трудности были связаны с высоким и нестабильным напряжением на электродах, образованием непроводящей солевой корки на катодах, пассивацией анодов, значительным загрязнением алюминия продуктами их коррозии.
В настоящей статье обобщаются результаты исследований базовых физико-химических свойств (температура ликвидуса, электропроводность, растворимость оксида алюминия) расплавленных смесей KF-NaF-AlF 3 (КО=1,3-1,5) с добавками CaF 2 и LiF, которые могут быть использованы в качестве легкоплавких электролитов-растворителей Al2O3 для низкотемпературного получения алюминия. Следует отметить, что криолитовое отношение – это отношение мольных концентраций фторида щелочного металла (NMF) к фториду алюминия (NAlF3): КО = N MF /N AlF3 . Для смешанных криолитовых расплавов криолитовое отношение рассчитывали как отношение суммы мольных концентраций фторидов щелочных металлов к мольной концентрации AlF 3 . Например, для смеси KF-NaF-AlF 3 КО = (N KF + N NaF )/N AlF3 , а для смеси KF-NaF-LiF-AlF3 КО = (NKF + NNaF + NLiF)/NAlF3. Влияние CaF2 на свойства криолитовых расплавов изучали на примере систем (KF-NaF-AlF 3 )-CaF 2 . При расчете КО этих смесей мольную концентрацию CaF2 не учитывали.
Температура ликвидуса
Для определения технологических параметров наиболее важным свойством электролита является температура ликвидуса, от величины которой зависит рабочая температура электрохимического процесса.
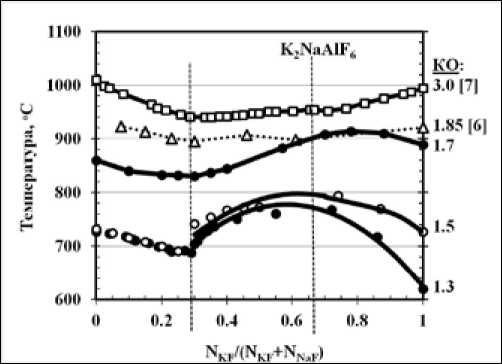
Рис. 1. Температура ликвидуса расплавов KF-NaF-AlF3 с различным КО
Температуру ликвидуса измеряли методом термоанализа, а также определяли по изменению сопротивления электролита при его охлаждении [5]. Разница значений температур, полученных двумя методами, не превышала 5 градусов.
Изменение температуры ликвидуса смешанных криолитовых расплавов KF-NaF-A1F3 в зависимости от соотношения концентраций KF и NaF в интервале КО 1,3-1,7 показано на рис. 1, где отражены также результаты, полученные в работах [6, 7] для смесей с КО=3 и 1,8.
Добавки NaF до 15 мас. % (область концентраций NKF/(NKF+NNaF)=0,67-1,0) к расплаву KF-A1F 3 с КО<1,7 существенно повышают температуру ликвидуса, тогда как такие же добавки NaF к калиевому криолиту с более высоким КО (1,8-3,0) ее понижают. Добавки KF к расплаву NaF-A1F 3 в области концентраций NKF/(NKF+NNaF)=0,0-0,3 понижают температуру ликвидуса расплавленных смесей при любых КО.
Для проведения низкотемпературного электролиза криолит-глиноземных электролитов интересны составы расплавов KF-NaF-A1F3 с высокой концентрацией KF и низким криоли-товым отношением. Для расчета температуры ликвидуса смешанных криолитовых расплавов KF-NaF-A1F3 в интервале КО 1,3-1,7 и соотношения концентраций фторидов щелочных металлов NKF/(NKF+NNaF)=0,3-1, с помощью компьютерной программы Origin выведено общее регрессионное уравнение :
Тлик = 2582.85-2488.7КО+2П- N- 655.9^ N 2 +
+868.9КО2 +420.97-КО- N ± 12, (1)
где Тлик - температура ликвидуса, К; N=NKF/(NKF+NNaF); KO=(NKF+NNaF)/NA1F3. Дисперсионный анализ проводили для уровня значимости 0,05. Коэффициент детерминации R2 = 0,95. Адекватность модели проверяли при сравнении ее с экспериментальными точками (рис. 2).
Растворимость оксида алюминия
Снижение температуры, безусловно, приводит к понижению растворимости оксида алюминия. Необходимо было найти такие составы электролитов, в которых растворимость оксида – 563 –
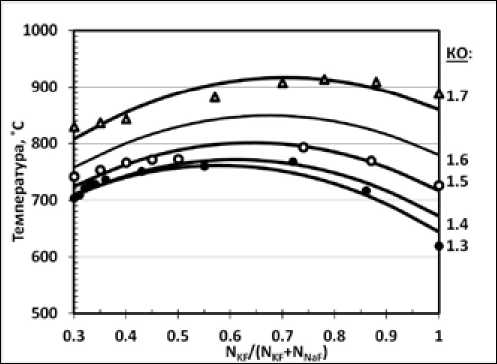
Рис. 2. Экспериментальные и рассчитанные по уравнению (1) значения температуры ликвидуса расплавов KF
-NaF-AlF3. Точки – эксперимент, линии – расчет алюминия составляет не менее 4 мас. %; ориентиром для такого выбора служила величина рабочей концентрации глинозема (2-4 мас. %) в традиционной промышленной ванне.
Растворимость оксида алюминия в криолитовых расплавах определяли методом изотермического насыщения с потенциометрическим контролем точки насыщения [8]. Максимальная относительная погрешность этого метода составляет 7,8 %.
Экспериментальные значения растворимости Al 2 O 3 в расплавах KF-AlF 3 и KF-NaF-AlF 3 (КО=1,3-1,5) с любым соотношением KF и NaF в температурном интервале от 800 °С до точки ликвидуса расплава соответствующего состава были обобщены регрессионным уравнением
S = –19.367 + 3.385 · КО + 0.015 · T + 3.494 · N ± 0.22, (2)
где S – растворимость глинозёма, мол. %; T – температура, К; N=NKF/(NKF+NNaF); КО=(NKF+NNaF)/ N AlF3 . Сравнение экспериментально определенной и рассчитанной по уравнению (2) растворимости оксида алюминия в расплавленных смесях KF-NaF-AlF3 при 800 °С представлено на рис. 3. Там же приведены данные по растворимости глинозема в смесях KF-NaF-AlF 3 с КО=1,3 при температуре 750 °С, полученные H. Yan [8]. Все результаты хорошо согласуются в электролитах с высокой концентрацией KF.
Добавки LiF в калиевый криолит с КО=1,3 и 1,5 снижают растворимость Al2O3 сильнее по сравнению с добавками NaF такой же концентрации (рис. 4). Это объясняется различием ионных потенциалов щелочных металлов. Катионы лития, имея значительно больший ионный потенциал (µ(Li+)=1,7), чем катионы натрия (µ(Na+)=1,01), прочнее связаны с ионом фтора в алюминий-фторидных комплексах, что приводит к осложнению процесса формирования алюминий-оксидно-фторидных комплексов при растворении Al 2 O 3 . Резкого падения растворимости глинозема с введением LiF не наблюдается, если его (в количестве не более 3 мас. %) добавлять в смешанные криолиты KF-NaF-AlF 3 .
Как известно, CaF2 добавляется в промышленный электролит главным образом для понижения температуры электролиза. Однако добавки CaF 2 понижают растворимость Al 2 O 3 в – 564 –
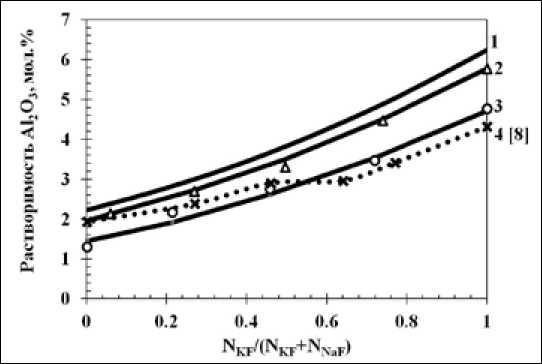
Рис. 3. Экспериментальные и рассчитанные по уравнению (2) значения растворимости Al2O3 в расплавах KF-NaF-AlF3 при 800 ° С. Точки - эксперимент, линии - расчет. КО: 1 - 1,6; 2 - 1,5; 3 - 1,3; 4 - 1,3 [8] (750 °С)
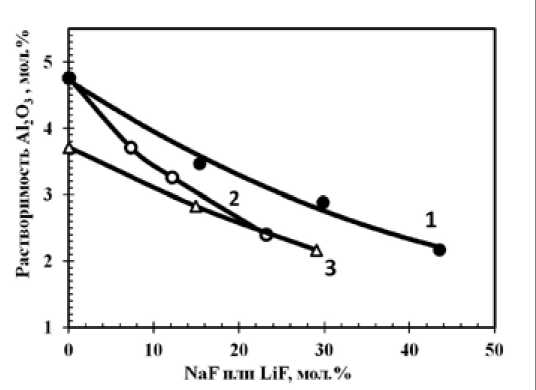
Рис. 4. Растворимость Al 2 O 3 при 800 °С в электролитах (КО=1,3): 1 – (KF-AlF 3 )-NaF; 2 – (KF-AlF 3 )-LiF; 3 – KF-NaF-LiF(3 мас. %)-AlF 3 (КО=1,3)
криолитах, что не является проблемой в условиях традиционного электролиза, поскольку рабочая концентрация Al2O3 гораздо ниже его растворимости. Но влияние CaF2 на растворимость Al 2 O 3 становится более заметным при проведении низкотемпературного электролиза, где концентрация Al2O3 близка к насыщению. Если растворимость Al2O3 в расплавах KF-NaF-AlF 3 повышается с увеличением содержания KF, то обратная тенденция наблюдается, если в расплавленную смесь добавлять CaF2 (рис. 5). Чем выше концентрации CaF2 и KF в расплаве (KF-NaF-AlF 3 )-CaF 2 , тем меньше растворимость в нём Al 2 O 3 . То есть в электролитах, основным компонентом которых служит калиевый криолит с низким КО, присутствие CaF2 нежелательно.
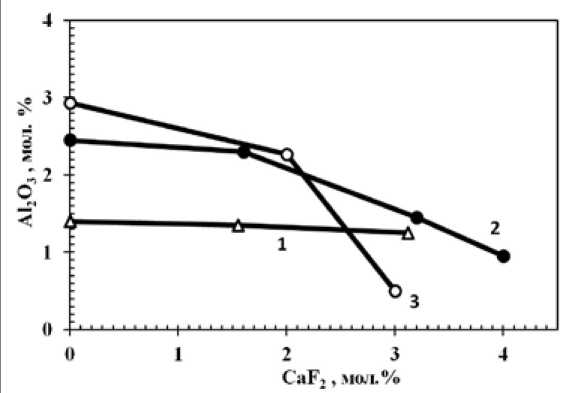
Рис. 5. Растворимость Al 2 O 3 в кальцийсодержащих электролитах (КО=1,3) при 850 °С: 1 – NaF-AlF 3 ; 2 – NaF-KF-AlF 3 c N KF /(N NaF +N KF )=0,21; 3 – NaF-KF-AlF 3 c N KF /(N NaF +N KF )=0,46
Электропроводность
С понижением температуры падает не только растворимость оксида алюминия, но и электропроводность, которая влияет на технологические аспекты производства, определяя тепловой баланс ванны и общие энергозатраты электрохимических процессов.
Метод измерения электропроводности фторидных и фторидно-оксидных расплавов заключался в комбинированном использовании ячеек с капилляром (BN) и с параллельными молибденовыми электродами [9]. Была учтена температурная зависимость константы ячеек, что обеспечило точность измерений электропроводности агрессивных расплавов в широком температурном интервале.
Электропроводность расплавов KF-NaF-AlF3 растет с увеличением концентрации NaF и КО. Эту зависимость в интервале от 800 °С до температуры ликвидуса расплава соответствующего состава можно описать уравнением lnκ = 3.44–2445.41/T– 2.219·NAlF3 + 0.501·NNaF ·0.6956·(NNaF)2 ± 0.011, (3)
где κ – удельная электропроводность, Ом-1.см-1; Т – температура, К; N NaF и N AlF3 – концентрации NaF и AlF3, мол. %.
Электропроводность смешанных KF-NaF-AlF 3 электролитов с КО 1,2-1,5 при температурах 750-820 °С исследовал J. Yang с соавторами [10]. Измерения проводили методом «постоянно меняющейся константы ячейки». Приведенные величины электропроводности имеют значения ниже полученных нами. Максимальное отклонение значений составляет менее 10 %. Такое расхождение можно объяснять погрешностью измерения используемых методик, а также качеством приготовленных солей.
Добавки LiF в большей степени увеличивают электропроводность KF-AlF 3 по сравнению с добавками NaF такой же концентрации (рис. 6). Если электропроводность расплава KF-NaF-AlF 3 от концентрации NaF представляет собой линейную зависимость, то электропроводность – 566 –
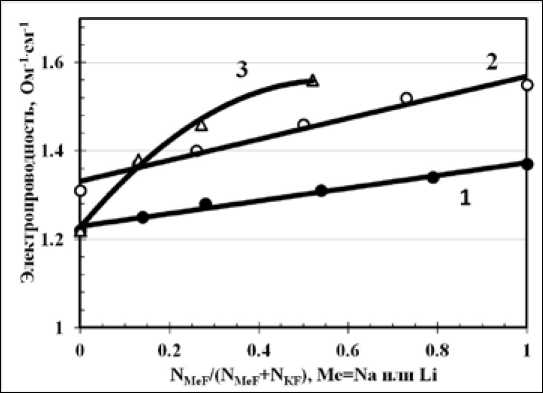
Рис. 6. Электропроводность расплавов при 800 °С: 1 – KF-NaF-AlF 3 (КО=1,3); 2 – KF-NaF-AlF 3 (КО=1,5); 3 – KF-LiF-AlF 3 (КО=1,3)
KF-LiF-AlF 3 описывается уже полиномом второй степени. Это связано с тем, что катионы Li+, основные переносчики заряда в этих электролитах, обладая высоким ионным потенциалом, образуют прочные электростатические связи с комплексными анионами расплава, тем самым теряя свою подвижность, что сказывается на величине электропроводности.
Исследование особенностей влияния Al 2 O 3 на удельную электропроводность калиевых, натриевых криолитовых расплавов и их смесей с низким КО в интервале температур 700-800 °С показало, что добавки Al 2 O 3 в расплавы с низким КО приводят к понижению электропроводности в меньшей степени, чем это происходит в электролитах с высоким КО.
Полученные данные для смешанных калий-натриевых глиноземсодержащих криолитов в зависимости от состава и температуры обобщены уравнением lnκ = 2.24 – 0,029∙NAl2O3+ 0.00296∙NNaF + 0.319∙КО – 2624.4/T ± 0.012, (4)
где κ – удельная электропроводность, Ом-1.см-1; N Al2O3 , N NaF – концентрации Al 2 O 3 и NaF, мол. %; КО=(NKF+NNaF)/NAlF3; T – температура, K. Уравнение (4) справедливо в области растворимости Al 2 O 3 при температурах от 800 °С до температуры ликвидуса соответствующего состава электролита.
Выбор электролита для низкотемпературного электролиза
Основываясь на физико-химических характеристиках смесей калиевого и натриевого криолитов, можно выбрать состав легкоплавкого электролита с оптимальными свойствами для проведения низкотемпературного электролиза глинозема. Главным показателем является достаточная растворимость глинозема в выбранном электролите при рабочей температуре электролиза. Необходимо учитывать, что все потенциальные добавки в расплав NaF-AlF3 уменьшают температуру первичной кристаллизации расплавленной смеси, однако все добавки к расплаву КF-AlF3 с КО < 1,7, исключая AlF3, повышают температуру ликвидуса. Принимая – 567 – это положение во внимание, все легкоплавкие криолитовые расплавы, электролиты – кандидаты для низкотемпературного получения алюминия, можно разделить на две группы:
-
1. Электролиты, основанные на натриевом криолите NaF-AlF3 с 1,7>КО>2,0 – интервал рабочих температур 800-900 °С;
-
2. Электролиты, основанные на калиевом криолите КF-AlF3 с 1,3>КО>1,7 – интервал рабочих температур 700-800 °С.
Минимальная температура, теоретически возможная для электролиза глинозема в исследуемых расплавах, 700 °С, которую может обеспечить электролит состава КF-AlF 3 с КО=1,3. Фторид натрия, вносимый вместе с глиноземом и постепенно накапливающийся в электролизной ванне, значительно повышает температуру ликвидуса калиевого криолита. Для того чтобы избежать этой проблемы, рекомендуются составы электролитов KF-NaF-AlF3 с КО=1,3-1,5, содержащие 12-15 мас. % NaF, поскольку возможное возрастание концентрации NaF приведет лишь к снижению температуры ликвидуса. Электролиты такого состава имеют растворимость глинозема не менее 4,5 мас. % в интервале температур 700-800 °С. При добавлении 1 мас. % Al2O3 температура ликвидуса расплавов КF-AlF3 и KF-NaF-AlF3 с КО=1,3 и 1,5 понижается, в среднем, на 3-4 градуса.
Электропроводность всех исследованных расплавов значительно ниже электропроводности промышленных электролитов, которая, как правило, составляет не менее 2,1 Ом-1·см-1. Добавка 12 мас. % NaF увеличивает электропроводность расплава KF-AlF3 (КО=1,3) на 6 %, а добавка LiF 3 мас. % (такое количество LiF кажется наиболее целесообразным для практики) к расплаву KF-AlF3 увеличивает электропроводность на 8 %. Обе добавки могут компенсировать снижение электропроводности, вызванное присутствием глинозема (4 мас. % Al 2 O 3 снижает электропроводность расплавов KF-NaF-AlF3 с КО=1,3 на 7 %).
Присутствие CaF 2 в легкоплавких электролитах на основе калиевого криолита нежелательно, так как он негативно влияет на температуру ликвидуса, электропроводность и растворимость глинозема в калийсодержащих расплавах.
При более высоком криолитовом отношении как электропроводность расплава, так и растворимость в нем Al 2 O 3 возрастают, но при этом существенно увеличивается температура ликвидуса и исчезает главное преимущество легкоплавких калиевых электролитов – возможность проводить электролиз в ячейках с инертными анодами при температуре ниже 800 °С.
Работа выполнена по интеграционному проекту УрО РАН 12-И-3-2056.


