Электронно-микроскопические особенности парафолликулярных клеток щитовидной железы крыс после 60-дневного введения тартразина и препарата мексидол®
Автор: Лузин В.И., Морозов В.Н.
Журнал: Саратовский научно-медицинский журнал @ssmj
Рубрика: Патологическая анатомия
Статья в выпуске: 2 т.19, 2023 года.
Бесплатный доступ
Цель: установить влияние чистого тартразина, вводимого в течение 60 суток, а также в комбинации с препаратом Мексидол® на структурные особенности парафолликулярных клеток щитовидной железы крыс на электронно-микроскопическом уровне. Материал и методы. Тридцать белых крыс-самцов массой 200-210 г разделены на пять групп по 6 крыс в каждой. I группа - контрольная; II и III группы - крысы в течение 60 суток получали тартразин в концентрации 750 и 1500 мг/кг; IV и V группы - в аналогичных условиях вводили Мексидол® из расчета 50мг/кг Качественные изменения парафолликулярных клеток изучали при помощи электронной микроскопии, а количественные - морфометрии. Результаты. После воздействия тартразина в цистернах гранулярной эндоплазматической сети выявлялось мелкозернистое или волокнистое содержимое, а в некоторых митохондриях - участки разрушенного матрикса. Отношение площадей эу- и гетерохроматина уменьшалось во II и III группах на 5,7 и 56,9% соответственно, а диаметр секреторных гранул - на 12,3 и 19% соответственно по сравнению с контролем. Отношение эу- и гетерохроматина в V группе увеличивалось на 79,6%, а диаметр секреторных гранул - на 8,2 и 6,5% в IV и V группах соответственно, по сравнению сданными II и III групп. Заключение. Введение тартразина в разных дозах в течение 60 дней вызывает дозозависимые качественные и количественные изменения ультраструктуры парафолликулярных клеток, а введение препарата Мексидол® на этом фоне вызывает уменьшение их выраженности.
Мексидол, морфометрия, парафолликулярные клетки, тартразин, ультраструктура, щитовидная железа
Короткий адрес: https://sciup.org/149143911
IDR: 149143911 | УДК: 591.147.1612.086.3]:613.29 | DOI: 10.15275/ssmj1902194
Electronic microscopic features of parafollicular cells of rat’s thyroid gland after 60 days introduction of tartrazine and mexidol®
Objective: To establish the effect of the administration of tartrazine for 60 days, as well as Mexidol® under these conditions, on the structural features of the parafollicular cells of the rat's thyroid gland at the electron microscopic level. Material and methods. Thirty white male rats weighing 200-210 g were divided into five groups six rats each. The Group I is the control; the Groups II and III - rats received tartrazine at a concentration of 750 and 1500 mg/kg for 60 days; the Groups IV and V - under similar conditions Mexidol® was administered at the rate of 50 mg/kg. Qualitative changes in parafollicular cells were studied using electron microscopy, and quantitative changes - by morphometry Results. The fine-grained or fibrous contents were detected in the cisterns of the rough endoplasmic reticulum, and areas of the destroyed matrix in some mitochondria after exposure to tartrazine. The ratio of area eu-chromatin/heterochromatin decreased in the Groups II and III by 5.7% and 56.9%, respectively, and the diameter of secretory granules - by 12.3% and 19%, respectively, compared with the Group I. The ratio of area euchromatin/heterochromatin increased by 79.6% in Group V, and diameter of secretory granules - by 8.2% and 6.5% in the Groups IV and V respectively, compared with the data of the Groups II and III. Conclusions. The introduction of tartrazine in different doses for 60 days causes dose-dependent qualitative and quantitative changes in the ultrastructure of parafollicular cells, and the introduction of Mexidol® against this background causes a decrease in their severity.
Текст научной статьи Электронно-микроскопические особенности парафолликулярных клеток щитовидной железы крыс после 60-дневного введения тартразина и препарата мексидол®
EDN: LZYKUY
-
1Введение. Тартразин является представителем азокрасителей, имеющим ярко-желтый или оранжевый цвет и хорошую растворимость в воде. Данная пищевая добавка обычно применяется в процессе изготовления продуктов питания, косметики, различных форм лекарственных средств [1]. Обладая насыщенным желтым или оранжевым цветом, тартразин улучшает привлекательность внешнего вида продукта, что пропорционально сопровождается увеличением к нему интереса со стороны покупателей и повышает прибыль для производителей.
Несмотря на то, что содержание тартразина в продуктах регламентируется нормативно-правовыми актами, остаются вопросы о безопасности его использования для здоровья человека. Имеются сведения о генотоксическом и тератогенном действиях тартразина [2, 3], его способности вызывать аллергические реакции (астма, сыпь) [4], изменения поведения у детей (гиперактивность в сочетании с дефицитом внимания), а также морфологии и биохимических маркеров почек и печени, головного мозга [5, 6].
Установлено то, что тартразин также оказывает влияние на метаболизм кальция в организме, увеличивая его внутритканевое содержание и уменьшая его концентрацию в крови [7]. Однако данных о морфологических изменениях парафолликулярных клеток щитовидной железы, которые вовлечены в регуляцию кальциево-фосфорного обмена, в литературе не содержится. Отсутствуют также сведения о возможных фармакологических путях коррекции изменений структурной организации данных клеток в условиях длительного введения тартразина. Учитывая, что одним из механизмов неблагоприятного воздействия тартразина является его способность выступать в роли прооксиданта, в качестве фармакокорректора выбран препарат Мексидол ® , обладающий, помимо прочих, антиоксидантными свойствами [8].
Цель — установить влияние чистого тартразина, вводимого в течение 60 суток, а также в комбинации с препаратом Мексидол® на структурные особенности парафолликулярных клеток щитовидной железы крыс на электронно-микроскопическом уровне.
Материал и методы. Для исследования использовано 30 белых половозрелых крыс-самцов массой 200–210 г. Животных распределили на пять групп по 6 крыс в каждой — четыре экспериментальных и одну контрольную. I группа (К) — контрольная, сформирована из животных, которым внутрижелу-дочно вводили физиологический раствор. Во II группе (Т1) лабораторные животные подвергались 60-суточному воздействию тартразина (в концентрации 750мг/кг) путем его зондового введения; в III группе
(Т2) — аналогичному воздействию, но в удвоенной концентрации (1500 мг/кг). IV и V группы были сформированы для установления эффективности использования препарата Мексидол® для коррекции неблагоприятного воздействия пищевой добавки. С этой целью крысам IV группы (Т1+М) внутримышечно вводили 1 мл 5%-го раствора Мексидол ® в дозе 50 мг/кг в течение 60-суточного воздействия тартразина в дозе 750 мг/кг, а в V группе Мексидол ® (Т2+М) назначался на фоне аналогичного срока действия тартразина в дозировке 1500 мг/кг массы тела (компания-производитель тартразина — Roha Dyechem Pvt Ltd, India; Мексидол ® — общество с ограниченной ответственностью — медицинский центр «Эллара» по заказу научно-производственной компании «Фармасофт», Москва, Россия). Все действия персонала с лабораторными животными в ходе эксперимента, уход за ними в условиях вивария были в соответствии с правилами, установленными Европейской конвенцией по защите животных, используемых в фундаментальных исследованиях [9]. Протокол исследования утвержден на заседании комиссии по биоэтике ГУ ЛНР «Луганский государственный медицинский университет им. Святителя Луки», протокол №2 от 25.03.2022. После завершения срока эксперимента животных выводили из исследования методом декапитации. Обработка кусочков щитовидной железы происходила в соответствии с стандартным протоколом электронномикроскопического исследования [10], после чего срезы железы фотографировались и подвергались анализу. В компьютерной программе Nis-Elements BR 4.60.00 (Nikon Corporation, Japan) осуществляли измерения площади ядер парафолликулярных клеток, площадей эу- и гетерохроматина и высчитывали их соотношение. В цитоплазме клеток проводили замеры диаметров секреторных гранул и средней площади митохондрий. Обработку данных осуществляли с помощью компьютерных программ Statistica 10.0 (StatSoft Inc., USA) и Microsoft Office Excel 2017 (Microsoft, USA) (рассчитывали среднее, стандартную ошибку среднего, медиану). Для оценки типа распределения признаков использовали критерий Шапиро — Уилка. В случаях нормального распределения, а также равенства дисперсий, для сравнения средних использовали Т -критерий Стьюдента. Равенство дисперсий оценивали по F -критерию Фишера. В случае распределений, не соответствующих нормальному закону, а также при неравенстве дисперсий использовали непараметрический U -критерий Манна — Уитни. Статистически значимыми считали различия при p <0,05.
Результаты. Парафолликулярные клетки щитовидной железы половозрелых крыс контрольной группы имеют типичное строение. После воздействия тартразина первой концентрации (750 мг/кг/массы тела) парафолликулярные клетки щитовидной железы были крупных размеров, вытянутой формы.
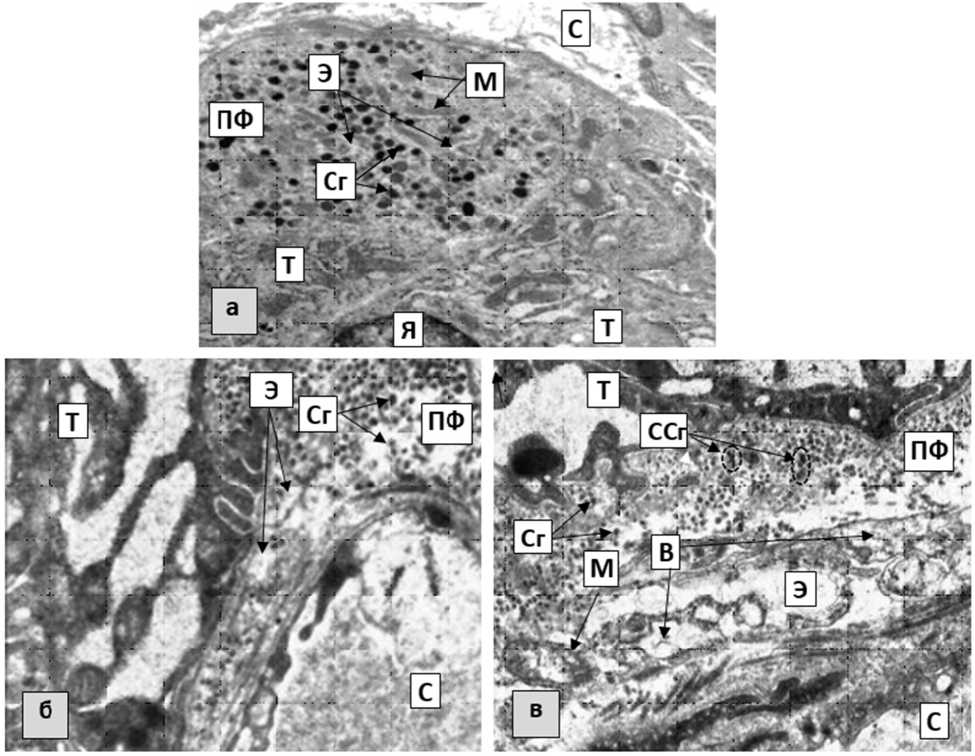
Рис. 1. Участки щитовидной железы половозрелых крыс:
а — контрольная группа, б — экспериментальная группа, принимающая тартразин в концентрации 750мг/кг/массы тела, в — экспериментальная группа, принимающая тартразин в концентрации 1500мг/кг/массы тела: Т — тироцит, ПФ — парафолликулярная клетка, Я — ядро, Э — шероховатая эндоплазматическая сеть, М — митохондрии, Сг — секреторные гранулы, ССг — электронно-плотные скопления секреторных гранул, В — единичные волокнистые структуры, С — сосуд. Увеличение х 12000
Ядро содержало скопления гетерохроматина преимущественно под кариолеммой. Участки гранулярной эндоплазматической сети были неравномерно расширены с мелкозернистым содержимым умеренной электронной плотности. Митохондрии имели овальную форму, с умеренным электронно-плотным содержимым. Секреторные гранулы были многочисленны, преимущественно мелкие, разной электронной плотности, неравномерно распределялись в цитоплазме клетки (рис. 1).
При использовании тартразина удвоенной концентрации (1500 мг/кг/массы тела) парафолликулярные клетки имели крупные размеры и вытянутую форму. Ядро содержало скопления гетерохроматина, который располагался на периферии ядра, а также в виде глыбок в центральных участках кариоплазмы. В цитоплазме цистерны гранулярной эндоплазматической сети были неравномерно расширены. В некоторых участках в просветах канальцев встречались единичные волокнистые структуры разной ориентации и расположенные рыхло друг к другу. Митохондрии имели овальную форму и умеренную электронную плотность. Некоторые из них содержали электронно-светлые участки неправильной формы с разрушенным содержимым. Секреторные гранулы были многочисленными, преимущественно мелкими, разной электронной плотности, неравномерно распределенными в цитоплазме клетки. Некоторые из них располагались очень близко друг к другу, поэтому выглядели в виде электронно-плотных скоплений.
При измерениях структурных компонентов парафолликулярных клеток во II группе было выявлено то, что площадь ядра была меньше аналогичного показателя контрольной группы на 20,5%, площадь, занимаемая эухроматином, — на 22,3%, гетехрома-тином — на 17,5%, а соотношение площадей эух-роматина и гетехроматина — на 5,7%. В III группе площадь ядра уменьшалась на 28,7%, площадь, занимаемая эухроматином, — на 52,1%, соотношение площадей эухроматина и гетехроматина — на 56,9%, а площадь гетехроматина — напротив, возрастала на 11,1%. Диаметр секреторных гранул в цитоплазме парафолликулярных клеток во II и III группах был меньше, чем у крыс контрольной группы, на 12,3 и 19% соответственно, а средняя площадь митохондрий в цитоплазме — на 15,8 и 24,8% соответственно (таблица).
Морфометрические показатели парафолликулярных клеток щитовидной железы крыс контрольной и экспериментальных групп, M±m
|
Показатели |
Группа |
||||
|
I |
II |
III |
IV |
V |
|
|
Площадь ядра, мкм2 |
14,28±0,16 |
11,36±0,21* |
10,19±0,11* |
12,25±0,14 ‣ |
11,11±0,20 ‣ |
|
Площадь, занимаемая эухрома-тином, мкм2 |
9,00±0,10 |
7,00±0,10* |
4,32±0,07* |
7,59±0,09 ‣ |
6,32±0,09 ‣ |
|
Площадь, занимаемая гетерохроматином, мкм2 |
5,28±0,08 |
4,36±0,08* |
5,87±0,07* |
4,66±0,07 ‣ |
4,79±0,09 ‣ |
|
Соотношение площадей эу- и гетерохроматина |
1,70±0,0098 |
1,61±0,0078* |
0,74±0,0032* |
1,63±0,0061 |
1,32±0,0053 ‣ |
|
Диаметр секреторных гранул, нм |
161,58±1,92 |
141,71±1,70* |
130,85±1,90* |
153,38±1,94 ‣ |
139,33±1,58 ‣ |
|
Средняя площадь митохондрий, мкм2 |
10,03±0,14 |
8,45±0,18* |
7,54±0,18* |
9,14±0,08 ‣ |
8,21±0,10 ‣ |
П р и м еч а н и е : * — достоверное отличие показателей II и III групп от контрольных значений; ‣ — достоверное отличие параметров IV и V групп от показателей II и III групп соответственно.
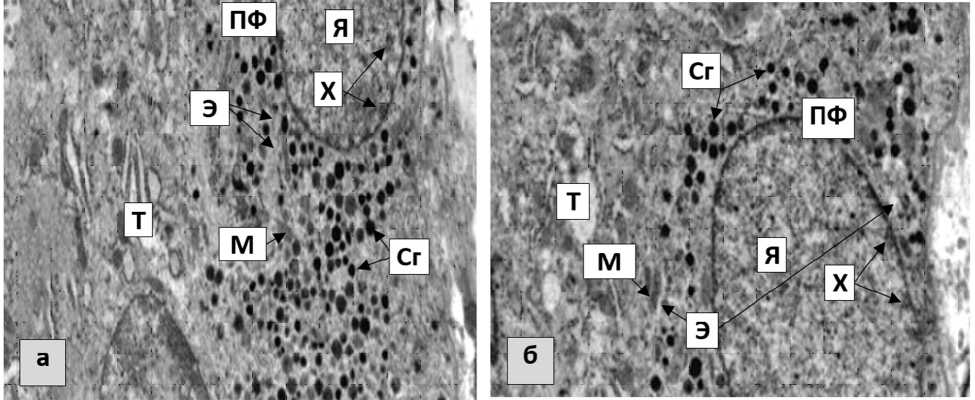
Рис. 2. Участки щитовидной железы половозрелых крыс:
а — экспериментальная группа животных, получавшая Мексидол ® после воздействия тартразина в концентрации 750 мг/кг/массы тела, б — экспериментальная группа животных, получавшая Мексидол ® после воздействия тартразина в концентрации 1500мг/кг/массы тела: Т — тироцит, ПФ — парафолликулярная клетка, Я — ядро, Х — гетерохроматин, Э — шероховатая эндоплазматическая сеть, М — митохондрии, Сг — секреторные гранулы. Увеличение х 12000
После воздействия Мексидол ® у животных, получавших тартразин в концентрации 750мг/кг/массы тела, наблюдалось приближение морфологических особенностей строения парафолликулярных клеток щитовидной железы к таковым у контрольной группы. Клетки были крупных размеров, овальной формы. Вытянутое или круглое ядро имело небольшие глыбки хроматина в кариоплазме. В цитоплазме гранулярная эндоплазматическая сеть образовывала уплощенные цистерны с содержимым средней электронной плотности, определялось умеренное количество преимущественно овальных митохондрий. Многочисленные секреторные гранулы разных размеров, электронной плотности занимали околоя-дерную и базальную части клетки.
После воздействия Мексидол® у животных, получавших тартразин в концентрации 1500мг/кг/массы тела, также наблюдалось частичное нивелирование морфологических изменений парафолликулярных клеток щитовидной железы. Сохранялись участки гранулярной эндоплазматической сети с расширенными цистернами, выявлялись одиночные или расположенные группами, разного размера секреторные гранулы в цитоплазме (рис. 2).
В IV и V группах использование Мексидол ® в качестве корректора позволило уменьшить выраженность изменений морфометрических параметров парафолликулярных клеток щитовидной железы крыс. В IV группе площадь ядра была больше аналогичного параметра группы без введения Мексидол® на 7,8%, площадь, занимаемая эухроматином, — на 8,5%, а площадь, занимаемая гетехроматином, и соотношение площадей эу- и гетерохроматина — статистически значимо не изменялись. В V группе площадь ядра увеличилась на 9%, площадь, занимаемая эухроматином, — на 46,5%, площадь, занимаемая гетехроматином, уменьшилась на 18,7%, а соотношение площадей эу- и гетерохроматина было больше на 79,6%. Диаметр секреторных гранул и средняя площадь митохондрий в цитоплазме парафолликулярных клеток возрастали, по сравнению с данными групп без введения препарата Мексидол ® ,
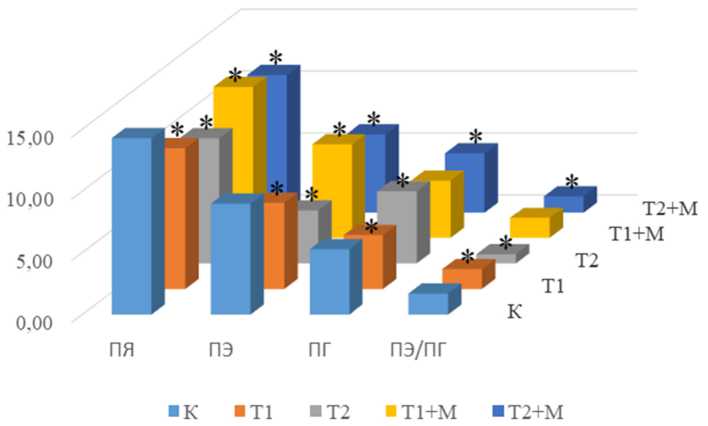
Рис. 3. Параметры ядра парафолликулярных клеток:
ПЯ — площадь ядра, ПЭ — площадь, занимаемая эухроматином, ПГ — площадь, занимаемая гетерохроматином, ПЭ/ПГ — соотношение площадей эу- и гетерохроматина
180.00
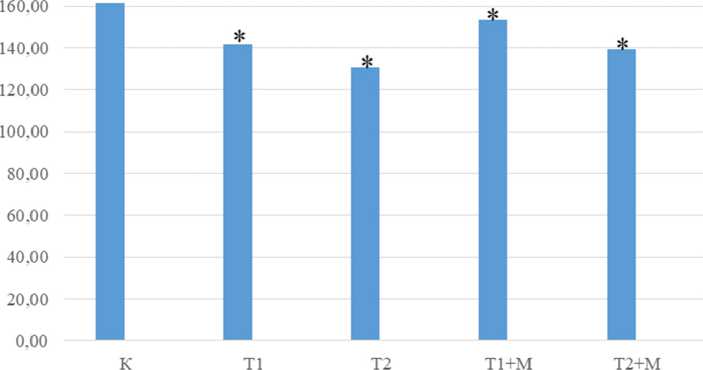
Рис. 4. Изменения диаметра секреторных гранул в цитоплазме парафолликулярных клеток, нм
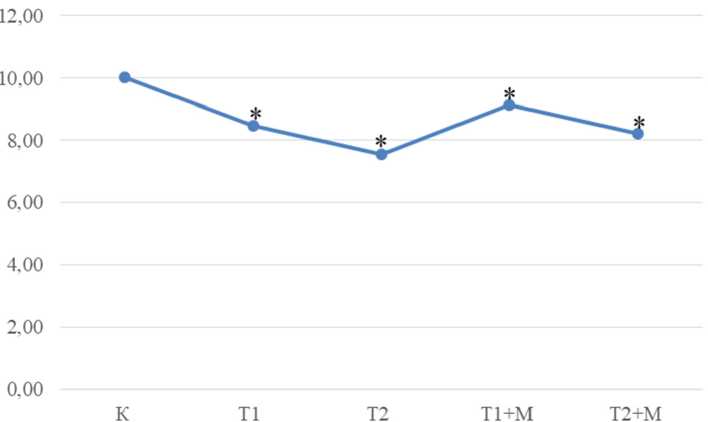
Рис. 5. Изменения средней площади митохондрий в цитоплазме парафолликулярных клеток, мкм2
на 8,2; 6,5% и на 8,1; 8,8% в IV и V группах соответственно (рис. 3, 4, 5).
Обсуждение. Парафолликулярные клетки (каль-цитониноциты) щитовидной железы контрольной группы половозрелых крыс имеют сходные морфологические особенности строения с данными, полученными J. Dadan с соавт. [11].
Использование тартразина вызывало дозозависимые изменения парафолликулярных клеток щитовидной железы половозрелых крыс (значительное скопления гетерохроматина под кариолеммой, неравномерно расширенные цистерны гранулярной эндоплазматической сети, в некоторых случаях с волокнистыми структурами разной ориентации, мелкие гранулы разной электронной плотности, в ряде случаев расположенные в виде скоплений и наличие единичных митохондрий с поврежденными кристами). По результатам исследования G. E. El-Desoky с соавт., тартразин снижает уровень глутатионпероксидазы, супероксиддисмутазы, увеличивает количество маркеров оксидативного стресса, одним из основных последствий которого, по данным С. P Gonzalez-Hunt, M. Wadhwa, L. H. Sanders, является повреждение генетического материала [12, 13]. Так, согласно исследованиям 2019 г. S. Shakoor с со-авт., тартразин оказывает генотоксический эффект в клетках нервной, соединительной и эпителиальной тканей, что может нарушать синтез белка и выведение его из канальцев и вызывает так называемый стресс эндоплазматической сети [14], таким образом оказывая действие непосредственно на парафолликулярные клетки. Необходимо также отметить: по данным S. Shakoor с соавт. 2022 г., использование пищевого красителя достоверно уменьшает уровень трийодтиронина (Т3) и тироксина (Т4) у экспериментальных крыс, что косвенно свидетельствует о гипофункции тироцитов [15]. При этом в работах J. Dadan с соавт., а также А. М. Махмурова, М. А. Юлдашевой, А. Ю. Юлдашева обращено внимание на однонаправленные ультрамикроскопические изменения ти-роцитов и парафолликулярных клеток щитовидной железы экспериментальных животных, что указывает на паракринное воздействие одних клеток на другие [11, 16]. Согласно материалам L. Alioui с соавт. [17] употребление тартразина уменьшает уровень свободного кальция, а также, исходя из результатов исследования M. Cemek с соавт., повышает уровень тканевого кальция в печени экспериментальных животных, что может снижать эндогенный синтез кальцитонина [6]. Анализ изложенных данных литературы позволяет объяснить то, что выявленные ультрами-кроскопические особенности парафолликулярных клеток щитовидной железы крыс после воздействия тартразина связаны со снижением функциональной активности данных клеток путем прямого механизма действия препарата на клетки, опосредованно — через воздействие на уровень кальция в крови и тканях, а также паракринно — через влияние тироцитов на парафолликулярные клетки.
После воздействия препарата Мексидол® наблюдается позитивная дозозависимая динамика (чем меньше концентрация тартразина, воздействующего на организм, тем более выражена позитивная динамика изменений в строении парафолликулярных клеток) изменений морфологической картины в сторону приближения структурных особенностей парафолликулярных клеток к контрольным значениям. По данным А. В. Щулькина, Мексидол® способен снижать уровень маркеров оксидативного стресса (в частности малонового диальдегида, нейтрализовать продукты перекисного окисления липидов), повышать активность глутатионпероксидазы, а также препарат способен проникать в митохондриальный матрикс и связывать активные формы кислорода, таким образом оказывая антиоксидантный и анти-гипоксический эффекты [8]. Данные материалы позволяют предположить то, что антиоксидантный эффект указанного препарата позволяет снизить генотоксический эффект и нивелировать оксидатив-ный стресс, вызванный использованием тартразина в разных концентрациях на клетки щитовидной железы крыс, что соответственно частично или полностью позволяет восстановить биосинтез белка и синтез секреторных гранул с гормоном.
Выводы.
Список литературы Электронно-микроскопические особенности парафолликулярных клеток щитовидной железы крыс после 60-дневного введения тартразина и препарата мексидол®
- Kobun R, Shafiquzzaman S, Sharifudin MS. Review of extraction and analytical methods for the determination of tart-razine (E 102) in foodstuffs. Crit Rev Anal Chem. 2017; 47 (4): 309-24. DOI: 10.1080/10408347.2017.1287558.
- Khayyat L, Essawy A, Sorour J, et al. Tartrazine induces structural and functional aberrations and genotoxic effects in vivo. Peer J. 2017; (5):e3041. DOI: 10.7717/peerj.3041.
- Ovalioglu АО, Ovalioglu TC, Canaz G, et al. Effects of tartrazine on neural tube development in the early stage of chicken embryos. Turk Neurosurg. 2020; 30 (4): 583-7. DOI: 10.5137/1019-5149. JTN.28793-19.6.
- Matsyura O, Besh L, Besh O, et al. Hypersensitivity reactions to food additives in pediatric practice: two clinical cases. Georgian Med News. 2020; (307): 91-5.
- Bhatt D, Vyas K, Singh S, et al. Tartrazine induced neu-robiochemical alterations in rat brain sub-regions. Food Chem Toxicol. 2018; (113): 322-7. DOI: 10.1016/j.fct.2018.02.011.
- Cemek M, Buyukokuroglu ME, Sertkaya F, et al. Effects of food color additiveson antioxidant functions and bioel-ement contents of liver, kidney and brain tissues in rats. Journal of Food and Nutrition Research. 2014; 2 (10): 686-91. DOI: 10.12691/jfnr-2-10-6.
- Albasher G, Maashi N, Alfarraj S, et al. Perinatal exposure to tartrazine triggers oxidative stress and neurobehavioral alterations in mice offspring. Antioxidants (Basel). 2020; 9 (1): 53. DOI: 10.3390/antiox9010053.
- Schulkin AV. Mexidol: modern aspects of the pharmaco-kinetics and pharmacodynamics. Farmateka. 2016; s4: 65-71.
- European convention for the protection of vertebrate animals used for experimental and other scientific purpose: Council of Europe 18.03.1986. Strasbourg, 1986; 52 p.
- Reynolds ES. The use of lead citrate at high pH as an electron opaque stain in electron microscopy. J Cell Biol. 1963; 17(1): 208-12. DOI: 10.1083/jcb.17.1.208.
- Dadan J, Zbucki R, Andrzejewska A, et al. Activity of thyroid parafollicular (C) cells in rats with hyperthyroidism — preliminary ultrastructural investigations. Roczniki Akademii Medycznej w Biatymstoku. 2004; 49 (1): 132-4.
- El-Desoky GE, Wabaidur SM, AlOthman ZA, et al. Regulatory role of nano-curcumin against tartrazine-induced oxidative stress, apoptosis-related genes expression, and genotoxicity in rats. Molecules. 2020; 25 (24): 5801. DOI: 10.3390/mole-cules25245801.
- Gonzalez-Hunt CP, Wadhwa M, Sanders LH. DNA damage by oxidative stress: Measurement strategies for two genomes. Current Opinion in Toxicology. 2018; (47): 87-94. DOI: 10.1016/j.cotox.2017.11.001.
- Shakoor S, AN F, Ismail A, et al. Toxicity of tartrazine, curcumin and other food colorants; possible mechanism of adverse effects. Online Journal of Veterinary Research. 2019; 23 (6): 466-86.
- Shakoor S, Ismail A, Rahman Z, et al. Impact of tartrazine and curcumin on mineral status, and thyroid and reproductive hormones disruption in vivo. International Food Research Journal. 2022; 29 (1): 186-99. DOI: 10.47836/ifrj. 29.1.20.
- Махмуров A.M., Юлдашева M.A., Юлдашев А.Ю. Ультраструктура клеток фолликулов щитовидной железы при гипо- и гиперкальциемии. Вестник экстренной медицины. 2019; 12 (2): 55-60.
- Alioui L, Mehedi N, Youcef В, et al. Tartrazine induced oxidative damage in mice liver and kidney. South Asian Journal of Experimental Biology. 2017; 7 (6): 271-8. DOI: 10.38150/sajeb. 7(6).


