Эмбриогенез в культуре микроспор брокколи
Автор: Домблидес Е.А., Козарь Е.В., Шумилина Д.В., Заячковская Т.В., Ахраменко В.А., Солдатенко А.В.
Журнал: Овощи России @vegetables
Рубрика: Селекция и семеноводство сельскохозяйственных растений
Статья в выпуске: 1 (39), 2018 года.
Бесплатный доступ
Изучен процесс эмбриогенеза и отработаны элементы технологии получения удвоенных гаплоидов брокколи B. oleracea L convar. botryts L) Alef. var. italica Plenck в культуре микроспор in vitro. Было выявлено, что успешное развитие эмбриоидов происходит из микроспор, изолированных из бутонов длиной 4 и 5 мм, где преимущественно содержатся микроспоры - на поздней вакуолизированной, пыльца - на ранней двухклеточной стадии развития. Оптимальным режимом температурной обработки является обработка 32°С в течение первых 2-х суток после введения в культуру. Эмбриоиды были получены из пяти образцов брокколи: Arcadia F1, Everest, Green Valiant, Marathon F1, Furio. Наибольший выход эмбриоидов был получен у образца Green Valiant, где он составил до 140 эмбриоидов на чашку Петри, а наименьший - у Furio (до 3 эмбриоидов/чашку Петри). Первые деления в культуре микроспор у всех образцов наблюдали уже на 2-3 сутки культивирования. Дальнейшее развитие эмбриоидов шло по двум направлениям -путем прямого развития или с образованием суспензороподобных структур. Эмбриоиды, содержащие суспензор, развивались медленнее, чем бессуспензорные. Мы наблюдали образование эмбриоида не только на дистальном (по отношению к микроспоре) конце суспензороподобной структуры, но и образование цепочки из эмбриоидов, а также все возможные близнецовые комбинации эмбриоидов. Было показано, что метод получения эмбриоидов в культуре микроспор in vitro может быть использован не только для получения удвоенных гаплоидных растений, но и служить моделью для фундаментальных исследований по изучению этапов развития зиготических эмбриоидов и суспензоров.
Эмбриогенез, культура микроспор, dh-растения, суспензороподобные структуры, брокколи
Короткий адрес: https://sciup.org/140223741
IDR: 140223741 | УДК: 635.356:581.33
Embryogenesis in culture of isolated microspore of broccoli
The process of embryogenesis and technological experimental protocol has been studied and applied to produce doubled haploid plants from microspore cultured in vitro in broccoli B. oleracea L. convar. botrytis (L.) Alef. var. italica Plenck. It was shown that successful embryoid development occurred from microspore isolated from buds 4-5 mm long, containing microspores at late vacuolated stage and pollen grain at twocell stage. The optimal temperature of treatment was 32 C° within 2 days after culture was launched. The embryoids were produced from the following broccoli accessions: Arcadia F1, Everest, Green Valiant, Marathon F1, and Furio. The highest embryoid yield was obtained from accession Green Valiant, and consisted of 140 embryoids per Petri dish, whereas the lowest yield was in Furio, up to 3 embryoids per Petri dish. The first microspore division was observed in all accessions in 2-3 days of cultivation. Further development of embryoids went either directly into usual embryoid or into suspensor-like structures. The embryoids with suspensor developed more slowly than embryoids without one. We observed the embryoid formation not only at distal end towards microspore originated the suspensor-like structure but also the formation of chain of embryoids, and all variation of twin embryoid combinations. The study of process of embryogenesis in isolated microspores in vitro showed that this method can be used both to produce doubled haploid plants and study the developmental stages of zygotic embryos and suspensors.
Текст научной статьи Эмбриогенез в культуре микроспор брокколи
Капуста брокколи в последнее время становится все более востребованной у потребителей благодаря своему богатому биохимическому составу и большой питательной ценности. Ее используют в качестве диетического и лечебно- профилактического продукта. Потребительский спрос в условиях современного рынка постоянно растет и меняется. Это создает необходимость наличия у селекционера генотипически разнообразного и стабильного материала, который позволит быстро удовлетворять требования современного производства. Решение этой проблемы возможно за счет применения биотехнологических методов в создании новых высокопродуктив- ных сортов и гибридов. Наиболее сложным, трудоемким и продолжительным звеном в процессе создания гибридов F1 является выведение константных родительских линий, на создание которых уходит от 6 до 12 лет при использовании традиционных методов селекции. В большинстве развитых стран в настоящее время для ускорения селекции широко используются технологии получения удвоенных гаплоидов (DH-технологии) (Dunwell, 2010), что позволяет ускорить селекционный процесс, создавая выровненные линии за 1-2 года. Основные методы получения гаплоидов, их классификация рассмотрены в ряде обзоров (Maluszynski et al., 2003; Dunwell, 2010; Asif, 2013). Одной из самых востребованных технологий, использующейся для ускорения селекционного процесса, является культура изолированных микроспор in vitro. Изолированные микроспоры при определенных условиях (оптимальная комбинация условий культивирования и стрессового воздействия) могут быть переведены с нормального гаметофитного пути развития на спорофитный, образуя при этом эмбриоиды, переходящие в гаплоиды (Hs) или в удвоенные гаплоиды (DH-растения). Отсутствие в культуре микроспор соматических тканей позволяет не ставить под сомнение происхождение полученных растений. Первые успешные исследования по культуре микроспор капустных культур проведены в начале 1980-х годов (Lichter, 1982). Позднее был разработан базовый протокол культуры микроспор рапса, который служит основой DH-технологии для растений рода Brassica L. (Pechan, Keller, 1988). Число работ, касающихся разработки DH-технологии для капусты брокколи, незначительно, несмотря на то, что эта разновидность капусты считается наиболее отзывчивой к андрогенезу (Arnison et al., 1990; Takahata, Keller, 1991; Chauvin et al., 1993; Takahata et al., 1993; Farnham et al., 1998; Dias,1999; Gu et al., 2004).
Целью наших исследований являлось изучение процесса эмбриогенеза в культуре микроспор брокколи для создания эффективной технологии получения удвоенных гаплоидов у этой культуры.
Материалы и методы Растительный материал и условия выращивания донорных растений
В работе использовали сортооб-разцы брокколи, переданные из коллекции ФГБНУ «Федеральный исследовательский центр
Всероссийский институт генетических ресурсов растений имени Н.И. Вавилова» (табл.).
Донорные растения выращивали в климатической камере при режиме 19°С круглосуточно, 16 час день/8 час ночь, освещение – 9000 люкс.
При отборе бутонов проводили цитологическое исследование стадий развития микроспор. Для визуализации микроспор и пыльцы использовали методику дифференциального окрашивания (Alexander,
1969) и микроскоп Axio Imager А2, с помощью которых определяли зависимость между размером бутона и стадией развития микроспор.
Культура микроспор
Бутоны собирали с растений, находящихся на начальной стадии цветения, и стерилизовали 30 с в 96% этаноле, затем в течение 5 мин в 50% водном растворе коммерческого препарата «Белизна» с добавлением Твина-20 (1 капля на 100 мл), с последующим трехкратным промыванием в стерильной дистиллированной воде.
Стерильные бутоны помещали в ½ NLN среду (Lichter, 1982) с 13%-содержанием сахарозы и PH 5,8 из расчета 30 бутонов на 6 мл среды. В пробирку также помещали стерильный магнит, после чего на магнитной мешалке проводили измельчение бутонов. Суспензию микроспор фильтровали через нейлоновый фильтр с размером ячеек 40 μm и осаждали 5 мин на центрифуге типа Eppendorf 5804R (Германия) при 125 g. Осадок с микроспорами ресуспендировали в ½ NLN среде и повторяли центрифугирование. Промывку микроспор проводили дважды.
В каждую чашку Петри до разлива жидкой среды вносили по 250 мкл автоклавированной 1% суспензии активированного угля в 0,5% агарозе. После выделения и промывки микроспоры из 5 бутонов помещали в чашки Петри диаметром 6 см с питательной средой вышеуказанного состава (5 мл), в которой они инкубировались при 32°С в темноте в течение двух суток, далее инкубация проходила при 25°С в темноте до образования эмбриоидов.
Получение растений-регенерантов
Появившиеся эмбриоиды на семядольной стадии (cotyledonstage) своего развития, помещали в чашки Петри на среду В-5 (Gamborg, 1968), содержащую 2% сахарозу и 7,0 г/л агара. Для образования вторичных эмбриоидов экспланты переносили на среду ½ МС (Murashige and Skoog, 1962) с 2% сахарозы, 0,1 мг/л бензиламинопурина (БАП) и 3,0 г/л фитогеля. Образовавшиеся побеги и эмбриоиды отделяли и переносили на среду МС с 2% сахарозы и 3,0 г/л фитогеля. Культивирование проводили на стеллажах с люминесцентными лампами при 25°С и фотопериоде 14 часов, освещенности 2,5 тыс. люкс.
Выращивание растений-регенерантов Растения с нормально развитыми листьями и корневой системой переносили в вегетационные сосуды, заполненные смесью торфа и перлита (7:3), накрывали перфори- рованными пластиковыми стаканчиками для адаптации растений к условиям in vivo. Выращивали растения-регенеранты в тех же условиях, что и донорные растения.
Результаты
Одним из важнейших факторов, влияющих на эмбриогенез в культуре микроспор, является определение оптимальной для введения в культуру in vitro стадии развития мужского гаметофита. Известно, что у растений рода Brassica способностью перехода с гаметофитно-го пути на спорофитный обладают микроспоры поздней одноклеточной стадии и пыльцевые зерна на ранней двухклеточной стадии развития (Pechan, Keller, 1988; Baillie et al., 1992; Telmer et al., 1992; Kott, 1998). Методом дифференциального окрашивания микроспор и последующего анализа фазы развития была изучена зависимость между стадией развития микроспоры/пыльцы и размером бутона капусты брокколи (рис.1.). Известно, что в бутонах одного размера в пыльниках одновременно содержатся микроспо-ры/пыльца на разных стадиях развития, однако преимущественное количество обычно занимают две близлежащие стадии. Было выявлено, что в бутонах 4-5 мм содержатся микроспоры на поздней вакуализи-рованной и ранней двухклеточной стадии развития. На образце Arcadia F1 при введении в культуру мы использовали бутоны от 3 до 6 мм. Было выявлено, что в вариантах, где микроспоры были изолированы из бутонов длиной 4 и 5 мм происходило успешное развитие эмбриоидов, причем из бутонов 4 мм эмбриоидов образовывалось практически в пять раз больше, чем из бутонов 5 мм (11,2±1,78 и 2±0,35 эмбриоидов/на чашку Петри соответственно). Из микроспор на ранней стадии развития (3 мм) и двухклеточной пыльцы (6 мм) регенерации эмбриоидов не происходило. Полученные данные согласуются с литературными данными. Определение зависимости между развитием микроспор и длиной бутона позволило в дальнейших опытах использовать микроспоры на наиболее восприимчивой стадии развития, проводя отбор бутонов по длине.
К числу важных факторов, способных вызывать индукцию эмбриогенеза у представителей рода Brassica , относится тепловая обработка микроспор в чашках Петри сразу после введения в культуру in vitro . Чаще всего для этой цели используют тепловые режимы от 32°С до 40°С с различной временной экспозицией (от 1 до 10 суток) (Шмыкова и др., 2015). Эффективность индукции эмбриогенеза зависит от генотипа, температуры и времени воздействия. В
Таблица. Количество образовавшихся эмбриоидов у образцов брокколи Table. The number of embryoids developed in accessions of broccoli
Выход эмбриоидов достаточно сильно отличался у различных генотипов (табл.1). Наибольший выход эмбриоидов из бутонов размером 4±0,5 мм был получен у образца Green Valiant, где он составил до 140 эмбриоидов на чашку Петри, а наименьший – у Furio (до 3 эмбриои-дов/чашку Петри). Первые деления в культуре микроспор у всех образцов наблюдали уже на 2-3 сутки культивирования. Дальнейшее развитие эмбриоидов шло по двум направлениям – путем прямого развития или с образованием суспензороподобных структур. Второй путь развития наблюдался чаще всего в культуре микроспор образцов Green Valiant и Marathon F1, у которых был отмечен наибольший выход эмбриоидов, причем развитие эмбриоидов у этих двух генотипов происходило по двум путям одновременно.
Изучению процесса развития эмбриоида в процессе эмбриогенеза в культуре микроспор in vitro уделяется в последнее время большое значение, поскольку именно во время перехода эмбриоида от недифференцированной глобулярной стадии развития к сердечковидной и торпедовидной происходит потеря эффективности у большинства опубликованных протоколов. Эксперименты на модельных культурах микроспор (рапс) выявили некоторые факторы (различные регуляторные белки, ауксины, гибберели-новая кислота и другие фитогормоны), которые напрямую или опосредовано вовлечены в развитие эмбриоидов из микроспор (Prem et al., 2012). Многие из них играют общую роль как при эмбриогенезе in vitro , так и во время зиготического эмбриогенеза, где их синтез или регуляция опосредована эндоспермом или другими тканями завязи и семени. Образование и развитие
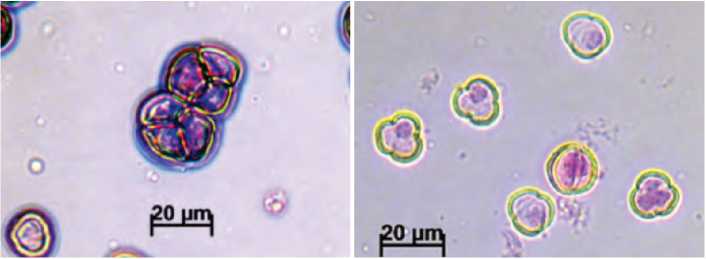
А. Тетрады и ранние одноклеточные микроспоры (форма округлая, цитоплазма плотная, ядро крупное) (бутон 2 мм)
Б. Ранние одноклеточные микроспоры (по мере увеличения размера, форма микроспоры приобретает трехлопастной вид) (бутон 3 мм)
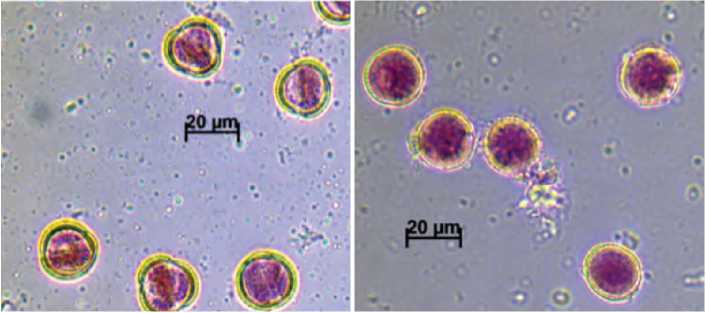
В. Одноклеточные микроспоры и поздние одноклеточные микроспоры (наблюдается образование нескольких мелких вакуолей, которые впоследствии сливаются в одну большую вакуоль, а ядро при этом смещается и занимает пристеночную позицию) (бутон 4 мм)
Г. Поздние одноклеточные микроспоры и двухклеточные пыльцевые зерна (форма поздних микроспор по мере роста становится округлой и на этом этапе происходит ассиметричный митоз, в результате чего образуются двухклеточное пыльцевое зерно) (бутон 5 мм)
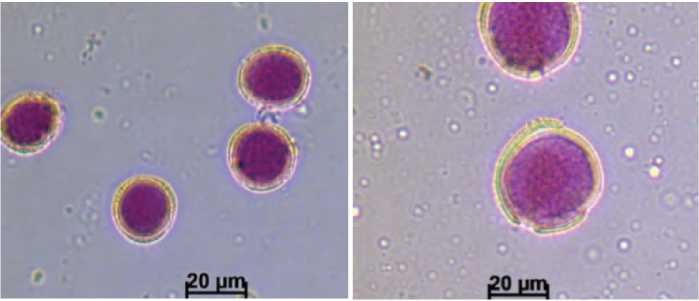
Д. Двухклеточная пыльца (состоит из вегетативной и генеративной клетки, цитоплазма темно окрашена, вакуоли не видны, ядра без предварительной фиксации просматриваются плохо) (бутон 6 мм)
Е. Зрелые пыльцевые зёрна (после второго митотического деления генеративной клетки, образуются два спермия, цитоплазма ярко окрашена, диаметр пыльцевого зерна увеличевается почти в два раза) (бутон 7 мм)
Рис. 1. Микроспоры и пыльца в бутонах брокколи разного размера (окраска дифференциальным красителем).
Figure 1. Microspore and pollen in broccoli buds of different sizes (use of differentiation dye).
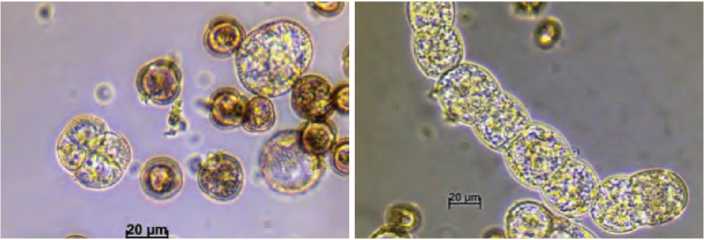
А. первые деления в культуре микроспор (3 суток)
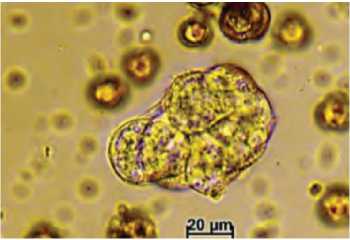
В. (10 суток)
Б. первые деления в культуре микроспор при развитии суспензора (7 суток)
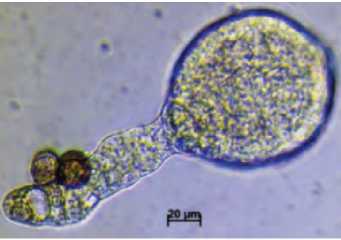
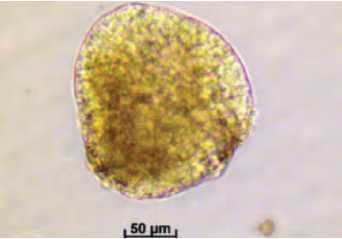
Д. Эмбриоид на глобулярной стадии развития (14 суток)
Г. образование эмбриоида на дистальном (по отношению к микроспоре) конце суспензороподобной структуры (14 суток)
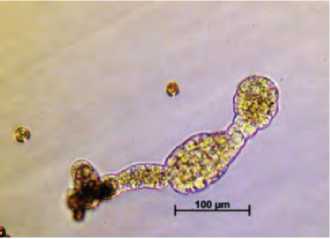
Е.Начальная стадия формирования цепочки из эмбриоидов на суспензороподобной структуре (20 суток)
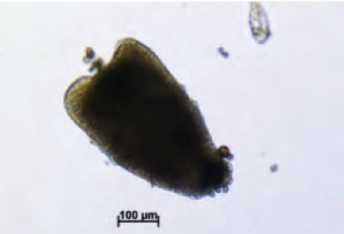
Ж. Эмбриоид на сердцевидной стадии развития (18 суток)
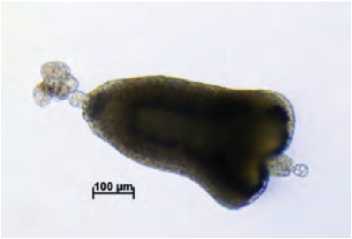
З. Эмбриоид с суспензором на сердцевидной стадии развития (25 суток)
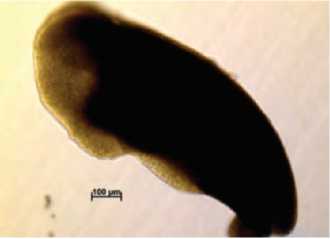
И. Эбриоид на начальной семядольной стадии развития (21 сутки)
Рис. 2. Образование и развитие эмбриоидов в культуре микроспор брокколи (А, В, Д, Ж, И – развитие без суспензора; Б, Г, Е, З, К – развитие с суспензороподобной структурой).
Figure 2. Formation and development of embryoids through culture of isolated microspore of broccoli (А, В, Д, Ж, И – development without suspensor; Б, Г, Е, З, К – development with suspensor-like structures).
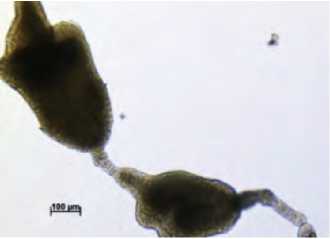
К. Цепочка из эмбриоидов на сердцевидной стадии развития (25 сутки)
зародыша с суспензороподобной структурой в культуре микроспор происходит сходно с развитием зиготического зародыша семейства Капустные, у которого происходит образование суспензора в процессе делений базальной клетки (образующейся при делении зиготы). В случае зиготического зародыша, полностью дифференцированный суспензор напоминает нить, состоящую из 8-13 клеток. Обнаруженная высокая степень полиплоидизации суспензора (некратная величине С) на глобулярной и сердцевидной стадии развития зиготического зародыша свидетельствует о его высокой метаболической активности, которая может быть связана с выполняемой суспензором функцией «выкармливания» зародыша на ранних стадиях его развития (Ермаков, 1990). Суспензор выполняет функцию накопления и транспорта к зародышу питательных веществ, растительных гормонов, таких как гиббереллиновая кислота, ауксин, цитокинины и абсцизовая кислота (Yeung, Meinke, 1993; Friml, 2003). Суспензор может быть как местом синтеза, так и поставщиком фитогормонов. В культуре микроспор суспензороподобные структуры, возможно, выполняют аналогичную роль снабжения эмбриоида запасными веществами и участвуют в регуляции его роста и тканевой дифференциации. В наших опытах развитие эмбриоидов происходило не синхронно, в одной чашке присутствовали эмбриоиды на разных стадиях развития. Было отмечено, что эмбриоиды, содержащие суспензор, развивались медленнее, чем бессуспензорные (рис. 2), что согласуется с данными, полученными при наблюдении за культурой микроспор B. napus (Supena, 2004) и B. rapa ssp. chinensis (Шумилина и др., 2015). Мы наблюдали образование эмбриоида не только на дистальном (по отношению к микроспоре) конце суспензороподобной структуры (рис. 2Г), но и образование цепочки из эмбриоидов (рис. 2Е, 2 К), а также всевозможные близнецовые комбинации эмбриоидов, описанные ранее для рапса (Supena et al., 2008).
На 30 день культивирования большая часть эмбриоидов достигала уже семядольной стадии (cotyledon-stage) и была готова для пересадки на твердую питательную среду для регенерации растений (рис. 3А). На свету уже на 2 день эмбриоиды приобретали зеленую окраску и значительно увеличивались в размере (рис. 3Б). Примерно через месяц растения-регенеранты укоренялись (рис. 3С), могли быть высажены в грунт для адаптации к условиям in vivo (рис. 3Д).
В результате проведенных исследований был изучен процесс эмбриогенеза и отработаны элемен- ты технологии получения удвоенных гаплоидов брокколи в культуре микроспор in vitro. Полученные DH-растения брокколи после самоопыления и оценки по хозяйственно ценным признакам могут быть включены в селекционный процесс в качестве гомозиготных линий, а также использоваться в молекулярно-генетических исследованиях. Изучение процесса эмбриогенеза в культуре микроспор in vitro свидетельствуют о том, что этот метод может быть использован не только для получения удвоенных гаплоидных растений, но и служить моделью для фундаментальных исследований по изучению этапов развития зиготических эмбриоидов и суспензоров.

-
А. Эмбриоиды в чашке Петри на семядольной стадии развития (cotyledon-stage) – 30 дней культивирования


Б. Активация хлорофилла и зеленой пигментации семядолей/эмбриода на 5 сутки культивирования на агаризованнойсреде В-5 с 2% сахарозой

-
В. Укоренение растений-регенерантов на среде МС с 2% сахарозой и 3,0 г/л фитогеля
Г. Адаптация растений-регенерантов к условиям in vivo
Рис. 3. Регенерация растений брокколи из эмбриоидов.
Figure 3. Broccoli plant regeneration from embryoids.
Список литературы Эмбриогенез в культуре микроспор брокколи
- Эмбриология растений: использование в генетике, селекции, биотехнологии: /под ред. И. П. Ермакова. -М., Агропромиздат, 1990. Т. 2/пер. с англ. Э. С. Терехина . -1990. -461 с.
- Шмыкова Н.А., Шумилина Д.В., Супрунова Т.П. Получение удвоенных гаплоидов у видов рода Brassica L.//Вавиловский журнал генетики и селекции. 2015; 19(1): 111 -120 DOI: 10.1134/S1062359015040135
- Шумилина Д.В., Шмыкова Н. А., Бондарева Л. Л., Супрунова Т. П. Влияние генотипа и компонентов среды на эмбриогенез в культуре микроспор капусты китайской Brassica rapa ssp. ohinensis сорта Ласточка//Известия РАН, серия биологическая, 2015. № 4. С. 368-375 DOI: 10.7868/S000233291504013X
- Alexander M.P. Differential staining of aborted and nonaborted pollen.//Stain technol. 1969. V.44. №3. P.117-122.
- Arnison P.G., Keller W.A. A survey of the anther culture response of Brassica oleracea L cultivars grown under field conditions.//Plant Breed.1990. V.104. P.125-133.
- Asif M (2013), Progress and Opportunities of Doubled Haploid Production, SpringerBriefs in Plant Science DOI 10.1007/978-3-319-00732-8_1
- Baillie A.M.R., Epp D.J., Hutcheson D. and Keller W.A. In vitro culture of isolated microspores and regeneration of plants in Brassica campestris//Plant Cell Rep. 1992. V.11. P.234-237.
- Chauvin J. E., Yang Q., Jeune B. Le., Herve Y. Odention d'embryons par culture d'anthtres chen le chou-fleur et le brocoli et evaluation des potentialites du materiel obtenu pour la creation varietale.//Agronomie, 1993. V.13. P.579-590.
- Dias J.S. Effect of activated charcoal on Brassica oleracea microspore culture embryogenesis//Euphytica. 1999. P.108. V.65-69.
- Dunwell J.M. (2010) Haploids in flowering plants: origins and exploitation. Plant Biotechnol. J., 2010, 8: 377-424 ( ) DOI: 10.1111/j.1467-7652.2009.00498.x
- Farnham M.W. Doubled-haploid broccoli production using anther culture effect of anther source and seed set characteristics of derived lines//J. Amer. Hort Sci. 1998. V.123. P.73-77.
- Friml J., Vieten A., Sauer M., Weijers D., Schwarz H., Hamann T., Offringa R. & Jergens G. Efflux-dependent auxin gradients establish the apical-basal axis of Arabidopsis//Nature.2003. V.426. P. 147-153.
- Gamborg O.L., Miller R.A., Ojima K. Nutrients requirements of suspension cultures of soybean root cells//Exp Cell Res. 1968. V.50. P.151-158.
- Gu H.H., Hagberg P., Zhou W.J. Cold pretreatment enhances microspore embryogenesis in oilseed rape (Brassica napus L.). Plant Growth Regul. 2004;42:137-143
- Kott L.S. Application of double haploid technology in breeding of oilseed Brassica napus//AgBiotech News Inf.1998. V. 10(3). P.69-74.
- Lichter R. Induction of haploid plants from isolated pollen of Brassica napus. Z. Pflanzenphysiol., 1982, 105: 427-434.
- Maluszynski M, Kasha KJ, Forster BP, Szarejko I (2003) Doubled haploid production in crop plants: a manual. Kluwer, Dordrecht
- Murashige T., Skoog F. A revised medium for rapid growth and bio assays with tobacco tissue cultures. Physiologia Plantarum, 1962, 15: 473-497
- Pechan P.M., Keller W.A. Identification of potentially embryogenic microspores in Brassica napus//Physiol Plant.1988. V. 74. P. 377-384.
- Prem et al.: A new microspore embryogenesis system under low temperature which mimics zygotic embryogenesis initials, expresses auxin and efficiently regenerates doubled-haploid plants in Brassica napus. BMC Plant Biology 2012 12:127 DOI: 10.1186/1471-2229-12-127
- Supena E.D.J. Innovations in micrcspore embryogenesis in Indonesian hot pepper (Capsicum annuum L.) and Brassica napus L.//Ph.D. thesis Wageningen University, Wageningen, The Netherlands. 2004. PP 131.
- Supena EDJ, Winarto B, Riksen T, Dubas E, van Lammeren A, Offringa R, Boutilier K, Custers J. Regeneration of zygotic-like microspore-derived embryos suggests an important role for the suspensor in early embryo patterning. J Exp Bot. 2008;59:803-814 DOI: 10.1093/jxb/erm358
- Takahata Y., Keller W.A. (1991) High frequency embryogenesis and plant regeneration in isolated microspore of Brassica oleracea L. Plant Sci,74:235-242.
- Takahata Y., Takany Y., Kaisuma N. Determination of microspore population to obtain high frequency embryogenesis in broccoli (Brassica oleracea L.).//Plant Tiss Cult Lett. 1993. V.10. P.49-53.
- Telmer C.A., Simmonds D.H., Newcomb W. Determination of developmental stage to obtain high frequencies of embryogenic microspores in Brassica napus//Physiol Plant.1992. V.84. P.417-424.
- Yeung E.C. and Meinke D.W. Embryogenesis in angiosperms: development of the suspensor//Plant Cell. 1993. V.5. P.1371-1381.


