Эндогенный SEMA4D в контроле пролиферации и апоптоза Т-лимфоцитов
Автор: Валиева Ю.В., Некрасова И.В., Куклина Е.М.
Журнал: Вестник Пермского университета. Серия: Биология @vestnik-psu-bio
Рубрика: Медико-биологические науки
Статья в выпуске: 3, 2018 года.
Бесплатный доступ
Семафорин IV класса Sema4D - молекула, широко представленная в иммунной системе. Она конститутивно экспрессируется Т-лимфоцитами, а при активации переходит в растворимую форму, не теряя функциональной активности. Свои эффекты в иммунной системе данная молекула реализует, как правило, через Sema4D/CD72-зависимую регуляцию клеток-мишеней. В настоящей работе мы показали, что Т-лимфоциты могут выступать не только как источник семафорина, но и как мишень для него. В частности, продемонстрировано стимулирующее действие эндогенного Sema4D на пролиферативный ответ Т-клеток и, напротив, ингибирующее - в отношении апоптоза этих клеток. Выявленные эффекты указывают на непосредственное участие эндогенного семафорина в контроле ранних этапов активации Т-лимфоцитов.
Т-лимфоциты, иммунный ответ, пролиферация, апоптоз
Короткий адрес: https://sciup.org/147227036
IDR: 147227036 | УДК: 612.018
Endogenous SEMA4D in control of proliferation and apoptosis of T-lymphocytes
Semaphorin IV class Sema4D is a molecule widely represented in the immune system. It is constitutively expressed by T-lymphocytes, and when activated, it passes into a soluble form while retaining functional activity. The molecule realizes its effects in the immune system via Sema4D / CD72-dependent regulation of target cells. In the present work, we have shown that T-lymphocytes can act not only as a source of semaphorin, but also as a target for it. In particular, the stimulating effect of endogenous Sema4D on the proliferative response of T cells and, on the contrary, the inhibitory effect on the apoptosis of these cells was demonstrated. The revealed effects indicate the direct involvement of endogenous semaphorin in the control of early stages of T-lymphocyte activation.
Текст научной статьи Эндогенный SEMA4D в контроле пролиферации и апоптоза Т-лимфоцитов
Sema4D, или CD100, – молекула, принадлежащая IV классу семафоринов [Semaphorin …, 1999]. Подобно другим членам семафоринового семейства, она участвует в процессах аксонального наведения в ходе роста нейронов [Kolodkin, Matthes, Goodman, 1993]. Наряду с этим, Sema4D широко представлен в иммунной системе и играет важную роль в ее функционировании. Он конститутивно экспрессируется на мембране Т-лимфоцитов [Bougeret et al., 1992], а при активации клеток усиливает экспрессию и переходит в растворимую форму за счет протеолитического отщепления, сохраняя при этом функциональную активность [Hérold et al., 1995; Wang et al., 2001; Elhabazi et al., 2001]. В связи с этим, Т-лимфоцит рассматривался традиционно исключительно как источник
Sema4D в иммунной системе, растворимого или мембранного, а мишенями его действия считали клетки, экспрессирующие низкоаффинный сема-фориновый рецептор CD72 [Kumanogoh, Kikutani, 2001; Mizui et al., 2009].
Однако в недавней работе показано [Куклина, Некрасова, Валиева, 2017], что Т-лимфоциты несут на мембране высокоаффинный рецептор для Sema4D, плексин В1, экспрессия которого ранее приписывалась исключительно неиммунным тканям [Takamatsu et al., 2010; Zhang et al., 2013]. Помимо этого, Sema4D может выступать не только как лиганд, но и как рецептор, проводя сигнал в клетку, на которой экспрессирован [Hérold et al., 1995; Zhang et al., 2013]. В связи с этим можно предположить, что Т-лимфоциты являются не только источником, но и мишенью действия
Sema4D. Целью работы было определение роли эндогенного Sema4D в активации Т-лимфоцитов.
Материалы и методы
В работе использовали лейкоциты здоровых доноров. ( n =10). От всех доноров получено информированное согласие на участие в исследовании. Лейкоциты выделяли из гепаринизированной венозной крови центрифугированием в градиенте плотности фиколла-верографина (1.077 г/см3) («Pharmacia»). В работе использовали CD3+Т-лимфоциты, фракционированные на иммуномаг-нитных частицах с помощью соответствующей системы для выделения (“R&D Systems”). Т-клетки в концентрации 1 × 106 клеток/мл (для оценки пролиферации) или 2 × 106 клеток/мл (для оценки апоптоза) культивировали 72 или 24 ч., соответственно, в среде RPMI 1640 (“Gibco. Thermo Fisher Scientific”) с добавлением 10%-ной эмбриональной телячьей сыворотки (Serva), 1 мМ HEPES (“Sigma-Aldrich”), 300 мг/мл L-глутамина (“Serva”) и 100 мг/мл гентамицина (“Pharmacia”) при 37оС и 5% СО 2 в условиях поликлональной активации (система для активации на основе моноклональных антител к CD3/CD28, “Invitrogen”).
Изучение роли эндогенного Sema4D в регуляции ранних этапов активации лимфоцитов проводили с учетом не только основного варианта ответа клеток на стимуляцию, пролиферации, но и альтернативного – апоптоза (программированной клеточной гибели). Пролиферативный ответ оценивали по включению в клетки синтетического аналога тимидина, 5-бром-2’-дезоксиуридина (BrdU), с помощью набора для иммуноферментного анализа (Amersham). BrdU добавляли в образцы за 18 ч. до окончания культивирования. Апоптоз Т-лимфоцитов оценивался по экспрессии на мембране фосфатидилсерина (маркер раннего апоптоза) – с помощью соответствующего лиганда, аннексина V, меченого флуоресцеинизотиоцианатом (AnnV*FITC, “R&D Systems”), и по включению в клетку пропидия йодида (PI, маркер позднего апоптоза) флуоресцентного ДНК- интеркалирую-щего красителя (“Sigma-Aldrich”). Оценка проводилась методом проточной цитометрии. Источником эндогенного Sema4D в культуре служили сами Т-лимфоциты [Hérold et al., 1995; Wang et al., 2001; Elhabazi et al., 2001].
Для оценки роли Sema4D в активации лимфоцитов использовали его блокаду анти-Sema4D антителами (10 μg/mL, Santa Cruz Biotech), которые добавляли в культуру за 1 ч. до активации лимфоцитов. Статистическая обработка проводилась с использованием t-критерия Стьюдента.
Результаты и их обсуждение
Исследование показали непосредственное участие Sema4D в пролиферативном ответе Т-лимфоцитов на поликлональную активацию (анти-CD3/CD28): при блокаде Sema4D наблюдалось статистически значимое снижение индекса пролиферации как для CD4, так и для CD8 Т-
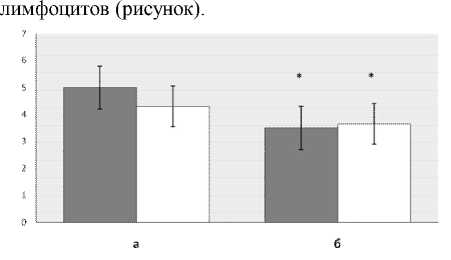
Роль Sema4D в пролиферативном ответе Т- лимфоцитов на поликлональную активацию: а) без блокады Sema4D, б) на фоне блокады Sema4D. * - p < 0.05 (в сопоставлении с соответствующим показателем без блокады); заштрихованный столбец – CD4+Т-лимфоциты, незаштрихованный – CD8+Т-лимфоциты
Уровень активационно-индуцированного апоптоза, напротив, возрастал в случае блокады Sema4D, как для CD4+, так и для CD8+Т-лимфоцитов (таблица), указывая на антиапоптоти-ческую активность семафорина.
Роль Sema4D в регуляции апоптоза Т-лимфоцитов
|
Условия экспрессии |
Процент Ann V-связывающих Т-лимфоцитов |
||
|
CD4+Т-лимфоциты |
CD8+Т-лимфоциты |
||
|
Монокультура Т-лимфоцитов |
Без блокады |
6.7±1.7 |
6.6±0.8 |
|
На фоне блокады |
8.8±3.1 |
5.4±1.5 |
|
|
Совместная культура Т/В-лимфо-цитов |
Без блокады |
5.3±1.1 |
5.4±1.5 |
|
На фоне блокады |
10.9±3.1* |
8.8±2.9* |
|
Примечание. * - p < 0.05 (в сопоставлении с соответствующим показателем без блокады).
Эти изменения касались не только экспрессии раннего маркера апоптоза, фосфатидилсерина (рецептора аннексина V), но и содержания Т-лимфоцитов, находящихся в поздней фазе апоптоза (позитивных и по аннексину V, и по PI), Важно отметить, что данные эффекты блокатора Sema4D выявлены в Т-лимфоцитах только в присутствии аутологичных В-клеток, тогда как в монокультуре Т-лимфоцитов уровень апоптоза имел лишь тенденцию к повышению.
По-видимому, для эффективной реализации ан-тиапоптотического действия Sema4D требуется кооперативное взаимодействие Т-лимфоцитов с другими клетками, на которых уровень экспрессии рецепторов для него существенно выше – В-лимфоцитами или дендритными клетками.
Заключение
В целом, полученные результаты показали следующее: 1) Sema4D контролирует пролиферативный ответ Т-лимфоцитов на активацию, выступая как позитивный регулятор; 2) Sema4D также участвует в регуляции альтернативного пути ответа клеток на стимуляцию – активационно-индуцированного апоптоза, играя негативную роль в этом процессе.
Реципрокный эффект Sema4D в отношении пролиферации и апоптоза Т-лимфоцитов должен усиливать активацию Т-клетки в ответ на антиген. Данный эффект может достигаться при действии как мембран-связанного семафорина, так и растворимого, причем растворимый Sema4D в ходе активации лимфоцита может действовать как аутокринный или паракринный фактор, подобно интерлейкину 2.
Работа поддержана грантом РФФИ № 15-0405694.
Список литературы Эндогенный SEMA4D в контроле пролиферации и апоптоза Т-лимфоцитов
- Куклина Е.М., Некрасова И.В., Валиева Ю.В. Участие семафорина Sema4D в Т-зависимой активации В-лимфоцитов // Бюллетень экспериментальной биологии и медицины. 2017. Т. 163, № 4. С. 444-448.
- Bougeret C. et al. Increased surface expression of a newly identified 150-kDa dimer early after human T lymphocyte activation. // J. Immunol. 1992. Vol. 148. P. 318-323.
- Elhabazi A. et al. Biological activity of soluble CD100. I. The extracellular region of CD 100 is released from the surface of T lymphocytes by regulated proteolysis // J. Immunol. 2001. Vol. 166. P. 4341-4347.
- Herold C. et al. Activation signals are delivered through two distinct epitopes of CD100, a unique 150 kDa human lymphocyte surface structure previously defined by BB18 mAb // Int. Immunol. 1995. Vol. 7. P. 1-8.
- Kolodkin A., Matthes D., Goodman C. The sema-phorin genes encode a family of transmembrane and secreted growth cone guidance molecules // Cell. 1993. Vol. 75. P. 1389-1399.
- Kumanogoh A., Kikutani H. The CD100-CD72 interaction: a novel mechanism of immune regulation // Trends Immunol. 2001. Vol. 22. P. 670-676.
- Mizui M. et al. Immune semaphorins: novel features of neural guidance molecules // J. Clin. Immunol. 2009. Vol. 29. P. 1-11.
- Semaphorin Nomenclature Committee. Unified nomenclature for the semaphorins/collapsins // Cell. 1999. Vol. 97. P. 551-552.
- Takamatsu H. et al. Roles of Sema4D-plexin-B1 interactions in the central nervous system for patho-genesis of experimental autoimmune encephalo-myelitis // J. Immunol. 2010. Vol. 184. P. 1499-1506.
- Wang X. et al. Functional soluble CD100/Sema4D released from activated lymphocytes: possible role in normal and pathologic immune responses // Blood. 2001 Vol. 97. P. 3498-3504.
- Zhang Y. et al. Sema 4D/CD100-plexin B is a multifunctional counter-receptor // Cell Mol. Immunol. 2013. Vol. 10. P. 97-98.


