Эндокринная регуляция репаративного процесса при возмещении межсегментарного дефекта костей в области коленного сустава методом чрескостного остеосинтеза
Автор: Болотов Д.Д., Куфтырев Л.М.
Журнал: Гений ортопедии @geniy-ortopedii
Рубрика: Оригинальные статьи
Статья в выпуске: 2, 2003 года.
Бесплатный доступ
Произведена оценка изменения концентрации в сыворотке крови гормонов: соматотропина, кальцитонина, паратирина, инсулина и циклических нуклеотидов: 3´5´аденозинмонофосфата и 3´5´гуанозинофосфата у 12 пациентов с дефектами суставных концов костей, образующих коленный сустав, до, в процессе и после реконструктивно-восстановительных операций на основе чрескостного остеосинтеза.
Коленный сустав, возмещение дефекта, аппарат илизарова, радиоиммунологический анализ, гормоны, циклические нуклеотиды
Короткий адрес: https://sciup.org/142120595
IDR: 142120595
Endocrinic control of reparative process during bone intersegmental defect filling in the knee region using transosseous osteosynthesis technique
Changes of the following hormones in blood serum were assessed: sokmatotropin, calcitonin, parathyrine, insulin and cyclic nucleotides - 3´5´adenisinemonophosphate and 3´5´guanosine phosphate in 12 patients with defects of bone articular ends, forming the knee, before, during and after reconstructive-and-restorative surgeries on the basis of transosseous osteosynthesis.
Текст научной статьи Эндокринная регуляция репаративного процесса при возмещении межсегментарного дефекта костей в области коленного сустава методом чрескостного остеосинтеза
Изучению возможностей организма адаптироваться к лечению методом чрескостного остеосинтеза способствуют исследования на уровне механизма активного воздействия на формирование костной ткани и ее минерализации. Общепризнанно, что процесс биологической минерализации возможен при определенном сочетании общих регуляторных факторов, обеспечивающих положительный минеральный баланс организма. Процессы минерализации костной ткани в живом организме сводятся к факторам, регулирующим синтез органической матрицы, и гомеостазу минеральных веществ [2, 6]. В этом отношении значительную ценность представляет изучение уровня остеотропных гормонов.
Многолетними исследованиями, выполненными в нашем Центре, установлено, что репаративный остеогенез в условиях чрескостного остеосинтеза протекает, по меньшей мере, в двух последовательно сменяющих друг друга фазах.
Каждая из них - фаза резорбции (катаболическая, пролиферативная) и анаболическая (фаза дифференцировки и минерализации) контролируется компонентами системной нейрогуморальной регуляции - адаптивными и остеотропными гормонами и местными факторами роста. Между системными и местными регуляторами репаративного процесса существуют взаимоотношения взаимного модулирования и кооперации физиологического действия, вторичными мессенджерами тех и других являются ионы кальция и циклические нуклеотиды [1, 5, 10, 11].
Известно также, что опухолевый процесс, поражающий костную ткань, связан с изменением гормонального фона, репаративный остеогенез при возмещении костного дефекта после удаления опухоли имеет свои особенности в плане системной нейрогуморальной регуляции [3, 7, 8]. Однако имеющиеся в настоящее время данные недостаточны для вынесения суждения о роли, какую играют эти особенности при ле- чении онкологических больных с применением методов чрескостного остеосинтеза. Целью нашего исследования является анализ динамики ряда показателей гормонального статуса у больных с пострезекционными дефектами дисталь- ного суставного конца бедренной кости по поводу опухолей, которым осуществляли возмещение межсегментарного дефекта в области коленного сустава.
МАТЕРИАЛ И МЕТОДЫ
Под наблюдением находилось 12 больных с опухолями дистального суставного конца бедренной кости (гигантоклеточна – 8, остеогенна саркома – 3, хондросаркома – 1) в возрасте от 16 до 46 лет. Давность патологии составляла от 0,5 до 15 лет. Всем пациентам после резекции произведены реконструктивно-стабилизирующие операции с применением технологий чрескостного остеосинтеза для замещения дефектов: методикой било-кального последовательного дистракционнокомпрессионного остеосинтнза – у 7, полилокаль-ного последовательного дистракционнокомпрессионного остеосинтеза – у 3, полилокаль-ного последовательного дистракционнокомпрессионного остеосинтеза с одновременным удлинением голени на одном уровне – у 1, моно-локального компрессионного с удлинением голе- ни на одном уровне – у 1. Больных обследовали в следующие сроки: до операции, еженедельно в течение первого месяца и дважды в месяц в последующем в процессе дистракции и фиксации, на 7-й день и ежемесячно после снятия аппарата.
Концентрацию гормонов: соматотропина (СТГ), кальцитонина (КТ), паратирина (ПТГ), инсулина (ИН) и циклических нуклеотидов: 3´5´аденозинмонофосфата (цАМФ) и 3´5´гуанозинофосфата (цГМФ) определяли методом радиоиммунологического анализа (РИА) (выполнялся совместно с к.м.н. Н.В. Офицеровой), используя гамма-счетчик фирмы «Tracor Europa» (Голландия) и наборы следующих фирм: «Bic Malincrodt» (Германия), «CIS» (Франция), «Amersham» (Великобритания).
РЕЗУЛЬТАТЫ
Исходные гормональный фон и сывороточные уровни циклических нуклеотидов, как и их динамика на протяжении этапов лечения, отражены на рисунках 1-6. До вмешательства больные с хроническими дефектами дистального конца бедра, образовавшимися после удаления опухолей, как правило, имели в сравнении с нормой повышенные уровни ПТГ (в 2,2 раза, р<0,01), цАМФ (в 1,8 раза , р<0,01), СТГ (в 1.5 раза, р<0,05), тенденцию к снижению концентрации КТ на 10% (р < 0,05) и практически нормальные уровни цГМФ и ИН (р<0,1). Принимая во внимание ту роль, которую отдельные гормоны играют в поддержании скелетного гомеостаза [2], можно сказать, что равновесие между костеобразованием и резорбцией у больных с хроническими дефектами костей после удаления опухолей изменено в сторону увеличения резорбции.
Динамика концентрации ПТГ была сходна с изменениями его уровня в сыворотке крови при замещении дефектов костей нижней конечности у больных, не имеющих онкологической патологии [4, 9]: резко повышаясь в послеоперационном периоде до 4,71 нг/мл (в 6,7 раза, р<0,001), он оставался высоким на всем протяжении периода дистракции, в 3-4 месяца фиксации отмечалось новое его увеличение на достоверном уровне (р<0,01), связанное, по-видимому, с ремоделированием новообразованной кости, и снижение предоперационного уровня наблюдалось только после снятия аппа- рата. Динамика содержания цАМФ в сыворотке крови в значительной мере соответствовала описанной для ПТГ, что предполагает в действии последнего не только внутриклеточное увеличение активности аденилатциклазы, но и влияние на перераспределение цАМФ между внутриклеточными компартментами и тканевой жидкостью.
В процессе дистракции наблюдалось плавное непрерывное увеличение содержания в крови СТГ, достигавшего максимального значения (6, 53 нг/мл, р<0,01) к 14-му дню фиксации. Затем происходило постепенное его снижение, однако к концу фиксации уровень этого гормона оставался увеличенным в 3,2 раза (р<0,01). После снятия аппарата содержание СТГ падало и к 30-му дню этого периода наблюдения существенно не отличалось от дооперационного (р<0,05).
Изменения содержания в крови КТ и цГМФ в целом повторяли изменения СТГ, достигая наибольшего содержания также к 14-му дню фиксации, увеличиваясь до 153 пг/мл (в 1,5 раза, р<0,05) для КТ и 6,03 пмоль/мл (в 3,6 раза, р<0,01) для цГМФ. При этом концентрация цГМФ в процессе дистракции плавно, постепенно снижалась, оставаясь увеличенной к концу дистракции в 2 раза и постепенно приближаясь после снятия аппарата к верхней границе нормы, но не доходя до нее. Концентрация КТ оставалась увеличенной в 1,4-1,5 раза в течение первых трех месяцев фиксации с последующим снижением, но оставалась повышенной в 1,2 раза к концу фиксации и также приближалась к верхней границе нормы после снятия аппарата, не доходя до нее.
В послеоперационном периоде наблюдалось резкое повышение концентрации цАМФ до 54,5 нМ/мл – 3,8 раза с последующим снижением до близкого к дооперационному уровню через 2 месяца дистракции и постепенным последующим снижением с незначительными колебаниями, оставаясь повышенным в 1,2-1,5 раза в течение последующей дистракции и фиксации. После снятия аппарата концентрация цАМФ еще более приближалась к норме, не доходя до ее верхней границы, но оставалась увеличенной в 1,1-1,2 раза.
Концентрация ИН в сыворотке крови находилась в пределах нормы, снижаясь в 1,4 раза в послеоперационном периоде и незначительно на 2-3 месяце после снятия аппарата.
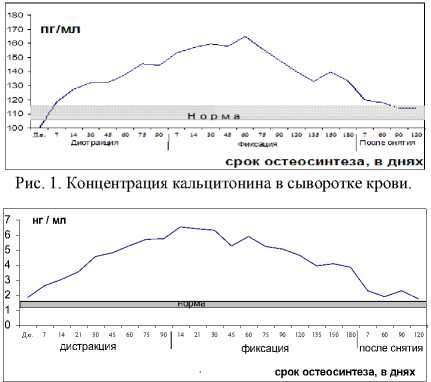
Рис. 2. Концентрация соматотропина в сыворотке крови.
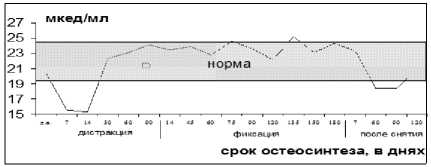
Рис. 3. Концентрация инсулина в сыворотке крови.
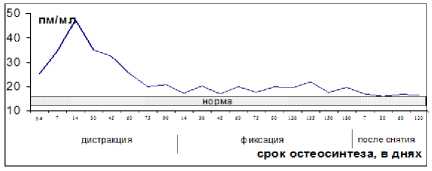
Рис. 4. Концентрация цАМФ в сыворотке крови.
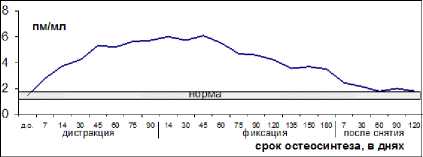
Рис. 5. Концентрация цГМФ в сыворотке крови.
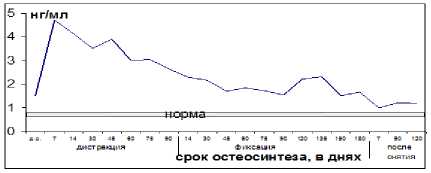
Рис. 6. Концентрация ПТГ в сыворотке крови.
ОБСУЖДЕНИЕ
Наличие в исходном состоянии повышения концентрации СТГ, стимулирующего образование коллагена, ПТГ, вызывающего деминерализацию костной ткани и цАМФ, изменяющего прохождение клеток через фазу митоза, а также незначительное снижение КТ, уменьшающего уровень кальция и неорганического фосфора в сыворотке крови, свидетельствовало о наличии в организме гормонального дисбаланса.
Резкое увеличение в первую неделю после операции ПТГ и цАМФ может свидетельствовать о напряжении адренергических реакций организма, ответственных за гормональный ответ на оперативное вмешательство, ПТГ, оставаясь повышенным (максимальное снижение до 1,51 нг/мл- в 2,2 раза выше в сравнении с контрольными цифрами к 5 месяцу фиксации), способствовал активной резорбции, кроме того, активизируя адемилатциклазу, стимулировал проникновение кальция в клетку, действуя на клеточном и монокулярном уровнях.
Повышение уровня ПТГ, а следовательно, и кальция в сыворотке крови, явилось причиной постепенного увеличения КТ, снижающего уровень кальция и неорганического фосфора, взаимодействующих по принципу обратной связи, в результате чего ускорялась минерализация кости. Одновременно с этим КТ снижает активность остеокластов, что также повышает минерализацию регенерата.
В отличие от КТ, пик повышения которого приходится на 2 месяц фиксации, у СТГ, имеющего сходную тенденцию повышения и снижения в сыворотке крови, пик повышения приходится на 14 день фиксации, что соответствует фазе наиболее активного образования коллагена.
Концентрация цГМФ, стимулирующей клеточную пролиферацию, изменяясь сходно с КТ и СТГ, плавно повышаясь, имеет пик концен- трации на 45 день фиксации, находясь между пиками повышения КТ и СТГ.
Колебание ИН не носило принципиального характера и может быть рассмотрено как реакция на оперативное вмешательство.
Таким образом, исходя из количественной оценки изменений концентрации гормонов, выявлена закономерность их воздействия, результатом которой явились условия, способствующие увеличению массы и минерализации регенератов при замещении межсегментарных дефектов в области коленного сустава.


