Эндоскопические цитопротективные технологии в лечении синдрома Меллори - Вейсса
Автор: Чередников Е.Ф., Юзефович И.С., Баранников С.В., Банин И.Н., Черных А.В., Ростиашвили Г.Г., Болховитинов А.Е., Шкурина И.А.
Журнал: Волгоградский научно-медицинский журнал @bulletin-volgmed
Статья в выпуске: 1 т.21, 2024 года.
Бесплатный доступ
Цель исследования разработать и применить в клинической практике метод эндоскопического лечения кровоточащих разрывов с использованием гемостатика «Альгистаб» у пациентов с синдромом Меллори Вейсса (СМВ). Материал и методы. В клиническое исследование вошел 121 пациент с СМВ, 65 пациентов составили основную группу (ОГ). Им применяли для лечения кровоточащих разрывов эндоскопические инсуффляции порошкообразного гемостатика «Альгистаб». В контрольной группе (КГ) у 56 пациентов эндогемостаз проводили инъекционными методами, диатермокоагуляцией, аргоноплазменной коагуляцией (АПК) и др. без гемостатика.
Синдром меллори - вейсса, эндоскопический гемостаз, цитопротективное лечение
Короткий адрес: https://sciup.org/142242047
IDR: 142242047 | УДК: 616-002.151-072.1-08
Endoscopic cytoprotective technologies in the treatment of Mallory - Weiss syndrome
The aim of the study was to develop and apply in clinical practice a method of endoscopic treatment of bleeding ruptures using Algistab hemostatic in patients with Mallory Weiss syndrome (MWS). Material and methods. The clinical study included 121 patients with MWS. 65 patients made up the main group (MG). They used endoscopic insufflations of the powdered hemostatic Algistab to treat bleeding ruptures. In the control group (CG) in 56 patients, endohemostasis was performed by injection methods, diathermocoagulation, argonoplasmic coagulation (APC), etc. without hemostatic.
Текст научной статьи Эндоскопические цитопротективные технологии в лечении синдрома Меллори - Вейсса
Синдром Меллори – Вейсса (СМВ) в течение последних лет занимает ведущее место в структуре кровотечений неязвенной этиологии. Значительное количество повторных кровотечений, проведение оперативных вмешательств, общая летальность у больных с СМВ вызывают тревогу у хирургов [1, 2].
В вопросах лечения СМВ большое значение занимают методы эндогемостаза. Следует отметить, что при использовании даже комбинированных методов эндоскопического гемостаза рецидивы геморрагии возникают в 5,7–13,3 % случаев [3, 4].
Важно указать, что больные с разрывногеморрагическим синдромом являются пациентами трудоспособного возраста, что свидетельствует о социально-экономической значимости этого недуга. В этой связи совершенствование и поиск эффективных методов эндоскопического лечения СМВ является актуальным [5–6].
ЦЕЛЬ РАБОТЫ
Разработать метод эндоскопического лечения СМВ, который позволит обеспечить надежный гемостаз, снизит частоту повторных кровотечений, улучшит заживление дефектов.
МЕТОДИКА ИССЛЕДОВАНИЯ
В клиническое исследование вошел 121 пациент с СМВ. Исследование проведено при разрешении Этического комитета ВГМУ им. Н. Н. Бурденко (протокол 2, от 24.03.2023 г.).
Клинические исследования проведены на базе Специализированного Центра БУЗ ВО «ВГКБ СМП №1». Среди пациентов мужчин было 99 (81,8 %), женщин – 22 (18,2 %). Возраст составил 48,18 ± 15,08 (M ± Ϭ) лет.
Факторы, способствующие появлению СМВ: злоупотребление алкоголем – 99 (81,8 %), физическое перенапряжение – 8 (6,6 %), рвота – 12 (9,9 %), кашель – 2 (1,7 %).
По локализации кровоточащие дефекты распределились в следующем порядке: пищеводно-желудочный переход – у 111 (91,7 %), пищеводные – у 3 (2,5 %), кардиальные – у 7 (5,8 %) пациентов.
Расположение дефектов по стенкам было следующим: на задней стенке – у 44 (36,4 %) больных, на правой стенке – у 40 (33,1 %) больных, на левой стенке – у 21 (17,4 %) и на передней – у 16 (13,1 %) пациентов.
Длина кровоточащих дефектов была от 0,3 до 2,9 см. Различали большие (от 2,5 и больше), средние (1,0–2,5 см) и малые (до 1,0 см) разрывы. Малые размеры в нашей работе были выявлены у 56 (46,3 %) пациентов, средние – у 61 (50,4 %) и большие дефекты – у 4 (3,3 %) пациентов.
По глубине дефекты встречались в пределах слизистой оболочки (I стадия) – у 34 (28,1 %) пациентов, слизисто-подслизистой основы (II стадия) – у 71 (58,7 %) пациентов и доходили до мышечной оболочки (III стадия) – у 16 (13,2 %) больных. IV стадия разрывно-геморрагического синдрома в нашем исследовании не встречалась.
В большинстве случаев разрывы были единичными – у 85 (70,2 %), множественные дефекты встречались у 36 (29,8 %) пациентов.
Активность кровотечения при СМВ определяли по J. Forrest (1974). Пациенты распределились так: тип геморрагии FIA-FIB отмечен у 12 (9,9 %) пациентов, тип FIIA-FIIB – у 68 (56,2 %) пациентов и тип FIIC – у 41 (33,9 %) пациентов.
По классификации А. И. Горбашко (1985) у 15 (12,4 %) пациентов отмечалась тяжелая степень кровопотери, средняя – у 48 (39,7 %) и легкая – у 58 (47,9 %) пациентов.
Все пациенты распределены были на две группы случайной выборкой: основную группы (ОГ), 65 человек, и контрольную группу (КГ), 56 человек. Пациенты обеих групп сопоставимы.
В табл. 1 представлена характеристика групп проведенного исследования.
Пациентам ОГ с кровотечением FIA-FIB (6 человек) использовали комбинированный эндогемостаз: в начале производили обкалывание аминокапроновой кислотой (АКК), затем на дефект воздейтсвовали аргоно-плазменной коагуляцией (АПК) и после этого на область разрыва инсуффлировали полимерный «Альги-стаб» (рис. 1).
Таблица 1
Характеристика групп проведенного исследования
|
Показатель |
ОГ ( n = 65) |
КГ ( n = 56) |
P |
Всего |
|
Мужчины |
54 (83,1 %) |
45 (80,4 %) |
p > 0,05 |
99 (81,8 %) |
|
Женщины |
11 (16,9 %) |
11(19,6 %) |
p > 0,05 |
22 (18,2 %) |
|
Возраст |
40,7 ± 1,1 |
44,7 ± 1,2 |
p > 0,05 |
|
|
Характер кровотечения по J. Forrest, 1974 |
||||
|
FIA-FIB |
6 (9,2 %) |
6 (10,7 %) |
p > 0,05 |
12(9,9 %) |
|
FIIA-FIIB |
38 (58,5 %) |
30 (53,6 %) |
p > 0,05 |
68 (56,2 %) |
|
FIIC |
21 (32,3 %) |
20 (35,7 %) |
p > 0,05 |
41 (33,9 %) |
|
Степень тяжести кровопотери по А. И. Горбашко, 1982 |
||||
|
Легкая |
30 (46,2 %) |
28 (50,0 %) |
p > 0,05 |
58 (47,9 %) |
|
Средняя |
27 (41,5 %) |
21 (37,5 %) |
p > 0,05 |
48 (39,7 %) |
|
Тяжелая |
8 (12,3 %) |
7 (12,5 %) |
p > 0,05 |
15 (12,4 %) |
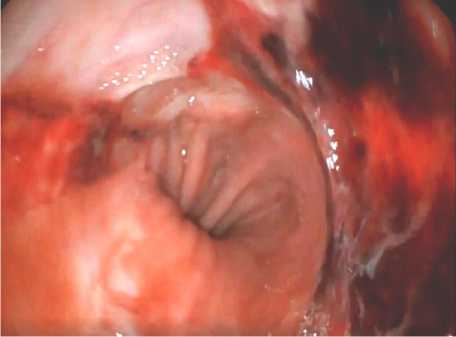
Рис. 1. Больной П. 32 лет. Синдром Меллори – Вейсса. Два разрыва области пищеводно-желудочного перехода: по правой и левым стенкам с признаками продолжающегося кровотечения
У больных ОГ с кровотечением FIIA-FIIB (38 человек) применяли способ эндоскопического лечения путем нанесения на тромбированный сосуд или сгусток гемостатика «Альги-стаб» (Патент РФ № 2762121) по разработанной методике для предупреждения повторного кровотечения. Больным с угрозой рецидива геморрагии (FIA-FIB и FIIA-FIIB) проводился эндо- скопический мониторинг с интервалом 12–24 часа. У пациентов с типом FIIС (21 человек) на дефект производили нанесение порошкообразного альгстаба по разработанной методике (Патент РФ № 2762121).
Всем больным ОГ повторную лечебную эндоскопию с нанесением на дефект альгиста-ба осуществляли через 4–5 суток (рис. 2).
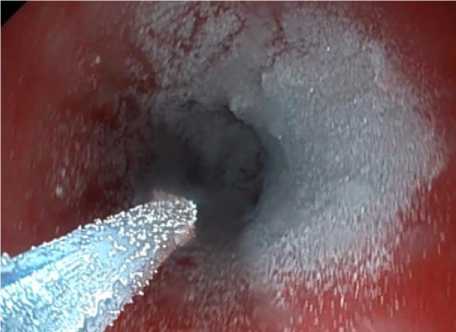
Рис. 2. Больной П. 32 лет. Синдром Меллори – Вейсса. 4-е сутки стационарного лечения. Дополнительно производится эндоскопическое лечение альгистабом
В КГ (56 человек) использовали обкалывание АКК, АПК, диатермокоагуляция и другое без применения гемостатических средств.
В комплексном лечении все пациенты получали ингибиторы протонной помпы (ИПП), общую гемостатическую и симптоматическую терапии.
Эффективность лечения пациентов с СМВ оценивали по основным критериям: гемостаз окончательный, частота повторных кровотечений, сроки и качество заживления разрывов (рубцевание, эпителизация), смертность.
Обработку данных статистическими методами проводили в программе MSExcel. Рассчитывали стандартные показатели: среднее (М), медиану (Ме), верхний и нижний квартили. Значимость различий по количественным показателям определяли с помощью критерия Манна – Уитни. По качественным признакам значимость различий оценивали тестом Фишера и Z-критерием с поправкой Йетса.
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ И ИХ ОБСУЖДЕНИЕ
Проведенный анализ лечения пациентов с СМВ с типом кровотечения FIIC показал, что в ОГ (21 человек) сразу после нанесения гемостатика на кровоточащий дефект порошкообразный альгистаб превращался в гидрогелевый слой, который плотно фиксировался к краям и дну дефекта, удерживаясь на их поверхности до 4–5 суток. При этом гидрогелевый слой закрывал дефект, сгусток и тромбированный сосуд от соляной кислоты и пепсина, предотвращая повторные кровотечения. Одновременно с этим было отмечено, что альгстаб оказывал цитопротективный эффект, способствуя благоприятному течению репаративного процесса. У всех пациентов ОГ улучшалось общее состояние, гемодинамика стабилизировалась, приближались к норме гематологические анализы. У пациентов с типом FIIC ОГ операций, повторных геморрагий и летальных исходов не наблюдалось. В КГ (20 человек) с типом FIIC у пациентов с СМВ операций, повторных геморрагий и летальных исходов также не было.
Пациентов с FIIA-FIIB было 68 человек. В ОГ (38 человек) применяли эндоскопический гемостаз альгистабом с профилактической целью. В КГ (30 человек) проводили эндоскопическую профилактику возобновления кровотече- ния путем АПК разрыва без нанесения гемостатика. В ОГ с FIIA-FIIB повторное кровотечение было отмечено у 2 из 38 человек с глубоким разрывом в области эзофагокардиального перехода справа. У них возобновившееся кровотечение остановлено в результате повторного использования разработанного способа.
Осложнений в данной группе не было. В КГ с FIIA-FIIB возобновление кровотечения было у 6 из 30 пациентов. 5 пациентам не потребовалось проведение операции и кровотечение у них было остановлено эндоскопически. 1 пациент с массивным рецидивным кровотечением взят в операционную, где умер на операционном столе. Кроме этого, в этой группе умер еще 1 пациент от основного соматического заболевания.
В группе пациентов с FIA-FIB было 12 человек. В ОГ 6 пациентам проводили комбинированный эндогемостаз с гемостатиком «Аль-гистаб».
Отмечено, что у всех 6 пациентов ОГ с FIA-FIB гемостаз был достигнут в 100 % случаев, повторных кровотечений, операций и летальных исходов не было. В КГ с FIA-FIB первичный эндогемостаз был успешен у всех 6 пациентов (100 %), но кровотечение возобновилось у 2 пациентов. У этих пациентов кровотечение при повторной эндоскопии было остановлено успешно. Иных осложнений у данных больных не наблюдалось.
Подводя анализ клиническим исследованиям по применению порошкообразного гемостатика «Альгистаб» в комплексном лечении пациентов с синдромом Меллори – Вейсса, следует отметить, что процесс заживления дефектов в ОГ при местном цитопротективном лечении по сравнению с КГ протекал качественнее и быстрее. Так, средний срок заживления дефектов в ОГ был 5,0 (4,0–6,0) дня ( р < 0,0001), а в КГ дефекты зажили в срок 10,0 (7,5–12,0) дня ( р < 0,0001). Причем, при местном лечении альгистабом в ОГ дефекты зажили у 60 (92,3 %) пациентов путем эпителизации, и лишь у 5 (7,7 %) пациентов разрывы зажили с образованием нежного рубца. В КГ заживление дефектов происходило путем рубцевания у 22 (39,3 %), а у 34 (60,7 %) пациентов зажили дефекты путем эпителизации.
Результаты лечения пациентов в сравниваемых группах показаны в табл. 2.
Таблица 2
|
Показатель |
ОГ ( n = 65) |
КГ ( n = 56) |
P |
|
Гемостаз окончательный |
63 (96,9 %) |
48 (85,7 %) |
р = 0,043 |
|
Рецидивные кровотечения |
2 (3,1 %) |
8 (14,3 %) |
р = 0,043 |
|
Летальность |
- |
2 (3,6 %) |
- |
|
Сроки заживления |
5,0 (4,0–6,0) |
10,0 (7,5–12,0) |
р = 0,0001 |
|
Эпителизация дефектов |
60 (92,3 %) |
34 (60,7 %) |
р = 0,0001 |
Показатели эффективности лечения в сравниваемых группах (абс/%)
Из данных, отраженных в таблице, видно, что разработанный способ эндоскопического гемостаза с применением альгистаба усиливает гемостатический эффект, уменьшает число рецидивных геморрагий, способствует быстрому и качественному заживлению дефектов.
ЗАКЛЮЧЕНИЕ
Разработанный метод местного лечения СМВ с использованием гемостатика «Альги-стаб» позволил получить окончательный гемостаз в 96,9 % случаев и уменьшить частоту повторных геморрагий с 14,3 до 3,1 % ( р = 0,043). Инсуффляция альгистаба при местном лечении СМВ способствует образованию цитопротек-торной гидрогелевой пленки на кровоточащих дефектах, создает условия для качественной репаративной регенерации путем эпителизации дефектов до 92,3 % ( р = 0,0001) и уменьшения сроков заживления с 10,0 (7,5–12,0) до 5,0 (4,0– 6,0) ( р = 0,0001) дней.
Список литературы Эндоскопические цитопротективные технологии в лечении синдрома Меллори - Вейсса
- Князева Н. А., Фоменко К. А., Стяжкина С. Н. Желудочно-кишечные кровотечения при синдроме Меллори - Вейсса в клинической практике. Modern Science. 2020;5(1):228-232.
- Wilkins T., Wheeler B., Carpenter M. Upper Gastrointestinal Bleeding in Adults: Evaluation and Management. Am Fam Physician. 2020;101(5):294-300. EDN: MIQSGI
- Валеев М. В., Тимербулатов Ш. В. Гастродуоденальные кровотечения. Анализ результатов лечения в условиях районной больницы. Вестник Национального медико-хирургического центра им. Н. И. Пирогова. 2020;15(1):39-42. 10.25881/BPNMSC. 2020.61. 63.007. DOI: 10.25881/BPNMSC.2020.61.63.007 EDN: TLRNBV
- Тимербулатов Ш. В., Валеев М. В. Обострение язвенной болезни как причина развития синдрома Меллори - Вейсса. Описание серии случаев. Пермский медицинский журнал. 2019;36(4):97-103. DOI: 10.17816/pmj36497-103 EDN: QLGFKY
- Cherednikov E. F., Yuzefovich I. S., Maleev Yu. V. et al. The Use of the Hemostatic Agent Zhelplastan in Combination with a Granulated Sorbent in the Treatment of Patients with MalloryWeiss Syndrome. International Journal of Biomedicine. 2021;11(2):160-163. DOI: 10.21103/Article11(2)_OA7 EDN: ESKGCN
- Юзефович И. С., Баранников С. В., Чередников Е. Ф. Профилактическое цитопротективное лечение синдрома Меллори - Вейсса в условиях специализированного центра. Профилактическая медицина. 2021;24:5-7:91.


