Эндотелиальная дисфункция у больных хронической болезнью почек
Автор: Курапова Марина Владимировна, Низямова Алия Рифхатовна, Ромашева Екатерина Павловна, Давыдкин Игорь Леонидович
Журнал: Известия Самарского научного центра Российской академии наук @izvestiya-ssc
Статья в выпуске: 3-6 т.15, 2013 года.
Бесплатный доступ
В статье рассматриваются вопросы состояния эндотелия у больных хронической болезнью почек. Обследован 91 пациент с хронической болезнью почек I-III стадии. Использован комплекс биохимических, иммуноферментных и инструментальных методов исследования. Выявлена активация эндотелия (повышение уровня ЭД-1 и СРБ), усиливающаяся при снижении скорости клубочковой фильтрации. У больных хронической болезнью почек с начальными проявлениями дисфункции почек выявлены нарушения регуляции сосудистого тонуса, которые связаны с функцией эндотелия.
Функция эндотелия, эндотелиальная дисфункция, хроническая болезнь почек, эндотелин-1, с-реактивный белок
Короткий адрес: https://sciup.org/148202107
IDR: 148202107 | УДК: 616.61-008.64-074:611
Endothelian dysfunction at patients with kidneys chronic disease
In article the questions an endothelia state at patients with kidneys chronic disease are considered. 91 patients with kidneys chronic disease of I-III stage are surveyed. The complex of biochemical, immunofermental and tool methods of research is used. Activation of endothelia (ED-1 and CRP levels increase), amplifying at decrease in speed of glomerular filtration is revealed. At patients with kidneys chronic disease with initial manifestations of kidneys dysfunction the violations of regulation the vascular tone which are connected with function an endothelia are revealed.
Текст научной статьи Эндотелиальная дисфункция у больных хронической болезнью почек
Распространенность заболеваний почек сопоставима с такими социально значимыми заболеваниями, как гипертоническая болезнь, сахарный диабет и ожирение. По данным исследования NHANES, дисфункция почек достигает примерно 13,1% в общей популяции [3]. Признаки повреждения почек и/или снижение скорости клубочковой фильтрации выявляются как минимум у каждого десятого представителя общей популяции [14]. Результаты проведенных исследований в России показали, что снижение функции почек наблюдается у 36% лиц в возрасте старше 60 лет [8, 9]. Существенное влияние на развитие и прогрессирование хронической болезни почек (ХБП) оказывают инфекции, прием лекарственных препаратов, алкоголь, курение, состояние окружающей среды, климат, характер и традиции питания, генетические особенности населения данной популяции и др. [13, 16]. Сердечно-сосудистые осложнения являются основной причиной смерти пациентов с нарушенной функцией почек (на додиализном и диализном лечении). По данным нефрологических регистров разных стран, сердечно-сосудистые осложнения составляют до 48% в структуре смертности больных, находящихся на программном гемодиализе. В мировой литературе, посвященной проблеме кардиоваскулярных нарушений у больных с терминальной стадией ХБП, получающих заместительную почечную терапию, основное внимание уделяется ишемической болезни сердца (ИБС), нарушениям сердечного ритма, поражению клапанов сердца, перикардитам, артериальной гипертензии, нарушениям диастолической и
Курапова Марина Владимировна, аспирантка Низямова Алия Рифхатовна, аспирантка
Ромашева Екатерина Павловна, кандидат медицинских наук, ассистент кафедры госпитальной терапии с курсом трансфузиологии
систолической функции левого желудочка, гипертрофии левого желудочка сердца [12]. Известно, что в патогенезе сердечно-сосудистых осложнений у данной группы пациентов большое значение имеет нарушение функции эндотелия [5]. В соответствии с современными представлениями эндотелиальная дисфункция – это патологическое состояние эндотелия, в основе которого лежит нарушение продукции эндотелиальных факторов, при котором эндотелий не в состоянии обеспечить гемореологический баланс крови и приводящее к нарушению функций и органов и систем [10]. Эндотелиальная дисфункция является первым этапом развития атеросклероза, а у пациентов, получающих заместительную почечную терапию, ускоренный атерогенез подтвержден клиническими исследованиями [1, 2].
В настоящее время среди механизмов прогрессирования гломерулярных поражений почек существенное значение придают нарушениям функции эндотелия [4, 6]. Согласно экспериментальным данным, полученным Смирновым А.В. с соавторами, одним из факторов прогрессирования ХБП является нарушение зависимой от эндотелия вазодилатации [17,18]. Эндотелий-зависимая вазоконстрикция, в основном, связана с выработкой эндотелина-1 (ЭД-1), синтез которого стимулируется снижением напряжения сдвига, растяжением сосудистой стенки, норадреналином, тромбином, тяжелой гипоксией тканей, ангиотензином-II, ар-ги-нином, вазопрессином, брадикинином, инсулином, глюкокортикоидами, тромбоксаном А2, повышением внеклеточного калия, факторами роста (эндотоксином или интерлейкином-1, трансформирующим фактором роста b1) и др. Ингибирует продукцию эндотелина-1 небольшое число факторов (цГМФ, NO, предсердный и мозговой натрийуретический пептиды). В норме ЭД-1 синтезируется только при стимуляции эндотелия [18]. К косвенным показателям состояния эндотелиальных клеток относятся содержащиеся в крови субстанции, уровень которых коррелирует с эндотелиальной дисфункцией: С-реактивный белок (СРБ), липопротеиды низкой плотности, липопротеиды очень низкой плотности, гомоцистеин, асимметричный диметиларгинин (ADMA), липопротеин (а), ксантиоксидаза, интерлейкин-lß, фактор некроза опухоли α, интерлейкин-8 и другие [15]. СРБ, как центральный белок острой фазы воспаления, может усиливать продукцию других цитокинов, активировать систему комплемента, стимулировать захват ЛПНП макрофагами, усиливать адгезию лейкоцитов сосудистым эндотелием, т.е. увеличивать воспалительный каскад. При взаимодействии с другими провоспалительными медиаторами он участвует в привлечении моноцитов в зону атеросклеротической бляшки. По данным Framingham Study, уровни СРБ меньше 1 мг/л, 1-3 мг/л и больше 3 мг/л соответствовали низкому, умеренному и высокому риску развития сердечно-сосудистых событий [7]. Связь эндотелиальной дисфункции с поражением функции почек представляется закономерной, но является малоизученной. Особый интерес представляет зависимость снижения скорости клубочковой фильтрации от эндотелиальной дисфункции.
Цель работы: оценить степень выраженности эндотелиальной дисфункции у больных ХБП IIII стадий.
Для решения данной задачи было проведено одномоментное проспективное исследование. Обследовано 30 практически здоровых человек (средний возраст 30,9±1,7 года) и 91 больной ХБП, находившийся на стационарном обследовании и лечении в нефрологическом отделении Клиник Самарского медицинского государственного университета. Диагноз ХБП был верифицирован на основании данных осмотра больных, результатов лабораторных и ультразвуковых методов обследования, биопсии почки. Критериями исключения являлись возраст младше 18 и старше 65 лет, наличие сахарного диабета I и II типа, скорость клубочковой фильтрации менее 30 мл/мин., наличие онкологического процесса. Все пациенты, включенные в исследование, были разделены на 3 группы в зависимости от скорости клубочковой фильт-рации (СКФ), рассчитанной по формуле MDRD (Modification of Diet in Renal Disease) [5]. Сравнительная характеристика групп по полу и возрасту представлена в таблице №1.
Таблица 1. Сравнительная характеристика групп
|
Показатель |
Здоровые (n=30) |
ХБП I стадии (n=30) |
ХБП II стадии (n=30) |
ХБП III стадии (n=31) |
|
мужчины |
13(43,33%) |
9 (30%) |
8 (26,67%) |
16 (51,61%) |
|
женщины |
17 (56,67%) |
21(70%) |
22(73,33%) |
15 (48,39 %) |
|
возраст, годы |
30,9±1,70 |
33,70±2,57 |
52,77±2,76 |
55,10±11,93 |
Неравномерное распределение по гендерному признаку в группах с ХБП I и II стадии связано с тем, что основной причиной болезни являлись хронические воспалительные интерстициальные заболевания почек (хронический пиелонефрит и хронический тубуло-интерстициальный нефрит). С эпидемиологической точки зрения женщины болеют в 6 раз чаще мужчин в молодом и среднем возрасте в связи с анатомо-физиологическими и гормональными особенностями.
Кроме общеклинического обследования, принятого в нефрологическом стационаре, всем больным определяли уровень эндотелина-1 имму-ноферментным анализом с помощью тест-системы Biomedical ENDOTELIN (1-21) ЗАО «БиоХим-Мак». Исследовалась гемомикроциркуляция методом лазерной допплеровской флоуметрии (ЛДФ) на лазерном анализаторе капиллярного кровотока ЛАКК-02 производства НПП «Лазма» (г. Москва) с проведением окклюзионной пробы. Область исследования – зона Захарьина-Геда в точке, расположенной по срединной линии на 4 см проксимальнее шиловидных отростков локтевой и лучевой костей на задней (наружной) поверхности предплечья. Общее время проведения пробы – 11 минут, из них 5 минут – регистрация исходного кровотока, затем 3-х минутная окклюзия, и в течение последующих 3 минут регистрировалось восстановления кровотока после окклюзии. Для расчета средних значений изменений числовых параметров перфузии использовался математический аппарат обработки случайных процессов программного обеспечения LDF. Статистическую обработку количественных показателей проводили с использованием программы «STATISTICA 6.0» для Windows с использованием параметрических и непараметрических методов. Определяли среднее арифметическое значение (M), среднее квадратичное отклонение (σ), среднюю ошибку среднего арифметического (m). Различия считали достоверными при р<0,05. У больных ХБП I-II стадий уровень СРБ был достоверно выше, чем в контрольной группе и соответствовал средней степени риска кардиальных событий [7]. Среднее значение СРБ у больных ХБП III стадии ассоциировано с высоким риском кардиальных событий [7].
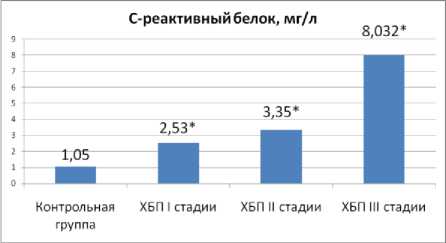
Примечание : *- здесь и далее различия статистически достоверны (р<0,05) по сравнению с группой контроля
Рис. 1. Величина С-реактивного белка в зависимости от стадии ХБП
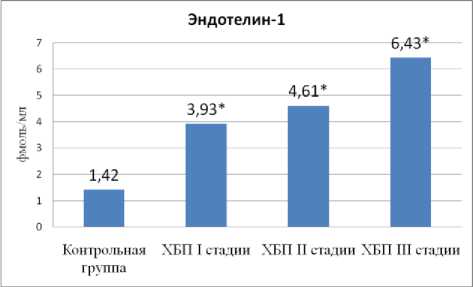
Рис. 2. Уровень эндотелина-1 в зависимости от стадии ХБП
У больных ХБП выявлено увеличение уровня ЭД-1 по сравнению с группой контроля. На рис. 2 представлено увеличение уровня ЭД-1 по мере снижения скорости клубочковой фильтрации. Повышение уровня эндотелина-1 в крови подтверждает факт нарушения выработки вазоактивных веществ, то есть наличия у больных ХБП эндотелиальной дисфункции. Увеличение продукции ЭД-1 нарастает по мере снижения СКФ.
При анализе результатов ЛДФ-грамм было выявлено снижение средней перфузии в микро- циркуляторном русле (М) у больных ХБП вне зависимости от стадии по сравнению с контрольной группой (табл. 2). Минимальная средняя перфузия составляла 2,42±0,23 перф. ед. у больных ХБП I стадии. Повышение перфузии у больных ХБП III стадии может быть связано как с ослаблением артериолярного сосудистого тонуса, которое приводит к увеличению объема крови в артериолах, так и с явлениями застоя крови в венулярном звене. У больных с ХБП по сравнению с группой контроля выявлено достоверное снижение модуляции мик-роциркуляторного русла. Снижение среднего квадратичного отклонения амплитуды колебаний кровотока от значения показателя перфузии (σ) связано с механизмами регуляции микроциркуляции. Увеличение коэффициента вариации (Kv) у больных ХБП по сравнению с группой контроля ассоциировано с повышением нейрогенного и мио-генного тонусов сосудов в результате активации эндотелиальной секреции. Снижение коэффициента вариации в группе ХБП III стадии по сравнению с ХБП I стадии может свидетельствовать об уменьшении эндотелиальной секреции вазодилататоров.
Таблица 2. Показатели микроциркуляции
|
Показатель |
Здоровые (n=30) |
ХБП I стадии (n=30) |
ХБП II стадии (n=30) |
ХБП III стадии (n=31) |
|
М, перф.ед. |
4,955±0,36 |
2,42±0,23* |
2,98±0,27* |
3,80±0,40* |
|
σ, перф.ед. |
2,03±0,23 |
1,23±0,39* |
1,21±0,22* |
1,53±0,22* |
|
Kv,% |
25,39±4,23 |
62,63±12,07* |
51,46±5,31* |
45,05±8,76* |
|
РКК,% |
301,97±1,70 |
397,47±25,97* |
298,04±33,56* |
254,95±20,90* |
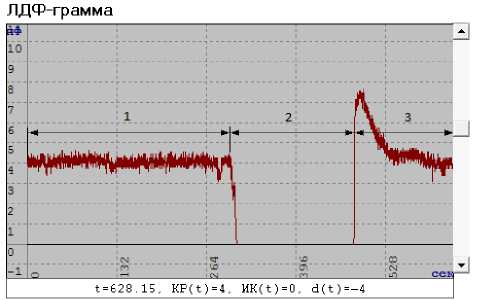
Рис. 3. ЛДФ-грамма больного ХБП III стадии:
1 – ЛДФ-грамма базального кровотока; 2 – период окклюзии; 3 – восстановление микроциркуляторного русла в постокклюзионном периоде
Во всех группах больных ХБП по сравнению с группой контроля выявлено уменьшение резерва кровотока (РКК), что может наблюдаться при увеличении притока крови в микроциркуля-торное русло и при явлениях стаза и застоя крови в венулах. При данных состояниях также отмечается увеличение числа функционирующих капилляров. Кроме того, при возникновении реактивной постокклюзионной гиперемии, часть кинетической энергии притекающих эритроцитов неизбежно расходуется на преодоление инертности форменных элементов, находящихся в состоянии стаза [11]. В связи с этим у больных ХБП наблюдается гиперемический гемодинамический тип микроциркуляции (рис. 3). Резерв кровотока у больных хронической болезнью почек прямо пропорционален скорости клубочковой фильтрации.
Выводы:
-
1. Больные ХБП I и II стадий имеют средний риск развития сердечно-сосудистых осложнений, а при снижении скорости клубочковой фильтрации ниже 59 мл/мин/1,73м2 (ХБП III стадии) риск развития кардиальных событий значительно возрастает.
-
2. Выраженность эндотелиальной дисфункции, проявляющейся увеличением выработки ЭД-1, возрастает с уменьшением скорости клубочковой фильтрации.
-
3. У больных ХБП наблюдается гиперемиче-ский гемодинамический тип микроциркуляции, связанный с застоем крови в венулах.
-
4. Снижение скорости клубочковой фильтрации сопровождается нарушениями в микроциркуля-торном русле.
Список литературы Эндотелиальная дисфункция у больных хронической болезнью почек
- Ho-dac-Pannekeet, M.M. Analysis of non enzymatic glycosylation in vivo: impact of different dialysis solutions/M.M. Ho-dac-Pannekeet, M.F. Weiss, D.R. Waart et al.//Perit. Dial. Int. 1999. Vol. 19, №2. P. 68-74.
- Foley, R.N. The prognostic importance of left ventricular geometry in the uremic cardiomyopathy/R. N. Foley, P. S. Parfrey, I. D. Harnett//J. Am. Soc. Nephrol. 1995. Vol. 5. P. 2024-2031.
- Jones, C.A. Serum creatinine levels in the US population: Third National Health and Nutrition Examination Survey/C.A Jones., G.M. McQuillan Kusek et al.//Am. J. Kidney Dis. 1998. №32. P. 992-999.
- Kang, D.H. Role of microvascular endothelium in progressive renal disease/D.H. Kang, J. Kanellis, C. Hugo et al.//J. Am. Soc. Nephrol. 2002. № 13. P. 806-816.
- Levey, A.S. Cardiovascular disease in chronic renal disease/A.S. Levey, G. Eknoyan//Nephrol. Dial Transplant. 1999. Vol. 14. P. 828-833.
- O’Riordan, E. Endothelial cell dysfunction: the syndrome in mankind/E. O’Riordan, J. Chen, S. Brodsky et al.//Kidney Int. 2005. №67. P.1654-1657.
- Ridker, P.M. C-reactive protein,the metabolic syndrome, and risk of incident cardiovascular events:an 8-year follow-up of 14719 initially healthy American women/P.M. Ridker, J.E. Buring, N.R. Cook, N. Rifai//Circulation. 2003. №107. Р. 391-397.
- Агранович, Н.В. Особенности течения хронического пиелонефрита у лиц пожилого и старческого возраста/Н.В. Агранович, С.А. Кнышова//Медицинский вестник Северного Кавказа. 2011. № 4. С. 85-87.
- Бикбов, Б.Т. Состояние заместительной терапии больных с хронической почечной недостаточностью в Российской Федерации в 1998-2007 гг. (Аналитический отчёт по данным Российского регистра заместительной почечной терапии)/Б.Т. Бикбов, Н.А. Томилина//Нефрология и диализ. 2009. №3. С. 144-223.
- Давыдкин, И.Л. Основы клинической гемостазиологии. Монография/И.Л. Давыдкин, В.А. Кондурцев, Т.Ю. Степанова, С.А. Бобылев. -Самара, 2009. 436 с.
- Крупаткин, А.И. Лазерная допплеровская флоуметрия микроциркуляции крови. Руководство для врачей/А.И. Крупаткин, В.В. Сидоров. -М., 2005. 125 с.
- Мухин, H.A. Кардиоренальные соотношения и риск сердечнососудистых заболеваний/Н.А. Мухин, В.С. Моисеев//Вестник Российской Академии медицинских наук. 2003. № 11. С. 50-55.
- Мухин, Н.А. Хронические прогрессирующие нефропатии и образ жизни современного человека/Н.А Мухин, И.М. Балкаров, С.В. Моисеев и др.//Терапевтический архив. 2004. №76 (9). С. 5-10.
- Нефрология: ил. (Серия « Библиотека врача-специалиста»)./под ред. Е.М Шилова. 2-е изд., испр. и доп. -М: «ГЭОТАР-Медиа», 2010. 696 с.
- Петрищев, H.H. Дисфункция эндотелия. Причины, механизмы, фармакологическая коррекция. -СПб, 2003. 184 с.
- Смирнов, А.В. Превентивный подход в современной нефрологии/А.В Смирнов, И.Г. Каюков, А.М Есаян. и др.//Нефрология. 2004. №8 (3). С. 7-14.
- Смирнов, А.В. Хроническая болезнь почек: на пути к единству представлений/А.В Смирнов, А.М. Есаян, И.Г. Каюков//Нефрология. 2002. № 6 (4). С. 11-17.
- Смирнов, А.В. Уровень эндотелина -1 и реактивность сосудов микроциркуляторного русла кожи у больных на ранних стадиях хронической болезни почек/А.В. Смирнов, Н.Н. Петрищев, И.Ю.Панина и др.//Терапевтичекий архив. 2011. №6. С. 13-15.


