Эндоваскулярная эмболизация простатических артерий как первый этап лечения гиперплазии предстательной железы больших размеров
Автор: Скрябин Е.С., Ханалиев Б.В., Батрашов В.А., Марчак Д.И.
Журнал: Вестник Национального медико-хирургического центра им. Н.И. Пирогова @vestnik-pirogov-center
Рубрика: Клинические наблюдения
Статья в выпуске: 1 т.20, 2025 года.
Бесплатный доступ
Представлено клиническое наблюдение пациента с доброкачественной гиперплазией предстательной железы больших размеров, осложнившейся наличием хронической задержкой мочеиспускания и нарушением сократительной способности детрузора мочевого пузыря. Это привело к развитию острой задержки мочеиспускания - экстренного состояния, требующего безотлогательного дренирования мочевого пузыря. После проведения дополнительных методов обследования пациенту была выполнена эндоваскулярная эмболизация артерий предстательной железы. Вторым этапом лечения выполнена трансуретральная резекция предстательной железы.
Доброкачественная гиперплазия предстательной железы, эндоваскулярная эмболизация простатических артерий, цистостома, трансуретральная резекция предстательной железы
Короткий адрес: https://sciup.org/140309963
IDR: 140309963 | DOI: 10.25881/20728255_2025_20_1_147
Endovascular embolization of prostatic arteries as the first stage of treatment of large benign prostatic hyperplasia
The article presents a clinical observation of a patient with large benign prostatic hyperplasia, complicated with the presence of chronic urinary retention and detrusor atony. These changes in the lower urinary tract led to the development of acute urinary retention - an emergency condition requiring immediate drainage of the bladder. After additional examination methods, the patient underwent endovascular embolization of prostatic arteries. Subsequently, the second stage of treatment was transurethral resection of the prostate gland.
Текст научной статьи Эндоваскулярная эмболизация простатических артерий как первый этап лечения гиперплазии предстательной железы больших размеров
Актуальность
Гиперплазия предстательной железы (ГПЖ) – одно из самых распространенных урологических заболевания у мужчин. Исследования показывают, что распространенность и заболеваемость ГПЖ увеличивается с возрастом, достигая максимума в возрасте около 79 лет. В некоторых регионах распространенность ГПЖ среди мужчин старше 40 лет состав- ляет около 10% и также увеличивается с возрастом [1; 2]. Несмотря на значитель-нос распространение, факторы риска развития ГПЖ остаются неизученными (за исключенением возраста и мужского

Скрябин Е.С., Ханалиев Б.В., Батрашов В.А., Марчак Д.И.
ЭНДОВАСКУЛЯРНАЯ ЭМБОЛИЗАЦИЯ ПРОСТАТИЧЕСКИХ АРТЕРИЙ КАК ПЕРВЫЙ ЭТАП ЛЕЧЕНИЯ ГИПЕРПЛАЗИИ ПРЕДСТАТЕЛЬНОЙ ЖЕЛЕЗЫ БОЛЬШИХ РАЗМЕРОВ пола). Стандартным методом хирургического лечения гиперплазии предстательной железы (при отсуствии противопоказаний) в настоящий момент является трансуретральная резекция предстательной железы (ТУР-ПЖ). Исследование, проведенное в США, показало, что в течение первого года после хирургического лечения ГПЖ частота сложнений после ТУР-ПЖ составляет около 17%, после фотоселективной вапоризации – 19% и 26% после водной термотерапии. Это свидетельствует о том, что значительное количество пациентов сталкивается с осложнениями после хирургического лечения [2]. Риск развития осложнений в интра- и послеоперационном периоде в первую очередь связаны с длительностью выполнения оперативного вмешательства, снижением сократительной способности детрузора мочевого пузыря и наличием сопуствующей патологии. Учитывая тот факт, что длительность оперативного вмешательства прямым образом может повлиять на функциональные результаты в послеоперационном периоде, ТУР-ПЖ не рекомендовано выполнять пациентам с объемом предстательной железы более 80–100 см3. Хоть ГПЖ может протекать и бессимптомно, наиболее частым проявлением данного состояния является развитие симптомов нижних мочевых путей (СНМП). Разделяют симптомы фаз накопления и опорожнения. К симптомам фазы опорожнения относят затрудненное и/или прерывистое мочеиспускание, натуживание при мочеиспускании. К симптомам фазы накопления относят учащенное мочеиспускание малыми порциями, ночная поллакиурия, ургентные позывы к мочеиспусканию, недержание мочи, чувство неполного опорожнения мочевого пузыря. Первые шаги в лечении ГПЖ направлены на объективную оценку симптомов и выбор подходящей терапии в зависимости от их тяжести. Согласно медицинской литературе, начальная оценка включает использование Международной шкалы симптомов простаты (IPSS) для диагностики и мониторинга эффективности лечения [3; 4]. Так, для пациентов с легкими симптомами или без значительных жалоб рекомендуется наблюдательная тактика с изменением образа жизни, включая ограничение потребления жидкости перед сном, уменьшение потребления кофеина и алкоголя, а также выполнение уражне-ний для укрепления мышц тазового дна [5]. Если симптомы умеренные или тяжелые, начальная медикаментозная терапия включает в себя прием альфа-блокаторов и ингибиторов 5-α-редуктазы, которые обеспечивают улучшение качества мочеиспускания и некоторого уменьшения объема предстательной железы [6]. Но прием медикаментозных препаратов не всегда позволяет добиться удовлетворительного результата, если консервативная терапия не приносит желаемого результата или возникают осложнения и побочные эффекты, может потребоваться проведение хирургического вмешательства. Показаниями к проведению операции является рецидивирующая задержка мочи, выраженность симптомов инфравезикальной обструкции, наличие камней мочевого пузыря, большое количество остаточной мочи, неэффективность консервативной терапии. В арсенале урологической помощи появляются всё новые и миниинвазивные методы лечения, которые характеризуются наличием более низкой частотой развития осложнений. Одним и методов миниин-вазивной хирургической помощи пациентам с СНМП является эмболизация простатических артерий (ЭПА).
ЭПА в контексте ГПЖ представляет собой минимально инвазивную процедуру, направленную на уменьшение СНМП, связанных с ГПЖ. В основе эффекта ЭПА лежит снижение артериального притока крови к предстательной железе, вследствие этого наступает ишемия и некроз органа и выраженное уменьшение объема, что приводит к снижению выраженности СНМП. Этот метод становится все более популярным благодаря своей эффективности и низкой встречаемости развития осложнений по сравнению с хирургическими методами. ЭПА рассматривается как альтернатива для пациентов с умеренными и тяжелыми СНМП, которые не реагируют на медикаментозное лечение. Исследования показывают, что ЭПА может быть эффективной у значительной части пациентов, улучшая качество жизни и снижая симптомы. Основные осложнения встречаются редко и включают в себя постэмболизационный синдром (локальная боль, гипертермия), острую задержку мочеиспускания. В сравнении с эндоурологическими оперативными вмешательствами, ЭПА имеет меньший риск развития осложнений и не требует общей анестезии или длительной госпитализации [7–9]. Перед проведением ЭПА необходимо выпонение МСКТ органов малого таза в ангиорежиме для определения ангиоархитектоники малого таза и выявления типа отхождения простатической артерии, оценки наличия коллатеральных ветвей. ЭПА показала сопоставимые результаты в сравнеии в ТУР-ПЖ в отношении улучшения симптомов и качества жизни, хотя ТУР-ПЖ может быть более эффективной в снижении объема простаты и увеличении максимального потока мочи (Qmax) согласно урофлоуметрии.
У пациентов с большим объемом предстательной железы (более 150 см3) целесообразно назначение альфа-блокаторов и ингибиторов 5- α -редуктазы с целью уменьшения объема простаты. Однако, для достижения эффекта 5- α -редуктазы необходимо постоянно принимать минимум 6 месяцев. Если учитывать факт наличия сопутствующей патологии у пациента и осложнений ГПЖ, проведение консервативной терапии на такой длительный срок не рекомендуется, что в свою очередь может усугубить ситуацию и усилить СНМП. Ниже представлено клиническое наблюдение пациента с гиперплазией предстательной железы больших размеров, которому проведено поэтапное лечение.
Клиническое наблюдение
Пациент С., 73 года, 11.01.2024 г. консультирован урологом НМХЦ им. Н.И. Пирогова с жалобами на мочеиспускание вялой струей, чувство неполного опорожнения мочевого пузыря. Из анамнеза известно, что с 2019 г. наблюдается урологом по поводу гиперплазии предстательной железы, самостоятельно принимает альфа-блокаторы с незначительным положительным клиническим эффектом. При обследовании выявлено сначительное снижение Qmax до 4,4 мл/с по данным урофлоуметрии (Рис. 1). Наличие значительного объема остаточной мочи по данным УЗИ – до 250–300 мл после каждой микции. По данным МРТ органов малого таза выявлено наличие выраженной гиперплазии предстательной железы – 180 см3 (Рис. 2).
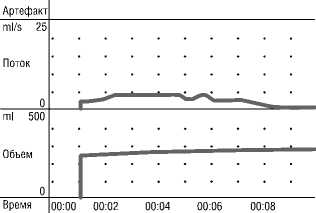
Средняя скорость потока: 2,5 ml/s Макс, скорость потока: 4,4 ml/s Время до макс, потока: 1,9 s Выделенный объём: 271,6 ml
Рис. 1. Урофлоуметрия пациента до проведения лечения.

Скрябин Е.С., Ханалиев Б.В., Батрашов В.А., Марчак Д.И.
ЭНДОВАСКУЛЯРНАЯ ЭМБОЛИЗАЦИЯ ПРОСТАТИЧЕСКИХ АРТЕРИЙ КАК ПЕРВЫЙ ЭТАП ЛЕЧЕНИЯ ГИПЕРПЛАЗИИ ПРЕДСТАТЕЛЬНОЙ ЖЕЛЕЗЫ БОЛЬШИХ РАЗМЕРОВ
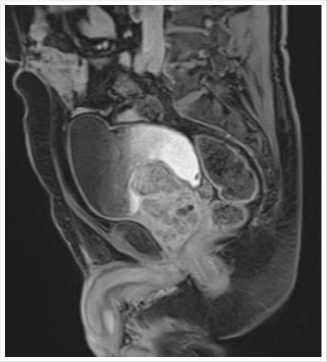
Рис. 2. Сагиттальный срез МРТ пациента на догоспитальном этапе, объем простаты 180 см3 с наличием выраженной средней доли.
В амбулаторных условиях пациент обследован и консультирован смежными специалистами. Диагностировано наличие выраженной сопутствующей патологии: гипертоническая болезнь 3 стадии, 3 степени, риск сердечно-сосудистых осложнений 4, ИБС, постинфарктный кардиосклероз. НК ХСН 2. ФК 2, ожирение 2 степени, сахарный диабет 2 типа (медикаментозно компенсированный), жировой гепатоз. Учитывая степень и тяжесть основного заболевания с развитием осложнений, пациенту рекомендовано проведение ЭПА, от которой пациент на момент осмотра отказался. 10.02.2024 г. у пациента возник эпизод острой задержки мочеиспускания, который потребовал выполнения троакарной цистостомии. 15.02.2024 г. пациент повторно консультирован урологом НМХЦ им. Н.И. Пирогова, повторно предложено проведение ЭПА. По данным МСКТ органов малого таза в ангиорежиме выявлено отхождение артерии простаты в средней трети внутренней половой артерии (Рис. 3).
14.03.2024 г. пациент в плановом порядке госпитализирован в НМХЦ им. Н.И. Пирогова, выполнена ангиография с последующей ЭПА. При осмотре по данным УЗИ мочеполовой системы: УЗ-признаки выраженной ГПЖ (объем простаты 190 см3), нарушение эвакуатор-ной функции мочевого пузыря. Анализ крови на ПСА общий – 6,7 нг/мл. Учитывая объем ГПЖ, наличие цистостмиче-ского дренажа, биопсию предстательной железы принято решение не выполнять. 15.03.2024 г. выполнена суперселективная эмболизация простатических артерий (Рис. 4, 5).
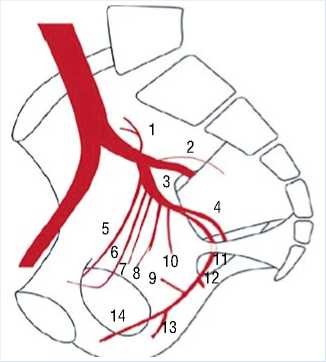
Рис. 3. Схематическое изображение исходящих артериальных ветвей из внутренней подвздошной артерии, вариант отхождения простатической артерии у данного пациента (Ulf Teichgr a ber, Ren e Aschenbach, Ioannis Diamantis, 2018) 1 – Подвздошно-поясничная артерия, 2 – внутренняя крестцовая артерия, 3 – верхняя ягодичная артерия, 4 – нижняя ягодичная артерия, 5 – запирательная артерия, 6 – пупочная артерия, 7 – верхняя пузырная артерия, 8 – нижняя пузырная артерия, 9 – артерия предстательной железы, 10 – верхняя прямокишечная артерия, 11 – внутренняя половая артерия, 12 – нижняя прямокишечная артерия, 13 – промежностная артерия, 14 – дорсальная артерия полового члена.
Ранний послеоперационный период протекал гладко, без осложнений. Проводилась плановая противовоспалительная и симптоматическая терапия. 18.03.2024 г. в удовлетворительном состоянии выписан под наблюдение урологом по месту оказания медицинской помощи. При контрольном обследовании по данным УЗИ от 24.05.2020 г.: УЗ-признаки ДГПЖ, объем предстательной железы 152 см3, хронического простатита, кистозной дегенерации предстательной железы. 20.07.2024 г. осмотрен урологом НМХЦ им. Н.И. Пирогова, пациент отметил возобновление самостоятельного мочеиспускания (Рис. 6). Выполнена урофлоуметрия, при которой отмечено увеличение Qmax до 6,5 мл/с.
При контрольном УЗИ органов мочеполовой системы отмечено уменьшение объема предстательной железы до 110 см3. Несмотря на выраженный клинический эффект, по истечении 5 месяцев с момента оперативного вмешательства, в виде уменьшения объема предстательной железы с 190 см3 до 110 см3, пациент предъявлял жалобы на наличие цисто-
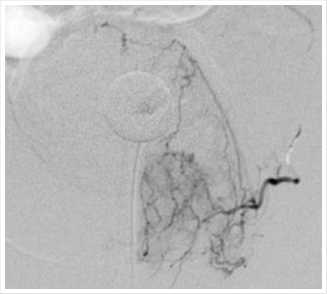
Рис. 4. Выявление простатической артерии. Отмечаются контуры цистостомического дренажа в полости мочевого пузыря.
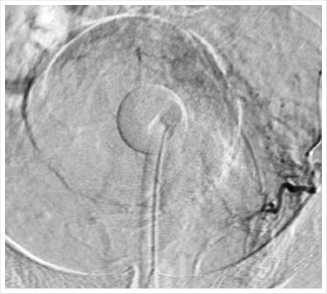
Рис. 5. Достигнут эффект «стоп-контраст» – кровоток в артериях предстательной железы остановлен.
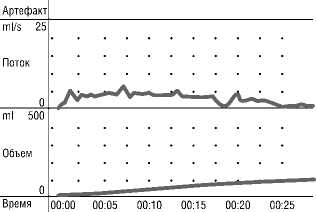
Средняя скорость потока: 2,9 ml/s Макс, скорость потока: 6,5 ml/s Время до макс, потока: 7,2 s Выделенный объём: 83,0 ml
Рис. 6. Урофлоуметрия пациента через 4 месяца после ЭПА. Отмечается увеличение скорости максимального потока.
стомического дренажа и желание восстановить адекватное самостоятельное мочеиспускание. После компенсации сопутствующей патологии пациенту было предложено хирургическое лечение в объеме — трансуретральной резекции предстательной железы. При обследовании противопоказаний для проведения планируемого оперативного лечения на момент осмотра не выявлено.
Скрябин Е.С., Ханалиев Б.В., Батрашов В.А., Марчак Д.И.
ЭНДОВАСКУЛЯРНАЯ ЭМБОЛИЗАЦИЯ ПРОСТАТИЧЕСКИХ АРТЕРИЙ КАК ПЕРВЫЙ ЭТАП ЛЕЧЕНИЯ ГИПЕРПЛАЗИИ ПРЕДСТАТЕЛЬНОЙ ЖЕЛЕЗЫ БОЛЬШИХ РАЗМЕРОВ
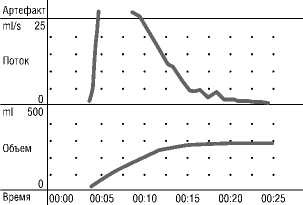
Средняя скорость потока: 10,6 ml/s
Макс, скорость потока: 35,4 ml/s
Время до макс, потока: 3,0 $
Выделенный объём: 266,0 ml
Рис. 7. Урофлоуметрия пациента на 4 сутки после ТУР-ПЖ.
23.08.2024 г. в плановом порядке выполнено оперативное вмешательство: трансуретральная резекция предстательной железы. В послеоперационном периоде проводилась комплексная симптоматическая, гемостатическая, противовоспалительная терапия. 25.08.2024 г. уретральный катетер удален. 26.08.2024 г. цистостомический дренаж удален, восстановлено самостоятельное мочеиспускание. Кожно-мочепузырный свищ зажил первичным натяжением. По данным урофлоуметрии от 27.08.2024 г. объем мочеиспускания – 266 мл, средняя скорость потока 10,6 мл/с, максимальная – 35,4 мл/с (Рис. 7). 28.08.2024 г. в удовлетворительном состоянии выписан под амбулаторное наблюдение урологом по месту оказания медицинской помощи. В настоящее время пациент доволен результатом проведенного лечения, жалоб не предъявляет.
Таким образом, данное клиническое наблюдение показывает перспективу применения эмболизации артерий предстательной железы у пациентов со значительным объемом простаты и наличием абсолютных противопоказаний для проведения стандартного объема вмешательства в виде трансуретральной резекции предстательной железы. Учитывая первоначальный объем предстательной железы врач-уролог может прогнозировать длительность оперативного вмешательства и вероятность развития кровотечения. ЭПА может быть использована в качестве первого этапа лечения пациентов с крупным объемом ГПЖ. Эмболизация приводит к постепенному снижению объема простаты, что помогает минимализировать длительность хирургического вмешательства. Учитывая факт того, что кровоток в простате значительно уменьшается, ткань предстательной железы подвергается ише-мизации с последующим замещением паренхимы органа на соединительную ткань. Для хирурга-уролога это может стать ключевым этапом для проведения адекватной и «радикальной» ТУР-ПЖ – интраоперационное кровотечение после ЭПА значительно снижается.
Список литературы Эндоваскулярная эмболизация простатических артерий как первый этап лечения гиперплазии предстательной железы больших размеров
- Bryn ML, Kevin TM, William AR, Granville LL The rising worldwide impact of benign prostatic hyperplasia 2021; 127(6): 722-728. DOI: 10.1111/bju.15286
- Kaplan S, Kaufman RP, Mueller T, et al. Retreatment rates and postprocedural complications are higher than expected after BPH surgeries: a US healthcare claims and utilization study. Prostate Cancer Prostatic Dis. 2024; 27: 485-491. DOI: 10.1038/s41391-023-00741-8
- Arnold MJ, Gaillardetz A, Ohiokpehai J. Benign Prostatic Hyperplasia: Rapid Evidence Review. Am Fam Physician. 2023; 107(6): 613-622.
- Smetana GW, Smith CC, Singla A, Libman H. How Would You Manage This Patient With Benign Prostatic Hyperplasia?: Grand Rounds Discussion From Beth Israel Deaconess Medical Center. Ann Intern Med. 2023; 176(4): 545-555. DOI: 10.7326/M23-0113 EDN: FFKWID
- Expert Panel on Urological Imaging; Alexander LF, Oto A, Allen BC, et al. ACR Appropriateness Criteria® Lower Urinary Tract SymptomsSuspicion of Benign Prostatic Hyperplasia. J Am Coll Radiol. 2019; 16(11S): S378-S383. DOI: 10.1016/j.jacr.2019.05.031
- Haile ES, Sotimehin AE, Gill BC. Medical management of benign prostatic hyperplasia. Cleve Clin J Med. 2024; 91(3): 163-170. DOI: 10.3949/ccjm.91a.23027
- Ini' C, Vasile T, Foti PV, et al. Prostate Artery Embolization as Minimally Invasive Treatment for Benign Prostatic Hyperplasia: An Updated Systematic Review. J Clin Med. 2024; 13(9): 2530. DOI: 10.3390/jcm13092530
- Naidu SG, Narayanan H, Saini G, et al. Prostate Artery Embolization-Review of Indications, Patient Selection, Techniques and Results. J Clin Med. 2021; 10(21): 5139. DOI: 10.3390/jcm10215139
- Bilhim T, Bagla S, Sapoval M, et al. Prostatic Arterial Embolization versus Transurethral Resection of the Prostate for Benign Prostatic Hyperplasia. Radiology. 2015; 276(1): 310-1. DOI: 10.1148/radiol.2015141853


