Эндоваскулярная реваскуляризация обструктивно поражённого венозного подвздошно-бедренного сегмента различной протяжённости при посттромботической болезни
Автор: Шевченко Ю.Л., Литвинов А.А., Стойко Ю.М., Марчак Д.И., Ермаков Д.Ю.
Журнал: Вестник Национального медико-хирургического центра им. Н.И. Пирогова @vestnik-pirogov-center
Рубрика: Редакционные статьи
Статья в выпуске: 1 т.20, 2025 года.
Бесплатный доступ
Тромбоз глубоких вен и связанная с ним посттромботическая болезнь (ПТБ) представляют собой значимую медико-социальную проблему, особенно в случаях поражения подвздошно-бедренного сегмента вен. Около 70% пациентов с проксимальным венозным тромбозом сталкиваются с полной окклюзией либо частичной реканализацией, что приводит к стойкой обструкции венозного оттока и прогрессированию ПТБ. Современные методы лечения в виде эндоваскулярной дезобструкции и венозного стентирования показывают неоднозначные клинические результаты, в связи с этим существует необходимость в изучении факторов риска, влияющих на эффективность этих вмешательств в зависимости от протяженности обструкции.Цель исследования: оценить эффективность и безопасность эндоваскулярного лечения пациентов с посттромботической проксимальной обструкцией венозного русла подвздошно-бедренного сегмента различной протяженности.Материалы и методы: в ретроспективное исследование включены 99 пациентов с ПТБ, осложненной посттромботической обструкцией подвздошнобедренного сегмента, которым с 2016 по 2024 гг. были проведены эндоваскулярные реканализации. Пациенты разделены на две группы в зависимости от протяженности обструкции подвздошно-бедренного сегмента. В I группу (28 пациентов) вошли пациенты с обструктивным поражением подвздошного сегмента, во II группу (71 пациент) - с обструктивным поражением подвздошных, общей бедренной и поверхностной бедренной вен (подвздошно-бедренный сегмент). Клиническая оценка пациентов проводилась согласно международной классификации CEAP, а также с использованием клинических опросников Villalta, VCSS и CIVIQ-20. Основными показателями эффективности лечения являлись снижение суммы баллов по клиническим шкалам Villalta, VCSS, CIVIQ-20, а также подтверждение проходимости УЗДС стентированного участка подвздошно-бедренного сегмента различной протяженности через 3 месяца после выписки.Результаты: технический успех эндоваскулярной реканализации в обеих группах достигнут у всех пациентов. В обеих группах отмечено статистически значимое улучшение показателей согласно клиническим шкалам Villalta, VCSS, CIVIQ-20 (p function show_abstract() { $('#abstract1').hide(); $('#abstract2').show(); $('#abstract_expand').hide(); }
Посттромботическая болезнь, венозная обструкция, венозное стентирование, эндоваскулярная реканализация
Короткий адрес: https://sciup.org/140309975
IDR: 140309975 | DOI: 10.25881/20728255_2025_20_1_4
Endovascular stenting of obstructive lesions of varying extent in patients with post-thrombotic syndrome
Deep vein thrombosis (DVT) and its associated post-thrombotic syndrome (PTS) represent a significant medical and social challenge, particularly in cases involving the iliofemoral venous segment. Approximately 70% of patients with proximal venous thrombosis experience complete occlusion or partial recanalization, leading to persistent venous outflow obstruction and progression of PTS. Current treatment methods, including endovascular desobstruction and venous stenting, show mixed clinical results, highlighting the need to study the risk factors affecting the efficacy of these interventions.Objective: To evaluate the effectiveness and safety of endovascular treatment in patients with post-thrombotic proximal obstruction of the iliofemoral venous segment of varying lengths.Materials and Methods: This retrospective study included 99 patients with PTS complicated by post-thrombotic obstruction of the iliofemoral venous segment who underwent venous stenting between 2016 and 2024. Patients were divided into two groups based on the length of the iliofemoral segment occlusion. Clinical assessment was conducted using the international CEAP classification and clinical questionnaires such as Villalta, VCSS, and CIVIQ-20. The primary outcomes of treatment effectiveness were reductions in scores on the Villalta, VCSS, and CIVIQ-20 scales, as well as confirmation of patency of the stented iliofemoral segment via ultrasound duplex scanning three months post-discharge.Results: Technical success of stenting was achieved in all patients across both groups. Both groups showed statistically significant improvements in clinical scores (Villalta, VCSS, CIVIQ-20; p function show_eabstract() { $('#eabstract1').hide(); $('#eabstract2').show(); $('#eabstract_expand').hide(); }
Текст научной статьи Эндоваскулярная реваскуляризация обструктивно поражённого венозного подвздошно-бедренного сегмента различной протяжённости при посттромботической болезни
Тромбоз глубоких вен является важной медико-социальной проблемой с достаточно высокой частотой встречаемости, в России и Европе она оценивается примерно в 1 случай на 1000 человек в год [1; 2]. В зависимости от локализации тромбоза, у 23–60% пациентов развивается посттромботическая болезнь (ПТБ), несмотря на высокую приверженность к назначенной оптимальной медикаментозной терапии [3]. При этом 40% случаев проксимального тромбоза локализуется в подвздошно-бедренном венозном сегменте [4]. Несмотря на антикоагулянтную терапию и компрессионное лечение, адекватной реканализации просвета венозного русла пораженного сегмента у 70% таких пациентов так и не происходит, что приводит к стойкой обструкции венозного оттока, который является ключевым звеном развития ПТБ [5].
Проблема венозного стентирования получила актуальность во второй половине XX века, когда были проведены первые экспериментальные исследования венозных стентов на животных. Но уже в 1988 г. Zollikofer с соавт. сообщили о выполненном венозном стентировании у 4 пациентов с послеоперационным стенотическим сужением вен и гемодиализных шунтов [6]. А в 1991 г. Elson J.D. и соавт. продемонстрировали результаты эндоваскулярного стентирования у 7 пациентов с тромботическими поражениями верхней и нижней полых вен [7]. Среди отечественных учёных большой вклад в изучение механизмов развития ПТБ внесли А.Н. Веденский, В.С. Савельев, В.И. Прокубовский и другие [8].
Среди открытых реконструктивных вмешательств наиболее распространенной считалась методика перекрестного аутовенозного шунтирования, предложенная E.S. Palma в 1960 г. и применяемая при односторонних коротких проксимальных окклюзиях подвздошных вен [9]. Различными авторами сообщались результаты проходимости шунтов от 63 до 89% в ходе наблюдения за пациентами после данных вмешательств [10–12]. В литературе опубликована серия результатов операций Palma, включающая 412 реконструкций с проходимостью шунтов от 70 до 83% в сроки наблюдения от 3 до 5 лет [13]. В России наибольший опыт применения операции Palma представлен в статье А.Н. Веденского, Ю.М. Стойко, В.В. Сабельникова в 1997 г. В исследование были включены 328 больных с односторонней обструкцией подвздошного сегмента, которым было выполнено перекрестное аутовенозное шунтирование. Авторы отметили клиническое улучшение в 90% случаев в ближайшем послеоперационном периоде [14].
Но в настоящее время с развитием эндоваскулярных методик, направленных на минимизацию хирургического воздействия, основным методом лечения окклюзий или-офеморального сегмента при ПТБ является дезобструкция венозного русла, осуществляемая путем баллонной ангиопластики и стентирования окклюзированного участка [15]. С учетом наличия фиброзных изменений венозной стенки, а также локализации поражения в области функционально активных зон, на сегодняшний день разработаны специализированные венозные стенты с характеристиками, отвечающими современным требованиям для полноценного функционирования в венозном русле [16].
Однако проблема с применением новых методов и инструментов полностью не решена: показатели технического успеха и проходимости стентов в послеоперационный период оказались достаточно различными. В метаанализе M.K. Razavi (2015), включившем 37 исследований и 2869 пациентов с нетромботическим, острым и хроническим тромботическими формами обструкций венозного русла, автор сообщает о показателях проходимости стентов через 1 год наблюдения, варьирующихся от 79% до 99% и зависящих от характера и генеза формирования обструктивного поражения вен [17]. В систематическом обзоре, включающем 16 исследований с участием 2373 пациентов, M.J. Seager и соавт. (2016) пришли к выводу, что данные вмешательства особенно эффективны у тяжелых пациентов с трофическими язвами, приводят к их устойчивому заживлению и облегчению симптомов в 56–100% случаев. Но при этом показатели проходимости стентированного участка в послеоперационном периоде по данным исследователей составляли от 32 до 98,7% [18]. В метаанализе W. Wang, включающего 14 исследований с участием 1987 пациентов, которым выполнялось стентирование хронических окклюзий вен, продемонстрировано, что показатели первичной проходимости стентов после восстановления просвета колеблются от 67,0 до 98,7% [19]. В связи с этим до сих пор представляется весьма актуальным оценка клинической эффективности эндоваскулярных методик в зависимости от протяженности поражения подвздошно-бедренного венозного сегмента, а также изучение факторов, влияющих на результат эндоваскулярного лечения пациентов с посттромботической болезнью и обструктивным поражением проксимальных отделов венозного русла нижних конечностей.
Цель исследования: оценить эффективность и безопасность эндоваскулярного лечения пациентов с посттромботической проксимальной обструкцией венозного русла подвздошно-бедренного сегмента различной протяженности.
Материалы и методы
В ретроспективное исследование включены 99 больных ПТБ, осложненной посттромботической обструкцией подвздошно-бедренного сегмента, которым с 2016 по 2024 гг. было проведено венозное стентирование в отделении рентгенохирургии клиники грудной и сердечнососудистой хирургии им. Св. Георгия НМХЦ им. Н.И. Пирогова. Пациенты разделены на две группы в зависимости от протяженности обструкции подвздошно-бедренного сегмента. Из них 28 пациентов (1-я группа) имели обструктивное поражение только одного (подвздошного)

венозного сегмента, а у 71 пациента (2-я группа) имелось протяженное обструктивное поражение подвздошных, общей бедренной и поверхностной бедренной вен (подвздошно-бедренный сегмент).
Критерии включения в исследование: тяжелая форма ХЗВ (С3–С6 по классификации CEAP) с наличием тромботической обструкции подвздошно-бедренного венозного сегмента различной протяженности.
Критерии невключения в исследование: возраст младше 18 лет, острая стадия тромбоза глубоких или поверхностных вен нижних конечностей, диффузная обструкция глубоких вен нижних конечностей с окклюзией глубокой бедренной вены. Пациенты с выраженной недостаточностью функции почек, тяжелый коморбид-ный фон.
Медиана возраста больных составила 39,9 (IQR 30–46,5) и 40 (IQR 31,5–48) лет в 1 и 2 группах, соответственно, p = 0,102. В обеих группах преобладал женский пол: в I группе 6 мужчин (21,4%) и 22 женщины (78,6%), во II группе 29 мужчин (40,8%) и 42 женщины (59,2%). Клиническая оценка пациентов обеих групп до и после вмешательства соответствовала международной классификации CEAP, а также оценка тяжести заболевания осуществлялась с помощью клинических опросников Villalta и VCSS, а качество жизни оценивалась по шкале CIVIQ-20 (Табл. 1).
Большинство пациентов 1 и 2 групп предъявляли субъективные жалобы на боль и тяжесть, а также на чувство распирания в бедре и голени пораженной нижней конечности, усиливающихся при физической нагрузке. Среди клинических проявлений у больных обеих групп отмечался отек пораженной конечности перманентного характера, что соответствовало клиническому классу С3 по классификации CEAP (в I группе – 26 больных (92,9%), во II группе 57 больных (80,3%)). 3 пациента (4,2%) из II группы имели трофические нарушения кожных покровов, проявляющиеся гиперпигментацией и липодерматосклерозом, соответствующие клиническому классу C4 по классификации CEAP. Наиболее тяжелым клиническим проявлением считалось наличие трофических язв в области голени (клинический класс C6 по классификации CEAP), и отмечавшееся у 2 пациентов I группы (7,1%) и 3 пациентов (4,2%) II группы. При этом еще 8 пациентов (11,3%) из II группы имели их ранее в анамнезе (клинический класс C5 по классификации CEAP). Пациенты обеих групп были привержены к назначенной им ранее компрессионной и медикаментозной терапии.
В качестве визуализирующих методик на доопера-ционном этапе преимущество отдавалось выполнению МР-флебографии, МСКТ-флебографии или прямой восходящей флебографии. Ангиографические характеристики пациентов первой группы (28 больных) проявлялись в виде окклюзивного поражения только подвздошного сегмента с отсутствием посттромботических изменений нижележащих венозных сегментов (Рис. 1 А). Во второй группе (71 пациент) имелось протяженное окклюзивное поражение подвздошного сегмента, а также общей бедренной и поверхностной бедренной вен (Рис. 1 Б).
На дооперационном этапе прямая восходящая флебография вен нижних конечностей выполнялась на ангиографической установке Toshiba Infinix 9000 по стандартному протоколу с оценкой полученных результатов двумя независимыми специалистами.
В процессе стентирования больным имплантировались специализированные венозные стенты с плетеной структурой (Wallstent), а также стенты, выполненные в результате лазерной резки (Abre, Venovo), которые широко используются в отечественной и зарубежной эндоваскулярной хирургии.
Оперативное вмешательство пациентам I и II групп выполнялось через подколенный доступ. С целью
Табл. 1. Клинико-демографическая характеристика пациентов
|
Критерий |
Группа I |
Группа II |
p |
|
Пол |
6 (21,4%) |
29 (40,8%) |
0,102 |
|
– мужской, n (%) |
|||
|
Возраст, полных лет (Me [IQR]) |
39,5 [30–46,5] |
40 [31,5–48] |
0,762 |
|
ИМТ, кг/м2 (Me [IQR]) |
26,7 [24,3–28,5] |
26,4 [23,2–31] |
0,98 |
|
Сторона поражения |
24 (85,7%) |
57 (80,3%) |
0,773 |
|
– слева, n (%) |
Тяжесть заболевания по классификации CEAP
|
– C3, n (%) |
26 (92,9%) |
57 (80,3%) |
0,223 |
|
– C4, n (%) |
– |
3 (4,2%) |
0,556 |
|
– C5, n (%) |
– |
8 (11,3%) |
0,101 |
|
– C6, n (%) |
2 (7,1%) |
3 (4,2%) |
0,620 |
|
Villalta, количество баллов (Me [IQR]) |
10 [8–11] |
14 [12–15,5] |
<0,001* |
|
VCSS, количество баллов (Me [IQR]) |
8 [6–9,5] |
10 [9–12] |
<0,001* |
|
CIVIQ-20, количество баллов (Me [IQR]) |
53 [45,5– 62] |
66 [56–71,5] |
<0,001* |
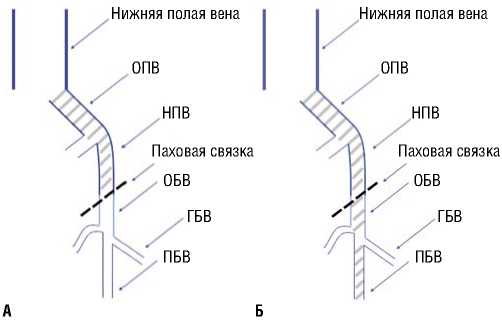
Рис. 1. Схематическое изображение обструктивного поражения подвздошного сегмента у пациентов I группы (а) и подвздошно-бедренного сегмента у пациентов II группы (б).

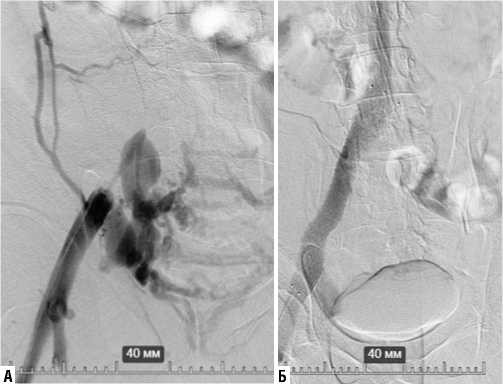
Рис. 2. Результаты ангиографии пациента I группы до (а) и после (б) выполнения стентирования подвздошного венозного сегмента.
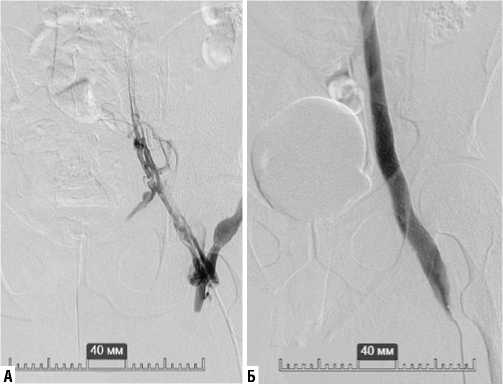
Рис. 3. Результаты ангиографии пациента II группы до (а) и после (б) выполнения стентирования подвздошного-бедренного венозного сегмента.
снижения риска интраоперационных тромботических осложнений внутривенно вводили 100 ЕД/кг раствора гепарина натрия. Реканализация окклюзии осуществлялась антеградно с использованием поддерживающего катетера при помощи гидрофильных проводников по принципу эскалации их жесткости. Баллонная ангиопластика выполнялась поэтапно: начиная с низкопрофильных катетеров малого диаметра, заканчивая баллонным катетером из нейлона с диаметром, соответствующим номинальному диаметру венозного русла в данном сегменте (Рис 2, 3).
В послеоперационном периоде пациенты получали эноксапарин подкожно в дозировке 1мг/кг массы тела 2 раза/сут. в течение 2 недель с последующим переходом на пероральную антитромботичесекую терапию в комбинации ривароксабан 20мг/сут. и клопидогрел 75 мг/сут. на срок не менее 6 месяцев.
В первые сутки после стентирования выполнялся ультразвуковой контроль проходимости стентированного участка с определением значений пиковой скорости кровотока в зоне имплатированного стента. Исследование проводилось на УЗ-аппарате экспертного класса General Electric Vivid E9 (Рис. 4).
Клиническая оценка пациентов в послеоперационном периоде происходила через 6 месяцев после выполненного вмешательства. Повторная оценка проходимости стентированного участка происходила в то же время посредством выполнения ультразвукового дуплексного сканирования (УЗДС) вен нижних конечностей.
Статистический анализ
Статистические расчеты проведены в программе SPSS 26. Оценено соответствие данных нормальному распределению (использовался критерий
Шапиро–Уилка). Показатели описательной статистики включали число наблюдений (n), медиану (Ме), межквартильный размах [IQR]. В случаях, когда распределение
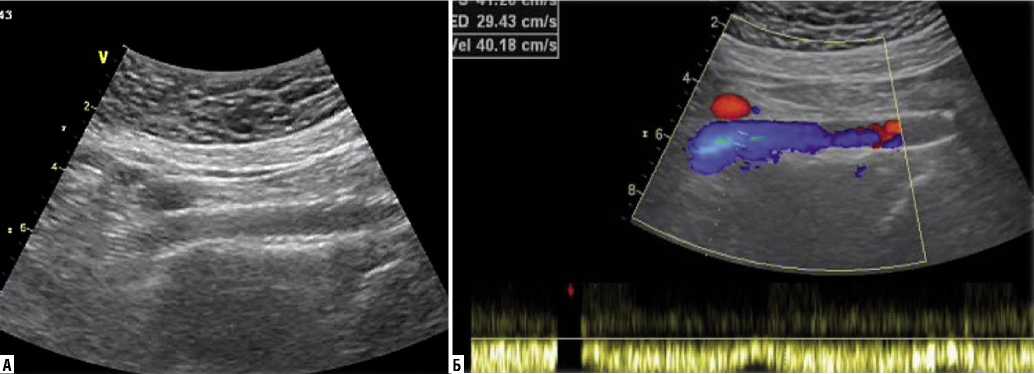
Рис. 4. Ультразвуковой контроль проходимости стентированного участка (а) и определение значений пиковой скорости кровотока в стенте (б).
Табл. 2. Сравнение показателей по клиническим шкалам до и после операции
Результаты
В раннем послеоперационном периоде пациенты обеих групп отмечали снижение интенсивности, а в некоторых случаях и полное купирование ранее предъявляемых жалоб: субъективно уменьшено или полностью исчезло чувство тяжести в пораженной конечности, увеличена толерантность в физической нагрузке. Среди пациентов с незаживающими трофическими язвами у 1 пациента из I группы и у 2 пациентов из II группы достигнута полная эпитализация язвенного дефекта в срок до 6 месяцев. Отмечено статистически значимое улучшение клинических показателей в обеих группах по сумме баллов согласно клиническим шкалам VILLALTA, VCSS, CIVIQ-20 (Табл. 2).
После выполненного эндоваскулярного вмешательства проходимость стентированного участка через 6 месяцев подтверждена у 27 пациентов (93,2%), во второй группе – 60 пациентов (83,3%). Среди 11 пациентов II группы, у которых ранний послеоперационный период осложнился тромбозом стентированного участка, у 2 пациентов отмечена деформация конструкции имплантированного стента.
При оценке факторов риска в обеих группах выявлены два предиктора, значимо влияющие на вероятность развития тромбоза стентированного участка в послеоперационном периоде: протяженность поражения более 1 венозного сегмента (ОШ 2,644; 95 % ДИ 1,552–12,664, p = 0,049) и скорость кровотока в стентированном участке менее 13 см/с (ОШ 94,500, 95 % ДИ 15,139–589,888, p<0,001) (Табл. 3).
Проведен многофакторный анализ влияния значений пиковой скорости венозного кровотока в зоне стентированного участка на результат оперативного лечения обеих групп: выявлено пороговое значение
Табл. 3. Оценка факторов риска на вероятность развития тромбоза стентированного участка
|
Параметр |
ОШ |
95% ДИ |
p |
|
Возраст старше 40 лет |
0,369 |
0,105–1,290 |
0,083 |
|
Мужской пол |
0,506 |
0,130–1,977 |
0,708 |
|
ИМТ >30 кг/м2 |
1,217 |
0.342–4.339 |
0,762 |
|
Левосторонний тромбоз |
1,257 |
0,253 – 6,236 |
0,78 |
|
Клинический класс выше С3 по шкале CEAP |
0,935 |
0,187–4,686 |
0,66 |
|
15 и более баллов по шкале Villallta |
0,397 |
0,082–1,917 |
0,468 |
|
Более 10 баллов по шкале VCSS |
0,617 |
0,191–1,992 |
0,897 |
|
Более 60 баллов по шкале CIVIQ |
2,899 |
0,745–11,271 |
0,293 |
|
Протяженность поражения более 1 венозного сегмента |
2,644 |
1,552–12,664 |
0,049* |
|
Значение пиковой скорости кровотока в стентированном участке менее 13 см/с |
94,500 |
15,139–589,888 |
<0,001* |
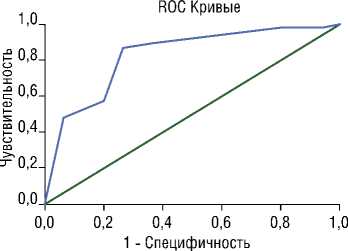
Диагональные сегменты, сгенерированные связями AUC = 0,829
Рис. 5. ROC-кривая оценки взаимосвязи значений пиковой скорости венозного кровотока в зоне стентированного участка обеих групп с результатом проходимости стента в раннем послеоперационном периоде.
V = 13 см/с, при котором отмечается значимое увеличение риска развития тромбоза стентированного участка в раннем послеоперационном периоде (чувствительность 98,8%, специфичность 80,0%) (Рис. 5).
Обсуждение
Эндоваскулярная реканализация и стентирование обструктивного поражения подвздошно-бедренного
венозного сегмента у пациентов с тяжелыми формами хронических заболеваний вен является приоритетным, а в ряде случаем безальтернативным методом лечения. Однако ликвидация протяженных обструктивных поражений 2 группы, затрагивающих сразу несколько венозных сегментов, является более сложным оперативным вмешательством с более высоким риском возможных тромботических венозных осложнений. В частности, у 2 пациентов II группы, у которых ранний послеоперационный период осложнился тромбозом стентированного участка, деформация имплантированного стента произошла именно в области функционально активной зоны на уровне верхней ветви лобковой кости. В связи с этим можно предположить, что имплантация стентов на данных участках может быть ограничена, а их конструкция требует технического усовершенствования.
Результаты исследования показали, что эндоваскулярное стентирование значительно улучшает клинические показатели и качество жизни пациентов с посттромботической обструкцией венозного русла подвздошно-бедренного сегмента в обеих группах. После вмешательства наблюдалось значительное снижение тяжести заболевания согласно шкалам VILLALTA и VCSS, а также улучшение качества жизни согласно шкале CIVIQ-20. Однако пациенты во второй группе, с протяженным поражением венозного сегмента, продемонстрировали более выраженные положительные изменения по всем шкалам, что может быть связано с более тяжелым исходным состоянием этих пациентов и эффектом восстановления венозной проходимости на протяженном участке поражения.
Следует отметить, что такие факторы, как возраст пациентов, пол, ИМТ, сторона поражения и исходный клинический класс заболевания по шкале CEAP не оказали статистически значимого влияния на конечные результаты лечения. Кроме того, показатели по шкалам VILLALTA и VCSS, превышающие критические значения до операции в 1 и 2 группах не оказали значимого влияния на результаты после стентирования.
Наиболее значимыми факторами, влияющими на риск тромбоза стентированного участка в послеоперационном периоде, оказались протяженность поражения более одного венозного сегмента (ОШ 2,644; p = 0,049) и пиковая скорость кровотока в стентированном участке менее 13 см/с (ОШ 94,500; p<0,001). Несмотря на выявленную значимость этих факторов, представляется, что эти факторы взаимосвязаны, так как у пациентов с распространенным посттромботическими изменениями скорость венозного кровотока может быть существенно ограничена, что увеличивает риск тромбоза в послеоперационном периоде. Пиковая скорость кровотока в зоне имплантированного стента показала высокую чувствительность и специфичность в обеих группах. Это подтверждает необходимость персонифицированного подхода к изучению гемодинамических показателей в различных сегментах до и после оперативного вмешательства.
Выводы
-
1. Эндоваскулярная реваскуляризация со стентированием венозных обструкций подвздошно-бедренного сегмента различной протяженности является эффективным и относительно безопасным методом лечения тяжелых форм хронических заболеваний вен.
-
2. Пиковая скорость кровотока является важным фактором прогнозирования проходимости стентированного участка в раннем послеоперационном периоде. Пиковая скорость кровотока в зоне стентированного участка менее 13 см/с является значимым предиктором тромбоза стента в раннем послеоперационном периоде.
-
3. Стентирование протяженных обструктивных поражений венозного русла, затрагивающих несколько венозных сегментов, приводит к значительному клиническому улучшению и повышению качества жизни пациентов, однако сопряжено с более высоким риском тромботических осложнений. Это обстоятельство требует обязательного систематического контроля проходимости оперированного венозного сегмента, соответствующей антикоагулянтной и дезагрегантной терапии под регулярным лабораторным контролем системы гемостаза.


