Эндоваскулярное лечение больных острым коронарным синдромом без подъема сегмента ST с многососудистым поражением коронарного русла: выбор оптимальной стратегии реваскуляризации
Автор: Чернигина Т.П., Голощапов-аксенов Р.С., Максимкин Д.А., Стуров Н.В., Шугушев З.Х.
Журнал: Вестник Национального медико-хирургического центра им. Н.И. Пирогова @vestnik-pirogov-center
Рубрика: Оригинальные статьи
Статья в выпуске: 1 т.12, 2017 года.
Бесплатный доступ
346 пациентов были включены в исследование и первоначально рандомизированы в 3 группы. В I группу вошли 100 пациентов, которым полная реваскуляризация миокарда была выполнена при первоначальном ЧКВ. Во II группу вошли 124 пациента, кому полная реваскуляризация миокарда выполнялась в течение первичной госпитализации, а в III группу - 122 пациента, которым полная реваскуляризация выполнялась в различные сроки после первичной госпитализации. Критерии включения: больные ОКСбпST с многососудистым поражением коронарного русла (риск по SYNTAX score = 23-32); высокая и средняя степень риска по шкале GRACE; отсутствие в анамнезе реваскуляризации миокарда. Отдаленные результаты лечения прослежены у 192 пациентов. Через 12 месяцев у пациентов из III группы достоверно чаще возникали большие сердечно - сосудистые осложнения и повторные вмешательства на целевом сосуде. Выявлено, что выполнение полной реваскуляризации миокарда позднее 30 дней от момента диагностированного острого коронарного синдрома, отрицательно влияет на прогноз заболевания (r = 0,58, p 25, избыточная масса тела/ожирение и гиперхолестеринемия > 6.5 ммоль/л.
Окс без подъема сегмента st, многососудистое поражение, полная реваскуляризация
Короткий адрес: https://sciup.org/140188631
IDR: 140188631 | УДК: 616.132.2-008.6-036.11-089.15
Endovascular treatment of patients with acute coronary syndrome without ST-segment elevation and multivessel diseases: selecting the best strategy revascularization
346 patients were enrolled and initially randomized into 3 groups. In the I group included 100 patients who had complete myocardial revascularization was performed at the initial PCI. In the II group included 124 patients who complete myocardial revascularization was performed during initial hospitalization, and in the III group - 122 patients who complete revascularization was performed at different times after the initial hospitalization. Inclusion criteria: patients ACS without elevation ST with multivessel coronary disease (risk SYNTAX score = 23-32); high and medium risk for the GRACE scale; in the absence of a history of myocardial revascularization. Long-term results of treatment were evaluated in 192 patients. After 12 months, patients in group III was significantly more likely to have greater cardio - vascular complications and re-interventions on the target vessel. It was found that the performance of the complete myocardial revascularization within 30 days from the date of diagnosed acute coronary syndrome, a negative impact on the prognosis of the disease (r = 0,58, p 25, overweight / obesity, and high cholesterol> 6.5 mmol / l.
Текст научной статьи Эндоваскулярное лечение больных острым коронарным синдромом без подъема сегмента ST с многососудистым поражением коронарного русла: выбор оптимальной стратегии реваскуляризации
В последние годы отмечается увеличение частоты развития ОКС без подъема сегмента ST (ОКСбпST), по сравнению с ОКС с подъемом сегмента SТ, что особенно заметно по количеству госпитализаций в стационары и выполненных операций по реваскуляризации миокарда у таких пациентов [1].
Несмотря на впечатляющую доказательную базу по эффективности оптимальной медикаментозной терапии (ОМТ) при различных формах ИБС, включающей применение различных β -адреноблокаторов, антагонистов кальция, статинов, у больных ОКС, наиболее рациональной стратегией лечения является ее сочетание с различными методами реваскуляризации миокарда [2].
Одним из подтверждений этому являются данные шведского регистра, включающего более 46 тыс. больных ОКСбпST, которые показали, что ранняя инвазивная стратегия лечения ассоциируется с лучшими отдаленными результатами независимо от пола пациентов [3]. При этом результаты рандомизированных исследований довольно противоречивы. Так, например, у пациентов старше 75 лет отсутствует достоверная разница между ранней инвазивной и консервативной стратегиями лечения ОКСбпST [4]. Тем не менее, у пациентов старше 80 лет, инвазивное лечение ОКС ассоциируется с меньшей частотой серьезных сердечно-сосудистых событий в раннем послеоперационном периоде [5].
Вопрос, касающийся сроков выполнения эндоваскулярного вмешательства больным ОКСбпST, изучался в многочисленных рандомизированных исследованиях, таких как LIPSIA-NSTEMI TRIAL, RITA-3, FRICS II, ICTUS в которых было показано отсутствие достоверных различий между ранней и поздней инвазивной

стратегиями лечения по частоте развития серьезных сердечно-сосудистых событий. На основании этих результатов авторы пришли к единому мнению о том, что сроки выполнения ЧКВ у больных ОКСбпST не оказывают влияние на отдаленный прогноз [6–8]. При этом в исследовании Badings E.A. и др. (2013), аналогичные выводы были сделаны в отношении больных высокого риска фатальных осложнений.
Тем не менее, в рекомендациях Европейского общества кардиологов 2015 года указывается, что выбор стратегии и сроков инвазивного лечения больных ОКСбпST должен обязательно основываться на стратификации риска больных [10].
Как известно, больные ОКСбпST относятся к одной из наиболее сложных категорий для инвазивного лечения, так как у них часто встречается многососудистое поражение коронарного русла. При этом важной задачей врачей является правильное определение симптом-связанной артерии, так как инвазивная стратегия подразумевает, прежде всего, вмешательство в бассейне этой артерии, тогда как последующие манипуляции выполняются в различные сроки, по мере обращения пациента в клинику, а порой и не выполняется вовсе. Проблема выбора оптимальных сроков для выполнения полной реваскуляризации у больных ОКСбпST с многососудистым поражением коронарного русла остается открытым.
Целесообразность одномоментного многососудистого стентирования у больных ОКСбпST во время первоначального эндоваскулярного вмешательства изучалась лишь в единственном рандомизированном двухцентровом исследовании SMILE, в которое были включены 542 больных. Так, частота развития тяжелых сердечнососудистых осложнений в течение 12 месяцев при одномоментном стентировании была достоверно ниже, чем при многоэтапном, и составила 13,6 и 23,2%, соответственно, (p = 0,04). Аналогичная тенденция отмечалась и по частоте развития послеоперационных кровотечений [11]. Однако рекомендации о конкретных сроках выполнения полной реваскуляризации миокарда у больных ОКСбпST с многососудистым поражением коронарного русла в настоящее время отсутствуют. Кроме того, не изучены факторы риска, которые могут отрицательно влиять на прогноз при многососудистом поражении, в случае выполнения отсроченной полной реваскуляризации миокарда, что определяет актуальность и целесообразность проведения новых клинических исследований.
Материал и методы
Критерии включения : больные ОКСбпST с многососудистым поражением коронарного русла (риск по SYNTAX score = 23–32); высокая и средняя степень риска по шкале GRACE; отсутствие в анамнезе реваскуляризации миокарда.
Критерии исключения : больные с очень высоким риском по шкале GRACE; поражение ствола левой коронарной артерии (ЛКА).
Все больные методом конвертов были рандомизированы в три группы. В I группу вошли пациенты, которым полная реваскуляризация миокарда была выполнена во время первоначального эндоваскулярного вмешательства по поводу ОКС. Во II подгруппу вошли пациенты, которым изначально было выполнено стентирование симптом-связанной артерии, а полная реваскуляризация миокарда выполнялась в течение одной госпитализации. Ретроспективно была сформирована III группа пациентов, которым по аналогии со II группой в ходе первоначального вмешательства выполнялось стентирование симптом-связанной артерии, а полная реваскуляризация – в различные сроки после госпитализации.
Дополнительно все больные были рандомизированы в 2 подгруппы. В I подгруппе ЧКВ выполнялось трансрадиальным доступом, а во II подгруппе – трансфеморальным доступом.
Антиагрегантная терапия на дооперационном этапе включала в себя препараты ацетилсалициловой кислоты и ингибиторы P2Y12 рецепторов тромбоцитов (тикагрелор в нагрузочной дозе 180 мг, либо клопидогрел в нагрузочной дозе 600 мг). После ЧКВ антиагрегантная терапия была рекомендована в течение 12 месяцев: препараты ацетилсалициловой кислоты 75–100 мг/сутки и тикагрелор 180 мг/сутки, либо клопидогрел в дозе 75 мг/сутки.
Фармакологическая поддержка ЧКВ выбиралась согласно Рекомендаций Европейского общества кардиологов по лечению больных ОКСбпST 2015 года. При этом использовался нефракционированный гепарин (НФГ) в дозе 70 ЕД/кг, либо бивалирудин (0,75 мг/кг болюсно, с последующей инфузией со скоростью 1,75 мг/кг/час. во время ЧКВ и в течение 4-х часов после ЧКВ).
Рутинное применение ингибиторов GP IIb/IIIa рецепторов в исследовании не предусматривалось.
Артериальный доступ выполняли с учетом анатомических и рентгенологических ориентиров. С целью профилактики артериального спазма при трансрадиальном доступе, всем пациентам внутриартериально вводили верапамил и перлинганит. При повторных вмешательствах доступ выбирали аналогично первоначальной процедуре. При невозможности выполнения повторных вмешательств в подгруппе трансрадиального доступа тем же доступом, что и при первоначальной процедуре ЧКВ, переходили на трансфеморальный или плечевой доступ, и такие пациенты исключались из исследования.
Критерии оценки непосредственных результатов: суммарная частота сердечно-сосудистых осложнений; большие кровотечения (BARC 3 или 5).
Вторичные критерии оценки непосредственных результатов : кровотечение из места доступа (BARC 1 или 2); сосудистые осложнения, связанные с доступом.
Отдаленные клинические результаты планировалось проследить через 12 месяцев после эндоваскулярного вмешательства.
Критерии оценки отдаленных результатов: суммарная частота сердечно-сосудистых осложнений (смерть,

инфаркт миокарда, повторные вмешательства на целевом сосуде, повторные вмешательства на целевом поражении).
Для оценки отдаленных результатов пациенты приглашались на повторную амбулаторную консультацию, во время которой проводился сбор анамнеза, выполнялась нагрузочная проба и трансторакальная эхокардиография. Пациенты с положительной нагрузочной пробой были госпитализированы для выполнения коронарографии с последующим решением вопроса о повторном вмешательстве.
Стратификация риска сердечно-сосудистых осложнений и определение сроков выполнения катетеризации сердца проводились согласно шкале GRACE [12].
Оценка риска возможного послеоперационного кровотечения проводилась до эндоваскулярного вмешательства с помощью калькулятора CRUSADE [13].
Степень тяжести послеоперационных кровотечений квалифицировалась по шкале BARC (Bleeding Academic Research Consortium) [14].
Стентирование коронарных артерий выполнялось по стандартной методике и включало предилатацию, имплантацию стента, и, в случае необходимости, постдилатацию баллонными катетерами высокого давления.
При наличии у пациента бифуркационного стеноза, использовали два коронарных проводника, один из которых был гидрофильным. Боковая ветвь защищалась во всех ситуациях. Предпочтительной была одностентовая стратегия стентирования. В случае развития выраженного болевого синдрома, вследствие субтотального стеноза в устье боковой ветви, замедлении коронарного кровотока ниже TIMI III, выполнялась киссинг-дилатация «целующимися баллонами». Если после киссинг-дилатации указанные осложнения сохранялись, выполняли имплантацию второго стента в боковую ветвь.
Всем включенным в исследование больным были имплантированы стенты с лекарственным покрытием. Проведение внутрисосудистых методов визуализации не предусматривалось. Ангиографические результаты оценивались по данным количественной цифровой ангиографии и по шкале TIMI. Механическая тромбо-экстрация не применялась.
Результаты
Всего в исследование включено 346 больных ОКСбпST. В ходе рандомизации в I группу вошли 100 больных, во II группу – 124, а в III группу – 122 больных. Средний период выполнения полной реваскуляризации у больных III группы, c учетом этапного лечения, составил 6,5 ± 0,2 месяца.
В ходе дополнительной рандомизации, в зависимости от артериального доступа, больные распределились таким образом, что в I подгруппу вошли 155 человек, а во II группу – 191 человек.
Группы были сопоставимы по клинико-демографическим показателям (табл. 1).
Табл. 1. Клинико-демографическая характеристика пациентов
|
Показатель |
Группа I (n = 100) |
Группа II (n = 124) |
Группа III (n = 122) |
|
Мужчин |
81(81%) |
102(82,3%) |
98(80,3%) |
|
Женщин |
19(19%) |
22(17,7%) |
24(19,7%) |
|
Средний возраст |
68,4 ± 1,8 |
69,3 ± 1,1 |
66,4 ± 1,2 |
Данные анамнеза
|
Среднее количество инфарктов миокарда в анамнезе |
1,07 ± 0,8 |
1,16 ± 0,2 |
0,86 ± 0,2 |
|
ОНМК |
36(36%) |
48(38,7%) |
44(36,1%) |
|
Артериальная гипертензия |
100(100%) |
122 (98,4%) |
122 (100%) |
|
Сахарный диабет 2 типа |
48(48%) |
53(42,7%) |
54(44,2%) |
|
Курение |
92(92%) |
120(96,8%) |
115(94,3%) |
Лабораторные показатели
|
Средний уровень креатинина сыворотки |
116 ± 0,02 |
118 ± 0,12 |
113 ± 0,14 |
|
Средний уровень холестерина |
6,3 ± 0,14 |
6,7 ± 0,2 |
6,18 ± 0,11 |
|
Положительный тропониновый тест |
77(77%) |
82(66,2%) |
88(72,1%) |
Данные объективного статуса пациента
|
Недостаточность кровообращения (Killip) I II III |
82(82%) 14(14%) 4(4%) |
98(79,1%) 20(16,1) 6(4,8%) |
94(77%) 23(18,9%) 5(4,1%) |
|
Средние показатели ЧСС |
98 ± 0,54 |
101 ± 0,12 |
98 ± 0,18 |
|
Средние показатели уровня систолического АД |
111 ± 2,4 |
109 ± 1,8 |
108 ± 1,2 |
|
Средние показатели ФВ ЛЖ,% |
48 ± 1,48 |
47 ± 1,23 |
48 ± 0,33 |
Стратификация риска
|
По шкале GRACE: Высокий (>140) |
28(28%) |
37(29,8%) |
32(26,2%) |
|
Средний (110–140) |
72(72%) |
87(70,2%) |
90(73,8%) |
|
По шкале CRUSADE: Очень высокий (>50) |
10(10%) |
14(11,3%) |
17(14%) |
|
Высокий (41–50) |
42(42%) |
52(42%) |
50(41%) |
|
Умеренный (31–40) |
31(31%) |
37(29,8%) |
33(27%) |
|
Низкий (21–30) |
17(17%) |
21(16,9%) |
22(18%) |
Примечание : * – р > 0,05.
Согласно шкалы GRACE высокий риск сердечнососудистых осложнений выявлен у 28% больных из I группы, у 29,8% – из II группы и у 26,2% – из III группы (р > 0,05). По шкале CRUSADE во всех группах преобладал высокий риск кровотечения, при этом у 10, 11,3 и 14% пациентов, соответственно, группам, риск кровотечения был очень высоким (р > 0,05).
Ангиографические характеристики пациентов представлены в табл. 2.
Из таблицы видно, что подгруппы достоверно различались по частоте встречаемости бифуркационных стенозов коронарных артерий и трехсосудистого поражения, которые достоверно чаще встречались у пациентов из II и III подгрупп. При этом по показателям среднего количества имплантируемых стентов и показателям риска выполнения ЧКВ по шкале SYNTAX, различий не было.
Медикаментозная терапия перед ЧКВ включала: препараты ацетилсалициловой кислоты (300–500 мг),
ингибиторы P2Y12 рецепторов тромбоцитов (тикагре-лор 180 мг – 202 пациента (58,4%), либо клопидогрел 600 мг – 144 пациента (41,6%); ингибиторы АПФ, бета-адреноблокаторы, статины, морфин.
Для фармакологической поддержки ЧКВ у 55% пациентов был использован НФГ, а у остальных 45% пациентов – прямой ингибитор тромбина – бивалирудин.
Непосредственные результаты лечения представлены на рис. 1.
В раннем послеоперационном периоде достоверных различий по суммарной частоте сердечно-сосудистых осложнений и больших кровотечений в изучаемых группах не выявлено.
Суммарная частота интра- и послеоперационных сердечно-сосудистых осложнений в подгруппах, рандомизированных в зависимости от артериального доступа, достоверно не различалась и составила 7,1 и 8,4%, соответственно, (р = 0,6423).
Серьезные кровотечения (BARC 3 и 5) достоверно чаще возникали у больных из подгруппы трансфеморального доступа по сравнению с трансрадиальным и составили 2,6 и 0,6%, соответственно, (р = 0,0001).
Табл. 2. Ангиографическая характеристика пациентов
|
Характеристика |
I группа (n = 100) |
II группа (n = 124) |
III группа (n = 122) |
р |
|||
|
Абс. |
% |
Абс. |
% |
Абс. |
% |
||
|
Двухсосудистое поражение |
64 |
64 |
59 |
47,6 |
51 |
41,8 |
0,1245 |
|
Трехсосудистое поражение |
26 |
26 |
48 |
38,7 |
42 |
34,4 |
0,0021 |
|
Бифуркационные стенозы |
8 |
8 |
14 |
11,3 |
24 |
19,7 |
<0,0001 |
|
Устьевые стенозы |
2 |
2 |
3 |
2,4 |
5 |
4,1 |
0,0843 |
|
Средний диаметр имплантированных стентов, мм |
3,15 ± 0,01 |
3,2 ± 0,002 |
3,18 ± 0,12 |
0,0764 |
|||
|
Среднее количество стентов на одного пациента |
2,8 ± 0,02 |
2,65 ± 0,012 |
2,43 ± 0,028 |
0,1318 |
|||
|
Средний показатель риска по шкале SYNTAX |
25 ± 1,18 |
27 ± 0,1 |
24 ± 1,12 |
0,0064 |
|||
Табл. 3. Сосудистые осложнения в месте артериального доступа
|
Вид осложнения |
Подгруппа I (n = 155) |
Подгруппа II (n = 191) |
р |
|
Стойкий артериальный спазм |
37 |
0 |
<0,0001 |
|
Артериовенозные фистулы |
2 |
7 |
0,0944 |
|
Ложная артериальная анервизма |
2 |
9 |
0,0881 |
|
Кровотечение из места доступа, не требующее дополнительного лечения (BARC I) |
2 |
28 |
<0,001 |
|
Кровотечение из места доступа, требующее лечения (BARC 2) |
0 |
7 |
<0,001 |
|
ИТОГО |
43 |
51 |
0,0783 |
Детальный анализ сосудистых осложнений, которые развивались в месте артериального доступа у больных изучаемых подгрупп, показал, что наиболее частыми из них были кровотечение из места доступа, артериовенозные фистулы, стойкий артериальный спазм, ложная аневризма (табл. 3).
Несмотря на отсутствие различий в подгруппах по суммарным показателям сосудистых осложнений, показатели частоты развития стойкого артериального спазма и кровотечений из места доступа достоверно различались. Так, стойкий артериальный спазм чаще встречался при выполнении ЧКВ радиальным доступом, тем не менее, кровотечения из места доступа (BARC 1 и 2), достоверно чаще возникали у больных, которым ЧКВ выполнялось трансфеморальным доступом.
В группе I вмешательство трансрадиальным доступом выполнено 45 больным, а трансфеморальным – 55, в группе II – трансрадиальным – 60 больным, а трансфеморальным – 64, в группе III – 50 и 72 больным, соответственно.
В ходе исследования было изучено влияние артериального доступа на частоту развития сердечнососудистых осложнений в изучаемых группах.
Так, при сравнении групп по частоте сосудистых осложнений в зависимости от артериального доступа, достоверных различий не выявлено (рис. 2).
Однако суммарные показатели сосудистых осложнений, включающие как большие кровотечения, так и кровотечения из места доступа, возникающие как при трансрадиальном, так и трансфеморальном доступах, в рассматриваемых группах достоверно различались и составили 17, 27,4 и 35,2%, соответственно I, II и III группам (р < 0,001), что напрямую связано с повторными вмешательствами.
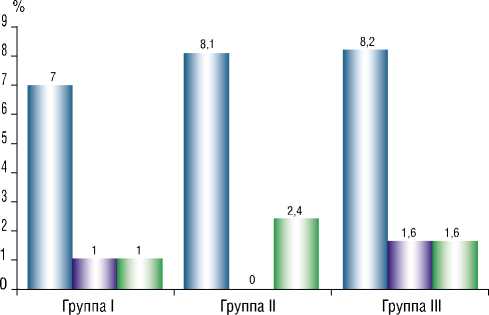
I ■ Суммарная частота сердечно-сосудистых осложнений
I I Острый тромбоз стента
I I BARG 3 или 5
Рис. 1. Непосредственные результаты лечения, в зависимости от сроков выполнения полной реваскуляризации миокарда, р > 0,05
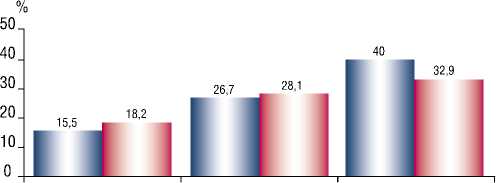
Группа I Группа II Группа III
I ■ Трансрадиальный
I I Трансфеморальный
Рис. 2. Частота сосудистых осложнений в месте артериального доступа в подгруппах, p > 0,05
Отдаленные клинические результаты лечения в сроки от 11 до 18 месяцев (средний срок 12 ± 0,14 месяцев) прослежены у 192 пациентов, из которых 60 пациентов были из I группы, 64 пациента – из II группы и 68 пациентов – из III группы (рис. 3).
Через 12 месяцев у пациентов из III группы, которым полная реваскуляризация миокарда выполнялась в отдаленные сроки после первичной госпитализации, достоверно чаще возникали большие сердечно-сосудистые осложнения и повторные вмешательства на целевом сосуде, тогда как в группе I и II различий по данным показателям не выявлено.
В изучаемых подгруппах пациенты распределились таким образом, что 91 пациент был из подгруппы трансрадиального доступа и 101 пациент – из подгруппы трансфеморального доступа. Суммарная частота сердечно-сосудистых осложнений была достоверно ниже в подгруппе трансрадиального доступа, по сравнению с подгруппой трансфеморального доступа и составила 2,2 и 6,9%, соответственно (р = 0,0312).
Многофакторный анализ позволил выделить факторы риска, при наличии которых, у больных ОКСбпST с многососудистым поражением целесообразно выполнять полную реваскуляризацию миокарда в период индексной госпитализации
В качестве возможных факторов риска рассматривались количественные: возраст, длина поражения артерии, диаметр пораженной артерии, степень риска по шкале SYNTAX score, индекс массы тела, функциональный класс сердечной недостаточности по классификации Killip, и качественные признаки: степень риска по шкале GRACE, пол, курение, кальциноз артерий, гиперхолестеринемия, сахарный диабет, инфаркт миокарда в анамнезе, артериальная гипертензия. Всего анализу подверглись 15 предполагаемых факторов риска (рис. 4).
Факторы размещены в таблице рангов, в зависимости от их значимости. К наиболее достоверным факторам, способствующим ухудшению прогноза больных ОКСбпST с многососудистым поражением коронарного русла, в случае выполнения отсроченной полной
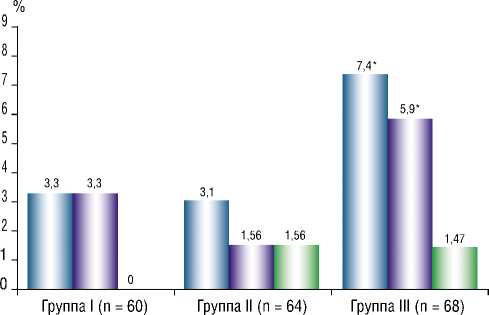
I I Суммарная частота сердечно-сосудистых осложнений
I I Повторные вмешательства на целевом сосуде
I I Повторные вмешательства на целевом поражении
Рис. 3. Отдаленные результаты в зависимости от сроков выполнения полной реваскуляризации, * – р < 0,05
Недостаточность кровообращения III класса по Killip
Высокий риск по шкале GRACE
Инфаркт миокарда в анамнезе
Субтотапьный стеноз в несимптомных артериях
Протяженность поражения в несимптомных.....
Степень риска по шкале SYNTAX >25
Сахарный диабет II типа
Избыточная масса тепа/ожирение
Уровень общего холестерина крови >6,5 ммопь/л
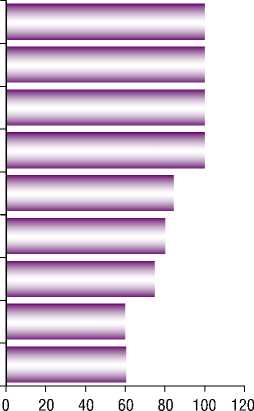
Рис. 4. Факторы неблагоприятного прогноза больных ОКСбпST реваскуляризации миокарда относятся: субтотальный стеноз в несимптомных артериях, недостаточность кровообращения III класса по Killip, инфаркт миокарда в анамнезе, высокий риск по шкале GRACE, протяженность поражения в несимптомных артериях более 20 мм, сахарный диабет, степень риска по шкале SYNTAXscore > 25, избыточная масса тела/ожирение и уровень холестерина крови > 6,5 ммоль/л.
Выявлена прямая положительная корреляция между сроками выполнения полной реваскуляризации и развитием сердечно-сосудистых осложнений, которая показала, что наиболее часто осложнения развиваются у больных, которым реваскуляризация выполнялась позднее 30 дней от момента диагностированного острого коронарного синдрома (r = 0,58, p < 0,05).
Обсуждение
Согласно рекомендаций Европейского общества кардиологов 2015 года, очевидным фактом является лишь то, что больным ОКСбпST с многососудистым поражением коронарных артерий следует обязательно выполнять реваскуляризацию миокарда, при этом решение о методе реваскуляризации должна принимать сердечная команда – Heart Team, с учетом стратификации риска больного [10].
Активное внедрение в клиническую практику эндоваскулярных методов лечения и накопление достаточного опыта их выполнения в течение последних 10–15 лет, способствовали уменьшению доли пациентов с ОКСбпST, подвергающихся аортокоронарному шунтированию [15]. В отсутствие данных рандомизированных исследований и четких рекомендаций значительный комплекс вопросов, связанных с выполнением операции аортокоронарного шунтирования данным пациентам, решается преимущественно индивидуально [16].
В настоящее время существует четыре стратегии эндоваскулярного лечения больных ОКСбпST. Три из них инвазивные (рутинное выполнение коронарографии с последующим решением вопроса о способе реваскуляризации), а четвертая основана на оценке наличия признаков ишемии (ischemia-guided strategy), либо клинически (повторные ангинозные боли в течение госпитализации, сохранение стенокардии напряжения более высокого уровня, чем ранее, несмотря на медикаментозную терапию), либо на основании данных неинвазивного тестирования. В случае подтверждения ишемии, выполняется коронарография [10, 17].
Пациенты самого высокого риска, с рефрактерной стенокардией, тяжелой сердечной недостаточностью и шоком, жизнеугрожающими аритмиями, гемодинамической нестабильностью обычно не включались в рандомизированные исследования, чтобы не создавать угрозы неприменения спасающих жизнь методов лечения. Поэтому таких пациентов на основании мнения экспертов в течение 2 час. берут на инвазивную диагностику, независимо от изменений на ЭКГ и биомаркеров [10].
При многососудистом поражении, преимущественно принято выполнять стентирование симптом-связанной артерии, тогда как сроки выполнения полной реваскуляризации миокарда могут быть самыми различными, что может неоднозначно отражаться на отдаленном прогнозе таких пациентов.
Представленное рандомизированное исследование направлено на изучение оптимальных сроков и объема выполнения реваскуляризации миокарда у больных ОКСбпST высокого и среднего риска с многососудистым поражением коронарных артерий, что до сих пор является предметом многочисленных дискуссий.
Согласно полученным данным, в раннем послеоперационном периоде, во время нахождения больного в стационаре, достоверных различий по суммарной частоте сердечно-сосудистых осложнений и больших кровоте- чений в изучаемых группах не выявлено. Однако, в ходе изучения влияния артериального доступа на частоту развития сердечно-сосудистых осложнений в изучаемых группах выявлено, что суммарные показатели сосудистых осложнений, включающие как большие кровотечения, так и кровотечения из места доступа, возникающие как при трансрадиальном, так и трансфеморальном доступах в рассматриваемых группах, достоверно различались и составили 17, 27,4 и 35,2%, соответственно, I, II и III группам (р < 0,001), что напрямую связано с повторными вмешательствами. При этом, в отдаленном периоде, подгруппы трансрадиального и трансфеморального доступов различались уже и по суммарной частота сердечно-сосудистых осложнений, которая была ниже в подгруппе трансрадиального, по сравнению с подгруппой трансфеморального и составила 2,2 и 6,9%, соответственно, (р = 0,0312).
Через 12 месяцев, у пациентов из III группы, которым полная реваскуляризация миокарда выполнялась в отдаленные сроки после первичной госпитализации, достоверно чаще возникали большие сердечно-сосудистые осложнения и повторные вмешательства на целевом сосуде, тогда как в группе I и II различий по данным показателям не выявлено. Следует отметить, что полученные нами результаты перекликаются с данными рандомизированного исследования SMILE, в котором отдается предпочтение одномоментному стентированию гемодинамически значимых стенозов магистральных артерий сердца. Однако особенностью нашего исследования является отсутствие преимуществ между стратегией одномоментного многососудистого стентирования и этапного стентирования в период индексной госпитализации. Это позволяет рассматривать последнюю стратегию в качестве приоритетной, в связи с тем, что она позволяет избежать длительной рентгеноскопии, использования больших объемов контрастного вещества и, в целом, осложнений, связанных с одномоментной имплантацией нескольких стентов.
Другой важной отличительной особенностью данного исследования является выявленная прямая положительная корреляция между сроками выполнения полной реваскуляризации и развитием сердечно-сосудистых осложнений у больных ОКСбпST с многососудистым поражением коронарного русла. При этом следует отметить, что большие сердечно-сосудистые события чаще возникают у тех больных, которым полная реваскуляризация выполнялась позднее 30 дней от момента диагностированного острого коронарного синдрома (r = 0,58, p < 0,05).
Кроме того, выявлены факторы неблагоприятного прогноза больных ОКСбпST с многососудистым поражением коронарного русла, при наличии которых целесообразно выполнять полную реваскуляризацию миокарда в период индексной госпитализации.
Таким образом, при выполнении ЧКВ у больных ОКС без подъема сегмента ST, радиальный доступ может рас-
сматриваться в качестве приоритетного, так как отличается меньшей частотой больших и малых кровотечений в раннем послеоперационном периоде и частотой тяжелых сердечно-сосудистых осложнений в отдаленном периоде. Выполнение полной реваскуляризации миокарда позднее 30 дней от момента диагностированного острого коронарного синдрома, отрицательно влияет на прогноз заболевания и проявляется увеличением частоты больших сердечно-сосудистых осложнений, по сравнению с больными, которым полная реваскуляризация выполнялась в течение первоначального эндоваскулярного лечения или первичной (индексной) госпитализации.
Пациентам с субтотальным стенозом в несим-птомных артериях, недостаточностью кровообращения III класса по Killip, инфарктом миокарда в анамнезе, высоким риском по шкале GRACE, протяженностью поражения в несимптомных артериях более 20 мм, сахарным диабетом, степенью риска по шкале SYNTAXscore > 25, избыточной массой тела/ожирением и уровнем холестерина крови > 6,5 ммоль/л, целесообразно выполнение полной реваскуляризации миокарда во время индексной госпитализации по поводу острого коронарного синдрома.
Список литературы Эндоваскулярное лечение больных острым коронарным синдромом без подъема сегмента ST с многососудистым поражением коронарного русла: выбор оптимальной стратегии реваскуляризации
- Бокерия Л.А., Алекян Б.Г. Рентгенэндоваскулярная диагностика и лечение заболеваний сердца и сосудов в Российской Федерации -2015 год. М.: НЦССХ им. Н.А. Бакулева; 2016.
- Филатов А.А, Крылов В.В. Результаты эндоваскулярного лечения больных инфарктом миокарда без зубца Q на электрокардиограмме. Международный журнал интервенционной кардиоангиологии. 2012; 30: 29-32.
- Alfredsson J., Lindbäck J., Wallentin L., Swahn E. Similar outcome with an invasive strategy in men and women with non-ST-elevation acute coronary syndromes: from the Swedish Web-System for Enhancement and Development of Evidence-Based Care in Heart Disease Evaluated According to Recommended Therapies (SWEDEHEART). Eur Heart J. 2011; 32: 3128-36.
- Savonitto S., Cavallini C., Petronio A.S., et al. Early aggressive versus initially conservative treatment in elderly patients with non-ST-segment elevation acute coronary syndrome: a randomized controlled trial. JACC: Cardiovasc Interv 2012; 5: 906-16.
- Tegn N., Abdelnoor M., Aaberge L. et al. Invasive versus conservative strategy in patients aged 80 years or older with non-ST-elevation myocardial infarction or unstable angina pectoris (After Eighty study): an open-label randomized controlled trial. Lancet. 2016; 387: 1057-65.
- Thiele H., Rach J., Klein N. et al. Optimal timing of invasive angiography in stable non-ST-elevation myocardial infarction: the Leipzig Immediate versus early and late Percutaneous coronary Intervention trial in NSTEMI (LIPSIA-NSTEMI Trial). Eur Heart J. 2012; 33(16): 2035-43.
- Henderson R.A., Jarvis C., Clayton T. et al. 10-Year Mortality Outcome of a Routine Invasive Strategy Versus a Selective Invasive Strategy in Non-ST-Segment Elevation Acute Coronary Syndrome: The British Heart Foundation RITA-3 Randomized Trial. J Am Coll Cardiol. 2015; 66(5): 511-20 DOI: 10.1016/j.jacc.2015.05.051
- Damman P., Nan van Geloven, Wallentin L. et al. Timing of Angiography With a Routine Invasive Strategy and Long-Term Outcomes in Non-ST-Segment Elevation Acute Coronary Syndrome: A Collaborative Analysis of Individual Patient Data From the FRISC II (Fragmin and Fast Revascularization During Instability in Coronary Artery Disease), ICTUS (Invasive Versus Conservative Treatment in Unstable Coronary Syndromes), and RITA-3 (Intervention Versus Conservative Treatment Strategy in Patients With Unstable Angina or Non-ST Elevation Myocardial Infarction) Trials. J Am Coll Cardiol Intv. 2012; 5(2): 191-199 DOI: 10.1016/j.jcin.2011.10.016
- Badings E.A., Salem H.K., Dambrink J.E. et al. Early or late intervention in high-risk non-ST-elevation acute coronary syndromes: results of the ELISA-3 trial. EuroIntervention. 2013; 9: 54-61.
- Roffi M., Patrono C., Collet J.P. et al. 2015 ESC Guidelines for the management of acute coronary syndromes in patients presenting without persistent ST-segment elevation: Task Force for the Management of Acute Coronary Syndromes in Patients Presenting without Persistent ST-Segment Elevation of the European Society of Cardiology (ESC). Eur Heart J. 2016 Jan 14; 37(3): 267-315. ehv320 DOI: 10.1093/eurheartj/
- Sardella G., Lucisano L., Garbo R. et al. Single-Staged Compared With Multi-Staged PCI in Multivessel NSTEMI Patients: The SMILE Trial. J Am Coll Cardiol. 2016 Jan 26;67(3): 264-72 DOI: 10.1016/j.jacc.2015.10.082
- Tang E.W., Wong C.K., Herbison P. Global Registry of Acute Coronary Events (GRACE) hospital discharge risk score accurately predicts long-term mortality post acute coronary syndrome. Am Heart J. 2007 Jan; 153(1): 29-35.
- Sumeet S., Bach R.G., Chen A.Y. et al. Baseline Risk of Major Bleeding in Non-ST-Segment-Elevation Myocardial Infarction The CRUSADE (Can Rapid risk stratification of Unstable angina patients Suppress Adverse outcomes with Early implementation of the ACC/AHA guidelines) Bleeding Score. Circulation. 2009, 119, 1873-1882.
- Mehran R, Rao SV, Bhatt DL, et al. Standardized bleeding definitions for cardiovascular clinical trials: A consensus report from the Bleeding Academic Research Consortium. Circulation. 2011; 123: 2736-2747.
- Martensson S., Gyrd-Hansen D., Prescott E. et al. Trends in time to invasive examination and treatment from 2001 to 2009 in patients admitted first time with non-ST elevation myocardial infarction or unstable angina in Denmark. BMJ Open. 2014; 4: e004052.
- Ганюков В.И., Тарасов Р.С., Кочергин Н.А., Барбараш О.Л. Чрескожное коронарное вмешательство при остром коронарном синдроме без подъема сегмента ST. Эндоваскулярная хирургия. 2016; 3(1): 19-5.
- Amsterdam E.A., Wenger N.K., Brindis R.G. et al. 2014 AHA/ACC guideline for the management of patients with non-ST-elevation acute coronary syndromes. JACC. 2014; 64 (24):2645-87.


