Эндоваскулярное лечение стено-окклюзионных поражений подключичных артерий
Автор: Карпенко Андрей Анатольевич, Игнатенко Павел Владимирович, Стародубцев Владимир Борисович, Гостев Александр Александрович
Журнал: Патология кровообращения и кардиохирургия @journal-meshalkin
Рубрика: Сосудистая хирургия
Статья в выпуске: 3 т.19, 2015 года.
Бесплатный доступ
Цель Оценить эффективность и безопасность эндоваскулярных вмешательств при стено-окклюзионных поражениях подключичных артерий. Материал Представлены результаты ретроспективного анализа эффективности эндоваскулярного метода лечения и методы стено-окклюзионных поражений подключичных артерий у 205 пациентов. В зависимости от вида поражения подключичной артерии пациенты были разделены на 2 группы. В первую группу вошли пациенты (n = 126; 61%) со стенозами, во вторую (n = 79; 39%) - с окклюзиями подключичных артерий. Результат проводимого лечения контролировался интраоперационно контрольной ангиографией, перед выпиской из стационара ультразвуковым дуплексным сканированием брахиоцефальных сосудов и исследованием неврологического статуса пациента. Период наблюдения составил от 6 мес. до 5 лет. результаты У одного пациента в первой группе (0,8%) интраоперационно развилось острое нарушение мозгового кровообращения в вертебробазилярном бассейне. У одного пациента во второй группе (1,2%) интраоперационно развилась транзиторная ишемическая атака в вертебробазилярном бассейне. Повторные вмешательства на оперированном сегменте в отдаленном периоде выполнили у 4 (3,1%) человек в первой группе и у 4 (5,0%) человек во второй группе (р = 0,419). Первичная проходимость за 3 года в первой группе составила 96,7%, во второй - 94,1% (р = 0,492). Выводы При окклюзиях подключичных артерий целесообразно первым этапом выполнять эндоваскулярную реканализацию с последующим стентированием. Эндоваскулярное лечение поражений подключичных артерий - эффективный и безопасный метод профилактики острого нарушения мозгового кровообращения в вертебробазилярном бассейне.
Окклюзия подключичных артерий, вертебробазилярная недостаточность, стил-синдром
Короткий адрес: https://sciup.org/142140690
IDR: 142140690 | УДК: 616.134
Endovascular treatment of steno-occlusive lesions of subclavian arteries disease
Objective. The purpose of our study is to access the safety and efficacy of endovascular interventions for treatment of steno-occlusive disease of the subclavian artery. Methods. 205 patients with a steno-occlusive disease of the subclavian artery (SA) were included in this single-center retrospective study. 126 (61%) patients with stenosis of SA formed the 1st group, while 79 (39%) patients with SA occlusion made up the 2nd group. The treatment process was monitored intraoperatively by means of angiography, serial color Doppler ultrasonography of brachiocephalic vessels and complete neurological evaluation prior to discharge. The patients were then followed up over a period from 6 months to 5 years. Results. During the perioperative period one stroke (0.8%) in the vertebrobasilar basin was registered in the 1 st group. In the 2nd group one transient ischemic attack (1.2%) was observed. Re-interventions in the long-term period were carried out in 4 (3.1%) cases in the 1st group and 4 (5%) cases in the 2nd group (р = 0.419). The cumulative primary stent patency at 3 years was 96.7% in the 1st group and 94.1% in the 2nd group (р = 0.492). Conclusion. In the case of occlusion of the subclavian artery it could be appropriate to perform endovascular recanalization followed by stenting as the first stage of surgery. Endovascular treatment of lesions is an effective and safe method of prevention of stroke in the vertebrobasilar basin.
Текст научной статьи Эндоваскулярное лечение стено-окклюзионных поражений подключичных артерий
создало ложное представление, что синдром позвоночно-подключичного обкрадывания – довольно редкое явление, сопровождающееся выраженной клинической симптоматикой [9]. С появлением таких неинвазивных методов диагностики, как УЗИ в 1970 г. и магнитно-резонансной ангиографии в 1992 г., выявили большее число бессимптомных пациентов [10, 11]. Однако тактика лечения этой патологии остается неоднозначной. Большинство исследователей асимп-томным пациентам рекомендуют проводить консервативную терапию, независимо от степени поражения подключичной артерии [6, 12]. Хирургическое лечение – шунтирование, чрескожную транслюминальную ангиопластику (ЧТКА) и стентирование – целесообразно осуществлять пациентам только с выраженной вертебробазилярной недостаточностью либо ишемией верхней конечности [13, 14].
Цель исследования – оценить эффективность и безопасность эндоваскулярных вмешательств при стеноокклюзионных поражениях подключичных артерий.
Материал и методы
Проведен ретроспективный анализ результатов эндоваскулярного лечения стено-окклюзионных поражений подключичных артерий в период с 2010 по 2014 г. в центре сосудистой и гибридной хирургии ФГБУ «НННИИПК им. акад. Е.Н. Мешалкина» Минздрава России. Выборка составила 205 пациентов с гемодинамически значимыми стенозами или окклюзиями подключичных артерий, перенесших эндоваскулярное лечение. Критериями включения пациентов в исследование являлись окклюзия или стеноз подключичной артерии более 70% при наличии симптоматики хронической ишемии верхней конечности и/или вертебробазилярной недостаточности, вызванной стил-синдромом. Из исследования исключали пациентов с гемодинамически незначимыми стенозами подключичных артерий, бессимптомными поражениями подключичных артерий, а также перенесших инфаркты миокарда менее 6 мес. назад, инсульты менее 3 мес. назад, недавнюю черепно-мозговую травму.
В зависимости от вида поражения подключичной артерии – стеноз или окклюзия – пациентов (n = 205) разделили на две группы. В первую группу вошли больные (n = 126; 61%) со стенозами, во вторую (n = 79; 39%) – с окклюзиями. По гендерным признакам, выраженности симптоматики, степени сердечной недостаточности, наличию артериальной гипертензии, холестеринемии достоверного различия в группах не было (р>0,05).
Всем пациентам под местной инфильтративной анестезией раствором лидокаина 2% проводили ангиопластику со стентированием пораженного сегмента подключичной артерии самораскрывающимися и баллонорасширяемыми стентами различных производителей.
Результат лечения контролировали интраоперационно ангиографией, перед выпиской из стационара ультразвуковым дуплексным сканированием брахиоцефальных сосудов и исследованием неврологического статуса пациента. Период наблюдения составил от 6 мес. до 5 лет. Результат оперативного вмешательства оценивался клинически – проявления вертебробазилярной недостаточности и ишемии конечности – и по данным ультразвукового дуплексного сканирования брахиоцефальных сосудов. Всем пациентам назначали дуплексное сканирование и контрольный осмотр невролога через 6 мес. после оперативного вмешательства.
Для проверки нормальности распределения параметров применяли W критерий Шапиро – Уилка. Количественные данные представлены в виде среднего ± стандартное отклонение. Попарные сравнения выполняли с применением U критерия Манна – Уитни. Качественные признаки сравнивали с применением критерия хи-квадрата Пирсона или точного теста Фишера. Статистически значимые предикторы развития стеноза или реокклюзии стентированной артерии определялись методом логистической регрессии и регрессией Кокса. Свобода от реокклюзии и стеноза оперированной артерии в двух группах сравнилась с использованием лог-ранг теста. Уровень отклонения нулевой гипотезы об отсутствии различий между группами принимали при р<0,05.
Результаты
Всем пациентам выполнили баллонную ангиопластику с последующим стентированием подключичной артерии. Средний возраст пациентов составил в первой группе 61±7 лет, во второй – 60,4±6,8 года. В первой группе у 79 пациентов (63%) стеноз был слева, у 47 (37%) – справа. Во второй группе у 70 пациентов (89%) окклюзирована левая подключичная артерия и у 9 (11%) – правая. Вертебробазилярная недостаточность являлась критерием включения в исследование и присутствовала у всех пациентов. В первой группе у 38 человек (30%) была клиника ишемии верхней конечности, во второй – у 37 пациентов (46,8%). Перед операцией всем пациентам проводили дуплексное сканирование брахиоцефальных сосудов и КТ-ангиографию ветвей
Таблица 1 Клинические характеристики пациентов двух группах
|
1-я группа, n (%) |
2-я группа, n (%) |
p |
|
|
Левая |
79 (62,7) |
70 (88,6) |
0,112 |
|
Сторона поражения |
|||
|
Правая |
47 (37,3) |
9 (11,4) |
0,002 |
|
Клиника ишемии верхней конечности |
38 (30,1) |
37 (46,8) |
0,069 |
|
ИБС |
109 (86,5) |
68 (86,1) |
0,533 |
|
ГБ |
104 (82,5) |
67 (84,8) |
0,491 |
|
Сопутствующая патология СД |
13 (10,3) |
10 (12,6) |
0,402 |
|
ХПН |
31 (24,6) |
17 (21,5) |
0,410 |
|
Поражение сонных артерий |
57 (45,2) |
37 (46,8) |
0,495 |
|
ОНМК в анамнезе |
20 (15,8) |
20 (25,3) |
0,120 |
|
Операции в анамнезе ЧТКА |
30 (23,2) |
17 (21,5) |
0,450 |
|
АКШ/МКШ |
16 (12,4) |
11 (13,9) |
0,490 |
дуги аорты с церебральной фазой. В первой группе сопутствующую ишемическую болезнь сердца (ИБС) диагностировали у 109 (86,5%), при этом в анамнезе ЧТКА была у 30 (23,2%), аортокоронарное шунтирование (АКШ) и маммарнокоронарное шунтирование (МКШ) – у 16 (12,4%) пациентов. Гипертоническую болезнь (ГБ) обнаружили у 104 (82,5%), сахарный диабет (СД) – у 13 (10,3%), хроническую почечную недостаточность (ХПН) у 31 (24,6%) больного. Во второй группе сопутствующую ИБС определили у 68 (86%), при этом ЧТКА выполнена 17 (21,5%) пациентам, АКШ и МКШ – 11 (13,9%) пациентам. Гипертоническую болезнь выявили у 67 (84,8%) наблюдаемых, СД – у 10 (12,6%), ХПН – у 17 (21,5%). В первой группе сопутствующее поражение сонных артерий было у 57 (45,2%), во второй – у 37 (46,8%) человек. Острое нарушение мозгового кровообращения (ОНМК) в каротидном бассейне в анамнезе как в первой, так во второй группе было у 20 человек (15,8 и 25,3% соответственно) (табл. 1).
Летальных случаев, развития инфаркта миокарда не было. Первичная неудача эндоваскулярного лечения, потребовавшая повторного вмешательства, была у 3 (2,3%) пациентов в первой группе, из них у 2 по причине остаточного стеноза и у 1 – тромбоза стентированного участка, который произошел в раннем послеоперационном периоде. Неудачная попытка реканализации окклюзии подключичной артерии была у 11 (13,9%) пациентов во второй группе (р = 0,0009). В 9 случаях выполнили успешные сонно-подключичные шунтирования, 2 пациентов направили на консервативное лечение.
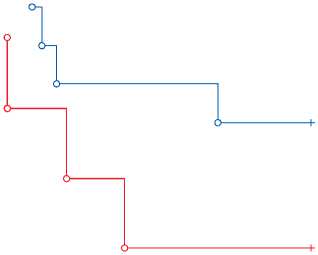
У одного пациента в первой группе (0,8%) интраоперационно развилось ОНМК в вертебробазилярном бассейне. У одного пациента во второй группе (1,2%) интраоперационно развилась транзиторная ишемическая атака (ТИА) в вертебробазилярном бассейне. В отдаленном периоде повторных ОНМК или ТИА не было ни в первой, ни во второй группе. В отдаленном периоде рестенозы, не потребовавшие повторного оперативного вмешательства, вследствие отсутствия вертебробазилярной недостаточности, зафиксированы у 7 (5,5%) пациентов первой группы и у 6 (7,5%) – второй (р = 0,38). Повторные вмешательства на оперированном сегменте в отдаленном периоде выполнены в первой группе у 4 (3,1%) человек в среднем через 13 мес., во второй – также у 4 (5,0%) человек в среднем через 12,6 мес. (р = 0,419). Первичная проходимость за 3 года в первой группе – 96,7%, во второй – 94,1% (р = 0,492) (рисунок).
В табл. 2 приведены результаты регрессионного анализа предикторов рестеноза или реокклюзии оперированной артерии в отдаленном послеоперационном периоде у всех пациентов.
Статистически достоверным оказался один предиктор – увеличение длины имплантированного стента. Отношение шансов составило 1,05, а отношение рисков – 1,06, что говорит об увеличении вероятности развития рестеноза в стентированной артерии на 5%, а рисков на 6% при увеличении длины стента на 1 мм. При этом изначальное состояние артерии (стеноз или окклюзия) достоверно не влияет на проходимость стента в отдаленном послеоперационном периоде.
Купирование вертебробазилярной недостаточности оценивалось клинически и наблюдалось у 114 (90,5%) пациентов первой группы и у 60 (76%) второй (р = 0,0047), а купирование ишемии верхней конечности – у
5 10 15 20 25 30 35
о Заверш.
+ Цензурир.
Группа 1
Группа 2
Месяцы
Первичная проходимость стентированных артерий за 3 года в первой и второй группах
34 (89,4%) пациентов первой группы и у 29 (78,4%) второй (р = 0,02).
Обсуждение
Хирургическое лечение стено-окклюзионных поражений подключичных артерий включает шунтирующие операции, эндартерэктомии и ЧКТА со стентированием. Первоначально симптомные поражения подключичной артерии лечили путем открытых реконструктивных вмешательств. Однако эндартерэктомии сопровождались высокой частотой дистальных эмболий с развитием ОНМК в вертебробазилярном бассейне, а трансторакальные вмешательства – интраоперационными осложнениями и летальностью [15]. В связи с этим получили широкое распространение экстраторакальные операции – подключично-сонная транспозиция и сонно-подключичное шунтирование [16]. Развитие эндоваскулярных методов лечения внесло существенный вклад в терапию вертебробазилярной недостаточности. По сравнению с открытой хирургией эндоваскулярные методы имеют значительно меньший процент интра- и
Таблица 2 Предикторы развития рестеноза
|
Предиктор |
ОШ 95% ДИ |
p |
ОР 95% ДИ |
p |
|
Возраст |
0,972 [0,931; 1,014] |
0,197 |
0,965 [0,867; 1,075] |
0,525 |
|
Пол (женский/мужской) |
0,505 [0,232; 1,102] |
0,085 |
0,327 [0,082; 1,310] |
0,115 |
|
Окклюзия подключичной артерии* |
0,562 [0,134; 2,354] |
0,428 |
1,759 [0,441; 6,994] |
0,424 |
|
Степень ишемии верхней конечности |
0,968 [0,783; 1,196] |
0,759 |
0,507 [0,195; 1,326] |
0,166 |
|
Степень ХНМК |
0,984 [0,639; 1,515] |
0,942 |
0,720 [0,373; 1,391] |
0,330 |
|
Ишемическая болезнь сердца |
0,671 [0,264; 1,704] |
0,399 |
0,929 [0,115; 7,499] |
0,945 |
|
Гипертоническая болезнь |
1,396 [0,541; 3,604] |
0,488 |
2,493 [0,607; 10,164] |
0,205 |
|
Хроническая почечная недостаточность |
0,837 [0,366; 1,915] |
0,673 |
0,448 [0,057; 3,512] |
0,445 |
|
Сахарный диабет |
0,771 [0,215; 2,769] |
0,689 |
1,142 [0,141; 9,218] |
0,901 |
|
Вид стента (самораскрывающиеся)** |
1,321 [0,487; 3,583] |
0,582 |
1,013 [0,254; 4,032] |
0,986 |
|
Длина стента, мм |
1,050 [1,01; 1,096] |
0,012 |
1,060 [1,008; 1,116] |
0,023 |
ОШ – отношение шансов; ОР – отношение рисков; ДИ – доверительный интервал; ХНМК – хроническое нарушение мозгового кровообращения; * по сравнению со стенозом; ** по сравнению с баллонорасширяемыми стентами послеоперационных осложнений и проводятся под местной анестезией [17–19]. Чрескожная баллонная ангиопластика является признанным методом выбора лечения стенозов подключичных артерий [20–26]. Однако считается, что при окклюзиях этих артерий баллонная ангиопластика не так эффективна, как при стенозах [23, 24, 26], и имеет более низкий процент успеха. В ретроспективном исследовании DeVries [13] проанализировано 110 пациентов со стено-окклюзионными поражениями подключичных артерий, которым проводили чрескожную транслюминальную ангиопластику. Трехлетняя проходимость после лечения достигнута у 93% пациентов с подключичными стенозами и у 65% с окклюзиями [13]. В нашем исследовании – у 95,9% пациентов с подключичными стенозами и у 92,6% с окклюзиями. Linni [27] и соавт. провели ретроспективное исследование, в котором выделили 2 группы пациентов со стено-окклюзионным поражением подключичных артерий: 40 пациентам провели ангиопластику со стентированием и 34 пациентам – сонно-подключичное шунтирование. Первичный неуспех ангиопластики был в 48% случаев с окклюзией подключичной артерии (30% всех ангиопластик), в то время как все сонно-подключичные шунты были удачными. По мнению авторов, эндоваскулярные методы предпочтительнее при стенозах, а открытое шунтирование при окклюзии подключичных артерий [27]. В нашем исследовании первичный неуспех ангиопластики был у 2,3% пациентов со стенозами подключичных артерий и у 13,9% пациентов с окклюзиями.
Частота инсультов в вертебробазилярном бассейне составляет 20% общего числа ишемических инсультов, причем смертность превышает 85% [1, 2]. Изучение комбинированных регистров по ОНМК в вертебробазилярном бассейне показало, что стено-окклюзионные поражения сосудов большого диаметра (подключичные артерии, брахиоцефальный ствол) являются причиной ОНМК в вертебробазилярном бассейне в 35% случаев [2, 28, 29]. Jung исследовал 54 пациента с синдромом подключичного обкрадывания и обнаружил по данным мультиспиральной компьютерной томографии головного мозга, что 50% пациентов с проявлениями вертебробазилярной недостаточности имеют старые очаги инсультов в бассейне задней мозговой циркуляции [30]. По данным DeVries и со-авт. [13], после ангиопластики подключичных артерий частота ОНМК в отдаленном периоде составила 3,6%. В нашем исследовании после проведенного лечения в отдаленном периоде ОНМК не возникало ни в первой, ни во второй группе.
Исследование показало эффективность эндоваскулярной коррекции как стенозов, так и окклюзий подключичных артерий при малом количестве пери- и послеоперационных осложнений, а также удовлетворительную проходимость реконструированного сосуда в отдаленном периоде. Неудачи при окклюзиях подключичных артерий обусловлены не рестенозами, а невозможностью первичной реканализации артериальной окклюзии. Эндоваскулярная методика имеет значительно меньший риск осложнений по сравнению с открытыми вмешательствами, поэтому эндоваскулярное оперативное вмешательство можно рекомендовать как метод выбора при лечении пациентов с окклюзиями подключичных артерий.
Выводы
При окклюзиях подключичных артерий целесообразно первым этапом выполнять эндоваскулярную реканализацию с последующим стентированием, поскольку данные оперативные вмешательства имеют значительно меньший риск осложнений по сравнению с открытыми вмешательствами, а первичная проходимость после эндоваскулярного лечения за 3 года составила 96,7% в группе со стенозами и 94,1% в группе с окклюзиями подключичных артерий.
Эндоваскулярное лечение поражений подключичных артерий является эффективным и безопасным методом профилактики ОНМК в вертебробазилярном бассейне. Дальнейшие проспективные рандомизированные исследования актуальны и научно обоснованы.
Список литературы Эндоваскулярное лечение стено-окклюзионных поражений подключичных артерий
- Gulli G., Marquardt L., Rothwell P.M., Markus H.S. Stroke risk after posterior circulation Stroke/transient ischemic attack and its relationship to site of vertebrobasilar stenosis pooled data analysis from prospective studies. Stroke. 2013. Vol. 44. № 3. P. 598-604.
- Labropoulos N., Nandivada P., Bekelis K. Stroke of the posterior cerebral circulation//Int. Angiol. 2011. Vol. 30. № 2. P. 105-14.
- Tan T.Y., Schminke U., Lien L.M., Tegeler C.H. Subclavian steal syndrome: can the blood pressure difference between arms predict the severity of steal?//J. Neuroimaging, 2002. Vol. 12. P. 131-35.
- Hennerici M., Klemm C., Rautenberg W: The subclavian steal phenomenon: a common vascular disorder with rare neurologic deficits//Neurology, 1988. Vol. 38. P. 669-73.
- Fields W.S., Lemak N.A. Joint study of extracranial arterial occlusion. VII. Subclavian steals -a review of 168 cases//JAMA, 1972. Vol. 222. P. 1139-43.
- Labropoulos N., Nandivada P., Bekelis K. Prevalence and Impact of the Subclavian Steal Syndrome//Ann. Surg. 2010. Vol. 252. P. 166-70.
- Nicholls S.C., Koutlas T.C., Strandness D.E. Clinical significance of retrograde flow in the vertebral artery//Ann. Vasc. Surg. 1991. Vol. 5. P. 331-36.
- Heidrich H., Bayer O. Symptomatology of the subclavian steal syndrome//Angiology. 1969. Vol. 20. P. 406-13.
- Herring M. The subclavian steal syndrome: a review//Am. Surg. 1977. Vol. 43. P. 220-28.
- Grossman B.L., Brisman R., Wood E.H. Ultrasound and the subclavian steal syndrome. Radiology. 1970. Vd. 94: P. 1-6.
- Drutman J., Gyorke A., Davis W.L., Turski P.A. Evaluations of subclavian steal with two-dimensional phase-contrast and two-dimensional time-of-flight MR angiography//Am. J. Neuroradiol. 1994. Vol. 15. P. 1642-45.
- Olsen K., Lund C. Subclavian steal syndrome. Tidsskr Nor Laegeforen//2006. Vol. 126. P. 3259-62.
- De Vries J.P., Jager L.C., van den Berg J.C. Durability of Percutaneous trans-luminal angioplasty for obstructive lesions of proximal subclavian artery: long term results//Vasca. J. Surg. 2005. Vol. 41. P. 19-23.
- Bates M.C., Broc M., Lavigne P.S., Stone P. Subclavian artery stenting: factors influencing long-term outcome. Catheter Cardiovasc. Intervet, 2004. Vol. 61. P. 5-11.
- Национальные рекомендации по ведению пациентов с сосудистой артериальной патологией. Часть 3. Брахиоцефальные артерии. М., 2012. С. 35-39.
- Dattilo J.B., Cambria R.P. Complications of repair of the supra -aortic trunks and the vertebral arteries.: in Towne J.B., Hollier L.H. (eds) Complications in vascular surgery. New York, Marcel Dekken, 2005. P. 457^66.
- Palchik E., Bakken A.M., Wolford H.Y. et al: Subclavian artery revascularization: an outcome analysis based on mode of therapy and presenting symptoms//Ann. Vasc. Surg. 2008. Vol. 22. P. 70-78.
- Wang K.Q., Wang Z.G., Yang B.Z. et al. Long-term results of endovascular therapy for proximal subclavian arterial obstructive lesions//Chin. Med. J. (Engl), 2010. Vol. 123. № 1. P. 45-50.
- Galkin P.V., Antonov G.I., Mitroshin G.E. et al. Surgical correction of cerebral blood flow steal syndrome by aortic branches stenosis//Khirurgiia (Mosk), 2009. Vol. 7. P. 15-21.
- Bogey W.M., Demasi R.J., Tripp M.D., Vithalani R., Johnsrude I.S., Powell S.C. Percutaneous transluminal angioplasty for subclavian artery stenosis//Am. Surg. 1994. Vol. 60. P. 103-106.
- Duber C., Klose K.J., Kopp H., Schmiedt W. Percutaneous transluminal angioplasty for occlusion of subclavian artery: short-and long-term results//Cardiovasc. Intervent. Radiol. 1992. Vol. 15. P. 205-210.
- Farina C., Mingoli A., Schultz R.D., Castrucci M., Feldhaus R.J., Rossi P., Cavallaro A. Percutaneous transluminal angioplasty versus surgery for subclavian artery occlusive disease//Am. J. Surg. 1989. Vol. 158. P. 511-514.
- Hebrang A., Maskovic J., Tomac B. Percutaneous transluminal angioplasty of the subclavian arteries: long-term results in 52 patients//AJR Am. J. Roentgenol. 1991. Vol. 156. P. 1091-1094.
- Kachel R., Basche S., Heerklotz I., Grossman K., Endler S. Percutaneous transluminal angioplasty (PTA) of supra-aortic arteries especially the internal carotid artery//Neuroradiology. 1991. Vol. 33. P. 191-194.
- Mathias K.D., Luth I., Haarmann P. Percutaneous transluminal angioplasty of proximal subclavian artery occlusions//Cardiovasc. Intervent. Radiol. 1993. Vol. 16. P. 214-218.
- Motarjeme A. Percutaneous transluminal angioplasty of supra-aortic vessels//J. Endovasc. Surg. 1996. Vol. 3. P. 171-181.
- Linni K., Ugurluoglu A., Mader N. et al. Endovascular management versus surgery for proximal subclavian artery lesions//Ann. Vasc. Surg. 2008. Vol. 22. № 6. P. 769-67.
- Markus H.S., van der Worp H.B., Rothwell P.M. Posterior circulation ischaemic stroke and transient ischaemic attack: diagnosis, investigation, and secondary prevention//Lancet Neurol. 2013. Vol. 12. № 10. P. 989-98.
- Карпенко А.А., Кужугет Р.А., Стародубцев В.Б., Игнатенко П.В., Ким И.Н., Горбатых В.Н. Непосредственные и отдален ные результаты различных методов реконструкции каротидной бифуркации//Патология кровообращения и кардиохирургия. 2013. № 1. С. 21-24.
- Jung K.-H., Kim J.-M., Lee S.-T. et al. Brain Response Characteristics Associated with Subclavian Steal Phenomenon//Journal of Stroke and Cerebrovascular Diseases. 2014. Vol. 23. P. 157-161.


