Энтальпия гидратации халькогенидов
Автор: Рябухин Александр Григорьевич, Груба Оксана Николаевна, Германюк Нина Васильевна
Журнал: Вестник Южно-Уральского государственного университета. Серия: Химия @vestnik-susu-chemistry
Рубрика: Физическая химия
Статья в выпуске: 4 т.6, 2014 года.
Бесплатный доступ
В работе показана возможность применения модифицированной модели для расчета стандартной энтальпии образования анионов халькогенов в газовой фазе и в водном растворе, стандартной энтальпии гидратации халькогенид-ионов. Сделаны предсказательные расчеты термохимических характеристик для аниона полония. Полученные величины энтальпий образования газообразных анионов позволили рассчитать для атомов халькогенов первые и вторые значения сродства к электрону.
Анион, халькогены, энтальпия образования, энтальпиягидратации, радиус "водного" аниона, сродство к электрону
Короткий адрес: https://sciup.org/147160299
IDR: 147160299 | УДК: 544.31.031
Hydration enthalpy of chalcogenides
Application’s possibility of the modified model, which calculate as formation standard enthalpy of chalcogens’ anions in a gas phase and water solution, as a standard enthalpy of chalkogenidions’ hydration is shown in work. Predictive calculations of thermochemical characteristics for polonium anion are made. The received sizes of gaseous anions’ formation enthalpies allowed to calculate for chalcogens’ atoms the first and second values of affinity to an electron.
Текст научной статьи Энтальпия гидратации халькогенидов
Халькогенидам в природе принадлежит важная роль: это кислородсодержащие горные породы, составляющие большинство, это кислород- и серосодержащие руды – основные источники металлов и халькогенидов.
Разнообразным технологиям переработки руд требуются данные по различным свойствам веществ в разных фазовых состояниях: газы, расплавы, растворы и другие.
В работе [1] на примере галид-ионов (для которых приведены надежные справочные сведения) показано, что модифицированное уравнение расчета энтальпии кристаллической решетки позволяет вычислить энтальпию образования газообразного и гидратированного аниона. Сущность модификации заключается в замене в расчетном уравнении межструктурного расстояния в кристалле на радиус иона.
В расчетах используются следующие единицы измерения: для энтальпии – кДж∙моль-1, для расстояний – ангстремы (10-8 см).
Уравнение для расчета энтальпии образования газообразных ионов имеет одинаковую форму для катионов и для анионов.
A fH ° = A H 0 + A H вз = 83,581728 ■ z 2 ■ f 1 - 103,19053 ■ A M ■ кч ■ z ■ f 2 • ( r ° ) - 1 . (1)
Здесь кч = 6 и АМ = 1,747565 (NaCl).
Для полных электронных аналогов двухзарядных катионов и анионов, имеющих электронное строение ( n - 1 ) s 2 p 6 ns 2 p 6 :
A fH ° = 83,581728 ■ z 2 ■ f + 103,19053 ■ 1,747565 ■ 6 ■ z ■ f 2 ■ ( r ° ) — 1 =
= 83,581728 ■ 4 ■ f 1 + 1081,99295 ■ 2 ■ f 2 ■ ( r ° ) — 1 ;
A fH ° =- 334,3269 ■ f 1 + 2163,9859 ■ f 2 ■ ( r ° ) — 1 . (2)
В работе [2] из расчетов по уравнениям модели энтальпий кристаллических решеток халькогенидов металлов подгруппы цинка вычислены A f H ° ( Хг2 - ,г ) для S2 - , Se2 - , Te2 - , Po2 - .
В случае полных электронных аналогов ( Se2 - - Po2 - )
- 1
f 1 = f ГЦК ■ f ОЦК = 2 [ 1 + 2 J 3V3 = 4,156922 ;
f 2 = f ГЦК - f ОЦК = 2 | 1 + тЬ- | 1 + -I = 1,68750 .
V 2 ) 8 V 9 )
После подстановки значений f 1 и f 2 в уравнение (2) получим
A fH ° ( Хг2 - ,г ) = - 1389,771 1 + 3651,7262 ( r ° ) - 1 . (3)
Исходные (справочные) данные и результаты расчетов по уравнению (3) приведены в табл. 1.
Таблица 1
Энтальпия образования газообразных анионов халькогенов
|
№ п/п |
Хг2 - |
r ° ( Хг2 -) , [2] |
A f H ° ( Хг2 - ,г ) , [2] |
A H вз , ур. (3) |
A f H ° ( Хг2 - ,г ) , ур. (3) |
|
1 |
2 |
3 |
4 |
5 |
|
|
1 |
S2 - |
1,78064 |
619,315±0,167 |
2050,187 |
660,416 |
|
2 |
Se2 - |
1,89371 |
537,935±0,430 |
1927,774 |
538,003 |
|
3 |
Te2 - |
2,06104 |
381,555±0,667 |
1771,263 |
381,492 |
|
4 |
Po2 - |
2,13724 |
318,174±0,753 |
1708,111 |
318,340 |
Из сравнения величин в колонках 3 и 5 следует хорошее согласие для ионов полных электронных аналогов - Se2 - , Te2 - и Po2 - . Для иона связующего элемента ( S2 - ) согласия нет (расхождение составляет 41,1). Для иона начального элемента ( О2 - ) расхождение между рассчитанной и экспериментальной величинами составило 188,3 ( A f H ° ( О2 - , г ) = 1069,218 [2]).
В работе [2] показано, что в таблицах ионных радиусов [3, 4] приводятся «водные» радиусы анионов. В основе расчетов ионных радиусов создатели таблиц использовали радиус иона кислорода O2 - в интервале от 1,32 до 1,46 А (10-8 см). В 1923 г. индийский ученый Вазашерна из рефрактометрических измерений растворов солей вычислил радиус иона кислорода, составивший 1,32∙10-8 см. Поэтому нельзя считать радиусы, приведенные в [3, 4], «кристаллическими».
Водные радиусы r в можно вычислить по уравнению модели эффективных ионных радиусов, используя свойства воды.
rK • rD • r A = 1,383 - 83,933735 - r A = 118,846356 - r A rK - r D - ( r A ) 2 1,383 - 83,933735 - ( r A ) 2 118,846356 - ( r A ) 2
Здесь rK = 1,383 – радиус молекулы воды, которая положительным концом диполя ориентирована к аниону (радиус rA), то есть выступает в роли катиона; rD - дебаевский радиус экранирования rD = rD (NaCl) - fz = 31,45393 - (1 + Jz2 -1) = 85,933735.
«Водные» радиусы ионов халькогенов приведены в табл. 2 и 3.
Таблица 2 Энтальпия образования анионов халькогенов в водном растворе
|
№ п/п |
Хг2 - |
r в, ур. (4) |
A f H ° ( Хг2 - ,р-р ) , [5] |
-A H вз , ур. (5) |
A fH ° ( Хг2 ,р-р ) , ур.(5) |
|
1 |
2 |
3 |
4 |
5 |
|
|
1 |
S2 - |
1,82945 |
36,40±1,26 |
522,223 |
93,428 |
|
2 |
Se2 - |
1,95263 |
126,575±2,092 |
489,280 |
126,372 |
|
3 |
Te2 - |
2,13744 |
168,91±2,092 |
446,975 |
168,677 |
|
4 |
Po2 - |
2,22267 |
отс. |
429,835 |
185,817 |
Таблица 3
Энтальпия гидратации анионов халькогенов
|
№ п/п |
Хг2 — , r в , ур. (4) |
A f H ° ( Хг2 — ,г ) , (табл. 1) |
A f H ° ( Хг2 — ,р-р ) , (табл. 2) |
—Ar H ° ( Хг2 —) , ур. (6) |
—A H вз , ур. (7) |
—Ar H ° ( Хг2 —) , ур. (7) |
|
1 |
2 |
3 |
4 |
5 |
6 |
|
|
1 |
S2 — 1,82945 |
619,315±0,167 |
93,428±1,26 |
525,887±1,427 |
2441,657 |
565,888 |
|
2 |
Se2 — 1,95263 |
537,935±0,430 |
126,372±0,430 |
411,631±2,522 |
2290,959 |
411,272 |
|
3 |
Te2 — 2,13744 |
381,555±0,667 |
168,677±0,667 |
212,815±2,751 |
2092,397 |
213,230 |
|
4 |
Po2 — 2,22267 |
318,174±0,753 |
185,817±0,753 |
132,523 |
2015,865 |
132,995 |
В модели гидратации катионов [2] показано, что в любых растворах, для которых принимается A f H ° ( Н + , р-р ) = 0, необходимо знать его действительное значение. Там же вычислено A f H ° ( Н + , р-р ) = 406,025 ± 0,008 .
Уравнение для расчета энтальпии образования анионов в водном растворе в нашем случае
A fH ° ( Хг2 — , p - p ) = 406,025 " z + A H 0 + A H вз ,
A f H ° ( Хг2 — , p - p ) = 406,025 " 2 — 83,581728 • 4 • f1 — 103,19053 • 1,747565 • 6 • 2 • г в — 1 =
= 812,050 — 196,398 — 955,3820 • г в — 1 ,
A fH ° ( Хг2
, p - p ) = 615,652 — 955,3 825 • r B — 1
.
(5)
( 8 f . = f ОЦК " f ГЦК = к 3^3
—
1 ) 42^2 = 0,587443 ;
7 з4з
f 2 = f ОЦК " f ГЦК = 3/3 "
1 +
к 3 7
— 1
= 0,441492 .
Исходные данные и результаты вычислений помещены в табл. 2.
. —
Из данных строк 2 и 3 ( Se2
и Te2 ) следует их хорошее согласие, что подтверждает
адекватность модели и позволяет произвести предсказательный расчет для A f H ° ( Ро2 ,р-р ) . У аниона связующего элемента ( S2 — ) согласия не наблюдается, как и в случае с расчетами A f H ° ( Хг2 — ,г ) . Здесь расхождение расчетных и справочных данных составило 57,0.
Согласно определению, энтальпия гидратации аниона
A г H ( A z —) = A f H ° ( A z — ,р-р ) — A f H ° ( A z — ,г ) . (6)
Ранее были вычислены хорошо согласующиеся значения A f H ° ( Хг2 — ,г ) и A f H ° ( Хг2 — ,р-р ) для анионов Se2 — и Te2 — . Это позволяет использовать расчеты по уравнению (6) с применением полученных термических характеристик в качестве контрольных.
Модифицированное уравнение для расчета энтальпии гидратации анионов халькогенов аналогично уравнению расчета энтальпии образования простых анионов халькогенов в водном растворе.
А г Н ( Хг2 - ) = 2 A fН ° ( Н + , р-р ) + А Н 0 + А Н вз;
А г Н ( Хг2 -) = 2 ■ 406,025 + 83,587128 ■ 2 2 ■ f - 103,19053 ■ 1,747565 ■ 6 ■ 2 ■ f 2 ■ r - =
= 812,050 + 1067,117 - 4472,3772 ■ r - 1; в
А г Н ( Хг2 -) = 1879,167 - 4472,3772 ■ г в - 1 .
f 1 = f ОЦК ■ f ГЦК = 3 f 1 + 9
1 L 4V2 )
1 +
2 ( 373 J
- 1
= 3,191836 ;
f 2 = f ОЦК ■ f ГЦК =
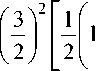
4\2 )
+ 343 J
- 1
= 2,066757 .
Исходные данные и результаты вычислений по уравнениям (6) и (7) приведены в табл. 3.
Из сравнения величин в колонках 4 и 6 следует хорошее согласие у элементов полных электронных аналогов. У сульфид-иона, являющегося ионом связующего элемента, расхождение между справочной и расчетной величинами составляет 39,6.
Согласие результатов расчетов энтальпии гидратации для иона полония ( Po2 - ) со справочным значением носит принципиальный характер, так как в вычислениях А г Н ° ( Ро2 -) была использована прогнозная величина А f H ° ( Ро2 - ,р-р ) (табл. 2).
Важнейшими характеристиками атомов являются потенциалы ионизации и сродство к электрону. Технология определения потенциалов ионизации хорошо отработана, чего нельзя сказать об определении сродства к электрону. Присоединение к атомам электрона с образованием устойчивого однозарядного аниона наблюдается у галогенов. Присоединение второго электрона с образованием двухзарядного аниона неизвестно, так как пока отсутствует метод измерения энтальпии присоединения второго электрона.
Численные величины А f H ° ( Хг2
,г ) , полученные из энтальпий кристаллических решеток
-
[2] (табл. 1), позволяют впервые рассчитать £ А и А 2 по уравнению
А fН ° ( Хг2 - ,г ) = А fH ° ( Хг0,г ) - F £ А - 2 ■ 6,1965, (8)
где F – постоянная Фарадея, 96484,56 Кл∙моль-1; 6,1965 – энтальпия 1 моль электронного газа.
Исходные данные и результаты расчетов по уравнению (8) приведены в табл. 4.
Таблица 4
Сродство атомов халькогенов к электрону
|
№ п/п |
Хг2 - |
А fH • ( Хг0,г ) , [6] |
А fH • ( Хг2 - ,г ) , (табл. 1) |
F £ А - 12,393, ур. (8) |
£ А , эВ, ур. (8) |
А 1 , эВ [6] |
А 2 , эВ |
|
1 |
2 |
2 |
4 |
5 |
6 |
7 |
|
|
1 |
S2 - |
276,980±1,046 |
619,315±0,167 |
342,335±1,826 |
3,61470± ±0,00169 |
2,0772± ±0,0005 |
1,4709± ±0,0194 |
|
2 |
Se2 - |
227,610±2,092 |
537,935±0,430 |
310,325±2,932 |
3,36508± ±0,00337 |
2,0201± ±0,0003 |
1,1962± ±0,0307 |
|
3 |
Te2 - |
168,615±1,255 |
381,555±0,667 |
212,940±1,935 |
3,06371± ±0,00226 |
(1,5213) |
(0,6857) |
|
4 |
Po2 - |
144,346±2,092 |
318,174±0,753 |
173,828±2,845 |
2,89839± ±0,02818 |
1,32 |
0,4816± ±0,0217 |
В колонке 5 помещены впервые полученные суммы величин сродства электронов к атомам халькогенов. К сожалению, для теллура экспериментальные данные о величине первого сродства электрона отсутствуют. Однако такие сведения имеются для селена и полония. Так как зависимость энтальпии образования газообразных халькогенид-ионов является линейной от обратного радиуса, то можно принять такой же вид зависимости и для первого сродства электрона.
А1 ( Te ) = а + А А 1 - 1 ( r Te )- 1 = - 4,1240 + 11,36517 ( r Te )- 1.
а( r °)
r Te = 2,06104; А 1 ( Te ) = 1,5213. Эта величина существенно отличается от примерной оценки [6]. Величина второго сродства к электрону для теллура А 2 ( Te ) , определенная по разности ^ А - A 1, составит (2,2070 - 1,5213) = 0,6857.
-
1. Подтверждена адекватность модифицированной модели энтальпии кристаллической решетки.
-
2. Хорошее согласие справочных и расчетных величин позволило произвести предсказательные вычисления энтальпии образования ионов полония в водном растворе.
-
3. Показано, что анионы связующего и тем более начального элементов обладают данными, не согласующимися с моделью.
-
4. Впервые рассчитана сумма сродства электронов к халькогенидам, что позволило вычислить вторые сродства и предсказать для теллура обе величины сродства.
-
1. Рябухин, А.Г. Энтальпия гидратации простых анионов галогенов / А.Г. Рябухин // Вестник ЮУрГУ. Серия «Химия». – 2014. – Т. 6, № 3. – С. 29-33.
-
2. Рябухин, А.Г. Эффективные ионные радиусы. Энтальпия кристаллической решетки. Энтальпия гидратации ионов: монография / А.Г. Рябухин. - Челябинск: Изд. ЮУрГУ, 2000. -115 с.
-
3. Справочник химика / под ред. Б.П. Никольского. - Л.: Химия, 1971. - Т. 1. – 1071 с.
-
4. Краткий справочник физико-химических величин / под ред. А.А. Равделя и А.М. Пономарева. – Л.: Химия, 1983. – 232 с.
-
5. Латимер, В.М. Окислительные состояния элементов и их потенциалы в водных растворах: пер. с англ. / под ред. проф. К.В. Астахова. - М.: Изд. иностр. лит., 1954. - 400 с.
-
6. Энергия разрыва химических связей. Потенциалы ионизации и сродство к электрону: спр. изд. / под ред. В.Н. Кондратьева. - М.: Наука, 1974. - 351 с.
Список литературы Энтальпия гидратации халькогенидов
- Рябухин, А.Г. Энтальпия гидратации простых анионов галогенов/А.Г. Рябухин//Вестник ЮУрГУ. Серия «Химия». -2014. -Т. 6, № 3. -С. 29-33.
- Рябухин, А.Г. Эффективные ионные радиусы. Энтальпия кристаллической решетки. Энтальпия гидратации ионов: монография/А.Г. Рябухин. -Челябинск: Изд. ЮУрГУ, 2000. -115 с.
- Справочник химика/под ред. Б.П. Никольского. -Л.: Химия, 1971. -Т. 1. -1071 с.
- Краткий справочник физико-химических величин/под ред. А.А. Равделя и А.М. Пономарева. -Л.: Химия, 1983. -232 с.
- Латимер, В.М. Окислительные состояния элементов и их потенциалы в водных растворах: пер. с англ./под ред. проф. К.В. Астахова. -М.: Изд. иностр. лит., 1954. -400 с.
- Энергия разрыва химических связей. Потенциалы ионизации и сродство к электрону: спр. изд./под ред. В.Н. Кондратьева. -М.: Наука, 1974. -351 с.


