Эпидемиология внутрибольничных инфекций в онкологическом стационаре, вызванных высокорезистентными (XDR) штаммами А. baumannii
Автор: Григорьевская Злата Валерьевна, Петухова Ирина Николаевна, Дьякова Светлана Андреевна, Дмитриева Наталья Владимировна
Журнал: Сибирский онкологический журнал @siboncoj
Рубрика: Лабораторные и экспериментальные исследования
Статья в выпуске: 3 (75), 2016 года.
Бесплатный доступ
Проблема формирования MDR ( multy-drug-resistant ) штаммов Аcinetobacter baumannii и распространения резистентности в клинике чрезвычайно актуальна для онкологических стационаров. Для грамотной организации мероприятий по прерыванию путей передачи инфекции в стационаре и распространения внутрибольничных патогенов важно определение идентичности циркулирующих штаммов микроорганизмов. Оценка истинных филогенетических отношений изучаемых штаммов возможна с помощью проведения кластерного анализа изолятов с последующим построением и анализом MSP Dendrogram в системе MALDI-TOF BIOTYPER.
Аcinetobacter baumannii, пути передачи инфекции, внутрибольничные патогены, идентичность штаммов
Короткий адрес: https://sciup.org/140253940
IDR: 140253940 | УДК: 616-006-036.22-022.3:616.9 | DOI: 10.21294/1814-4861-2016-15-3-62-66
Epidemiology of hospital-acquired infections caused by highly resistant strains in cancer patients
The problem of the prevalence of multiple drug resistant (MDR) strains of Аcinetobacter baumannii in hospi- tals is a major challenge for cancer centers. To organize the measures for interrupting nosocomial transmis- sion and spread of nosocomial pathogens, it is important to determine the identity of the circulating strains of microorganisms. Assessment of the true phylogenetic relationships of the studied strains is possible by means of a cluster analysis of the isolates, followed by the construction and analysis of MSP Dendrogram in MALDI-TOF BIOTYPER system.
Текст научной статьи Эпидемиология внутрибольничных инфекций в онкологическом стационаре, вызванных высокорезистентными (XDR) штаммами А. baumannii
Проблема формирования устойчивых штаммов микроорганизмов, в частности MDR ( multy-drug-re-sistant ) штаммов Аcinetobacter baumannii , и распространения резистентности в клинике чрезвычайно актуальна для онкологических стационаров [ 1, 3, 6 ] . Пациенты, инфицированные резистентными штаммами, становятся естественным резервуаром, носителями устойчивой флоры. Опасность кроссконтаминации – обсеменения объектов больничной среды и инфицирования других пациентов в такой ситуации очень велика [ 2 ] . Лечение инфекций, вызванных высокорезистентными микроорганизмами, – непростая задача. При таких инфекциях необходима длительная, комбинированная антибактериальная терапия, что затрудняет, а в некоторых случаях делает невозможным, проведение противоопухолевого лечения, ухудшая общий прогноз больного [ 8-10 ] . Резистентность микроорганизмов, вызвавших инфекционный процесс, непосредственно влияет на результаты лечения. В 1,5–1,6 раза увеличивается длительность госпитализации пациентов, стоимость лечения, достоверно возрастают показатели летальности от инфекции [ 1,2,4 ] . Для определения идентичности циркулирующих в клиниках штаммов высокорезистентных бактерий используют ПЦР-диагностику с определением генотипов микроорганизмов, а также при помощи системы MALDI-TOF BIOTYPER проводят кластерный анализ изолятов с последующим построением MSP Dendrogram, который с высокой степенью вероятности отражает истинные филогенетические отношения изучаемых штаммов [ 5, 7 ] .
Целью исследования явился анализ распространенности и идентичности штаммов MDR Аcinetobacter baumannii , выделенных в клинике с объектов внутрибольничной среды и из патологических материалов онкологических больных с инфекциями, вызванными А. baumannii .
Материал и методы
Проанализировано 153 штамма А.baumannii , из них 101 штамм получен от 98 онкологических пациентов. Патологические материалы были представлены отделяемым нижних дыхательных путей, раневым отделяемым и прочими биоматериалами (табл. 1). Также было проанализировано 187 объектов больничной среды (табл. 2).
Далее были определены биотипы исследуемых штаммов бактерий в соответствии с 8-значной экспертной системой обработки данных MicroScan и программным обеспечением системы WаlkАway. Выполнен кластерный анализ и видовая идентификация штаммов А. baumannii путем сопоставления получаемых масс-спектров с имеющимися базами данных. Анализ производили с помощью программного пакета MALDI Biotyper 2,0 (Германия, «Bruker»). Математические модели для классификации масс-спектров, накопленных для разных групп MDR А. baumannii , строили на основании генетического алгоритма кластеризации, являющегося модулем программы ClinProTools 2,1.
Результаты
В результате проведенного исследования среди 101 штамма А.baumannii , которые выделены у
таблица 1
Количество штаммов À. baumannii , выделенных из различных патологических материалов онкологических больных
виды анализируемых объектов больничной среды
онкологических больных, было обнаружено 17 различных биотипов комплекса A. baumannii/ haemolyticus (табл. 3). Из них 5 (29,4 %) биотипов А. baumannii были представлены «дикими» штаммами и имели чувствительность практически ко всем группам антибактериальных препаратов; 12 (70,6 %) биотипов представлены MDR штаммами. Однократно встречались 13 биотипов, двух- и трехкратно – 2 биотипа. Кроме того, 2 (11,8 %) из 17 биотипов MDR штаммов А. baumannii встречались многократно: 57 (56,4 %) штаммов из 101 были представлены биотипом 00062730; 26 (25,7 %) из 101 – биотипом 00062720.
Среди 52 штаммов А.baumannii , выделенных с объектов больничной среды, обнаружено 9 различных биотипов, из них 2 (22,2 %) биотипа были представлены «дикими» штаммами и имели чувствительность практически ко всем группам антибактериальных препаратов, 7 (77,8 %) биотипов представлены MDR штаммами. Однократно встречались 7 биотипов, многократно встречались 2 биотипа MDR штаммов А.baumannii из 9: 21 (39,6 %) штамм из 53 был представлен биотипом 00062730, 24 (45,3 %) из 53 – биотипом 00062720.
В целом, 83 (82,2 %) штамма А. baumannii из 101, выделенного из патологических материалов больных, и 45 (84,9 %) штаммов из 53, выделенных с объектов больничной среды, являются госпитальными и представлены биотипами 00062730 и 00062720. При оценке идентификационных тестов системы WalkAway установлено, что идентификационные коды биотипов 00062730 и 00062720 практически идентичны и отличаются только одним тестом: MIC к тобрамицину.
Биотипы комплекса A.baumannii ( A.baumannii/haemolyticus комплекса)
|
Виды биотипов |
Ia (n=101) |
IIb(n=53) |
|
00062730 |
57 (56,4 %) |
21 (39,6 %) |
|
00062720 |
26 (25,7 %) |
24 (45,3 %) |
|
00066730 |
3 (2,9 %) |
1 (1,9 %) |
|
40066730 |
2 (1,9 %) |
- |
|
00020620 |
1 (0,9 %) |
- |
|
40020620 |
1 (0,9 %) |
- |
|
00020660 |
1 (0,9 %) |
- |
|
00020720 |
1 (0,9 %) |
- |
|
00060720 |
1 (0,9 %) |
- |
|
00060730 |
1 (0,9 %) |
- |
|
00062330 |
1 (0,9 %) |
- |
|
40062730 |
1 (0,9 %) |
- |
|
00066720 |
1 (0,9 %) |
1 (1,9 %) |
|
00066770 |
1 (0,9 %) |
1 (1,9 %) |
|
00020620 |
1 (0,9 %) |
- |
|
42060660 |
1 (0,9 %) |
- |
|
42066730 |
1 (0,9 %) |
- |
|
00060620 |
- |
1 (1,9 %) |
|
02062720 |
- |
1 (1,9 %) |
|
02062620 |
- |
1 (1,9 %) |
|
02062730 |
- |
1 (1,9 %) |
Примечание: Ia – биотипы штаммов А. baumannii , выделенные от онкологических больных; IIb – биотипы штаммов А. baumannii , выделенные с объектов больничной среды.
таблица 4
Количество и чувствительность штаммов À.baumannii с биотипами 00062730 и 0006270
|
Антибиотики |
Биотипы/количество чувствительных штаммов (n=128) |
MIC mcg/ml |
|
|
00062730 (n=78) |
00062720 (n=50) |
||
|
Ампициллин/сульбактам |
6 (7,7 %) |
0 (0 %) |
<=8 |
|
Левофлоксацин |
37 (47,4 %) |
21 (42,0 %) |
<=2 |
|
Моксифлоксацин |
40 (51,3 %) |
17 (34,0 %) |
<=0,5 |
|
Цефтазидим |
0 (0 %) |
7 (14,0 %) |
<=8 |
|
Цефепим |
0 (0 %) |
25 (50,0 %) |
<=8 |
|
Имипенем/циластатин |
0 (0 %) |
0 (0 %) |
<=4 |
|
Меропенем |
0 (0 %) |
0 (0 %) |
<=4 |
|
Тетрациклин |
18 (23,1 %) |
19 (38,0 %) |
<=4 |
|
Колистин |
78 (100 %) |
50 (100 %) |
- |
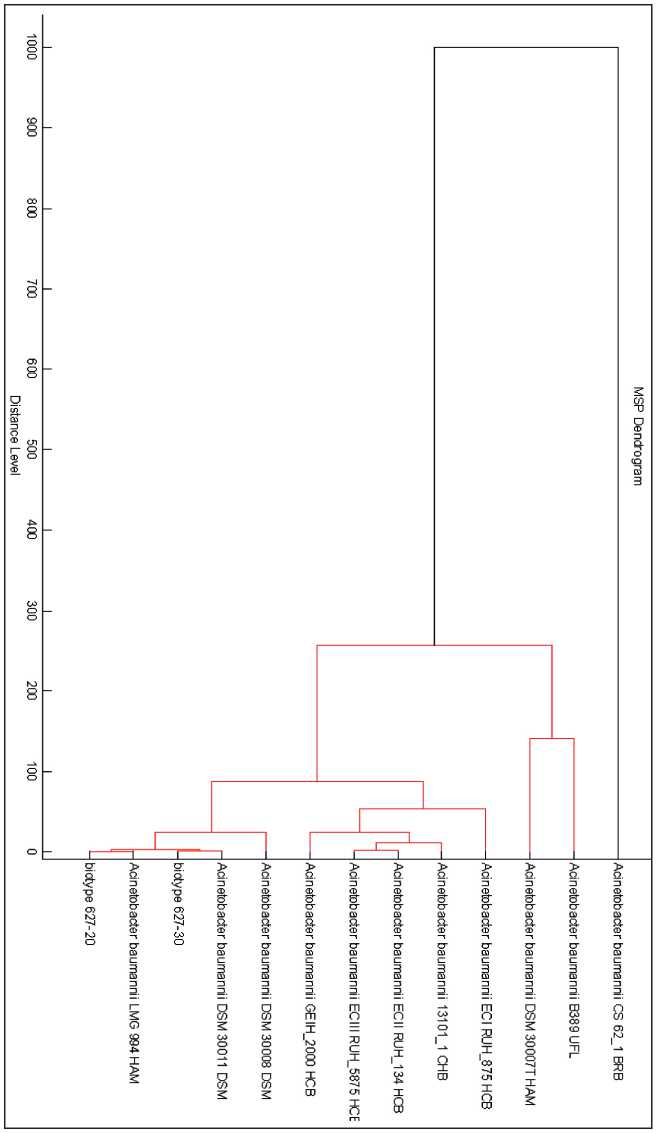
Рис. 1. Сопоставление биотипов MDR À. baumannii 00062730 и 00062720 с коллекционными штаммами À. bau-mannii в системе MALDI-TOF BIOTYPER
Список литературы Эпидемиология внутрибольничных инфекций в онкологическом стационаре, вызванных высокорезистентными (XDR) штаммами А. baumannii
- Григорьевская З.В., Дьякова. С.А. Формирование и распространение резистентных микроорганизмов в клиниках -всемирная проблема//Антимикробная терапия внутрибольничных инфекций/Под ред. Н.В. Дмитриевой, И.Н. Петуховой. М., 2014. 326 с
- Давыдов М.И., Дмитриева Н.В. Инфекции в онкологии. М., 2009. 472 с
- Ильина Е.Н. Создание интегрированной геномно-протеонной системы для типирования и изучения патогенов бактериальной и вирусной природы: Автореф. дис.... д-ра мед. наук. М., 2009. 264 с
- Antimicrobial resistance surveillance in Europe 2011. URL: http://www.ecdc.europa.eu (18.01.2016)
- Chan J.M., Halachev M.R., Loman N.J., Constantinidou C., Pal-len M.J. Defining bacterial species in the genomic era: insights from the genus Acinetobacter//BMC Microbiology. Vol. 12. P. 302 DOI: 10.1186/1471-2180-12-302
- Fishbain J., Peleg A.Y. Treatment of Acinetobacter infections//Clin. Infect. Dis. 2010. Vol. 51 (1). P. 79-84 DOI: 10.1086/653120
- Tak-chiu W.U. Carbapenem-resistant or Multidrug-resistant Acinetobacter baumannii -a Clinical’s perspective//The Hong Kong Medical Diary. 2011. Vol. 16 (4). P. 6-9
- Vila J., Pachon J. Therapeutic options for Acinetobacter baumannii infections//Expert Opin. Pharmacother. 2008. Vol. 9 (4). P. 587-599. Review DOI: 10.1517/14656566.9.4.587
- Григорьевская З.В. Актуальность проблемы госпитальных инфекций в онкологической клинике//Вестник РОНЦ им. Н.Н. Блохина РАМН. 2013. Т. 24, №. 3-4. С. 46-49
- Григорьевская З.В. Стратегия лечения нозокомиальных инфекций, вызванных резистентными микроорганизмами, в онкологической клинике: Дис.... д-ра мед. наук. М., 2015. 252 с
- Григорьевская З.В., Дьякова. С.А. Формирование и распространение резистентных микроорганизмов в клиниках -всемирная проблема//Антимикробная терапия внутрибольничных инфекций/Под ред. Н.В. Дмитриевой, И.Н. Петуховой. М., 2014. 326 с
- Давыдов М.И., Дмитриева Н.В. Инфекции в онкологии. М., 2009. 472 с
- Ильина Е.Н. Создание интегрированной геномно-протеонной системы для типирования и изучения патогенов бактериальной и вирусной природы: Автореф. дис.... д-ра мед. наук. М., 2009. 264 с
- Antimicrobial resistance surveillance in Europe 2011. URL: http://www.ecdc.europa.eu (18.01.2016)
- Chan J.M., Halachev M.R., Loman N.J., Constantinidou C., Pal-len M.J. Defining bacterial species in the genomic era: insights from the genus Acinetobacter//BMC Microbiology. Vol. 12. P. 302 DOI: 10.1186/1471-2180-12-302
- Fishbain J., Peleg A.Y. Treatment of Acinetobacter infections//Clin. Infect. Dis. 2010. Vol. 51 (1). P. 79-84 DOI: 10.1086/653120
- Tak-chiu W.U. Carbapenem-resistant or Multidrug-resistant Acinetobacter baumannii -a Clinical’s perspective//The Hong Kong Medical Diary. 2011. Vol. 16 (4). P. 6-9
- Vila J., Pachon J. Therapeutic options for Acinetobacter baumannii infections//Expert Opin. Pharmacother. 2008. Vol. 9 (4). P. 587-599. Review DOI: 10.1517/14656566.9.4.587
- Григорьевская З.В., Дьякова. С.А. Формирование и распространение резистентных микроорганизмов в клиниках -всемирная проблема//Антимикробная терапия внутрибольничных инфекций/Под ред. Н.В. Дмитриевой, И.Н. Петуховой. М., 2014. 326 с
- Давыдов М.И., Дмитриева Н.В. Инфекции в онкологии. М., 2009. 472 с
- Ильина Е.Н. Создание интегрированной геномно-протеонной системы для типирования и изучения патогенов бактериальной и вирусной природы: Автореф. дис.... д-ра мед. наук. М., 2009. 264 с
- Antimicrobial resistance surveillance in Europe 2011. URL: http://www.ecdc.europa.eu (18.01.2016)
- Chan J.M., Halachev M.R., Loman N.J., Constantinidou C., Pal-len M.J. Defining bacterial species in the genomic era: insights from the genus Acinetobacter//BMC Microbiology. Vol. 12. P. 302 DOI: 10.1186/1471-2180-12-302
- Fishbain J., Peleg A.Y. Treatment of Acinetobacter infections//Clin. Infect. Dis. 2010. Vol. 51 (1). P. 79-84 DOI: 10.1086/653120
- Tak-chiu W.U. Carbapenem-resistant or Multidrug-resistant Acinetobacter baumannii -a Clinical’s perspective//The Hong Kong Medical Diary. 2011. Vol. 16 (4). P. 6-9
- Vila J., Pachon J. Therapeutic options for Acinetobacter baumannii infections//Expert Opin. Pharmacother. 2008. Vol. 9 (4). P. 587-599. Review DOI: 10.1517/14656566.9.4.587


