Этапное хирургическое лечение больного гнойным стерномедиастинитом, осложненным тотальным остеомиелитом грудины
Автор: Левчук А.Л., Федык О.В., Катков А.А., Гудымович В.Г., Аблицов А.Ю., Белянин А.О., Миминошвили Л.Г., Мальсагова Д.Б.
Журнал: Вестник Национального медико-хирургического центра им. Н.И. Пирогова @vestnik-pirogov-center
Рубрика: Клинические наблюдения
Статья в выпуске: 1 т.21, 2026 года.
Бесплатный доступ
Частота инфекционных осложнений после стернотомии при кардиохирургических операциях составляет 4%, включая глубокое поражение с развитием переднего медиастинита и остеомиелита грудины. Наряду с проблемой профилактики этого грозного осложнения в кардиохирургии, актуальными вопросами остаются их ранняя диагностика и выбор хирургической тактики, которые определяются рядом факторов: тяжестью исходного состояния пациента, длительностью и объемом кардиохирургического оперативного пособия, сроками развития и распространенностью воспалительного процесса, а также диагностическими и лечебными возможностями медицинского стационара. Представленное клиническое наблюдение свидетельствует о том, что гнойный стерномедиастинит в распространенной форме (III тип по классификации Слесаренко С.С. (2005)) требует этапной хирургической тактики, включающей: активную хирургическую санацию раны с использованием технологии локального отрицательного давления, применение современных фармакологических средств местного (эпидермального фактора роста) и общего (целенаправленная антибиотикотерапия) воздействия, с последующим реконструктивно-восстановительным этапом (после купирования воспалительного процесса), – выполнение стабилизации грудины и замещением мягкотканного дефекта передней грудной стенки. Таким образом, этапный персонифицированный подход в лечении больного поздним гнойным стерномедиастинитом позволил добиться положительного результата с сохранением высокого уровня качества жизни пациента.
Глубокий гнойный стерномедиастинит, остеомиелит грудины, этапное хирургическое лечение
Короткий адрес: https://sciup.org/140314197
IDR: 140314197 | DOI: 10.25881/20728255_2026_21_1_155
Staged surgical treatment of purulent sternomediastinitis complicated by total osteomyelitis of the sternum
The incidence of infectious complications after sternotomy in cardiac surgery is 4%, including deep lesions with the development of anterior mediastinitis and osteomyelitis of the sternum. The solution to the problem of ensuring this formidable risk in cardiac surgery, current issues determine their early diagnosis and the choice of surgical tactics, which are developed by a number of factors: the severity of the patient’s initial condition, the duration and conclusion of cardiac surgery, the timing of development and prevalence of the inflammatory process, as well as the diagnostic and therapeutic capabilities of the medical hospital. The present clinical observation indicates that purulent sternomediastinitis in the form (type III according to the classification of Slesarenko S.S. (2005)) requires a staged surgical tactic, including: active surgical debridement of wounds using local negative pressure technologies, modern pharmacological agents of both (epidermal growth factor) and general (targeted antibiotic therapy) effects, followed by a reconstructive and restorative stage (after stopping the inflammatory process), performing restoration of the sternum and restoration of the soft tissue defect of the anterior chest wall. Thus, a staged personalized approach to visiting a patient with late purulent sternomediastinitis allows achieving a positive result while maintaining a high level of quality of life for the patient.
Текст научной статьи Этапное хирургическое лечение больного гнойным стерномедиастинитом, осложненным тотальным остеомиелитом грудины
Гнойно-септические осложнения со стороны передней грудной стенки после кардиохирургических оперативных вмешательств с трансстернальным доступом встречаются до 4% случаев [1]. Наиболее часто они проявляются нестабильностью остеосинтеза грудины, поверхностным инфицированием мягких тканей и глубокой стерномедиастинальной инфекцией [2]. Значимыми факторами риска в развитии стерномедиастинита считаются: ожирение, сахарный диабет, обструктивные заболевания легких, остеопороз грудины, наличие хронических очагов инфекции, технические погрешности интраоперационного остеосинтеза грудины, приводящие к его нестабильности [3]. Помимо гнойно-септического воспаления в клетчатке переднего средостения при стерномедиастините отмечается остеомиелитическое поражение грудины, а в ряде случаев и ребер с хондроперихондритом и остеоартрозом [4]. Объем гнойно-некротического пора- жения грудины и окружающих тканей по типу распространения, наличию возбудителя, клиническому течению и возникающим осложнениям принято классифицировать по Слесаренко С.С. (2005) [2; 3; 5]. Если ранние стерномедиастиниты, возникающие в ближайший месяц послеоперационного периода, протекают наиболее тяжело с превалированием обширного тотального нагноения раны с вовлечением в гнойный процесс клетчатки переднего средостения, то для поздних стерномедиастинитов характерно вялотекущее остеомиелитическое поражение грудины с ее нестабильностью и формированием гнойных лигатурных свищей в области послеоперационного рубца [5; 6]. Общепринятый комплекс диагностических инструментальных исследований, включающий: УЗИ мягких тканей грудной клетки и сердца, КТ грудины и плевральных полостей, фи-стулографию,- не всегда дает возможность достоверно определить масштаб зоны поражения гнойно-некротическим процессом. Только тщательная интраоперационная ревизия тканей позволяет наиболее точно оценить весь объем поражения и правильно выбрать этапность хирургического лечения у пациентов с этим осложнением.
В основе адекватного хирургического лечения стерномедиастинита лежит радикальная хирургическая обработка гнойно-некротического очага поражения мягких тканей грудной клетки и костных структур с полным иссечением всех участков нежизнеспособной подкожной медиастинальной клетчатки переднего средостения, очагов остеомиелита грудины и хрящей реберно-грудинных сочленений. При нестабильности ме-таллоостеосинтеза грудины необходимо обязательное удаление инфицированных проволочных швов с биопленками возбудителя, с адекватным дренированием операционной раны и контролем воспаления (бактериальное исследование на идентификацию возбудителя и маркеров воспаления) [6; 7].

При I и II типах гнойных стерноме-диастинитов (с мягкотканными некрозом, но без поражения грудины) обычно достаточно проведения адекватного хирургического лечения с открытым ведением раны или вакуум-терапией и использованием современных антисептиков (пронтосан) и препаратов серебра с эпидермальным фактором роста (мазь «Эбермин», крем «Велстик-PRO») [4; 8]. При распространенных формах гнойного послеоперационного стерномеди-астинита III типа (A, B, C) нами применяется тактика этапного хирургического лечения, которая подразделяется на: 1) санационный этап хирургической обработки (не исключается его повторное применение); 2) дренирующий этап с использованием вакуум-систем и повязок; 3) реконструктивно-восстановительный этап (после окончательного очищения раны и разрешения гнойно-воспалительного процесса) с использованием стабилизирующей кабельной системы (хомутов из PEEK (ZipFix) – США) для фиксации рукоятки и тела рассеченной грудины с целью устранения ее нестабильности. Кабель, как и хомуты имеют преимущество в большей площади контакта с костью (меньшая площадь прорезывания) и демонстрируют большую прочность при сопоставлении костных краев грудины, особенно после хирургической их адаптационной резекции по поводу остеомиелита [8; 9]. Пара-стернально установленные кабельные системы (ZipFix) надежно стабилизируют фрагментированные участки рукоятки и тела грудины, обладая высокой степенью биосовместимости, сочетающейся с их бактерицидными свойствами и простотой в технической эксплуатации при установке во время оперативного вмешательства [8; 9].
Пациент Х., 70 лет, с диагнозом нестабильной стенокардии и многососудистым поражением коронарного русла, был прооперирован в срочном порядке в Клинике грудной и сердечно-сосудистой хирургии имени Св. Георгия ФГБУ «НМХЦ им. Н.И. Пирогова» Минздрава России. Выполнено коронарное шунтирование (КШ) с аутовенозным шунтированием задней межжелудочковой ветви (ЗМЖВ) и ветви тупого края (ВТК), а также аутоартериальное шунтирование передней межжелудочковой ветви (ПМЖВ) левой внутренней грудной артерией (ЛВГА) на работающем сердце. В послеоперационном периоде на 2-е сутки отмечено осложнение в виде фибрилляции предсердий, а также выраженный кашель,
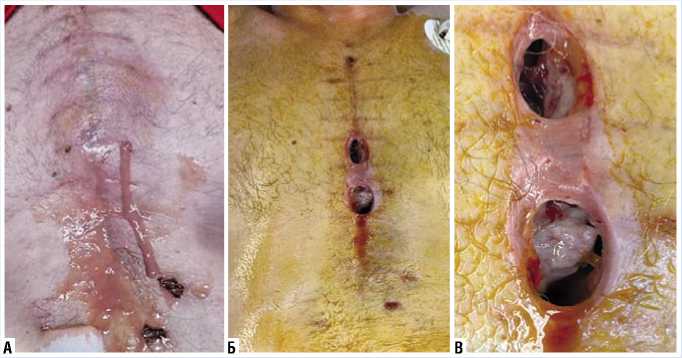
Рис. 1. Свищевая форма позднего послеоперационного гнойно-некротического стерномедиастинита.
что могло быть связано с длительным стажем курения (более 35 лет по 1 пачке в день). На 4-е сутки зафиксирован подъем температуры до 39 °C при уровне лейкоцитов 7,2х10 9 /л и значительном повышении С-реактивного белка (СРБ) до 134,7 мг/л. Проведенная на 5-е сутки КТ органов грудной полости выявила левосторонний малый гидроторакс и послеоперационные изменения клетчатки переднего средостения. Микробиологическое исследование бронхоальвеолярного лаважа показало наличие Lactobacillus salivarius (105 КОЕ/мл), Streptococcus mi-tis/oralis (106 КОЕ/мл) и Klebsiella oxytoca (103 КОЕ/мл). Посев крови подтвердил бактериемию, вызванную Staphylococcus aureus, в связи с чем была назначена антибактериальная терапия по рекомендации клинического фармаколога. К 6-м суткам состояние ухудшилось: отмечалось промокание послеоперационной повязки в средней и нижней трети, нагноение раны с расхождением краёв до 7 см, а посев раневого отделяемого вновь выявил Staphylococcus aureus (106 КОЕ/мл) на фоне роста уровня СРБ до 341 мг/л. На 8-е сутки, учитывая данные КТ-ОГК, подтверждающие несостоятельность швов грудины и остеомиелит, выполнено ревизионное вмешательство: краевая резекция грудины, санация переднего средостения с установкой дренажно-промывной системы и реостеосинтез с помощью металлической лигатуры и лески. Интраоперационно обнаружен диастаз краёв грудины и скопление серозного экссудата, в котором бактериологическое исследование подтвердило персистирующую инфекцию Staphylococcus aureus.
На 4-е сутки после повторной операции удалена дренажно-промывная система. На 5-е сутки отмечено про- мокание операционной раны в нижней трети. Края операционной раны разведены, установлена вакуумная система (VAC-системы). Вакуумную терапию проводили в течение 8 суток. Выполнено три смены VAC-повязок. На фоне комплексной терапии достигнута положительная динамика: нормализовались маркеры воспаления (лейкоциты - 5,3х109/л, СРБ – 60 мг/л), а бактериологические посевы раневого отделяемого стали отрицательными. На 14-е сутки наложены вторичные кожные швы в нижней трети раны, и на 20-е сутки пациент был выписан в удовлетворительном состоянии под наблюдение хирурга по месту жительства.
Через месяц пациент поступил в тяжелом септическом состоянии с жалобами на боли в грудине, слабость и наличие отделяемого в области послеоперационной раны (Рис. 1 А).
На КТ-ОГК отмечался диастаз краев грудины до 12 мм, края грудины местами нечеткие с признаками узурации, между краев грудины скопление воздуха (Рис. 2).
Диагностирован: поздний гнойный стерномедиастенит, свищевая форма, осложненный остеомиелитом грудины (III В тип). Проведено оперативное вмешательство.
На уровне средней трети грудины визуализируются два свищевых хода, дно раны представлено фрагментами грудины (Рис. 1 Б, В). Произведено иссечение некротизированных тканей кожи и подкожной-жировой клетчатки. При ревизии отмечается диастаз грудины и прорезывание стальных лигатур и лески на всем протяжении, сопровождающийся гнойным расплавлением в зоне проволочных швов и распространением

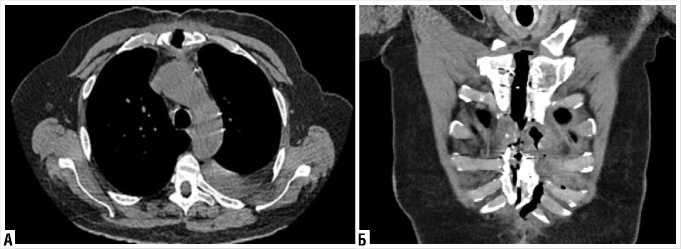
Рис. 2. КТ-грудины, средостения и плевральных полостей. Несостоятельность проволочного первичного остеосинтеза, признаки тотального остеомиелита тела и рукоятки грудины.
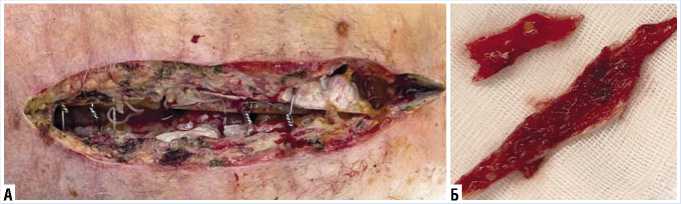
Рис. 3. Этап вторичной хирургической обработки гнойной полости переднего средостения и удаления костных секвестров грудины с проволочными лигатурами (I фаза течения раневого процесса).
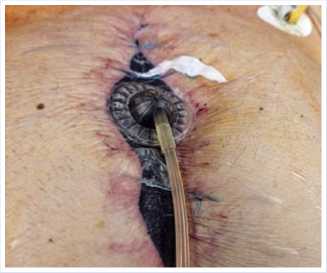
Рис. 4. Вакуум-терапия раны переднего средостения и диастаза краев грудины после секвестрэктомии.
гнойного экссудата в переднее средостение (Рис. 3 А).
Леска и стальные лигатуры удалены. Грудина фрагментирована и частично лизирована, выполнена радикальная остеонекрэктомия (Рис. 3 Б). Проведена санация с многократной обработкой 3% раствором перекиси водорода и последующим промыванием подогретым 0,9% изотоническим раствором натри-яхлорида с добавлением 0,5% раствора диоксидина. Учитывая распространенность гнойного-некротического процесса с удалением большей части грудины с частичным сохранением рукоятки, решено осуществлять открытое ведение
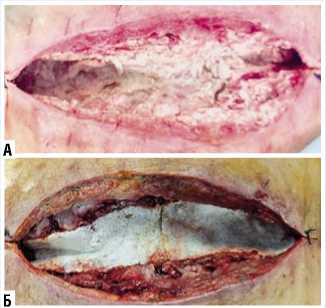
Рис. 5. Использование препаратов эпидермального фактора роста после снятия вакуум-терапии во II фазе течения раневого процесса (10-ые сутки послеоперационного периода).
раны с использованием VAC-системы (Рис. 4). Результат бактериального посева подтвердил наличие Staphylococcus aureus, возобновлена антибактериальная терапия.
Вакуумную терапию проводили в течение 14 суток. Выполнено четыре смены VAC-системы с санацией переднего средостения и местным применением эпидермального фактора роста (мазь «Эбермин», крем «Велстик-PRO») (Рис. 5 А, Б).
С появлением грануляций в ране и отрицательных бактериологических по-
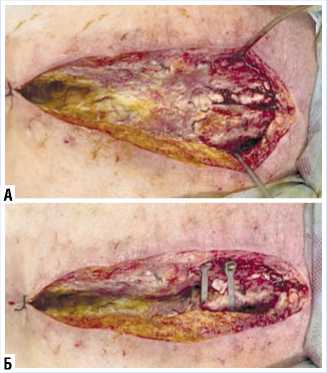
Рис. 6. Вторичная хирургическая обработка раны грудной клетки с наложением вторичного остеосинтеза рукоятки грудины методикой фиксации кабельными стежками (ZipFix).
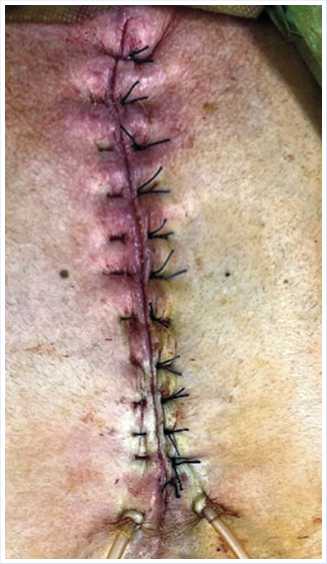
Рис. 7. Вид послеоперационной раны с вторичными швами (15-е сутки после ПХО).
севов, была выполнена ее вторичная хирургическая обработка (Рис. 6 А), остеосинтез жизнеспособной части рукоятки грудины с помощью двух стяжек «ZipFix» (Рис. 6 Б), установлена дренажная система, рана ушита узловыми швами по Донати (Рис. 7).
После удаления дренажей в послеоперационном периоде отмечалась экс-удация серозного отделяемого из отвер-
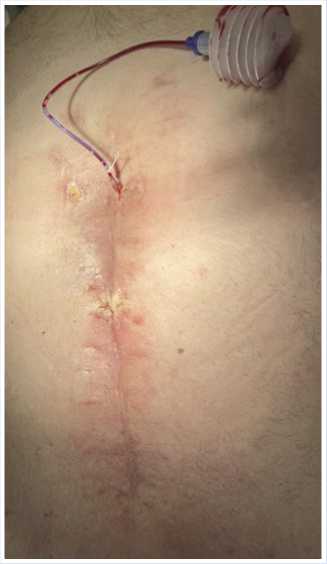
Рис. 8. Заживление раны вторичным натяжением с использованием активного дренажа Редона.
стия в нижней трети раны. На 14-е сутки после закрытия раны отменена антибактериальная терапия, в анализе крови лейкоциты 5,5х10 9 /л, СРБ - 10 мг/л. Заживление раны на вторичных швах (Рис. 7). На 24-е сутки выявлен отек и гиперемия кожи, флюктуация в верхней трети грудины. Выполнено вскрытие очага, эвакуация гнойного содержимого с промыванием полости раствором перекиси водорода и дренированием по Редону (Рис. 8). Результат бактериального посева подтвердил наличие Staphylococcus aureus, произведена замена антибактериальной терапии.
В дальнейшем после полного купирования гнойного процесса применялась мазь «Эбермин» до полного вторичного заживления раны (Рис. 9).
На контрольной КТ грудной клетки отмечено полное сопоставление рукоятки грудины, отсутствие признаков воспалительного процесса и скопления экссудата (Рис. 10 А, Б).
В течение всего послеоперационного периода пациент использовал стабилизирующий грудной бандаж с валикообразным пилотом (Рис. 11).
На 64-е сутки пациент был выписан из стационара. Качество жизни его значимо улучшилось на фоне проведённого лечения с увеличением физической
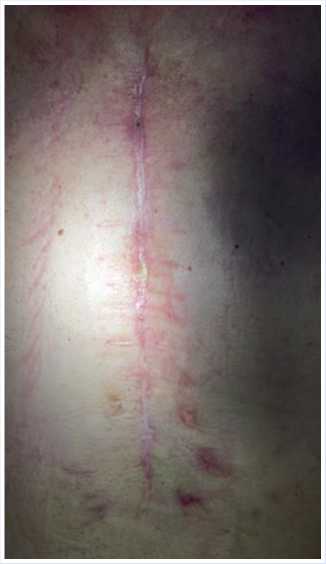
Рис. 9. Окончательный рубец операционной раны без признаков воспаления.
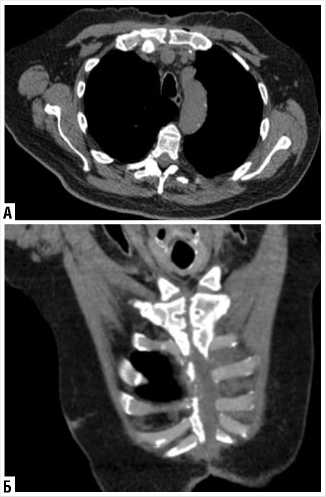
Рис. 10. Контрольное КТ грудной клетки после затягивания стернотомной раны после реконструктивно-восстановительной операции.
активности (подьем до 3-го этажа), что свидетельствует о правильности и эффективности выбранного этапного хирургического метода лечения.
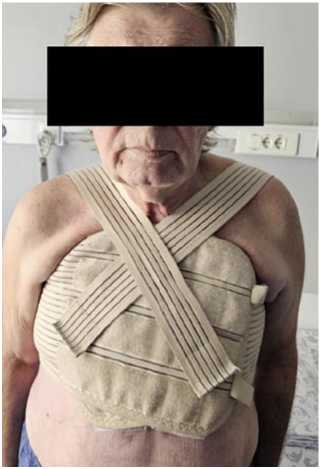
Рис. 11. Применение послеоперационного бандажа на грудную клетку у пациента после вторичного остеосинтеза грудины.
Таким образом, все раневые процессы, независимо от этиологии, подчиняются единым биологическим закономерностям регенерации. Это диктует необходимость применения общих принципов лечения с дифференцированным и этапным подходом, основанным на фазе раневого процесса и его особенностях. Ключевыми задачами являются: эрадикация патогенной микрофлоры, купирование воспаления и восстановление тканевой целостности. Оптимальные результаты достигаются при своевременном патогенетически обоснованном воздействии на каждом этапе лечения.
Заключение
Использование принципов этап-ности оказания специализированной хирургической помощи при развитии глубокого гнойно-некротического стер-номедиастинита после кардиохирургических оперативных вмешательств, применение вакуум-терапии в сочетании с препаратами эпидермального фактора роста и апробацией современных стабилизирующих систем (ZipFix), с целью подавления воспалительного процесса и устранения нестабильности грудины, – с высокой долей вероятности могут привести к снижению уровня летальности у этого тяжелого контингента больных.


