Эволюция протезирования митрального клапана
Автор: Елисеев И.Г., Лищук А.Н., Хавандеев М.Л., Музычин А.Л., Комендантова Ю.В., Гительзон Е.А., Файбушевич А.Г.
Журнал: Вестник Национального медико-хирургического центра им. Н.И. Пирогова @vestnik-pirogov-center
Рубрика: Обзоры литературы
Статья в выпуске: 3 т.19, 2024 года.
Бесплатный доступ
Работа освещает эволюцию протезирования митрального клапана, начиная с первых разработок до современных инновационных технологий. Рассматривается история развития методов протезирования как в России, так и в мире, их эффективность, преимущества и недостатки, а также последние разработки в области практики и технологий протезирования митрального клапана. В статье также предоставляется обзор результатов клинических исследований, проведенных с использованием различных типов протезов, и их влияние на выживаемость и качество жизни пациентов. Анализируются проблемы, с которыми сталкиваются врачи и исследователи в данной области, обсуждаются перспективы развития протезирования митрального клапана
Кардиология, хирургические техники, митральный клапан, протезирование, биопротезы
Короткий адрес: https://sciup.org/140307867
IDR: 140307867 | DOI: 10.25881/20728255_2024_19_3_118
Evolution of mitral valve replacement
The paper highlights the evolution of mitral valve prosthetics, from the first developments to modern innovative technologies. The history of development of prosthetic methods both in Russia and in the world, their effectiveness, advantages and disadvantages, as well as the latest developments in the practice and technology of mitral valve prosthesis are considered. The article also provides an overview of the results of clinical trials conducted using different types of prostheses and their impact on survival and quality of life of patients. The problems faced by physicians and researchers in this field are analyzed, and the prospects for the development of mitral valve prosthetics are discussed
Текст обзорной статьи Эволюция протезирования митрального клапана
Пороки клапанов сердца занимают второе место по распространенности после ИБС и гипертонической болезни. Среди всех органических заболеваний сердца доля пороков клапанов составляет 25%, причем на долю поражения митрального клапана (МК) приходится две трети от всех приобретенных пороков сердца [1; 2].
Эволюция хирургических методов лечения патологии МК насчитывает более века и берет свое начало от ранних отчетов британских кардиологов в начале XX столетия, а также частных хирургических наблюдений в 20-х гг. прошлого века. Многочисленные экспериментальные исследования в те годы, а также после Второй мировой войны способствовали широкому практическому внедрению закрытой митральной комиссуротомии (ЗМКТ), что стало первым успешным методом лечения митрального стеноза. Дальнейшее развитие хирургии МК было связано с использованием различных видов протезов и биопротезов клапанов, и в конечном итоге привело к значительному увеличению успешных операций по восстановлению клапана с использованием аннулопластики [3]. История кардиохирургии продемонстрировала значительные успехи в развитии методов лечения пороков клапанов сердца. Вне- дрение в клиническую практику метода протезирования клапанов открыло новые перспективы в лечении больных тяжелыми пороками клапанов сердца. Благодаря постоянным исследованиям и научным открытиям, хирургические методы становятся все более эффективными.
Прогресс митрального протезирования. Первое упоминание о хирургическом лечении митрального стеноза было сделано Т.Л. Брунтоном в 1902 г. Он предположил, что митральный стеноз в его тяжелейшей форме не поддается консервативному лечению, но если бы удалось разработать механический или хирургический метод улучшения работы сердца путем открытия клапана, то теоретически это было бы весьма эффективно. Врачи Лондона того времени критически отнеслись к его идеям, однако эти дискуссии послужили стимулом для проведения экспериментальных исследований митрального стеноза. В период с 1907 по 1914 гг. Кушинг [4], Бернгейм [5], Джегер [6], Таффье и Каррель [7] разработали экспериментальные модели для изучения митрального стеноза.
В 1923 г. была проведена первая успешная операция по поводу митрального стеноза на 11-летней пациентке. Э.К. Катлер выполнил восстановление МК у девушки, которая находилась в коме из-за ревматического стеноза

– девушка страдала сердечной недостаточностью с низким выбросом. Через срединную стернотомию в верхушку сердца был введен нейрохирургический тенотомический нож и проведена двусторонняя ЗМКТ. Пациентка пришла в себя, хорошо себя чувствовала после операции и была выписана из больницы через 14 дней [8]. Впоследствии Катлером было разработано устройство для лечения митрального стеноза, но оно приводило к тяжелой митральной регургитации. После Второй мировой войны Д.Э. Харкен проводил ЗМКТ пациентам со стенозом МК. В 1964 г. были представлены результаты исследований, проведенных на большом количестве пациентов (более полутора тысяч), которые прошли ЗМКТ, а также подчеркнута необходимость совместных усилий кардиохирургов, кардиологов и кардиоанестезиологов для эффективного лечения патологий митрального клапана [9].
Создание первых протезов было основано на повторении структуры естественных клапанов сердца. Были разработаны искусственные клапаны, имитирующие лепестковую форму, с использованием синтетических материалов. Эти клапаны функционировали, работая на двойной изгиб, по аналогии с естественными клапанами. Первое успешное протезирование аортального клапана с использованием данного типа протезов было выполнено C. Lillehei в 1958 г. [10]. Однако, протезы, созданные из синтетических материалов, оказались недолговечными, разрушаясь при нагрузках, соответствующих 1–6 годам эксплуатации. В связи с этим было необходимо искать альтернативные варианты клапанных систем, и одним из таких вариантов стал клапан вентильного типа с запирательным элементом в виде шарика [11; 12].
С появлением первого успешного сердечно-легочного шунтирования [13] был разработан набор процедур, которые можно было применять не только при митральном стенозе, но и при митральной регургитации – поражении, требующим более сложного лечения, чем митральный стеноз. К расширению использования реконструкции МК при митральной регургитации привели несколько факторов: результаты биопротезирования и протезирования клапанов, которые, хотя и были достаточно эффективными, в долгосрочной перспективе ухудшались; благоприятные долгосрочные данные, подтверждающие реконструктивные методики; улучшение степени протекции миокарда; признание важности взаимодействия папиллярной мышцы с хордой [14].
Первые операции по восстановлению функции клапана не дали желаемых результатов, и большинство хирургов считали, что лечение митральной регургитации требует замены клапана. В 1960 г. был имплантирован первый искусственный МК [15]. Он представлял собой прототип клапана с полиуретановыми лепестками и тканевой хордой, и был доступен небольшому числу пациентов. Первым доступным коммерческим протезом митрального клапана с физиологической гемодинамикой стал клапан Старра-Эдвардса [16]. Это был шариковый протез вентильного типа. Разработанный Старром и
Эдвардсом в 1960 г., этот протез стал стандартом митрального протезирования, но в настоящее время его использование ограничено.
Важным событием в развитии протезирования МК стала разработка биологического свиного клапана на каркасе, покрытом тефлоном, Карпентье и коллегами [17]. Однако было отмечено, что такие митральные протезы, которые не были обработаны глутаральдегидом, в течение 10 лет кальциницируются и теряют функциональность. Был проведен ряд исследований, чтобы понять патофизиологию этого дегенеративного процесса. Такое явление чаще наблюдалось при биопротезировании МК у молодых пациентов и приводило к увеличению риска повторных операций [18]. Впоследствии было доказано, что эта дисфункция ассоциирована с возрастом [19]. Также было показано [20], что определенные кальций-стимулирующие процедуры, в частности, гемодиализ, могут преждевременно повлиять на дисфункцию клапана.
В клинической практике существует множество протезов для замены клапанов сердца, включая механические и биологические. При выборе протеза учитываются его технические характеристики и данные о гемодинамике [21–23]. Механические протезы применяются в случаях структурной дисфункции, но испытывают постоянную необходимость в приеме антикоагулянтов, что увеличивает риск тромбоэмболических осложнений и кровотечений. Соединительнотканный паннус может нарушить функцию протеза и потребовать повторной коррекции. Биологические протезы также подвержены структурной дегенерации и могут потребовать замены [24]. Из-за осложнений, связанных с механическими и биологическими протезами, продолжаются исследования в области разработки более долговечных протезов. Уровень смертности при замене МК зависит от возраста, состояния клапанной кардиомиопатии и сопутствующих заболеваний пациента и находится в диапазоне 4–7%. Использование инвазивных методов замены клапана обычно связано с более низким уровнем летальности. Однако, на данный момент не существует надежных доказательств различия в десятилетней выживаемости между механическими и биологическими протезами у пациентов с аналогичными характеристиками.
На настоящее время существует четыре актуальные системы для миниинвазивной замены МК, включая Card-iAQ второго поколения. Первоначальная система CardiAQ была разработана А. Квадри для трансапикального и транссептального (ТС) проведения. Устройство состоит из саморасширяющегося нитинолового каркаса, трех створок из бычьей ткани, манжеты и ленты из полиэфирной ткани и креплений, покрытых полиуретановой пеной. Отточная часть устройства имеет коническую форму для предотвращения обструкции отточного тракта левого желудочка. Симметричная трехстворчатая конструкция не требует ротационного выравнивания при установке. Позиционирование является внутрианнулярным и супра-аннулярным. Размеры каркаса соответствуют размерам нативного митрального кольца от 36 до 39,5 мм. Фиксация

осуществляется с помощью покрытых пеной левожелудочковых креплений, предназначенных для фиксации и сохранения субвальвулярного аппарата. Современные направления в области реконструктивных и заместительных процедур на МК сердца сфокусированы на применении миниинвазивных методов. Это во многом обусловлено прогрессом в материаловедении и использованием роботизированных технологий, что способствует разработке современных инновационных подходов к хирургическому лечению пациентов с поражениями МК [25].
Существует несколько типов механических клапанов, включая шаровые (Старра-Эдвардса), дисковые (Бьорка-Шайли), двустворчатые (St. Jude Medical). Каждый из них имеет свои преимущества и недостатки. Механические протезы обладают более длительным сроком службы, но требуют постоянного приема антикоагулянтов из-за риска тромбообразования. Однако все протезы, включая механические, могут вызывать стеноз, особенно при малых размерах и интенсивном кровотоке. Низкопрофильные двустворчатые протезы, например, St. Jude Medical, обладают оптимальными гемодинамическими характеристиками, особенно при малых размерах, по сравнению с протезами Старра-Эдвардса. Среди механических протезов, клапан St. Jude Medical является наименее тромбогенным, особенно в митральном положении [26–28].
Доступы к МК. Виды, техники, преимущества и недостатки. Срединная стернотомия. Повторные операции на сердце традиционно выполняются через повторную срединную стернотомию. Однако, повторная операция на МК, выполняемая через срединную стернотомию, может быть особенно технически сложна и сопряжена со значительным риском травмы трансплантатов коронарных артерий и сосудистых структур, которые лежат непосредственно субстернально и могут прилегать к грудине [29]. Несмотря на развитие миниинвазивных техник, продольная срединная стернотомия по-прежнему остается самым распространенным хирургическим доступом для проведения операций. Это обусловлено высокой экспозицией и визуализацией органов переднего средостения и сердца, а также меньшей интенсивностью болевого синдрома (по сравнению с аналогичными доступами), а также простотой и скоростью его выполнения [30].
Вертикальная левая атриотомия. Традиционно во многих кардиологических центрах мира идеальной точкой доступа является подход к левому предсердию (ЛП) через борозду Сунергарда. Этот доступ – хорошо изученная, относительно простая процедура, которая обычно позволяет отлично визуализировать МК. Однако в некоторых случаях, когда доступ к ЛП затруднен, используется ТС подход. Это предполагает более длинный разрез, проходящий через межпредсердную перегородку и затрагивающий также ЛП, и считается, что он обеспечивает лучшую экспозицию клапана, как при ограниченном, так и при расширенном ТС подходе. В некоторых исследованиях сообщалось о неоднозначных результатах обоих подходов, в то время как в других отмечалось увеличение времени сердечно-легоч- ного шунтирования и, вероятно, предрасположенности к аритмогенности и, следовательно, более высокой частоте использования постоянного кардиостимулятора [31].
Правосторонняя мини-торакотомия. В середине 90-х гг. Carpentier была выполнена первая операция на МК с использованием правосторонней мини-торакотомии [32]. В 2013 г. И.О. Чернов с коллегами описали первый успешный опыт 114 операций через миниин-вазивный доступ [33]. Позднее Ю.Л. Шевченко широко внедрил правостороннюю торакотомию для коррекции митральных пороков сердца, а также многоклапанных пороков [34]. В России количество операций на МК, проводимых через миниинвазивный доступ, ограничено и осуществляется в единичных случаях, главным образом, в специализированных кардиохирургических центрах. В крупных же центрах США и Европы данная техника является рутинной практикой [35].
Предоперационное обследование пациентов, рассматриваемых для проведения операции на МК через минидоступ, должно быть тщательно спланированным, в дополнение к стандартному обследованию пациентов, которым проводится операция на МК (ЭхоКГ для определения механизма патологии клапана и доступа для других поражений клапана, оценка коронарных артерий, каротидный дуплекс и тестирование функции легких, если необходимо).
При любых кардиохирургических операциях небольшие изменения в позиционировании и подготовке пациента могут стать разницей между успехом и проблемой при использовании малоинвазивных методик. Пациент располагается в положении лежа на операционном столе в точке, позволяющей оператору удобно встать справа от операционного стола на уровне правого плеча. Обычно эта точка находится дальше к изножью кровати, чем при позиционировании для стернотомии, что позволяет работать двум операторам (хирургу и ассистенту).
Операция через правостороннюю мини-торакотомию имеет свои особенности. Интубация проводится однопросветной трубкой, установка ультразвукового датчика осуществляется в пищевод. Пациента укладывают на операционном столе с осевой ротацией туловища влево на 30°, правую верхнюю конечность отводят вправо или располагают вдоль туловища. После аппликации адгезивных электродов для дефибрилляции проводят обработку операционного поля антисептиками и покрывают его стерильным бельем. Мини-торакотомию длиной около 7 см выполняют в четвертом межреберье справа, оценивают состояние плевральной полости, при необходимости выполняют пневмолиз. После установки силиконового протектора для мягких тканей выполняют перикардиотомию, отводят листки перикарда при помощи швов-держалок.
В правой паховой области осуществляют доступ к общей бедренной артерии и вене под ультразвуковым контролем по методике Сельдингера. Канюлю вводят сначала в верхнюю полую вену, затем в общую бедренную артерию для начала нормотермического ишемического контроля

с вакуумной поддержкой. Устанавливают троакар диаметром 5 мм в переднеподмышечной линии справа в третьем межреберье, через который проводят видеокамеру и ин-суффлируют углекислый газ. Кардиоплегическую канюлю устанавливают в корень аорты, а аортальный зажим Читвуда проводят через прокол в четвертом межреберье справа по среднеподмышечной линии.
После пережатия аорты и консервации сердца Ку-стодиолом, вскрывают ЛП и устанавливают дренаж. Для доступа к сердцу вводят ретрактор через парастернальный прокол. Затем определяют объем хирургического вмешательства и начинают операцию.
Доступ к МК осуществляется через разрез в межпредсердной борозде. Разрушенные хорды были заменяются на неохорды с помощью петлевой техники с использованием швов Gore-Tex. Для стабилизации восстановленного клапана проводится аннулопластика. В случаях дегенерации МК его заменяют путем резекции передней створки, включая соответствующую хорду. Клапан иссекается на 2–4 мм от кольцевого пространства. Задняя створка, включая соответствующие хорды, сохраняется для поддержания аннуло-папиллярной непрерывности и предотвращения ухудшения функции левого желудочка. После операции ушивают ЛП и проводят деаэрацию сердца. Также устанавливают электрод временной электрокардиостимуляции к миокарду правого желудочка. После восстановления сердечного ритма операцию завершают и удаляют дренажи и канюли. Плевральную полость дренируют через отверстие в месте установки видеокамеры. Все раны закрывают [36].
Трансэзофагеальная ЭхоКГ (ТЭЭ) проводится пациентам перед отсоединением от сердечно-легочного шунтирования для оценки функции МК /- MR/- параваль-вулярной утечки и оценки наличия воздуха. Отключение проводится через вентиляционный катетер, установленный в восходящей аорте, под контролем ТЭЭ.
Схемы описанных доступов представлены на рис. 1.
В ходе традиционного подхода хирургии МК специалист осуществляет доступ к клапану путем проведения стернотомии, что подразумевает необходимость рассечения грудной клетки. При использовании методов миниинвазивной хирургии, в частности мини-торакотомии, можно значительно сократить объем операции по отношению к доступу к операционному полю.
Заключение
Хотя медианная стернотомия остается наиболее распространенным доступом к сердцу, альтернативные методы, такие как мини-торакотомия, становятся все более распространенными. По сравнению со стандартной срединной стернотомией, правосторонняя мини-торакотомия предлагает ряд преимуществ, включая уменьшение хирургической травмы, сохранение функциональности грудной клетки, снижение послеоперационного болевого синдрома, более быстрое восстановление после операции, уменьшение риска инфекционных осложнений и опти-
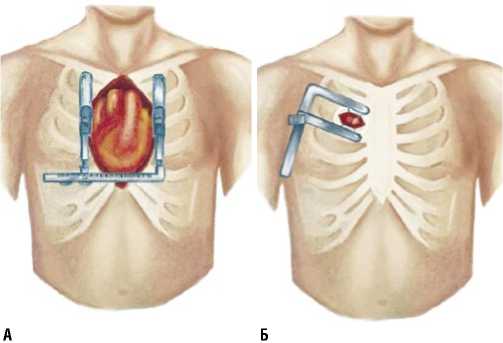
Рис. 1. Хирургические доступы. А – традиционный метод – стернотомия; Б – миниинвазивный метод – мини-торакотомия.
мальный эстетический внешний вид прооперированной области. Однако следует отметить некоторые недостатки, такие как увеличение продолжительности операции, возможные осложнения в виде ишемии и инфаркта миокарда [37]. Кроме того, отмечается возможный риск травмирования диафрагмального нерва при перикар-диотомии, повреждение бедренных сосудов во время канюляции, ограничение визуализации МК, сложность оценки сократимости и выполнения деаэрации сердца, невозможность проведения контактной дефибрилляции и прямого массажа сердца [38].
Миниинвазивная хирургия сердца получила международное признание, начиная с середины 90-х гг. ХХ в. Она стала альтернативой традиционному методу, который включает стернотомию, и зарекомендовала себя благодаря способности существенно снизить риск осложнений и смертности в периоперационный период. Миниинвазивная хирургия стала значительным прорывом в кардиохирургии и позволила проводить операции на сердце с меньшим риском для пациента. Она позволяет снизить время проведения операции, сократить больничные и реабилитационные периоды, а также ускорить восстановление пациента.
Список литературы Эволюция протезирования митрального клапана
- Бокерия Л.А. и др. Национальные рекомендации по ведению, диагностике и лечению клапанных пороков сердца. Рабочая группа по разработке рекомендаций. – М.: Изд-во им. А.Н. Бакулева РАМН, 2009. – 356 с.
- Урманбетов К.С. и др. История развития хирургического лечения митрального порока сердца (обзор литературы) // Вестник Кыргызской государственной медицинской академии имени И.К. Ахунбаева. – 2022. – №3. – С.10-17.
- Cohn LH, Edward GS. The evolution of mitral valve surgery: 1902–2002. American Heart Hospital Journal. 2003; 1(1): 40-46. doi: 10.1111/ j.1541-9215.2003.02081.x.
- Cushing H, Branch B. Experimental and clinical notes on chronic valvular lesions in the dog and their possible relation to a future surgery of the cardiac valves. The Journal of Medical Research. 1908; 17(4): 471.
- Bernheim BM. Experimental surgery of the mitral valve. Bull. Johns Hopkins Hosp. 1909; 20: 107-110.
- Jeger E. Die Chirurgie der Blutgetasse und des Herzens. Berlin, Germany: August Hirschwald, 1913.
- Carrel A, Th T. Etude anatomopathologique et experimentale sur la chirurgie des orifices du coeur. Presse méd. 1914; 22: 173-177.
- Cutler EC, Samuel AL. Cardiotomy and valvulotomy for mitral stenosis; experimental observations and clinical notes concerning an operated case with recovery. The Boston Medical and Surgical Journal. 1923; 188.26: 1023-1027. doi: 10.1056/NEJM192306281882601.
- Ellis LB, Dwight E. Closed valvuloplasty for mitral stenosis: a twelve-year follow-up study of 1571 patients. New England Journal of Medicine. 1964; 270.13: 643-650. doi: 10.1056/NEJM196403262701301.
- Lillehei CW, et al. The surgical treatment of stenotic or regurgitant lesions of the mitral and aortic valves by direct vision utilizing a pump-oxygenator. Journal of Thoracic Surgery. 1958; 35.2: 154-191. doi: 10.1016/S0096-5588(20)30271-3.
- Шевченко Ю.Л., Цветкова Т.В., Гудымович В.Г., Василашко В.И. Отдаленный результат протезирования митрального и аортального клапанов сердца отечественными шаровыми протезами через 35 лет после операции (клиническое наблюдение с кратким обзором литературы) // Вестник Национального медико-хирургического Центра им. Н.И. Пирогова. – 2020. – Т.15. – №3-2. – С.172-178. doi: 10.25881/BPNMSC.2020.46.81.030.
- Искусственные клапаны сердца / Под ред. Ю.Л. Шевченко. – СПб.: ОЛМА Медиа Групп», 2007. – 448 с.
- Gibbon Jr, John H. Application of a mechanical heart and lung apparatus to cardiac surgery. Minn Med. 1954; 37.3: 171-180.
- Cohn LH, Edward GS. The evolution of mitral valve surgery: 1902–2002. American Heart Hospital Journal. 2003; 1.1: 40-46. doi: 10.1111/ j.1541-9215.2003.02081.x.
- Westaby S, Cecil B. Landmarks in cardiac surgery. 1997. (No Title).
- Starr A, Lowell E. Mitral replacement: clinical experience with a ball-valve prosthesis. Annals of surgery. 1961; 154.4: 726. doi: 10.1097/00000658-196110000-00017.
- Carpentier A, et al. Biological factors affecting long-term results of valvular heterografts. J Thorac Cardiovasc Surg. 1969; 58.4: 467-83.
- Cohn LH, et al. Fifteen-year experience with 1678 Hancock porcine bioprosthetic heart valve replacements. Annals of Surgery. 1989; 210.4: 435. doi: 10.1097/00000658-198910000-00003.
- Jones EL, et al. Ten-year experience with the porcine bioprosthetic valve: interrelationship of valve survival and patient survival in 1,050 valve replacements. The Annals of thoracic surgery. 1990; 49.3: 370-384. doi: 10.1016/0003-4975(90)90240-7.
- Schoen FJ, John J, Collins Jr, Lawrence H. Long-term failure rate and morphologic correlations in porcine bioprosthetic heart valves. The American journal of cardiology. 1983; 51.6: 957-964. doi: 10.1016/S0002-9149 (83)80173-8.
- Федоров С.А. и др. Сравнительная оценка клинических и гемодинамических результатов имплантации ксеноаортальных и ксеноперикардиальных биологических протезов при коррекции дегенеративных пороков аортального клапана // Комплексные проблемы сердечно-сосудистых заболеваний. – 2018. – Т.7. – №2. – С.50-60. doi: 10.17802/ 2306-1278-2018-7-2-50-60.
- Ганюков В.И., Тарасов Р.С., Ганюков И.В. Транссептальное эндоваскулярное протезирование митрального клапана // Российский кардиологический журнал. – 2020. – №8. – С.158-172. doi: 10.15829/ 1560-4071-2020-3842.
- Клышников К.Ю. и др. Функциональные характеристики биопротезов «Юнилайн» // Комплексные проблемы сердечно-сосудистых заболеваний. – 2017. – Т.6. – №3. – С.6-12. doi: 10.17802/2306-1278-2017-6-3-6-12.
- Клышников К.Ю. и др. Повторное протезирование клапанов сердца: подходы и устройства (обзор литературы) // Кардиоваскулярная терапия и профилактика. – 2023. – Т.22. – №2. – С.97-106. doi: 10.15829/1728-8800-2023-3377.
- Проскурин Д.А. Протезирование митрального клапана // Аллея науки. – 2018. – Т.3. – №7. – С.17-20.
- Vogt S, et al. Heart valve replacement with the Björk-Shiley and St Jude Medical prostheses: A randomized comparison in 178 patients. European Heart Journal. 1990; 11.7: 583-591. doi: 10.1093/oxfordjournals.eurheartj.a059763.
- Murday AJ, et al. A prospective controlled trial of St. Jude versus Starr Edwards aortic and mitral valve prostheses. The Annals of thoracic surgery. 2003; 76.1: 66-73. doi: 10.1016/s0003-4975(03)00118-8.
- Burckhardt D, et al. Clinical evaluation of the St. Jude Medical heart valve prosthesis: A two-year follow-up of 150 patients. The Journal of Thoracic and Cardiovascular Surgery. 1984; 88.3: 432-438.
- Daemen JHT, et al. Right minithoracotomy versus median sternotomy for reoperative mitral valve surgery: a systematic review and meta-analysis of observational studies. European Journal of Cardio-Thoracic Surgery. 2018; 54.5: 817-825. doi: 10.1093/ejcts/ezy173.
- Карпенко И.Г. и др. Современные методы остеосинтеза грудины после продольной срединной стернотомии (обзор литературы) // Вестник новых медицинских технологий. Электронное издание. – 2022. – Т.16. – №2. – С.30-43. doi: 10.17116/Cardiobulletin20231801149.
- Harky A, et al. Left atrial or transeptal approach for mitral valve surgery: a systematic review and meta-analysis. Current Problems in Cardiology. 2021; 46.3: 100602. doi: 10.1016/j.cpcardiol.2020.100602.
- Carpentier A, et al. Open-heart operation under videosurgery and minithoracotomy. First case (mitral valvuloplasty) operated with success. Comptes rendus de l’Academie des sciences. Serie III, Sciences de la vie. 1996; 319.3: 219-223.
- Чернов И.И. и др. Первый опыт мини-инвазивных операций на митральном клапане // Клиническая и экспериментальная хирургия. Журнал имени академика Б.В. Петровского. – 2013. – №2(2). – С.20-23.
- Шевченко Ю.Л., Пятириченко И.А. Правосторонний доступ в хирургии многоклапанных пороков // Грудная и сердечно-сосудистая хирургия. – 1997. – №2. – С.51.
- Пиданов О.Ю. и др. Миниинвазивные вмешательства у пациентов с митральными пороками сердца // Грудная и сердечно-сосудистая хирургия. – 2018. – Т.60. – №1. – С.19-27. doi: 10.24022/0236-2791-2018-60-1-19-27.
- Кондратьев Д.А. и др. Правосторонняя мини-торакотомия как безопасный и эффективный доступ в хирургии соединительнотканной дисплазии митрального клапана // Клиническая и экспериментальная хирургия. – 2020. – Т.8. – №3. – С.40-50. doi: 10.33029/2308-1198-2020-8-3-40-50.
- Евсеев Е.П. и др. Хирургическое лечение пороков сердца из правосторонней мини-торакотомии // Кардиология и сердечно-сосудистая хирургия. – 2021. – Т.14. – №1. – С.26-31.
- Щербатюк К.В., Комаров Р.Н., Пиданов О.Ю. Мини-торакотомия в хирургии митрального клапана // Хирургия. Журнал им. Н.И. Пирогова. – 2019. – №12. – С.121-125. doi: 10.17116/hirurgia2019121121.


