К вопросу о действии оксилипинов на прорастание семян гороха Pisum sativum L
Автор: Иванова А.Б., Ярин А.Ю., Анцыгина Л.Л., Гречкин А.Н.
Журнал: Сельскохозяйственная биология @agrobiology
Рубрика: Регуляторы роста растений
Статья в выпуске: 5 т.39, 2004 года.
Бесплатный доступ
Проводили сравнительное изучение воздействия новых биорегуляторов оксилипиновой природы на прорастание семян гороха сорта Татарстан. Определяли амилазную активность семян в период прорастания. Обсуждается возможность влияния экзогенных оксилипинов на скорость поступления в семена воды.
Короткий адрес: https://sciup.org/142133012
IDR: 142133012 | УДК: 633.358:581.142:577.152.321
Toward effect of oxylipines on germination of seeds of pea Pisum sativum L
The authors make the comparative investigation of effect of new bioregulators of oxylipin class - 9(2)-12-Hydroxy-9-dodecanoic (12-HDA) and etherol (EA) acids, and also methyljasmonate (MJ) - on germination of pea seeds of the Tatarstan variety. The amylase activity in seeds during of germination was determined. The differences were revealed in rate of germination under the influence of oxylipins at the concentrations of 10-9 and 10-6 M, but revealed no influence of activity of amylase complex. It was shown, that increased degree of seeds germination in one day after treatment by 12-HDA and MJ might be due to influence of this oxylipins on rate of water coming in seeds determining the development on early stages of ontogenesis and activating amylase and lipoxygenase activities in dormant seeds. The absence of EA effect on the emergence stage might be due to limiting water coming in because of the solidity of senescent seed cover.
Текст научной статьи К вопросу о действии оксилипинов на прорастание семян гороха Pisum sativum L
На ранних стадиях прорастания при активации липоксигеназ в тканях семян происходит интенсивная экспрессия генов, контролирующих эти процессы (8). Наличие среди продуктов окисления липоксигеназ биорегуляторов, контролирующих специфические этапы биосинтеза, может свидетельствовать о нарушении гормонального равновесия. Фосфорилирование полипептидов отдельных фракций в этот период связывают с действием липоксигеназ (9). Предполагается, что активирование оксилипинами протеинкиназ при прорастании семян сопровождается повышением активности гидролитических ферментов, накопление которых происходит в результате расщепления мембранных комплексов и перехода ферментов в свободное активное состояние, а также образования новых ферментов в алейроновом слое и зародыше (10). При этом оба процесса контролируются гормонами и другими регуляторами, в том числе, вероятно, и оксилипинами.
Задача нашей работы состояла в определении действия оксилипинов на прорастание семян гороха ( Pisum sativum L.) и активность амилолитического комплекса с целью выявления соединений, способствующих изменению субстратного обеспечения глюкозой процессов дыхания.
Методика. Объектом исследования служили семена гороха сорта Татарстан (Татарский НИИ сельского хозяйства), которые обрабатывали 0,05 % раствором марганцевокислого калия в течение 30 мин, а затем помещали в чашки Петри (по 50 шт.) и проращивали в следующих растворах: 12-ГДК, МЖ и этеролевая кислота (ЭК) — (9 Z, 11 Е ,1' Е ,3' Z ) -12-(1',3 '-гексадиенилокси)-9,11 -додекадиеновая кислота; концентрация оксилипинов составляла 10-9 и 10-6 М. Чашки выдерживали в термостате при 23 оС в течение 20 ч до проклевывания семян; доращивание проводили в дистиллированной воде (11). Продолжительность опытов составляла 3 сут (начиная с 20 ч — оптимальное время для оценки проклевывания семян). Аналитическая и биологическая повторность опыта 3-кратная. В контроле использовали дистиллированную воду.
(Р = 0,05) (13).
Результаты. Увеличение липоксигеназной активности в процессе развития зародыша предполагает регуляцию оксилипинами выхода семян из состояния покоя (8). По данным наших исследований, 12-ГДК и МЖ оказывали влияние на начало проклевывания семян гороха после замачивания. При этом рН всех исходных растворов после проращивания в них семян практически не изменялся (табл.).
Реакция среды (рН) проращивания семян гороха сорта Татарстан под влиянием оксилипинов
При концентрации МЖ 10–9 М наблюдалась как незначительная стимуляция прорастания (1-е сут), так и практическое (2-е сут) или полное отсутствие различий с контролем (3-и сут). При концентрации 12-ГДК 10–9 М на 1-е сут также выявлена незначительная стимуляция прорастания семян, скорость которого оказалась в 2 раза больше, чем в растворе МЖ (рис. 1, А и Б). Однако в конце 2- и 3-х сут доля проросших семян в опыте была ниже, чем в контроле. В 1-е сут оба вещества стимулировали прорастание семян как при высокой, так и при низкой М) различий между контролем и опы- том на 2-е сут не выявлено; на 3-и сут доля проросших семян в опыте снижалась. При низкой концентрации 12-ГДК доля проросших семян на протяжении всего эксперимента была аналогична таковой при высокой концентрации МЖ, и наоборот.
Этеролевая кислота практически не оказывала влияния на прорастание семян на протяжении 3 сут (исключение составляла концентрация 10–6 М) (см. рис. 1В). Незначительное и в основном статистически недостоверное воздействие ЭК могло быть связано с возрастом семян.
Различная степень прорастания семян при воздействии оксилипинов свидетельствует о широком диапазоне активности (как стимуляция, так и блокирование) регуляторов эндогенных фитогормонов; при этом не исключается нулевой эффект. Известно, что активность амилаз, расщепляющих крахмал до глюкозы, контролируется гибберелловой кислотой. Вместе с тем клетки алейронового слоя чувствительны ко многим фитогормонам, которые как раздельно, так и в сочетании с другими гормонами, регулируют ход синтеза и активность гидролитических ферментов. В регуляции этих процессов также возможно участие оксилипинов. При этом прорастание задерживается, если в семенах не образуется глюкоза (14). По-видимому, одним из механизмов стимуля- ции дыхания является повышение активности амилаз, приводящее к ускоренному прорастанию семени.
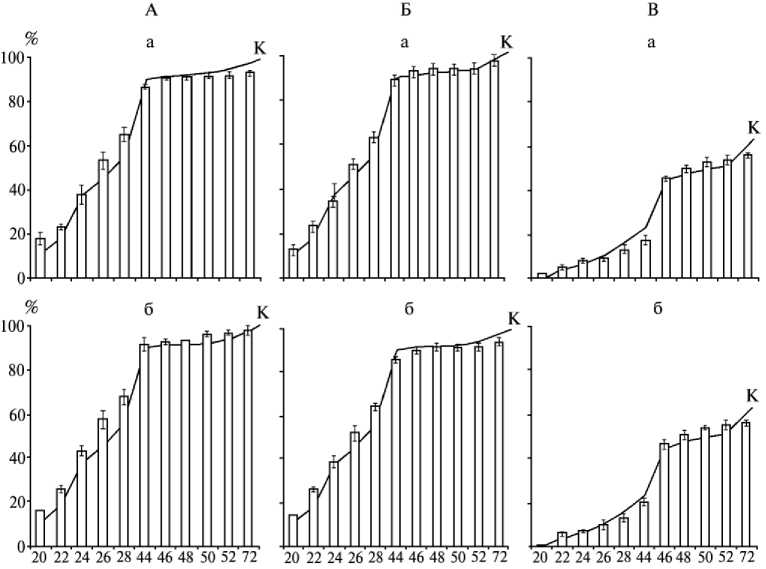
Время прорастания семя и, ч
Рис. 1. Доля проросших семян гороха сорта Татарстан (%) под влиянием 9( Z -12-гидрокси-9-додеценовой кислоты (А) , метилжасмоната (Б) и этеролевой кислоты (В) в различной концентрации: а и б — концентрация раствора соответственно 10–9 и 10–6 М; К — контроль (дистиллированная вода).
В нашем эксперименте при спектрофотометрическом определении негидролизованного амилазами остаточного крахмала не было выявлено полной зависимости амилазной активности от скорости прорастания семян под влиянием оксилипинов (см. рис. 1 и 2). Так, в течение первых суток не наблюдалось воздействия МЖ на активность амилаз (доля проросших семян при обеих концентрациях была выше, чем в контроле); на 2-е сут амилазная активность повышалась на 131 и 123 % при концентрации соответственно 10–9 и 10–6 М (см. рис. 1Б и 2а). Повышенная скорость прорастания семян через 24 ч после воздействия МЖ может быть связана со стимулирующим влиянием последнего на экспрессию липоксигеназных генов, активность которых максимально возрастает через 1 сут прораста-ния (15). По данным Voros с соавт., воздействие экзогенного МЖ вызывает кратковременную экспрессию липоксигеназного гена (максимальный эффект наблюдался через 12-18 ч) (16). При использовании 12-
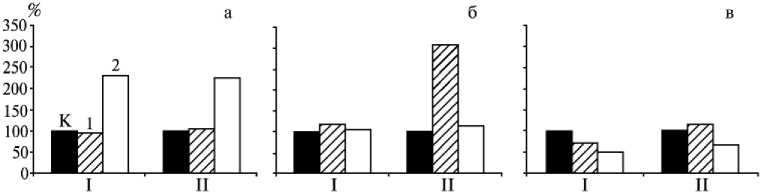
Концентрация оксилипинов, М
Рис. 2. Амилазная активность (% от контроля) прорастающих семян гороха сорта Татарстан под влиянием метилжасмоната (а) , 9( Z -12-гидрокси-9-додеценовой (б) и этеролевой кислот (в) в различной концентрации по времени прорастания: 1, 2 — соответственно через 1 и 2 сут; I и II — — концентрация раствора сответственно 10–9 и 10–6 М; К — контроль (дистиллированная вода).
ГДК (10–6 М) амилазная активность возрастала через 1 и 2 сут после замачивания 101
семян соответственно на 206 и 15 % по сравнению с контролем (см. рис. 2б). Значительная стимуляция амилазной активности на 1-е сут способствовала ускорению прорастания семян на протяжении всего эксперимента (см. рис. 1А). Незначительное повышение скорости прорастания семян при действии 12-ГДК в высокой концентрации в течение 2 сут могло быть обусловлено как прямым, так и опосредованным влиянием оксилипина, в результате стимуляции фосфорилирования некоторых полипептидов (в частности амилаз), приводящей к увеличению активности последних. Кроме того, скорость прорастания могла возрастать в связи с синтезом в зародышах гиббереллина, под контролем которого находится синтез амилаз в наружных слоях эндосперма (16). Активность амилаз под воздействием 12-ГДК (10–9 М) повышалась через 1 и 2 сут соответственно на 18 и 7 %. По-видимому, позитивное влияние этого оксилипина на субстратное обеспечение дыхания происходило только на ранних этапах развития семени.
Воздействие ЭК на активность амилаз существенно отличалось от такового МЖ и 12-ГДК (см. рис. 1 и 2). Несмотря на отсутствие влияния ЭК на скорость прорастания семян, наблюдалось значительное снижение амилазной активности как через 1, так и 2 сут, за исключением варианта с концентрацией ЭК 10–6 М, в котором активность амилазы была на 16 % выше, чем в контроле (через 1 сут). Следовательно, при использовании ЭК наблюдалось отсутствие корреляции между амилазной активностью и скоростью прорастания семян.
Таким образом, повышенная степень прорастания семян гороха через 1 сут после воздействия 9( Z )-12-гидрокси-9-додеценовой кислоты и метилжасмоната может быть связана с влиянием этих оксилипинов на скорость поступления в семена воды, определяющей развитие на первых этапах онтогенеза (4). Этот процесс сопряжен с активацией в покоящихся семенах ферментов, в том числе амилолитических и липоксигеназных. Не исключено, что отсутствие влияния этеролевой кислоты на этапе проклевывания в определенной мере связано с затрудненным поступлением в семена воды из-за жесткости стареющей семенной кожуры.
Л И Т Е Р А Т У Р А
-
1. Т а р ч е в с к и й И.А. Метаболизм растений при стрессе. Казань, 2001.
-
2. G r e c h k i n A.N. Recent developments in biochemistry of the plant lipoxygenase pathway. Progr. Lipid
Res., 1998, 37: 317-352.
-
3. B l e e E. Phytooxylipins and plant defense reactions. Prog. Lipid Res., 1998, 37, 1: 33-72.
-
4. О б р у ч е в а Н.В., А н т и п о в а О.В. Физиология инициации прорастания семян. Физиол. раст.,
1997, 2: 287-302.
-
5. И в а н о в а А.Б., Я р и н А.Ю., А н ц ы г и н а Л.Л. и др. Влияние 12-гидрокси-9( Z )-додеценовой
кислоты на рост и деление клеток корней гороха. Цитология, 2001, 43, 2: 166-171.
-
6. И в а н о в а А.Б., Я р и н А.Ю., А н ц ы г и н а Л.Л. и др. Влияние метилжасмоната на ростовые
процессы у гороха. Цитология, 2002, 44, 4: 369-373.
-
7. И в а н о в а А.Б., Я р и н А.Ю., А н ц ы г и н а Л.Л. и др. 12-гидрокси-9( Z )-додеценовая кислота — индуктор потребления кислорода и изменения рН внеклеточной среды отсеченными корнями пшеницы. Докл. РАН, 2001, 379, 6: 842-844.
-
8. F e u s s n e r I., H a u s e В., N e l l e n A. e.a. Lipid — body lipoxygenase is expressed in cotyledons during germination prior to other lipoxygenase forms. Planta, 1996, 198: 288-293.
-
9. К а р и м о в а Ф.Г., Т а р ч е в с к и й И.А., М у р с а л и м о в а Н.У. и др. Влияние продукта липоксигеназного метаболизма — 12-гидроксидодеценовой кислоты на фосфорилирование белков растений. Физиол. раст., 1999, 46: 148-152.
-
10. Г р и н Н., С т а у т У., Т е й л о р Д. Биология. М., 1990.
-
11. B e w l e y J.D. Protein and nucleic acid synthesis during seed germination and early seedling growth. In:
-
12. Т р е т ь я к о в Н.Н. Практикум по физиологии растений. М., 1982.
-
13. В о з н е с е н с к и й В.Л. Первичная обработка экспериментальных данных. Л., 1969.
-
14. О в ч а р о в К.Е. Физиология формирования и прорастания семян. М., 1976.
-
15. F e u s s n e r I., B a c h m a n n A., H o h n e М. e.a. All three acyl moieties of trilinolein are efficiently
oxygenated by recombinant His-tagged lipid body lipoxygenase in vitro. FEBS Lett., 1998, 431: 433-436.
-
16. V o r o s К., F e u s s n e r I., K u h n H. e.a. Characterization of a methyljasmonate - inducible lipoxygenase from barley ( Hordeum vulgare cv. Salome) leaves. Eur. J. Biochem., 1998, 251: 36-44.
Encyclopedia of plant physiol. New Ser. N. Y., 1982, 149: 559-591.
Институт биохимии и биофизики Казанского научного центра РАН, 420111, Казань, ул. Лобачевского, 2/31, а/я 30


