К вопросу о механизмах повреждения эндотелия кровеносных сосудов при ангиоинвазивном мукормикозе на фоне сахарного диабета
Автор: Смирнов А.В., Сасин А.Н., Ермилов В.В., Поплавский А.Э., Чернецкий О.А., Гуров Д.Ю., Самусев Р.П., Замараев В.С., Быхалов Л.С.
Журнал: Волгоградский научно-медицинский журнал @bulletin-volgmed
Статья в выпуске: 1 т.21, 2024 года.
Бесплатный доступ
Проблема микозов во время пандемии COVID-19 приобрела особое значение и остается актуальной по сегодняшний день. От 7 до 14 % пациентов с COVID-19 имеют сахарный диабет в качестве основного сопутствующего заболевания. Развитию мукормикоза у пациентов с COVID-19 способствуют применение глюкокортикостероидных препаратов, угнетающих иммунитет и повышающих уровень глюкозы в крови, декомпенсация сахарного диабета, эндотелиальная дисфункция, возраст (>65 лет), артериальная гипертензия. Представлено 2 наблюдения COVID-19-ассоциированного мукормикоза у пациентов с длительным плохо контролируемым сахарным диабетом II типа. При морфологическом исследовании в обоих случаях обнаружены несептированные ленточные гифы разного диаметра, ветвящиеся преимущественно под прямым углом. Следует предполагать, что возможными механизмами развития эндотелиальной дисфункции, приводящей к образованию тромбов, являются ангиопатические изменения вследствие сахарного диабета, прямое цитопатическое действие вируса SARS-CoV2, цитокиновый шторм, оксидативный стресс и продукты жизнедеятельности гриба. Тромбоз, в свою очередь, приводит к некрозу тканей и деструкции костей.
Коморбидная патология, сахарный диабет, мукормикоз
Короткий адрес: https://sciup.org/142242046
IDR: 142242046 | УДК: 616.1/.9
On the question of mechanisms of damage to the endothelium of blood vessels in angioinvasive mucormycosis on the background of diabetes mellitus
The problem of mycoses during the COVID-19 pandemic has acquired particular importance and remains relevant to this day. Between 7 and 14 % of patients with COVID-19 have diabetes as a major comorbidity. The development of mucormycosis in patients with COVID-19 is facilitated by the use of glucocorticosteroid drugs that suppress immunity and increase blood glucose levels, decompensation of diabetes mellitus, endothelial dysfunction, age (>65 years), and arterial hypertension. Two observations of COVID-19-associated mucormycosis in patients with long-term poorly controlled type 2 diabetes mellitus are presented. Morphological examination in both cases revealed aseptal ribbon hyphae of different diameters, branching mainly at right angles. It should be assumed that possible mechanisms for the development of endothelial dysfunction leading to the formation of blood clots are: angiopathic changes as a result of diabetes mellitus, direct cytopathic effect of the SARS-CoV-2 virus, cytokine storm, oxidative stress and waste products of the fungus. Thrombosis, in turn, leads to tissue necrosis and bone destruction.
Текст научной статьи К вопросу о механизмах повреждения эндотелия кровеносных сосудов при ангиоинвазивном мукормикозе на фоне сахарного диабета
Сахарный диабет (СД) – хроническое заболевание, характеризующееся гипергликемией и приводящее к значительному нарушению обмена веществ и тяжелым осложнениям. Частота развития СД и смертность ежегодно растет. Более 10 % летальных исходов у людей с СД связаны с инфекционными заболеваниями. Было показано, что от 7 до 14 % пациентов с COVID-19 имеют СД в качестве основного сопутствующего заболевания [1]. В последнее время появилось множество сообщений о высокой распространенности инвазивных микозов как осложнений COVID-19 [1, 2].
Мукормикоз – заболевание, вызываемое условно-патогенными грибами, наиболее частыми возбудителями мукормикоза являются представители семейства Mucoraceae . В последние годы заболеваемость мукормикозом во всем мире возросла [1]. Представители му-кормикоза имеют несептированные ленточные широкие гифы разного диаметра, ветвящиеся преимущественно под прямым углом и обладающие выраженной способностью к ангиоинвазии [2]. Данный вид грибов способствует развитию эндотелиальной дисфункции, воспалительной реакции, которая может привести к гнойному артерииту, тромбозу и прогрессирующему некрозу тканей [1, 3, 4]. Основные клинические формы мукормикоза: синоназальная, риноцеребральная, риноорбитальная, легочная, гастроинтестинальная, кожная и диссеминированная. Риноцеребральный и риноорби-тальный мукормикозы значительно чаще встречались у пациентов с СД [1, 5–8]. Основные причины, способствующие развитию мукорми-коза у пациентов с СД и COVID-19, – это гипоксия, гипергликемия, метаболический ацидоз, а также снижение фагоцитарной активности лейкоцитов из-за иммуносупрессии, вызванной приемом глюкокортикостероидов (ГКС) [7]. Носоглотка является входными воротами для возбудителей мукормикоза. Инвазия гриба сопровождается повреждением носа и близлежащих тканей (пазух, костей и тканей черепа, головного мозга). Мукормикоз имеет высокие показатели смертности (70–95 %) в первую очередь из-за поздней диагностики.
ЦЕЛЬ РАБОТЫ
Представление и клинико-морфологическая характеристика 2 случаев COVID-19-ассоции-рованного ангиоинвазивного мукормикоза на фоне СД II типа с анализом возможных механизмов развития данной патологии и повреждения эндотелия кровеносных сосудов.
МЕТОДИКА ИССЛЕДОВАНИЯ
Описано 2 клинических случая COVID-19 ассоциированного ангиоинвазивного мукормико-за у пациентов с длительным плохо контролируемым СД II типа. Проанализированы медицинская документация и материалы прижизненного микробиологического и патологоанатомических исследований. Фиксация полученного материала, а также изготовление парафиновых блоков и гистологических микропрепаратов с окраской гематоксилином и эозином и ШИК-реакцией проводились по стандартной методике. Последующее изучение выполнено под световым микроскопом Axio Imager. A2 с фотодокументированием с помощью цифровой фото/видеокамеры AxioCam 305 color.
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ И ИХ ОБСУЖДЕНИЕ
У обоих пациентов отмечался длительный плохоконтролируемый СД II типа с кетоацидозом (в первом случае кетоацитоз подтвержден лабораторно, во втором случае присутствовал высокий риск развития кетоацидоза, так как больная отмечала подъемы уровня глюкозы крови выше 20 ммоль/л). Женщины проходили лечение в инфекционном стационаре по поводу COVID-19, включая длительную и высокодоз-ную терапию ГКС.
В первом случае был выявлен риноцере-бральный мукормикоз (подтверждено микробиологически) с летальным исходом (79 лет), во втором случае – риноорбитальная форма мукормикоза (61 год).
При патологоанатомическом исследовании в первом случае макроскопически в слизистой оболочке носовой полости и твердого нёба обнаружены язвенно-некротические участки черного цвета. В левой подглазничной и скуловой областях обнаружены два некротических очага черного цвета, границы четкие, края сухие, на разрезе плотной суховатой консистенции – язвенно-некротический очаг бледно сероватокрасного цвета. В головном мозге на разрезах определяются очаги некроза (инфаркты головного мозга) белесовато-розового цвета, кашицеобразной консистенции, без четких границ, западающие на поверхности разреза. В просветах церебральных артерий определяются красные обтурирующие тромбы.
Во втором случае у пациентки в подглазничной области справа отмечалась отечнось кожи, конъюктивы, экзофтальм и гнойное отделяемое из глаза. В правом общем носовом ходе и наружном слуховом проходе обнаруживалось гнойно-слизистое отделяемое, перфорация барабанной перепонки.
В первом случае при исследовании микропрепаратов в головном мозге отмечались участки некроза с дегенеративными изменениями нейронов, очаги просветления, гематоксилиновые шары, очаговые диапедезные кровоизлияния, эритроцитарные стазы, смешанные тромбы в сосудах микроциркуляторного русла
(МЦР), умеренно выраженная воспалительная инфильтрация полиморфно-ядерными лейкоцитами стенки сосуда с деструкцией эндотелия (рис. 1, 2), периваскулярно были выявлены широкие ленточные гифы несептированного мицелия, при окраске с использованием ШИК-реакции в стенке артерии головного мозга обнаружены структуры несептированного мицелия во всех оболочках сосуда, в просвете сосуда смешанный тромб, адгезированный к интиме, в котором определяются гифы гриба (рис. 3). Кроме того, в межклеточном веществе стенок артерий, эластических мембранах и цитоплазме гладкомышечных клеток обнаружен ШИК-позитивный материал (углеводы, гликопротеиды, мукополисахариды).
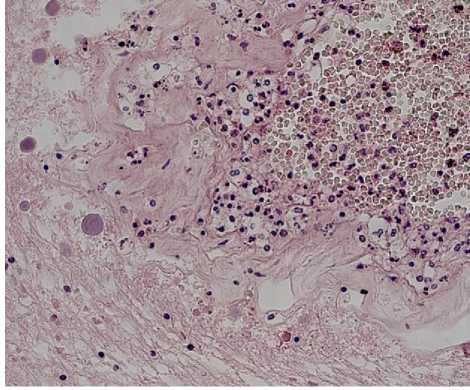
Рис. 1. Пациент № 1. Ткань головного мозга с наличием гематоксилиновых шаров, выраженным отеком и формированием микрокист. Фибриноидный некроз оболочек мозговой артерии с деструкцией эндотелия и формированием смешанного тромба. Окраска гематоксилином и эозином. Увеличение ×400
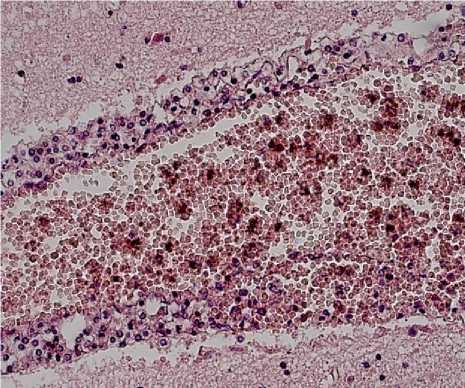
Рис. 2. Пациент № 1. Ткань головного мозга с периваскулярным отеком. Деструкция и умеренно выраженная воспалительная инфильтрация полиморфно-ядерными лейкоцитами стенки сосуда головного мозга с формированием смешанного тромба. Окраска гематоксилином и эозином. Увеличение ×400
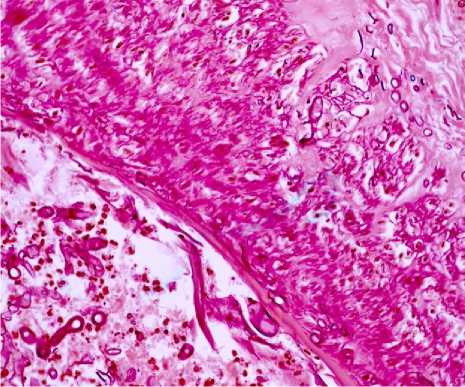
Рис. 3. Пациент № 1. Стенка сосуда с наличием несептированного мицелия в оболочках и просвете, деструкция эндотелия, структурные элементы смешанного тромба. ШИК-реакция. Увеличение ×400
В обоих случаях при микроскопическом исследовании слизистой оболочки носовой полости обнаруживаются широкие ленточные нити несептированного мицелия, часть из которых ветвится под прямым углом, некоторые гифы заканчиваются округлыми спорами (рис. 4), в просвете сосуда – смешанный тромб, в котором также определяются широкие лентовидные, не имеющие перегородок гифы, что подтверждает выраженную ангиотропность гриба и его способность к ангиоинвазии, приводящей к тромбозу с некрозом окружающих тканей [2].
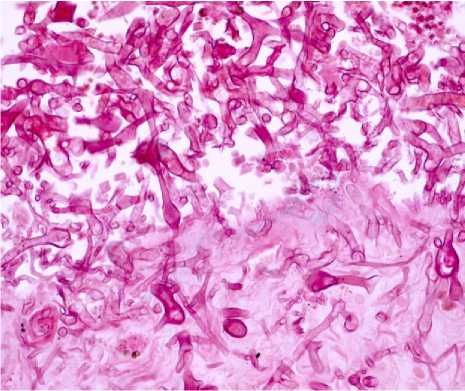
Рис. 4. Пациент № 1. Широкие лентовидные, не имеющие перегородок и ветвящиеся преимущественно под прямым углом гифы гриба в слизистой оболочке носовой полости. ШИК-реакция. Увеличение ×400
По нашему мнению, большую роль в патогенезе ангиоинвазии грибов играют морфофункциональные изменения в интиме сосудов, возникающие при СД (микроангиопатия), вызванные конечными продуктами гликирования, активными формами кислорода и оксида азота [1, 5], эндотелиальная дисфункция, развивающаяся за счет прямого цитопатического воздействия вируса SARS-CoV-2 на эндотелий, помимо этого, вирус повреждает эритроциты и, в следствие образования ферритина, происходит более выраженное повреждение внутренней оболочки сосудов микроциркуляторного русла, которое усугубляется действием оксида-тивного стресса, вазопатических влияний про-воспалительных цитокинов (цитокиновый шторм). Все вышеперечисленные механизмы способствуют ангиоинвазии гриба, продукты жизнедеятельности которого также повреждают сосудистую стенку, активации коагуляционного каскада с развитием коагулопатии и тромбоза в сосудах разного диаметра [5, 9, 10].
В обоих случаях тромбоз играл важнейшую роль в патогенезе повреждения тканей (головного мозга, глаза, слизистой носовой полости и костных структур). Важно отметить, что тромбоз возникал на фоне антикоагулянтной терапии, и это говорит о том, что, во-первых, при лечении данных состояний следует использовать большие дозы антикоагулянтов, а во-вторых, осуществлять тщательный мониторинг свертывающей и противосвертывающей систем крови, в особенности – Д-димера, который у данных больных определялся нерегулярно. Деструкция костной ткани, отмеченная в обоих случаях, развивается, по нашему мнению, в результате тромбоза, тромбоэмболии, микробной эмболии сосудов МЦР.
ЗАКЛЮЧЕНИЕ
Таким образом, у пациентов имелись предпосылки для развития микотической инфекции помимо плохо компенсированного СД, способствующего развитию иммунодефицитных состояний, COVID-19, лечение которого проводилось значительными дозами ГКС, что также могло обеспечивать угнетение иммунитета и рефрак-терность гипергликемии к терапии.
К факторам повреждения эндотелия сосудов у данных больных стоит отнести пожилой и старческий возраст больных и эссенциальную артериальную гипертензию.
Повреждение эндотелия сосудов и развитие васкулита при COVID-19 и СД возникает в результате влияния комплекса факторов атерогенной природы, ангиопатических изменений вследствие СД, вызванных конечными продуктами гликирования, кетоновыми телами, за счет влияния оксидативного стресса [1, 5], цитокино-вого воздействия, прямого цитопатического действия вируса SARS-CoV-2 на внутреннюю стенку сосуда [5, 9, 10], что способствует тромбозу, ангиоинвазии гриба и формированию микробных эмболов и, как следствие, некрозу.
Для ранней диагностики мукормикоза необходимо проводить скрининг пациентов, имеющих факторы риска развития иммунодефицитного состояния и эндотелиальной дисфункции, так как риск неблагоприятных исходов при запущенных случаях высок. Для своевременной диагностики и терапии микозов требуется высокая клиническая настороженность, что будет способствовать снижению развития осложнений и смертности от данной коморбидной патологии.
Список литературы К вопросу о механизмах повреждения эндотелия кровеносных сосудов при ангиоинвазивном мукормикозе на фоне сахарного диабета
- Morales-Franco B., Nava-Villalba M., Medina-Guerrero E. O. et al. Host-Pathogen Molecular Factors Contribute to the Pathogenesis of Rhizopus spp. in Diabetes Mellitus. Current tropical medicine reports. 2021;8(1):6-17. EDN: OMIJVK
- Ермилов В. В., Смирнов А. В., Дорофеев Н. А. и др. COVID-19-ассоциированный мукормикоз в офтальмологической практике Волгоградского региона. Архив патологии. 2022;84(5):43-49. EDN: TIKDME
- Scharf E. L., Cloft H. J., Wijdicks E. Mucor Thrombus. Neurocrit Care. 2016;24(2):268-272. EDN: PQCIKC
- Ochiai H., Iseda T., Miyahara S. et al. Rhino-cerebral mucormycosis-case report. Neurologia Medico-Chirurgica. 1993;33(6):373-376.
- Ozbek L., Topgu U., Manay M. et al. COVID-19-associated mucormycosis: a systematic review and meta-analysis of 958 cases. Clinical Microbiology and Infection. 2023;29(6):722-731. EDN: PZFJGC
- Tayabali K., Pothiwalla H., Narayanan S. Epidemiology of COVID-19-Associated Mucormycosis. Current Fungal Infection Reports. 2023;1-20.
- Gupta A., Kayarat B., Gupta N. COVID-19 associated Mucormycosis (CAM): Implications for perioperative physicians - A narrative review. Saudi J Anaesth. 2023;17(1):58-64. EDN: EQQBJQ
- Monroig V., Tarquinio K. M. Diabetic ketoacidosis and coronavirus disease 2019-associated mucormycosis: a case report. Journal of Medical Case Report. 2022;16(1 ):400.
- Пархоменко Ю. Г., Смирнов А. В., Быхалов Л. С. и др. Патоморфологические особенности поражения органов при коронавирусной инфекции, вызванной SARS-COV-2. Волгоградский научно-медицинский журнал. 2020;(2):52-57. EDN: PHFNWN
- Смирнов А. В., Бисинбекова А. И., Григорьева Н. В. и др. Патологическая анатомия коронавирусной инфекции в современных условиях. Волгоградский научно-медицинский журнал. 2021;(4):5-11. EDN: ZWUHKY


