К вопросу о металлической связи в плотнейших упаковках химических элементов
Автор: Филипенко Г.Г.
Журнал: Доклады независимых авторов @dna-izdatelstwo
Рубрика: Химия
Статья в выпуске: 1, 2005 года.
Бесплатный доступ
Обычно в литературе металлическая связь описывается, как осуществленная посредством обобществления внешних электронов атомов и не обладающая свойством направленности. Хотя встречаются попытки объяснения направленной металлической связи, т.к. элементы кристализуются в определенный тип решетки. В данной статье показано, что металлическая связь в плотнейших упаковках (гексагональной и гранецентрированной) между центральноизбранным атомом и его соседями в общем случае, предположительно, осуществляется посредством 9 направленных связей, в отличие от числа соседних атомов, равного координационному числу 12. Металлическая валентность элемента в его монокристалле и валентность этого элемента по кислороду, водороду - разные понятия.
Короткий адрес: https://sciup.org/148312246
IDR: 148312246
Текст научной статьи К вопросу о металлической связи в плотнейших упаковках химических элементов
Алгоритм построения модели
Выводы
Приложение 1. Металлическая связь в плотнейших упаковках (ГЕК, ГЦК)
Приложение 2. Теоретический расчет модуля всестороннего сжатия (В).
Пока невозможно в общем случае вывести из квантовомеханических расчетов кристаллическую структуру металла по электронному строению атома, хотя, например, Ганцхорн и Делингер указали на возможную связь между наличием кубической объемно-центрированной решетки в подгруппах титана, ванадия, хрома и наличием в атомах этих металлов валентных d - орбиталей. Нетрудно заметить, что четыре гибридные орбитали направлены по 174
четырем телесным диагоналям куба и хорошо приспособлены для связи каждого атома с его 8 соседями в кубической объемноцентрированной решетке. При этом оставшиеся орбитали направлены к центрам граней элементарной ячейки и, возможно, могут принимать участие в связи атома с шестью его вторыми соседями [3, стр.99].
Первое координационное число (К.Ч.1) "8" плюс второе координационное число (К.Ч.2) "6" равно "14". Попытаемся связать внешние электроны атома данного элемента со структурой его кристаллической решетки, учитывая необходимость направленных связей (химия) и наличие обобществленных электронов (физика), ответственных за гальваномагнитные свойства.
Согласно [1, стр. 20], число Z- электроны в зоне проводимости, получено авторами, предположительно, исходя из валентности металла по кислороду, водороду и обязано быть подвергнуто сомнению, т.к. экспериментальные данные по Холлу и модулю всестороннего сжатия близки к теоретическим только для щелочных металлов. ОЦК решетка, Z=1 не вызывает сомнений. Координационное число равно 8.
На простых примерах покажем, что на одну связь у алмаза при плотности упаковки 34% и координационном числе 4 приходится 34%:4=8,5%.
-
• У кубической примитивной решетки (плотность упаковки 52% и координационное число 6) приходится 52%:6=8,66%.
-
• У кубической объемноцентрированной решетки (плотность упаковки 68% и координационное число 8) приходится 68%:8=8,5%.
-
• У кубической гранецентрированной решетки (плотность упаковки 74% и координационное число 12 или 9) приходится 74%:12=6.16% или 74%:9=8,22%.
-
• У гексагональной решетки (плотность упаковки 74% и координационное число 12 или 9) приходится 74%:12=6,16% или 74%:9=8,22%.
Очевидно, что эти 8,66-8,22% несут в себе некий физический смысл. Оставшиеся 26% кратны 8,66 и 100% гипотетическая плотность упаковки возможна при наличии 12 связей. Но реальна ли такая возможность? Внешние электроны последней оболочки или подоболочек атома металла образуют зону проводимости. Число электронов в зоне проводимости влияет на постоянную Холла, коэффициент всестороннего сжатия и т.д. Построим модель металла-элемента так, чтобы оставшиеся, после заполнения зоны проводимости, внешние электроны последней оболочки или подоболочек атомного остова неким образом влияли на строение кристаллической структуры (например, для ОЦК решетки - 8 "валентных" электронов, а для ГЕК и ГЦК - 12 или 9).
Очевидно, что для подтверждения нашей модели необходимо сравнить экспериментальные и теоретические данные по Холлу, коэффициенту всестороннего сжатия и т.д.
Алгоритм построения модели
Ниже выполняется грубое, качественное определение количестваэлектронов в зоне проводимости метелла - элемента; объяснение факторов, влияющих на образование типа решетки монокристалла и на знак постоянной Холла.
Измерения поля Холла позволяют определить знак носителей заряда в зоне проводимости. Одна из замечательных особенностей эффекта Холла заключается, однако, в том, что в некоторых металлах коэффициент Холла положителен, и поэтому носители в них должны, видимо, иметь заряд, противоположный заряду электрона [1]. При комнатной температуре это относится к следующим металлам: ванадий, хром, марганец, железо, кобальт, цинк, цирконий, ниобий, молибден, рутений, родий, кадмий, церий, празеодим, неодим, иттербий, гафний, тантал, вольфрам, рений, иридий, таллий, свинец [2]. Решение этой загадки должна дать полная квантовомеханическая теория твердого тела.
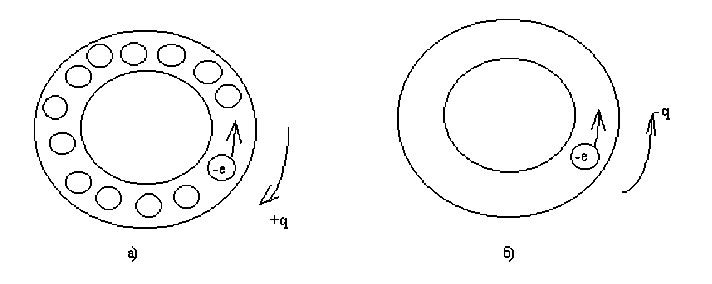
Рис. 1. Схематическое изображение зоны проводимости двух разных металлов: а) вариант первый; б) вариант второй (масштабы не соблюдены).
Примерно, как для некоторых случаев применения граничных условий Борна-Кармана, рассмотрим сильно упрощенный одномерный случай зоны проводимости. Вариант первый: тонкая замкнутая трубка, полностью заполненная электронами кроме одного. Диаметр электрона примерно равен диаметру трубки. При таком заполнении зоны, при локальном передвижении электрона, наблюдается противоположное движение "места" незаполнившего трубку, электрона, то есть движение неотрицательного заряда. Вариант второй: в трубке один электрон - возможно движение только одного заряда - отрицательно заряженного электрона. Из этих двух крайних вариантов видно, что знак носителей, определяемых по коэффициенту Холла, в какой-то степени, должен зависеть от наполнения зоны проводимости электронами - см. рис. 1.
На порядок движения электронов также будут накладывать свои условия и структура зоны проводимости, и температура, и примеси, дефекты, а для магнитных материалов и рассеяние на магнитных квазичастицах - магнонах.
В приведенной ниже табл. 1 нетрудно заметить, что почти все металлы-сверхпроводники в зоне проводимости содержат по два и более электронов от атома. Это металлы: цирконий, цинк, вольфрам, ванадий, таллий, титан, тантал, рутений, рений, свинец, осмий, ниобий, лантан, иридий, гафний, кадмий, алюминий. Отсюда, неприменимо одно-электронное приближение в гамильтониане кристалла для элементов, отдающих в зону проводимости более двух электронов, так как объединенное потенциальное и самосогласованное поле в некоторых случаях, например, в сильном электрическом поле, может быть непериодично постоянной решетки кристалла. А так же, очевидно, что потенциальная энергия попарного взаимодействия электронов для этих металлов, является главным членом в уравнении Шредингера.
Так как рассуждения наши грубые, учитываем в дальнейшем пока только наполнение зоны проводимости электронами. Заполним зону проводимости электронами так, чтобы внешние электроны атомных остовов оказывали влияние на образование типа кристаллизационной решетки. Предположим, что число внешних электронов на последней оболочке атомного остова, после заполнения зоны проводимости, равно числу атомов соседей -координационному числу [5]. Координационные числа ГЕК, ГЦК (гексагональной и гранецентрированной) плотнейших упаковок раены 12 и 18, а объемноцентрированной решетки (ОЦК) – равны 8 и 14 [3].
Построим табл. 1 с учетом вышеизложенного для комнатной температуры. В этой таблице обозначено:
RH - постоянная (коэффициент) Холла,
Z - предполагаемое число электронов, отданное одним атомом в зону проводимости,
Zостов - число внешних электронов атомного остова на последней оболочке,
Тип решетки - тип кристаллической структуры металла при комнатной температуре и в некоторых случаях для температур фазовых переходов (T).
Таблица 1.
|
Элемент |
RH 1010 (м3/K) |
Z (шт.) |
Zостов. (шт.) |
Тип решетки |
|
|
Натрий |
Na |
-2,30 |
1 |
8 |
ОЦК |
|
Магний |
Mg |
-0,90 |
1 |
9 |
ГЕК |
|
Алюминий |
Al |
-0,38 |
2 |
9 |
ГЦК |
|
Al |
-0,38 |
1 |
12 |
ГЦК |
|
|
Калий |
K |
-4,20 |
1 |
8 |
ОЦК |
|
Кальций |
Ca |
-1,78 |
1 |
9 |
ГЦК |
|
Кальций |
Ca |
T=737K |
2 |
8 |
ОЦК |
|
Скандий |
Sc |
-0,67 |
2 |
9 |
ГЕК |
|
Sc |
-0,67 |
1 |
18 |
ГЕК |
|
|
Титан |
Ti |
-2,40 |
1 |
9 |
ГЕК |
|
Ti |
-2,40 |
3 |
9 |
ГЕК |
|
|
Ti |
T=1158K |
4 |
8 |
ОЦК |
|
|
Ванадий |
V |
+0,76 |
5 |
8 |
ОЦК |
|
Хром |
Cr |
+3,63 |
6 |
8 |
ОЦК |
|
Железо |
Fe |
+8,00 |
8 |
8 |
ОЦК |
|
Fe |
+8,00 |
2 |
14 |
ОЦК |
|
|
Fe |
Т=1189K |
7 |
9 |
ГЦК |
|
|
Fe |
Т=1189K |
4 |
12 |
ГЦК |
|
Кобальт |
Co |
+3,60 |
8 |
9 |
ГЕК |
|
Co |
+3,60 |
5 |
12 |
ГЕК |
|
|
Никель |
Ni |
-0,60 |
1 |
9 |
ГЦК |
|
Медь |
Cu |
-0,52 |
1 |
18 |
ГЦК |
|
Cu |
-0,52 |
2 |
9 |
ГЦК |
|
|
Цинк |
Zn |
+0,90 |
2 |
18 |
ГЕК |
|
Zn |
+0,90 |
3 |
9 |
ГЕК |
|
|
Рубидий |
Rb |
-5,90 |
1 |
8 |
ОЦК |
|
Итрий |
Y |
-1,25 |
2 |
9 |
ГЕК |
|
Цирконий |
Zr |
+0,21 |
3 |
9 |
ГЕК |
|
Zr |
Т=1135К |
4 |
8 |
ОЦК |
|
|
Ниобий |
Nb |
+0,72 |
5 |
8 |
ОЦК |
|
Молибден |
Mo |
+1,91 |
6 |
8 |
ОЦК |
|
Рутений |
Ru |
+22 |
7 |
9 |
ГЕК |
|
Родий |
Rh |
+0,48 |
5 |
12 |
ГЦК |
|
Rh |
+0,48 |
8 |
9 |
ГЦК |
|
|
Палладий |
Pd |
-6,80 |
1 |
9 |
ГЦК |
|
Серебро |
Ag |
-0,90 |
1 |
18 |
ГЦК |
|
Ag |
-0,90 |
2 |
9 |
ГЦК |
|
|
Кадмий |
Cd |
+0,67 |
2 |
18 |
ГЕК |
|
Cd |
+0,67 |
3 |
9 |
ГЕК |
|
|
Цезий |
Cs |
-7,80 |
1 |
8 |
ОЦК |
|
Лантан |
La |
-0,80 |
2 |
9 |
ГЕК |
|
Церий |
Ce |
+1,92 |
3 |
9 |
ГЦК |
|
Ce |
+1,92 |
1 |
9 |
ГЦК |
|
|
Празеодим |
Pr |
+0,71 |
4 |
9 |
ГЕК |
|
Pr |
+0,71 |
1 |
9 |
ГЕК |
|
|
Неодим |
Nd |
+0,97 |
5 |
9 |
ГЕК |
|
Nd |
+0,97 |
1 |
9 |
ГЕК |
|
|
Гадолиний |
Gd |
-0,95 |
2 |
9 |
ГЕК |
|
Gd |
T=1533K |
3 |
8 |
ОЦК |
|
|
Тербий |
Tb |
-4,30 |
1 |
9 |
ГЕК |
|
Tb |
Т=1560К |
2 |
8 |
ОЦК |
|
Диспрозий |
Dy |
-2,70 |
1 |
9 |
ГЕК |
|
Dy |
Т=1657К |
2 |
8 |
ОЦК |
|
|
Эрбий |
Er |
-0,341 |
1 |
9 |
ГЕК |
|
Тулий |
Tu |
-1,80 |
1 |
9 |
ГЕК |
|
Иттербий |
Yb |
+3,77 |
3 |
9 |
ГЦК |
|
Yb |
+3,77 |
1 |
9 |
ГЦК |
|
|
Лютеций |
Lu |
-0,535 |
2 |
9 |
ГЕК |
|
Гафний |
Hf |
+0,43 |
3 |
9 |
ГЕК |
|
Hf |
Т=2050К |
4 |
8 |
ОЦК |
|
|
Тантал |
Ta |
+0,98 |
5 |
8 |
ОЦК |
|
Вольфрам |
W |
+0,856 |
6 |
8 |
ОЦК |
|
Рений |
Re |
+3,15 |
6 |
9 |
ГЕК |
|
Осмий |
Os |
<0 |
4 |
12 |
ГЕК |
|
Иридий |
Ir |
+3,18 |
5 |
12 |
ГЦК |
|
Платина |
Pt |
-0,194 |
1 |
9 |
ГЦК |
|
Золото |
Au |
-0,69 |
1 |
18 |
ГЦК |
|
Au |
-0,69 |
2 |
9 |
ГЦК |
|
|
Таллий |
Tl |
+0,24 |
3 |
18 |
ГЕК |
|
Tl |
+0,24 |
4 |
9 |
ГЕК |
|
|
Свинец |
Pb |
+0,09 |
4 |
18 |
ГЦК |
|
Pb |
+0,09 |
5 |
9 |
ГЦК |
Выводы
Несмотря на грубые допущения, из табл. 1 видно, что, чем больше атом элемента отдает электронов в зону проводимости, тем положительнее постоянная Холла, и, наоборот, постоянная Холла отрицательна для элементов, отдавших в зону проводимости один-два электрона, что не противоречит выводам Пайерлса , а также просматривается связь между электронами проводимости (Z) и валентными электронами (Zостов), обуславливающими кристаллическую структуру.
Фазовые переходы элемента из одной решетки в другую можно объяснить перебросом в зону проводимости металла одного из внешних электронов атомного остова или его возвратом из зоны проводимости на внешнюю оболочку остова под воздействием внешних факторов (давление, температура).
Пытались дать разгадку, а получили новую, довольно хорошо объясняющую физико-химические свойства элементов, загадку - это "координационное число орбиталей" равно 9 для ГЦК и ГЕК. Такое частое появление числа 9 в приведенной таблице наводит на мысль, что плотнейшие упаковки недостаточно исследованы.
Методом обратного отсчета от экспериментальных значений коэффициента всестороннего сжатия к теоретическим по формулам Ашкрофта и Мермина [1], определяя число Z, можно убедиться о его близком совпадении с приведенным в табл. 1.
Металлическая связь представляется обусловленной как обобществленными электронами проводимости, так и "валентными" - внешними электронами атомного остова.
Приложение 1. Металлическая связь в плотнейших упаковках (ГЕК, ГЦК)
Из рассуждений о числе направленных связей (или псевдосвязей, т.к. между соседними атомами металла находится зона проводимости), равном девяти по числу внешних электронов атомного остова для плотнейших упаковок, вытекает, что по аналогии с решеткой ОЦК (восемь атомов-соседей в первой координационной сфере) у ГЕК- и ГЦК-решеток в первой координационной сфере, должно быть девять, а имеем 12 атомов. Но 9 атомов соседей, связанных любым центральноизбранным атомом, косвенно подтверждаются экспериментальными данными по Холлу и модулю всестороннего сжатия (да и в опытах по эффекту де Гааза-ван -Альфена число осцилляций кратно девяти). Значит для трех атомов из 12, связей либо нет, либо 9 направленных связей центральноизбранного атома перебирают 12 атомов первой координационной сферы во времени и пространстве.
На рис. 2 показаны координационные сферы в плотнейших гексагональной и кубической упаковках [6]. Обратим внимание на то, что в гексагональной упаковке треугольники верхнего и нижнего оснований повернуты в одну и ту же сторону, а в кубической - в разные.
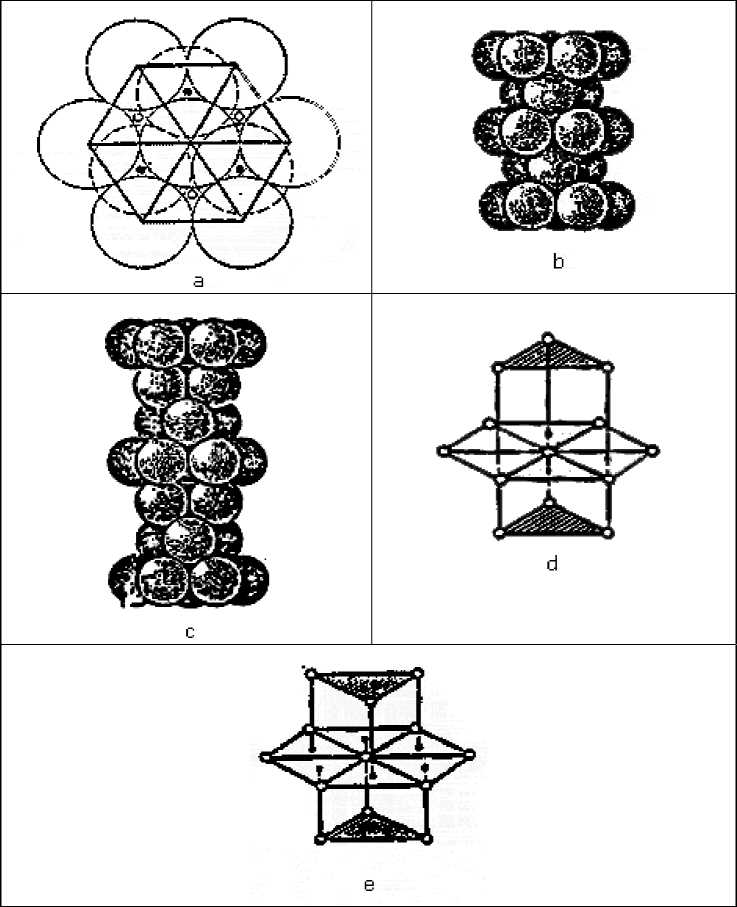
Рис. 2. Плотные упаковки
Приложение 2. Теоретический расчет модуля всестороннего сжатия (В).
Имеем:
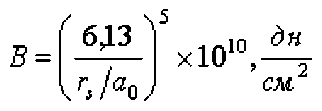
и
В - модуль всестороннего сжатия,
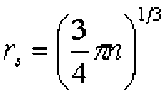
, где
а0 - боровский радиус, rs - радиус сферы, объем которой равен объему, приходящемуся на один электрон проводимости, n - плотность электронов проводимости.
Конечно, давление газов свободных электронов само по себе, одно, не полностью определяет сопротивление металла сжатию, тем не менее во втором случае расчета теоретический модуль всестороннего сжатия лежит ближе к экспериментальному, причем с одной стороны. Очевидно необходим учет второго фактора -влияние на модуль "валентных" или внешних электронов атомного остова, определяющих кристаллическую решетку [7].
1. Расчеты по Ашкрофту и Мермину.
|
Элемент |
Z |
r s /a 0 |
В теоретический |
В измеренный |
|
Cs |
1 |
5.62 |
1.54 |
1.43 |
|
Cu |
1 |
2.67 |
63.8 |
134.3 |
|
Ag |
1 |
3.02 |
34.5 |
99.9 |
|
Al |
3 |
2.07 |
228 |
76.0 |
2. Расчет по рассмотренным ваше моделям.
|
Элемент |
Z |
r s /a 0 |
В теоретический |
В измеренный |
|
Cs |
1 |
5.62 |
1.54 |
1.43 |
|
Cu |
2 |
2.12 |
202.3 |
134.3 |
|
Ag |
2 |
2.39 |
111.0 |
99.9 |
|
Al |
2 |
2.40 |
108.6 |
76.0 |


