Качество жизни у больных после лапароскопической герниопластики: рецидив заболевания и хронический болевой синдром
Автор: Луцевич О.Э., Алибеков К.Т., Урбанович А.С.
Журнал: Московский хирургический журнал @mossj
Рубрика: Абдоминальная хирургия
Статья в выпуске: 3 (77), 2021 года.
Бесплатный доступ
Введение. Основными факторами снижения качества жизни больных после хирургического лечения паховых грыж являются рецидив заболевания (Р) и развитие хронического болевого синдрома (ХБС).Материал и методы. Проанализированы результаты хирургического лечения 1897 пациентов с паховыми грыжами, которым выполнена лапароскопическая герниопластика методом ТАРР. Цель исследования - выявление причин развития ХБС и рецидива паховой грыжи в зависимости от вида и размера сетки, а также технических особенностей операции. У 842 больных при выполнении ТАРР использовали самофиксирующуюся сетку ProGrip™, у - 1054 больных - легкую композитную сетки VYPRO II.Результаты. В 1 группе рецидив заболевания отмечен у 1 больного (0,12 %) с сеткой S - менее 120 см2 , во 2 (контрольной) группе - у 7 (0,66 %), в том числе при использовании относительно больших сеток (более 140 см2 ). Причина рецидива - миграция сетки вследствие недостаточности ее размера или фиксации. ХБС отмечен у 1 пациента основной группы, тогда как в контрольной группе таких больных было 13 на 1054 наблюдений. Причины напрямую связаны со способом фиксации сетки: непосредственный контакт металлической скобки с веточкой нерва или развитие рубца в области шва, или фиксирующего элемента.Выводы. Самофиксирующийся имплант достаточного размера (не менее 10х15 см), обеспечивающий «прилипание» сетки по всей поверхности, надежно защищает пациента как от развития ХБС, так и рецидива заболевания. Косвенной причиной рецидива может явиться также увеличение массы тела пациента после операции.
Паховая грыжа, лапароскопическая герниопластика, осложнения, качество жизни
Короткий адрес: https://sciup.org/142231476
IDR: 142231476 | УДК: 616.361- | DOI: 10.17238/2072-3180-2021-3-9-14
Quality of life in patients after laparoscopic hernioplasty: relapse of the disease and chronic pain syndrome
Objective. The main factors of reducing the quality of life of patients after surgical treatment of inguinal hernias are recurrence of the disease (R) and the development of chronic pain syndrome (CPS).Material and methods. The results of surgical treatment of 1897 patients with inguinal hernias who underwent laparoscopic hernioplasty using the TARR method are analyzed. The aim of the study was to identify the causes of CPS development and recurrence of inguinal hernia, depending on the type and size of the mesh, as well as the technical features of the operation. In 842 patients, a self - fixing ProGrip ™ mesh was used, in 1054 patients - a light composite VYPRO II mesh.Results. In group 1, recurrence of inguinal hernia was noted in 1 patient (0.12%) with a small size of mesh (less than 120 cm2), in group 2 (control) - in 7 (0.66%), including when using relatively large mesh (more than 140 cm2). The cause of recurrence is the migration of the mesh due to its insufficient size or fixation. CPS was observed in 1 patient of the main group, whereas in the control group there were 13 such patients. The reasons are directly related to the method of fixing the mesh: direct contact of the metal bracket with a nerve branch or the development of a scar in the area of the suture or fixing element.Conclusions. A self-fixing implant of sufficient size (at least 10x15 cm), which ensures the" sticking " of the mesh over the entire surface, reliably protects the patient from both the development of CBC and the recurrence of the disease. An indirect cause of relapse may also be an increase in the patient's body weight after surgery.
Текст научной статьи Качество жизни у больных после лапароскопической герниопластики: рецидив заболевания и хронический болевой синдром
Актуальность. Лечение грыж паховой локализации является одной из самых обсуждаемых проблем современной хирургии. Неудовлетворенность результатами лечения этой широко распространенной патологии побуждает хирургов искать новые, более эффективные способы решения этой проблемы, включая использование новых технологий и материалов. Сегодня лапароскопическая герниопластика (ЛГП) является ведущим методом лечения паховых грыж, вытесняя открытые оперативные вмешательства. Преимущества ЛГП бесспорны, хорошо известны, и в периодической печати имеется много работ, подтверждающих этот факт [3, 5, 7, 9, 10, 13, 15, 16].
Эффективность любого хирургического вмешательства оценивается по нескольким факторам, и ведущим из них является качество жизни пациента после операции [7, 9, 10]. Одним из основных факторов, снижающих качество жизни у больных после хирургического вмешательства по поводу паховых грыж, являются рецидив заболевания и развитие хронического болевого синдрома [6, 9, 15].
Материал и методы
Работа основана на исследовании результатов хирургического лечения 1897 пациентов мужского пола в возрасте от 18 до 89 лет с паховыми грыжами, которым в период 2004–2018 гг. на клинических базах кафедры факультетской хирургии № 1 ГБОУ ВПО «Московского государственного медикостоматологического университета» имени А.И. Евдокимова Минздрава РФ (ЗАО ЦЭЛТ г. Москва, хирургическом отделении ГБУЗ ГКБ № 52 ДЗМ, ЦКБ РЖД № 2 г. Москва) была выполнена лапароскопическая герниопластика методом ТАРР (transabdominal preperitoneal plasty). При анализе результатов операций учитывали влияние типа и размера грыжи, а также технических особенностей хирургического вмешательства, на вероятность развития интра- и послеоперационных осложнений. Все показатели подвергали статистической обработке по стандартным методикам. Исследование носило ретроспективно-проспективный характер. Мы также провели анализ качества жизни больных после перенесенных видеохирургических герниопластик с помощью формализованной анкеты, предложенной Российским обществом герниологов. Анкету заполняли во время контрольных осмотров пациентов в послеоперационном периоде – через 6 месяцев, 1 и 3 года. Целью исследования было выявление связи вида и размера сетчатого аллотрансплантата, использованного во время операции, с вероятностью развития хронического болевого синдрома и рецидива паховой грыжи.
Наблюдаемые больные были разделены на две группы: в 1 (основной) группе мы использовали самофиксирующиеся имплантаты, у которых фиксация с тканями происходила по всей поверхности сетки за счет особенностей ее структуры (наличия фиксирующих элементов в виде мелких крючков на основе молочной кислоты по типу «застежки-липучки»). Пациенты 2 группы (контрольной) получали хирургическое пособие с использованием сетчатых имплантатов с «точечной фиксацией» интракорпоральным швом или 5–10 мм герниосте-р плером. В основную группу вошли 842 больных, перенесших ТАРР с использованием самофиксирующей сетки Parietene™ ProGrip™. Размер имплантируемой сетки подбирали в соответствии с рекомендуемыми на тот момент общепринятыми стандартами и экономической целесообразности. Первоначально использовали сетки размером 12–13х7,5 см (фирма-производитель выпускала сетку 15х15 см, ее разрезали пополам), последние годы используется стандартный размер импланта 15х10 см (выпускаемая производителем сетка 30х15 см позволяет получить из одного полотна 3 импланта). Контрольную группу составили 1054 больных, оперированных также по методике ТАРР, но с использованием легкой композитной сетки VYPROII
(табл. 1). Размеры имплантируемых сеток подбирались по тем же критериям, что и в основной группе.
Таблица 1
Отдаленные (свыше 3х недель) послеоперационные осложнения
Table 1
Long-term (over 3 weeks) postoperative complications
|
ProGrip™ |
*VIPRO II |
|||
|
Осложнения Complications |
(n=842) |
(n=1054) |
||
|
Абс. |
% |
Абс. |
% |
|
|
Хронический болевой синдром Chronic pain syndrome |
1 |
0,12 |
13* |
1,23 |
|
Рецидив грыжи Recurrent hernia |
1 |
0,12 |
7 |
0,66 |
*Повторно оперированы 3 больных.
Обе группы были сопоставимы по характеру патологии, срокам грыженосительства и возрастному составу (средний возраст 42±9,1 года). Больные пожилого и старческого возраста составили 21,5 %, при этом практически все они имели от 1 до 3 и более сопутствующих заболеваний других органов и систем. Хирургическое вмешательство (ЛГП) выполняли под общим обезболиванием после стандартного предоперационного амбулаторного обследования.
Результаты
Сравнительный анализ выявил достоверное снижение вероятности (p<0,005) развития рецидива заболевания в основной группе, при этом сроки наблюдения составили от 3 месяцев до 10 лет. В основной группе рецидивы имели место у 1 из 842 больных (0,12 %), тогда как в контрольной группе рецидивы отмечены у 7 из 1054 пациентов (0,66 %). При ретроспективном анализе протоколов и видеозаписей оперативных вмешательств нами были выявлены условия, способствующие более частому развитию рецидива при использовании обычных аллотрансплантатов с точечной фиксацией. В контрольной группе рецидивы наблюдались при всех стандартно применяемых размерах сетчатых имплантов, однако большая их часть пришлась на случаи, когда был использован имплантат площадью до 100см2 (12–13х7,5 см). Достоверной разницы в частоте развития рецидива между сетками площадью 125–140 см2 и более в этой группе выявлено не было. В основной группе рецидив грыжи отмечен при использовании сетки площадью менее 120 см2. Таким образом, следует признать, что на вероятность развития рецидива грыжи оказывает не только тип сетчатого имплантата, но и его размер. При использовании сеток площадью более
130 см2 в основной группе больных рецидивов не наблюдалось, даже у пациентов, которые значительно набрали массу тела за время, прошедшее с момента операции. В контрольной группе из 7 случаев рецидива у 6 больных отмечено увеличение массы тела на 15–24 %, при этом увеличение по всей группе контроля было недостоверным, и составило 5–7 % от исходных значений. В основной группе пациент с рецидивом увеличил массу тела на 8 %, что также представляется недостоверным, и колеблется в пределах среднестатистической погрешности. Наши данные согласуются с литературными данными [4, 8, 13].
Предположительно причиной рецидива заболевания у больного основной группы явилось смещение нижнего края сетки кверху вследствие недостаточного ее размера. В контрольной группе варианты транслокации сетки были значительно разнообразнее, наблюдалось как смещение нижнего края сетки кверху, так и миграция ее медиального или латерального края внутрь вновь формирующегося грыжевого канала. При этом даже относительно большой размер сетки (более 135 см2) не всегда гарантировал отсутствие рецидива заболевания. У двух больных в контрольной группе имело место «сморщивание» сетки в зоне отсутствия фиксирующего элемента (нижний край сетки). Недостаточный размер сетки у больных контрольной группы был достоверной причиной рецидива в 4 наблюдениях, в остальных случаях транслокация и «сморщивание» сеток как причина рецидива были связаны с недостатками «точечной» фиксации импланта.
В свою очередь, анализируя случаи развития хронического болевого синдрома, мы выявили, что вероятность его развития не связана с размерами сетчатого имплантата. Основным фактором риска развития этого осложнения в наших наблюдениях был способ фиксации сетчатого имплантата. В основной группе мы наблюдали всего 1 случай развития хронического болевого синдрома, тогда как в контрольной группе этих случаев было 13 на 1054 наблюдения. При повторном оперативном вмешательстве у пациента основной группы с хроническим болевым синдромом источником боли была обнаруженная лигатурная гранулема апоневроза в области наложения швов, суживающих наружное паховое кольцо (у больного с большой пахово-мошоночной грыжей была применена разработанная нами методика комбинированной лапароскопической герниопластики, предполагающей использование 2–3 см разреза в проекции наружного пахового кольца для прецизионного выделения грыжевого мешка и ушивания расширенного наружного кольца). После иссечения рубцовой ткани и инкапсулированной лигатуры больной был выписан в удовлетворительном состоянии. Наблюдение за отдаленными результатами проводилось в течение 6 месяцев, повторных жалоб не было. Этот единственный случай развития хронического болевого синдрома в основной группе нельзя считать связанным с типом сетчатого имплантата, так как он был обусловлен рубцовыми изменениями в области ушивания наружного пахового кольца. В дальнейшем мы стали использовать резорбирующуюся нить, и других случаев, связанных именно с этим вариантом дополнения герниопластики, мы не наблюдали.
Иная ситуация наблюдалась у больных контрольной группы: из 13 больных необходимость повторной операции возникла у 3 пациентов, в том числе у 2 – по поводу выраженного болевого синдрома в результате травматизации П-образной металлической скобкой надкостницы лонной кости при фиксации сетки к Купферовской связке. В обоих случаях развившееся травматическое воспаление надкостницы потребовало снятия фиксирующего элемента в сроки от 3 до 5 недель после первой операции. Еще у одного больного через 8 месяцев после операции было произведено иссечение рубцовой ткани в области фиксации сетки и удаление фиксирующего элемента (рис. 1). В других наблюдениях хронический болевой синдром удалось купировать или значительно снизить его интенсивность консервативными мероприятиями с использованием методов физиотерапии и периодического приема ненаркотических анальгетиков.
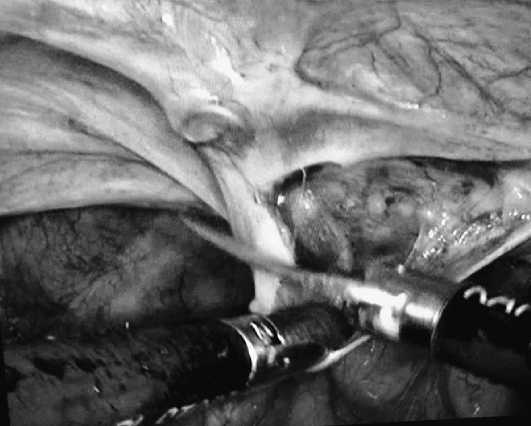
Рис. 1. Рубцовая ткань в области фиксирующего элемента после лапароскопической герниопластики (больной Г. 64 лет, 8 месяцев после операции по методике ТАРР с применением сетки VYPROII ) Fig. 1. Scar tissue in the area of the fixing element after laparoscopic hernioplasty (patient G. 64 years old, 8 months after surgery using the TARR method using a VYPROII mesh)
Отдаленные результаты были прослежены у всех 3 больных на протяжении от 6 месяцев до 4 лет. Результаты повторного оперативного вмешательства были признаны удовлетворительными. На основании анализа всех случаев развития хронического болевого синдрома в основной и контрольной группах можно сделать вывод, что причиной развития этого осложнения является развитие соединительнотканного рубца в области интракорпорального шва или фиксирующего элемента сетки, или непосредственный контакт фиксирующей металлической скобки с веточкой нерва. Различия в технике оперативных вмешательств сравниваемых групп были минимальны, и отличия заключались только в способах фиксации сетки. В свою очередь различия в способах фиксации стандартной облегченной несамофиксирующейся сетки не показали значимой зависимости развития хронического болевого синдрома от способа фиксации сетки. Это осложнение наблюдалось как у больных, которым во время операции фиксация проводилась герниостеплером, так и у больных с интракорпоральным швом нерасасывающейся нитью. Мы считаем, что основной и, возможно, единственной причиной развития хронического болевого синдрома является сдавление нервных волокон в месте фиксации сетчатого импланта металлическими скобками, интракорпоральным швом или грубым рубцово-воспалительным процессом вокруг нерассасывающегося фиксирующего элемента (нить, скобка).
Выводы
Исходя из своего опыта, мы считаем, что успех оперативного лечения паховых грыж сегодня определяется не только выбором эндовидеохирургической методики операции, но и качеством имплантируемой сетки: самофиксирующийся имплант достаточного размера (не менее 10х15 см), обеспечивающий «прилипание» сетки по всей поверхности и не требующий дополнительной фиксации металлическими скобками (винтами) или швами, надежно защищает пациента как от развития хронического болевого синдрома, так и рецидива заболевания. Косвенной причиной рецидива может явиться также увеличение массы тела пациента после операции.
Список литературы Качество жизни у больных после лапароскопической герниопластики: рецидив заболевания и хронический болевой синдром
- Бондарев Г.А., Логачев С.В., Мосолова А.В. Анализ рецидивов грыж передней брюшной стенки после хирургического лечения. Альманах Института хирургии им. А. В. Вишневского, 2017. № 1. С. 318–320.
- Быков А.В., Мяконький Р.В. Оценка частоты рецидива паховых грыж в зависимости от опыта оперирующего хирурга. Сборник тезисов V Съезда Юга России. Ростов-на-Дону, 2017. С. 124–125.
- Павлюк Г.В., Бужор П.В., Морару В.А. и др.Использование ауто- и аллопластических материалов в лечении рецидивных паховых грыж. Альманах Института хирургии им. А. В. Вишневского, 2017. № 1. С. 701–702.
- Пахомова А.Р., Кочетова Л.В., Петрушко С.И. и др. Конституционные особенности больных с паховыми грыжами [Электронный ресурс]. Современные проблемы науки и образования. 2016. № 6.
- Магомедов М.М., Магомедбеков Р.Э. К вопросу оценки выбора оптимального варианта герниопластики у мужчин репродуктивного возраста. Сборник тезисов V Съезда Юга России. Ростов- на-Дону, 2017. С. 197.
- Ильченко Ф.Н., Артемов Ю.В., Аблаев Э.Э. и др. Обоснование лечебно-диагностического алгоритма у больных с паховой грыжей с использованием данных УЗИ брюшной стенки. Вестник неотложной и восстановительной хирургии, 2016. Т. 1. № 2. С. 191–193.
- Беребицкий С.С., Беляков Ю.Н., Андреев В.А. и др. Особенности лечения рецидивных паховых грыж. Актуальные вопросы хирургии: Матер. Всерос. науч.-практ. конф. с междунар. участием, посвящ. 85-летию НУЗ «Отделенческая клиническая больница на станции Пенза ОАО «РЖД». Пенза, 2015. С. 88–90.
- Борисова И. Ю., Славин Л. Е., Алиуллова Р. Р. и др. Оценка частоты рецидивов после операций грыжесечения в зависимости от индивидуальных особенностей соединительной ткани пациентов. Актуальные вопросы герниологии: матер. конф. Москва, 2013. С. 25–26.
- Григорьев С.Г., Кривощеков Е.П., Иванов С.А., Григорьева Т.С. Паховые грыжи. Самара: ООО «Книга», 2013. 160 с.
- Тимербулатов В.М., Тимербулатов Ш.В., Гатауллина Э.З. и др. Послеоперационные вентральные грыжи: современное состояние проблемы. Медицинский вестник Башкортостана, 2013. Т. 8. № 5. С. 101–110.
- Хорава В.Г., Торгунаков А.П., Демидов Д.Г. и др. Преимущества предбрюшинной герниопластики из полулунного параректального доступа при хирургическом лечении рецидивных паховых грыж. Многопрофильная больница: интеграция специальностей: матер. XVIII Всерос. науч.-практ. конф. Москва, 2014. С. 166–167.
- Раимханов А.Д., Аймагамбетов М.Ж., Носо Й. Результаты хирургического лечения рецидивных и больших пахово-мошоночных грыж. Наука и здравоохранение, 2016. № 1. С. 89–97.
- Топурия Г., Топузов Э.Э., Абдулаев М.А. Выбор метода герниопластики при развитии рецидива после удаления паховой грыжи с использованием сетчатого аллотрансплантанта. Успехи современной науки и образования. 2016. Т. 6. № 10. С. 131–137.
- Калиш Ю.И., Аметов Л.З., Шаусупов А.Р. и др. Хроническая парапротезная инфекция после аллогерниопластики. Медицинские перспективы, 2016. Т. 21. № 4. С. 62–66.
- Амирджанова В.Н., Горячев Д.В., Коршунов Н.И., Pебров А.П., Сороцкая В.Н. Популяционные показатели качества жизни по опроснику SF-36 (результаты многоцентрового исследования качества жизни «Мираж»). Научно-практическая ревматология, 2008. № 1. С. 36–48.
- Кукош М.В., Власов А.В., Гомозов Г.И. Профилактика ранних послеоперационных осложнений при эндопротезировании вентральных грыж. Новости хирургии, 2012. Т. 20. № 5. С. 32–37.


