Кафедра факультетской педиатрии Саратовского государственного медицинского университета: история семидесятилетнего пути
Автор: Горемыкин В.И., Королва И.В., Просова Е.Е., Сидорович О.В., Елизарова С.Ю., Хижняк А.В., Кузнецова Н.А., Спиваковский Ю.М.
Журнал: Саратовский научно-медицинский журнал @ssmj
Рубрика: Научные школы и памятные даты
Статья в выпуске: 4 т.17, 2021 года.
Бесплатный доступ
В статье представлена история кафедры факультетской педиатрии Саратовского медицинского университета имени В. И. Разумовского. Прослежен путь становления научной школы педиатров начиная с периода создания кафедры в 1949 г. и до настоящего времени. Освещены основные научные направления работы кафедры за этот временной отрезок.
История кафедры, кафедра факультетской педиатрии, саратовский медицинский университет
Короткий адрес: https://sciup.org/149139778
IDR: 149139778 | УДК: 61:378.4+378.016:616-053.2:001.92
Department of faculty pediatrics of Saratov State Medical University: the history of a seventy-year journey
The article presents the history of the Department of Faculty Pediatrics at the Saratov Medical University named after V. I. Razumovsky. The path of the formation of the scientific school of pediatricians is traced from the period of the department's creation in 1949 to the present time. The main scientific directions of the department's work during this time period are highlighted.
Текст научной статьи Кафедра факультетской педиатрии Саратовского государственного медицинского университета: история семидесятилетнего пути
радикалами и антиоксидантами смещается в сторону последних, что может способствовать блоку апоптоза, управляемого активными формами кислорода, и стимуляции метастазирования [4, 5]. Ранее также было показано, что N-ацетилцистеин и витамин Е ускоряют метастазирование при экспериментальных раке легких и меланоме у мышей [6]. В то же время высокие дозы витамина С увеличивают внутриклеточную концентрацию активных форм кислорода (АФК) в клетках колоректального рака человека с мутациями KRAS или BRAF с последующими биоэнергетическим кризисом и гибелью опухолевых клеток [6, 7]. Иные данные имеются при совместном использовании антиоксидантов с цитостатиками. Ряд исследований показал способность мелатонина, обладающего антиоксидантным действием, усиливать цитотоксическое действие химиотерапевтических агентов на опухолевые клетки в зависимости от дозы, а также формы и типа рака [8, 9]. Другие средства с антиоксидантной активностью, в частности Мекси-дол и Ксимедон, не влияют на противоопухолевую и антиметастатическую эффективность комбинации «доксорубицин+паклитаксел» в эксперименте [10]. Следовательно, влияние антиоксидантов на конечный эффект антибластомной химиотерапии зависит от типа опухоли и механизмов действия противоопухолевых препаратов и антиоксидантов, используемых в лечении [11]. Именно поэтому необходимы дополнительные исследования в оценке возможности применения антиоксидантных средств при противоопухолевой химиотерапии.
Цель — оценить влияние липосомальных форм Ксимедона и Мексидола на противоопухолевую и ан-тиметастатическую эффективность липосомальной комбинации «доксорубицин/циклофосфамид» у подопытных крыс с карциномой Walker-256.
Материал и методы. Экспериментальное исследование проведено на базе кафедры фармакологии и клинической фармакологии ФГБОУ ВО «МГУ им. Н. П. Огарёва» с соблюдением принципов Европейской конвенции о защите позвоночных животных, используемых для экспериментов и других научных целей (Страсбург, 1986), национальных руководств (ГОСТы 33215–2014 и 34088–2017) и правил учреждения по содержанию и использованию лабораторных животных. Животные (116 крыс-самок Вистар с массой тела 170–270 г.) находились на стандартном режиме вивария и имели свободный доступ к воде и корму. Всех крыс разделили на две большие группы: в 1-й группе ( n =56) первичный опухолевый очаг формировался внутримышечным введением (в бедро задней лапки) взвеси клеток опухолевого штамма Walker-256 (W-256) (106 клеток на изотоническом растворе натрия хлорида), во 2-й ( n =60) — метастатический процесс моделировался подкожным введением того же количества опухолевых клеток в среднюю треть хвоста. Далее в каждой группе животных разделили на 11 подгрупп по 5–7 крыс: в 1-ю подгруппу входили крысы с перевитым штаммом W-256, не получавшие лечения (контроль); во 2-ю — крысы с W-256, получавшие доксорубицин (4 мг/кг) и циклофосфамид (45 мг/кг) в свободной форме однократно в боковую хвостовую вену на 11-е сутки после перевивки штамма W-256; в 3-ю — крысы с W-256, получавшие липосомальную комбинацию «доксорубицин (4 мг/кг) + циклофосфамид (45 мг/кг)» однократно внутривенно на 11-е сутки после перевивки штамма W-256; в 4-ю — крысы с W-256, получавшие липосомальные цитостатики (как в 3-й подгруппе) и липосомальный Ксимедон (50 мг/кг) внутривенно ежедневно с начала применения цитостатиков, в течение 5 суток; в 5-ю — крысы с W-256, получавшие липосомальные цитостатики и липосомальный Ксимедон (100 мг/кг) внутривенно ежедневно с начала применения цитостатиков, в течение 5 суток; в 6-ю — крысы с W-256, получавшие липосомальные цитостатики и липосомальный Мексидол (25 мг/кг) внутривенно ежедневно с начала введения цитостатиков, в течение 5 суток; в 7-ю — крысы с W-256, получавшие липосомальные цитостатики и липосомальный Мексидол (50 мг/кг) внутривенно ежедневно с начала применения цитостатиков, в течение 5 суток; в 8-ю и 9-ю — крысы с W-256, получавшие липосомальные цитостатики и «свободный» Ксимедон в дозах 50 и 100 мг/кг соответственно внутривенно ежедневно с начала применения цитостатиков, в течение 5 суток; в 10-ю и 11-ю — крысы с W-256, получавшие липосомальные цитостатики и «свободный» Мексидол в дозах 25 и 50 мг/кг соответственно внутривенно ежедневно с начала введения цитостатиков, в течение 5 суток.
Животным вводили официнальные лекарственные формы доксорубицина гидрохлорида («Ebewe Pharma», Австрия) в виде 0,04%-го раствора и циклофосфамида («Baxter oncology», Германия) в виде 0,45%-го раствора, разведенных на изотоническом растворе натрия хлорида. Субстанцию Ксимедона (гидроксиэтилдиметилдигидропиримидина) (ФГУП НИИ «Кристалл», Россия) применяли 10%-м раствором на изотоническом растворе натрия хлорида, Мексидол (этилметилгидроксипиридина сукцината) («Фармасофт», Россия) — официнальным 5%-м водным раствором. Липосомы с антибластомными средствами приготавливали гидратированием раствором доксорубицина (2 мг/мл) липидной пленки из растворенных в хлороформе циклофосфамида (120 мг), лецитина («Lipoid», Германия, 500 мг) и холестерина («Avanti Polar Lipids Inc.», США, 50 мг) с использованием роторного испарителя («Heidolph», Германия) и экструдера (LIPEX, Канада). Очистку липосом от не включившихся в них свободных фракций веществ выполняли путем ультрафильтрации. Анализатором размеров наночастиц NANO-flex (США) оценивали диаметр липосом, который колебался от 60 до 90 нм. Липосомы с Ксимедоном и Мексидо-лом приготавливали так же, используя водные растворы этих средств в концентрациях 50 и 100мг/мл (для Ксимедона) и 25 и 50мг/мл (для Мексидо-ла) для гидратации липидной пленки, получаемой из лецитина и холестерина. Концентрация веществ в липосомах определялась с использованием спектрофотометра Shimadzu (Япония) и составила для доксорубицина и циклофосфамида 1,86мг/мл и 21 мг/мл соответственно, для Ксимедона — 50 и 100мг/мл, для Мексидола — 25 и 50мг/мл.
Объем первичной опухоли в динамике ее роста оценивали на 11, 16 и 20-е сутки опыта, перемножая длину, ширину и высоту опухолевого узла, измеренных штангенциркулем. Всех животных выводили из опыта под наркозом тиопенталом натрия (50 мг/кг) на 20-е сутки эксперимента с последующим вылущиванием первичной опухоли и измерением ее массы. Влияние исследуемых средств на метастатический процесс в легких оценивали по следующим параметрам: визуально определяемое количество поверхностно расположенных метастазов в легких, частота метастазирования, диаметр поверхностных метастатических очагов и индекс ингибирования процесса метастазирования [12]. Число легочных метастазов считали с помощью бинокулярной лупы МБС-9 (увеличение 8×2) после фиксации легких в жидкости Карнуа.
Статистическую обработку цифровых данных осуществляли с расчетом средних арифметических значений ( М ) и их ошибок ( m ) с использованием пакета прикладных программ Statistica 10.0 (StatSoft, Inc.). Проверку нормальности распределения проводили с использованием теста Шапиро — Уилка. Значимость различий в группах по количественному признаку (в показателях объема, массы первичной опухоли, общего количества метастатических узлов в легких, крупных и мелких метастатических очагов) в связи с малыми выборками определяли при помощи U -критерия Манна — Уитни. Достоверность различий в показателях частоты метастазирования определяли при помощи критерия χ2. Различия считали достоверными, если p <0,05.
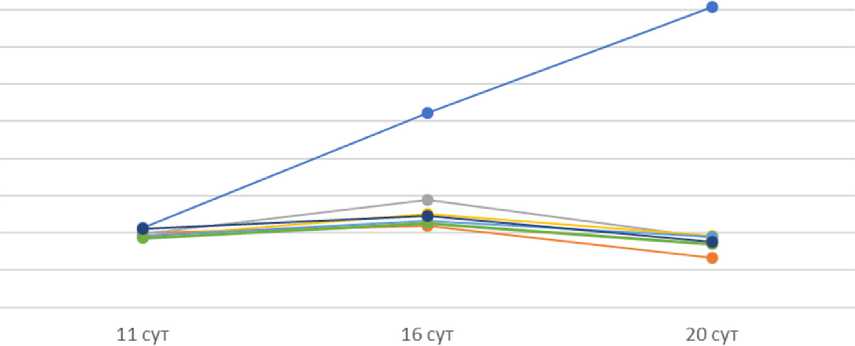
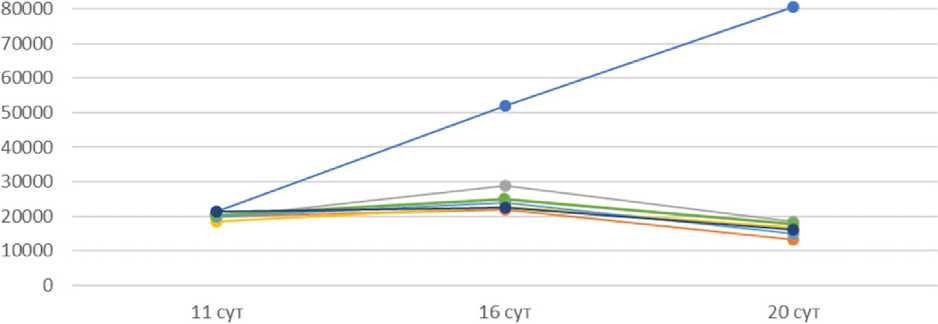
Результаты. Объем первичной опухоли среди крыс с W-256 на фоне применения медикаментозных комбинаций имел значимые изменения на протяжении всего эксперимента. Так, на 16-е сутки опыта объем первичного опухолевого узла во всех экспериментальных подгруппах был достоверно меньше, чем в контроле: во 2-й подгруппе — на 57,9%, в 3-й — на 44,5%, в 4-й — на 51,5%, в 5-й — на 55%, в 6-й — на 56%, в 7-й — на 54%, в 8-й — на 56,5%, в 9-й — на 53%, в 10-й — на 52,3%, в 11-й — на 56,7% ( р =0,001, рис. 1). К концу эксперимента, на 20-е сутки, размеры первичного опухолевого узла продолжали уменьшаться по сравнению с контролем: во 2-й подгруппе — в 6 раз, в 3-й и 5-й — в 4,3 раза, в 4-й — в 4,2 раза, в 6-й — в 4,8 раза, в 7-й — в 5,3 раза, в 8-й — в 4,7 раза, в 9-й — в 4,6 раза, в 10-й — в 4,5 раза, в 11-й — в 4,9 раза ( р <0,001, рис. 1).
мм3
-•-W-256
—♦—W-256+свободные доксорубицин/циклофосфамид
—•—W-256+липосомальные доксорубицин/циклофосфамид
-
— ♦—W-256+липосомальные доксорубицин/циклофосфамид+липосомы с ксимедоном 50 мг/кг
—♦-W-256+липосомальныедоксорубицин/циклофосфамид+липосомы с ксимедоном 100 мг/кг
-
— •—W-256+липосомальныедоксорубицин/циклофосфамид+свободный ксимедон 50 мг/кг
-
— •—W-256+липосомальныедоксорубицин/циклофосфамид+свободный ксимедон 100 мг/кг
А мм3
-e-W-256
-
— •—W-256+свободные доксорубицин/циклофосфамид
-
— •—W-256+липосомальные доксорубицин/циклофосфамид
-
— •—W-256+липосомальные доксорубицин/циклофосфамид+липосомы с мексидолом 25 мг/кг
-
— •—W-256+липосомальные доксорубицин/циклофосфамид+липосомы смексидолом 50мг/кг
-
• W-256+липосомальныедоксорубицин/циклофосфамид+свободный мексидол 25 мг/кг
-
—•—W-256+липосомальные доксорубицин/циклофосфамид+свободный мексидол 50 мг/кг
Б
Рис. 1. Динамика изменения объема первичной опухоли при совместном использовании липосомальных форм Ксимедона
(А) и Мексидола (Б) с липосомальной комбинацией «доксорубицин/циклофосфамид» у крыс с W-256
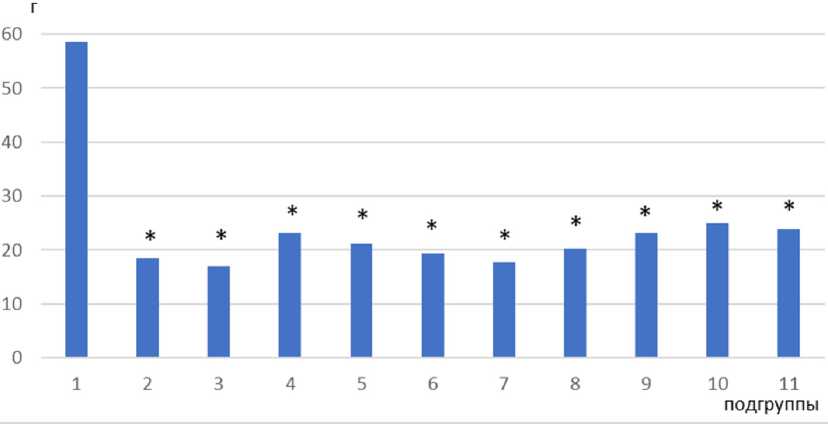
Рис. 2. Изменения массы первичной опухоли у крыс с W-256 при совместном использовании липосомальных форм Ксиме-дона и Мексидола с липосомальной комбинацией «доксорубицин/циклофосфамид»:
1 — контроль W-256 (контроль); 2 — W-256+свободные «доксорубицин/циклофосфамид»; 3 — W-256+липосомальные «доксорубицин/циклофосфамид»; 4 — W-256+липосомальные «доксорубицин/циклофосфамид»+липосомы с Ксимедоном 50 мг/кг; 5 — W-256+липосомальные «доксорубицин/циклофосфамид»+липосомы с Ксимедоном 100мг/кг; 6 — W-256+липосомальные «доксору-бицин/циклофосфамид»+липосомы с Мексидолом 25мг/кг; 7 — W-256+липосомальные «доксорубицин/циклофосфамид»+липосомы с Мексидолом 50мг/кг; 8 — W-256+липосомальные «доксорубицин/циклофосфамид»+свободный Ксимедон 50мг/кг; 9 — W-256+липосомальные «доксорубицин/циклофосфамид»+свободный Ксимедон 100мг/кг; 10 — W-256+липосомальные «доксоруби-цин/циклофосфамид»+свободный Мексидол 25мг/кг; 11 — W-256+липосомальные «доксорубицин/циклофосфамид»+свободный Мексидол 50мг/кг; ' — различия достоверны по сравнению с контролем
Масса первичного опухолевого узла после химиотерапии свободными цитостатиками (во 2-й подгруппе) к 20-м суткам опыта была в 3 раза меньше, чем в контроле ( р =0,005, рис. 2).
Химиотерапия липосомальными цитостатиками (в 3-й подгруппе) приводила к аналогичному снижению массы первичной опухоли — в 3,4 раза по сравнению с контролем ( р =0,003). Дополнительное использование липосомальной формы Ксимедона в дозах 50 и 100мг/кг (в 4-й и 5-й подгруппах) вместе с цитостатиками приводило к снижению массы первичной опухоли в 2,5 и 2,8 раза соответственно по сравнению с контролем ( р =0,01), а липосомальной формы Мексидола в дозах 25 и 50 мг/кг (в 6-й и 7-й подгруппах) — в 3 и 3,3 раза соответственно ( р =0,009, рис. 2). Использование свободной формы Ксимедона в дозах 50 и 100 мг/кг совместно с цитостатиками приводило к аналогичным результатам: масса первичной опухоли снижалась в 2,9 и 2,5 раза соответственно относительно контроля ( р =0,019). Использование свободной формы Мексидола в дозах 25 и 50 мг/кг совместно с цитостатиками приводило к снижению массы первичной опухоли в 2,3 и 2,4 раза соответственно относительно контроля ( р =0,02, рис. 2).
Частота метастазирования в подгруппах как с отдельным использованием липосомальных цитостатиков, так и в сочетании с липосомальными и свободными формами Ксимедона и Мексидола не отличалась от показателя в контроле (табл. 1).
Количество поверхностных метастазов в легких после использования свободной и липосомальной форм цитостатиков во 2-й и 3-й подгруппах одинаково эффективно уменьшалось в 9,3 и 9,2 раза соответственно относительно контроля (р=0,003, табл. 1). Аналогичные изменения были при сочетании липо сомальных цитостатиков и липосомальных форм Ксимедона и Мексидола: количество метастатических очагов в легких уменьшалось в 15-20 раз относительно контроля (р=0,016), не отличаясь при этом от показателя в подгруппе с использованием только липосомальных цитостатиков (табл. 1). Такие же изменения были в подгруппах с использованием свободной формы Ксимедона и Мексидола: число метастатических очагов в легких снижалось в 7–15 раз относительно контроля (р=0,015). При этом различий с показателем в подгруппе с отдельным введением липосомальных цитостатиков также не отмечалось.
Количество крупных метастазов (больше 1 мм в диаметре) в легких при использовании свободной формы цитостатиков достоверно снижалось до 10,3 против 28,6% в контроле ( р =0,039, рис. 3). Аналогичная тенденция была и при использовании липосомальной формы цитостатиков, однако достоверных различий с контролем не было.
Примечательно, что при сочетании липосомальных форм Ксимедона и Мексидола в исследуемых дозах и липосомальных цитостатиков полностью исчезали крупные метастазы в легких, и все метастатические очаги были менее 1 мм в диаметре (100% мелких метастатических очагов против 71,4% мелких и 28,6% крупных очагов в контроле, р =0,009, рис. 3). При сочетании свободных форм Ксимедона и Мексидола в исследуемых дозах и липосомальных цитостатиков количество крупных и мелких метастатических очагов в легких не отличалось ни от показателей в контроле, ни от показателей в подгруппе с отдельным использованием липосомальных противоопухолевых средств. Более того, при использовании свободного Мексидола в дозах 25 и 50 мг/кг было достоверное увеличение числа крупных метастазов до 29,5 и 32,6% соответственно относительно под-
Таблица 1
Влияние липосомальных форм Ксимедона и Мексидола на антиметастатический эффект липосомальной комбинации «доксорубицин/циклофосфамид»
|
Подгруппа |
Частота метастазирования, % |
Количество поверхностных метастазов в легких ( M±m ), % |
Индекс ингибирования процесса метастазирования, % |
|
1-W-256 (контроль) |
53,3±13,1 |
— |
|
|
2-W-256+свободные «доксорубицин/циклофосфамид» |
100 |
5,7±1,1 р 1=0,003 |
89,29 |
|
3-W-256+липосомальные «доксорубицин/ци-клофосфамид» |
5,9±0,9 р 1=0,003 |
89,02 |
|
|
4-W-256+липосомальные «доксорубицин/ци-клофосфамид»+ липосомы с Ксимедоном 50 мг/кг |
80 |
2,6±1,2 р 1=0,008 |
96,1 |
|
5-W-256+липосомальные «доксорубицин/ци-клофосфамид»+ липосомы с Ксимедоном 100 мг/кг |
60 |
3,0±1,7 р 1=0,008 |
96,63 |
|
6-W-256+липосомальные «доксорубицин/ци-клофосфамид»+ липосомы с Мексидолом 25 мг / кг |
3,5±0,8 р 1=0,016 |
93,44 |
|
|
/-W-256+липосомальные «доксорубицин/ци-клофосфамид»+ липосомы с Мексидолом 50 мг / кг |
100 |
3,2±0,5 р 1=0,016 |
93,91 |
|
8-W-256+липосомальные «доксорубицин/ци- клофосфамид»+ свободный Ксимедон 50 мг / кг |
3,6±1,4 р 1=0,009 |
93,25 |
|
|
9-W-256+липосомальные «доксорубицин/ци- клофосфамид»+ свободный Ксимедон 100 мг / кг |
7,8±2,7 р 1=0,013 |
88,3 |
|
|
10-W-256+липосомальные «доксорубицин/ци-клофосфамид»+ свободный Мексидол 25 мг / кг |
80 |
7,0±2,2 р 1=0,012 |
89,5 |
|
H-W-256+липосомальные «доксорубицин/ци- клофосфамид»+ свободный Мексидол 50 мг / кг |
9,0±3,1 р 1=0,015 |
86,5 |
Примечание: р 1 — достоверность различий относительно контроля.
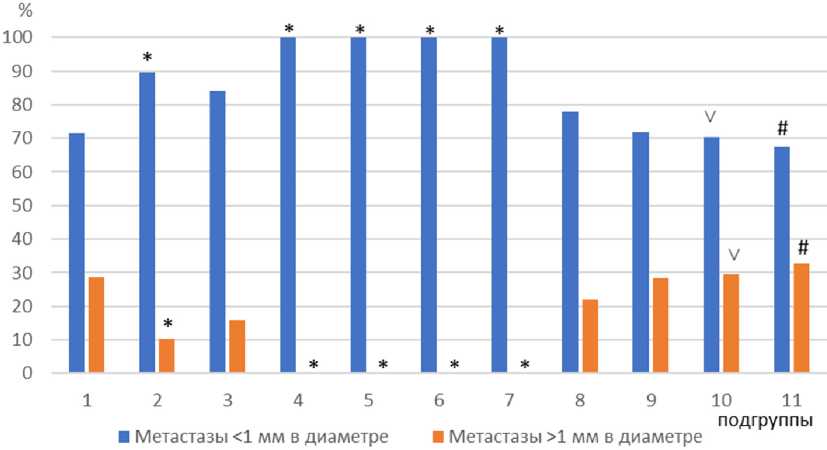
Рис. 3. Влияние сочетанного использования липосомальных форм Ксимедона и Мексидола с липосомальной комбинацией «доксорубицин/циклофосфамид» на диаметр метастатических очагов в легких у крыс с W-256:
1 — контроль W-256 (контроль); 2 — W-256+свободные «доксорубицин/циклофосфамид»; 3 — W-256+липосомальные «доксорубицин/циклофосфамид»; 4 — W-256+липосомальные «доксорубицин/циклофосфамид»+липосомы с Ксимедоном 50 мг/кг; 5 — W-256+липосомальные «доксорубицин/циклофосфамид»+липосомы с Ксимедоном 100мг/кг; 6 — W-256+липосомальные «доксору-бицин/циклофосфамид»+липосомы с Мексидолом 25мг/кг; 7 — W-256+липосомальные «доксорубицин/циклофосфамид»+липосомы с Мексидолом 50мг/кг; 8 — W-256+липосомальные «доксорубицин/циклофосфамид»+свободный Ксимедон 50мг/кг; 9 — W-256+липосомальные «доксорубицин/циклофосфамид»+свободный Ксимедон 100мг/кг; 10 — W-256+липосомальные «доксоруби-цин/циклофосфамид»+свободный Мексидол 25мг/кг; 11 — W-256+липосомальные «доксорубицин/циклофосфамид»+свободный Мексидол 50мг/кг; ' — различия достоверны по сравнению с контролем;v — различия достоверны по сравнению с подгруппой 6; • — различия достоверны по сравнению с подгруппой 7
групп с липосомальной формой Мексидола ( р =0,003), где крупные очаги полностью отсутствовали.
Обсуждение. Липосомальная комбинация «док-сорубицин/циклофосфамид» не показала преимущества перед комбинацией их свободной формы как в отношении торможения роста первичной опухоли, так и в отношении ингибирования процесса метастазирования. Липосомальная форма Ксимедона и Мексидола в обеих исследуемых дозах не влияет на реализацию противоопухолевого эффекта липосомальной комбинации «доксорубицин/циклофос-фамид», не снижая торможения роста первичной опухоли. В итоге масса первичной опухоли у животных в этих подгруппах не отличалась от массы опухоли у крыс, получавших только липосомальные цитостатики. Следует сказать, что не было различий в показателях массы первичной опухоли и между Ксимедо-ном и Мексидолом, применяемых как в липосомах, так и в свободной форме. Антиметастатический эффект липосомальной комбинации использованных цитостатиков не снижается при дополнительном применении липосомальной формы Ксимедона и Мек-сидола в исследуемых дозах. Это подтверждается отсутствием различий в количестве метастатических очагов в легких в сравниваемых подгруппах. Однако, в целом прослеживается тенденция большей эффективности сочетанного применения липосомальной комбинации «доксорубицин/циклофосфамид» с липосомальной формой Ксимедона и особенно Мексидола в сравнении со свободной формой этих средств в торможении роста метастатических очагов в легких, что требует дополнительного более глубокого отдельного изучения. Известно, что компоненты мембран липосом могут модифицировать фармакокинетические параметры лекарственных субстанций, включенных в липосомальные частицы. Комплекс «липосома — биологически активная субстанция» также может модулировать эффекты последней или приобретать иные механизмы действия на функциональные системы организма [13].
Заключение. Таким образом, липосомальная форма Ксимедона в дозах 50 и 100 мг/кг и Мекси-дола в дозах 25 и 50 мг/кг не оказывает значимого влияния на терапевтический эффект липосомальной комбинации «доксорубицин/циклофосфамид», следовательно, не снижает и не увеличивает ее противоопухолевую и антиметастатическую эффективность у крыс с карциномой Walker-256. Липосомальная форма Мексидола в обеих исследуемых дозах эффективнее его свободной формы при сочетании с цитостатиками меняет соотношение мелких и крупных легочных метастазов в сторону преобладания первых и исчезновения последних.
Список литературы Кафедра факультетской педиатрии Саратовского государственного медицинского университета: история семидесятилетнего пути
- Завьялов A.M., Андриянова E.A., Суворов В.В. Развитие педиатрии в Саратовской области: ретроспективный анализ. Бюллетень медицинских Интернет-конференций 2017; 7 (3): 642-5.
- Нуштаев И.А. Иннокентий Никандрович Быстренин (к 90-летию кафедры детских болезней Саратовского медицинского университета). Педиатрия 2003; 82 (4): 89-90.
- Попков B.M., Степанов С.А., Николенко B.H. Вклад клиник и кафедр Саратовского государственного медицинского института в подготовку кадров, медицинской помощи раненым и больным в период Великой Отечественной войны 1941-1945 гг. Саратовский научно-медицинский журнал 2010; 6 (2): 231-5.
- Профессора и заведующие кафедрами Саратовского государственного медицинского университета (1909-2009)/под. ред. П. В. Глыбочко. Саратов: Изд-во Сарат гос. мед. ун-та, 2008; 420 с.
- Людмила Евгеньевна Лагутина. Известия медицинского университета 2007; 8-9 (84-85): 3.
- Кафедра факультетской педиатрии. Медицинские кадры 1978; 4 (1063): 2.
- Свистунов А.А., Горемыкин В.И., Протопопов А.А. и др. Учебно-методический комплекс в педагогической деятельности кафедры педиатрического профиля. Саратовский научно-медицинский журнал 2009; 5 (3): 447-9.
- Саратовский ордена Трудового Красного знамени государственный медицинский институт: К 80-летию высшего медицинского образования в Саратове/под ред. В.Ф. Киричука, Л. Г. Горчакова. Саратов: Полиграфист, 1989; 190 с.
- Горемыкин В.И. Бронхиальная астма, патология билиарного тракта у детей: динамика формирования заболеваний, особенности психофизиологических и вегетативных нарушений, роль наследственности, анте- и перинатальной патологии: автореф. дис... д-ра мед. наук. СПб., 1999; 48 с.


