Кардио- и нейропротекция ингаляционными анестетиками в кардиохирургии
Автор: Борисов Кирилл Юрьевич, Шайбакова Вероника Леонидовна, Черпаков Ростислав Александрович, Левиков Дмитрий Ильич, Гребенчиков Олег Александрович, Лихванцев Валерий Владимирович
Журнал: Патология кровообращения и кардиохирургия @journal-meshalkin
Рубрика: Органопротекция
Статья в выпуске: 3 т.18, 2014 года.
Бесплатный доступ
Мнения исследователей относительно эффективности анестетического прекондиционирования миокарда и головного мозга до сих пор противоречивы. Последний феномен к тому же остается малоизученным. В настоящем исследовании предпринята попытка оценки эффективности модифицированной методики ингаляционной индукции и поддержания анестезии (ИИПА) на основе «импульсного» дозирования севофлурана и исключающей использование пропофола для защиты миокарда и центральной нервной системы (ЦНС) в процессе выполнения аортокоронарного шунтирования (АКШ) в условиях искусственного кровообращения (ИК) у 90 больных в возрасте от 45 до 75 лет. В группе исследования (ИИПА) осуществляли индукцию севофлураном и моделировали прекондиционирование за 10 мин до пережатия аорты (2 МАК анестетика). На этапе ИК применяли атаралгезию. В группе сравнения (тотальная внутривенная анестезия, ТВА) индукцию и поддержание анестезии осуществляли пропофолом и фентанилом, ингаляционные анестетики не применяли. Результаты обработаны методами вариационной статистики и представлены как M±σ. Межгрупповое сравнение производили с помощью t-критерия Стьюдента или U-критерия Манна - Уитни. Статистически значимыми считали различия при p
Кардиопротекция, нейропротекция, анестетическое прекондиционирование, севофлуран, искусственное кровообращение
Короткий адрес: https://sciup.org/142140622
IDR: 142140622 | УДК: 616
Cardioand neuroprotection with volatile anesthetics in cardiac surgery
The researcher's opinions about myocardial and brain anesthetic preconditioning efficiency are yet contradictive. In addition, the anesthetic neuroprotection phenomenon is poorly investigated. In this study the authors attempted to evaluate the efficiency of myocardial and central nervous system (CNS) protection by using a modified method of volatile induction and maintenance of anesthesia (VIMA) based on «pulse-like» sevoflurane dosing that excludes propofol usage. Ninety CABG patients aged 45-75 years were included in the study group (VIMA) and underwent volatile induction with sevoflurane and anesthetic preconditioning (2 MAC) for 10 min before aortic cross-clamping, with ataralgesia used during CPB. The control group patients (TIVA) received propofol and fentanyl, no inhalation anesthetics were applied. Preoperative concentrations of NTpro-BNP were comparable. There was no significant rise of NTpro-BNP concentration in the VIMA group during the postoperative period. In the TIVA group NTpro-BNP concentrations were 3.8 and 4.8 times as much as the baseline values at 24 and 48 postoperative hours respectively (р
Текст научной статьи Кардио- и нейропротекция ингаляционными анестетиками в кардиохирургии
Многочисленные экспериментальные [1, 2] и клинические [3, 4] данные свидетельствуют в пользу эффективности анестетического пре- и посткондиционирования миокарда. Менее исследован нейропротек-торный эффект ингаляционных анестетиков [5, 6]. Однако и в первом и особенно во втором случаях велика доля скептиков, считающих недоказанным клиническую эффективность обсуждаемого феномена (органопротекции) [7].
Литературные данные [8, 9] и проведенные нами экспериментальные исследования [10, 11] показали, что выраженность эффекта пре- и посткондиционирования во многом зависит от состава адъювантных препаратов и дозы ингаляционного анестетика, в нашем случае севофлурана. Так, в эксперименте получены убедительные доказательства того, что пропофол блокирует эффект анестетического прекондиционирования, по крайней мере, в течение 30–40 мин после введения [10]. Ранее в работах коллектива под руководством Ю.И. Гороховатского [8] был предложен «импульсный» режим дозирования севофлурана, позже показавший свою эффективность для прекондиционирования миокарда и в некардиальной хирургии [12].
В ходе выполнения настоящего исследования предполагалось проверить эффективность модифицированной методики ингаляционной индукции и поддержания анестезии на основе «импульсного» дозирования сево-флурана и исключающей использование пропофола для защиты миокарда и ЦНС в процессе выполнения аортокоронарного шунтирования в условиях искусственного кровообращения.
Материал и методы
Эффекты анестетического прекондиционирования миокарда и головного мозга севофлураном были изучены у 90 больных в возрасте 63,5±8,5 года в период с 2011 по 2012 г. Критерии включения в исследование: 1. Информированное согласие на участие в исследовании; 2. Возраст от 45 до 75 лет; 3. Фракция изгнания левого желудочка более 40%; 4. Плановый характер вмешательства; 5. Необходимость реваскуляризации миокарда в условиях искусственного кровообращения; 6. Изолированное аортокоронарное шунтирование; 7. Количество шунтов не менее 2; 8. Суммарный клинический балл по шкале MMSE 26 и более.
В исследование не вошли больные: 1. Перенесшие острый инфаркт миокарда или инсульт за 6 и менее месяцев до операции; 2. С психиатрическими заболеваниями; 3. Со стенозами брахиоцефальных артерий (БЦА) более 70%; 4. С исходно низкими абсолютными значениями церебральной оксигенации (40% и ниже).
Критерии исключения: 1. Деменция и наличие других психических заболеваний в анамнезе; 2. Превышение продолжительности искусственного кровообращения свыше 120 мин; 3. Хирургические осложнения .
Всем больным в непрерывном и/или постоянном режиме осуществляли мониторинг следующих параметров: 1) ЭКГ в 5 отведениях с подсчетом частоты сердечных сокращений (ЧСС), анализом характера ритма, аритмий и девиаций сегмента ST; 2) Артериальное давление неинвазивным и инвазивным методом через катетер, установленный в лучевой артерии; 3) Плетизмография с пульсок-симетрией; 4) Показатели внешнего дыхания и легочной механики; 5) Состав газонаркотической смеси; 6) Биспект-ральный индекс; 7) Активированное время свертывания на этапе искусственного кровообращения каждые 30 минут; 8) Общий анализ крови и газовый состав артериальной и венозной крови каждые 30 минут.
В зависимости от методики анестезиологического обеспечения все больные (табл. 1) были разделены на две группы:
Исследуемая группа (ИИПА) – анестезия на основе севофлурана с прекондиционированием в предперфузи-онном периоде и атаралгезией на этапе искусственного кровообращения. Ингаляционная индукция применялась с использованием максимальной концентрации анестетика с первым вдохом без предварительного заполнения дыхательного контура [13]. После интубации трахеи и замыкания дыхательного контура поток газовой смеси снижали до
0,5 л/мин, FiO2 устанавливали равным 60%, а дозу севофлу-рана поддерживали не менее 1 МАК. С целью адекватного обезболивания дополнительно вводили фентанил по 0,1– 0,2 мг каждые 60 минут или при необходимости. На протяжении всего оперативного вмешательства BIS удерживали в пределах 40–55. За 10 мин до наложения зажима на аорту дозу севофлурана увеличивали до 2 МАК на потоке свежих газов 2 л/мин – моделирование АПК. На этом этапе старались удерживать среднее АД выше 70 мм рт. ст. посредством увеличения темпа инфузии кристаллоидных растворов или степени кардиотонической и/или вазопрессорной поддержки, снижение BIS ниже 20 было принято допустимым. Перед началом искусственного кровообращения вводили фентанил 0,003 мг/кг, пипекурония бромид 0,01 мг/кг, мидазолам 0,1 мг/кг. После пережатия аорты ИВЛ прекращали. На этапе ИК при повышении BIS более 55 анестезию поддерживали введением фентанила 0,1 мг и мидазолама 0,1 мг/кг. После снятия зажима с аорты возобновляли ингаляцию севофлурана на потоке свежих газов 0,5 л/мин и FiO2 60%, дозу анестетика регулировали в зависимости от показателей гемодинамики, в целом стараясь поддерживать концентрацию на выдохе не менее 1 МАК.
Группа сравнения (ТВА) – анестезия на основе пропофола и фентанила без использования ингаляционных анестетиков. В группе сравнения после замыкания дыхательного контура устанавливали поток газовой смеси 2 л/мин и FiO2 50%, начинали постоянную инфузию пропофола в дозе 50–80 мкг/(кг/мин). Ингаляционные анестетики не применяли, инфузия пропофола продолжалась на протяжении всего оперативного вмешательства, а дозу корригировали в соответствии с показателями BIS, стараясь удерживать этот параметр в пределах 40–55. Для поддержания адекватной анальгезии каждые 30–40 минут вводили фентанил 0,1 мг. Перед началом ИК вводили фентанил 0,003 мг/кг и пипекурония бромид 0,01 мг/кг.
В каждой группе до индукции анестезии из центрального венозного катетера забирали 8,0 мл цельной крови, центрифугировали со скоростью 3 000 об./мин в течение 3 мин, после чего по 1,0 мл надосадочной плазмы переливали в чистые пробирки и замораживали при температуре –18 °С для последующей оценки исходных уровней NTpro-BNP и белка S100В – маркера повреждения нервной ткани – иммуноферментным методом. Для определения концентрации S100В пробы подобным образом забирали на этапах: после интубации трахеи, после сведения грудины, в конце операции, через 24 и 48 ч после оперативного вмешательства. Концентрацию NTpro-BNP определяли в динамике через 24 и 48 ч после окончания операции. Перед операцией и через 24 после ее окончания забирали кровь на анализ уровня тропонина T иммунохи-мическим методом.
Мониторинг церебральной оксигенации (rSO2) осуществляли монитором Invos Oximeter 5100B (Somanetics, США), датчики наклеивали на кожу правой и левой половины лба после обработки ее спиртом. После стабилизации показателей фиксировался базовый уровень. Мониторинг проводился интраоперационно непрерывно. В случае
|
Таблица 1 Общая характеристика |
Параметр |
ТВА, n = 45 |
ИИПА, n = 45 |
р |
|
Пол, n |
||||
|
пациентов в группах |
мужской |
41 |
40 |
>0,05 |
|
женский |
4 |
5 |
>0,05 |
|
|
Возраст, лет |
62,42±8,02 |
63,46±7,68 |
>0,05 |
|
|
Вес, кг |
77,5±7,67 |
77,8±9,61 |
>0,05 |
|
|
Функциональный класс стенокардии, n |
||||
|
II |
15 |
17 |
>0,05 |
|
|
III |
24 |
20 |
>0,05 |
|
|
IV |
6 |
8 |
>0,05 |
|
|
Постинфарктный кардиосклероз, n |
18 |
17 |
>0,05 |
|
|
Фракция выброса, %, n |
||||
|
40–45 |
10 |
12 |
>0,05 |
|
|
>45 |
35 |
33 |
>0,05 |
|
|
Артериальная гипертензия, n |
26 |
24 |
>0,05 |
|
|
Стеноз брахицефальных артерий, %, n |
||||
|
30–40 |
5 |
9 |
>0,05 |
|
|
40–50 |
3 |
5 |
>0,05 |
|
|
50–70 |
2 |
1 |
>0,05 |
|
|
Сахарный диабет, n |
3 |
5 |
>0,05 |
|
|
Аритмия, n |
2 |
5 |
>0,05 |
|
|
Аутоиммунный тиреоидит, n |
1 |
0 |
>0,05 |
|
|
Заболевание легких, n |
2 |
6 |
>0,05 |
|
|
Заболевание почек, n |
3 |
3 |
>0,05 |
|
|
EuroScore II, % |
1,75±0,79 |
1,79±0,73 |
>0,05 |
|
|
Суммарный клинический балл по шкале MMSE |
28,28±1,06 |
28,04±1,36 |
>0,05 |
снижения показателей rSO2 ниже 25% от исходного значения проверяли положение головы, увеличивали объемную скорость перфузии, при снижении среднего артериального давления ниже 60 мм рт. ст. начинали инфузию норэпинефрина, регулировали поток свежих газов, при необходимости добавляли в оксигенатор эритроцитарную массу, углубляли анестезию.
В обеих группах пациенты со снижением rSO2 были выделены в отдельную подгруппу «десатурированных» пациентов. Церебральная десатурация была определена как снижение уровня насыщения кислородом ткани мозга ниже 25% от исходного уровня в течение 1 мин и более.
О межгрупповых различиях по частоте развития сердечной недостаточности судили по количеству больных, требовавших инфузии дофамина в раннем послеоперационном периоде.
Оценку когнитивного статуса проводили у пациентов за 3-4 дня до операции и на 2-е сутки после нее. Данные, предоставленные нам, – часть исследования, проводимого аспирантом-неврологом Н.И. Шрадер на кафедре неврологии ГОУ ДПО «РМА ПДО» Минздрава России. Комплексное обследование включало нейропсихологическое тестирование. Применяли краткую шкалу исследования психического статуса – Mini-Mental State Examination (MMSE) [14].
В соответствии с критериями National Clinic Guideline Centre (NCGC) диагноз послеоперационный делирий выставлялся в результате комплексного исследования (осмотр + оценка по шкале MMSE) при балльной оценке по шкале MMSE менее 20% от исхода.
Результаты исследования проанализированы и обработаны методами вариационной статистики с помощью программы Statistica 6.0. Результаты представлены как среднее и стандартное отклонение (M±σ). Для оценки характера распределения в совокупности использовали тест Колмогорова – Смирнова. Межгрупповое сравнение признаков с симметричным распределением проводили с помощью t-критерия Стьюдента, при несимметричном распределении использовали U-критерий Манна – Уитни. Для определения значимости межгрупповых различий по частоте встречаемости признака использовали точный критерий Фишера. Статистически значимыми считали различия при p <0,05.
Результаты и обсуждение
В обеих исследуемых группах (табл. 2) использовали одинаковую тактику проведения анестезии, перфузии и инфузионной терапии. Также не отличалась и тактика ведения больных в отделении реанимации.
|
Таблица 2 |
Параметр |
ТВА, n = 45 |
ИИПА, n = 45 |
р |
|
Характеристика групп |
Кол-во шунтов |
2,71±0,56 |
2,74±0,63 |
>0,05 |
|
по интра- и послеопера- |
Длительность ИК, мин |
69,71±17,86 |
70,53±15,66 |
>0,05 |
|
ционным показателям |
Длительность пережатия аорты, мин |
42,97±11,12 |
43,38±11,47 |
>0,05 |
|
Характер восстановления сердечного ритма (кол-во больных – кол-во дефибрилляций) |
||||
|
фибрилляция желудочков |
2 – 1 |
1 – 1 |
>0,05 |
|
|
спонтанно, синусовый |
43 – 0 |
44 – 0 |
>0,05 |
|
|
Объем кровопотери, мл |
520±75 |
490±50 |
>0,05 |
|
|
Кол-во больных, нуждавшихся в инфузии дофамина в первые 24 часа после операции, n (%) |
23 (57,5) |
13 (32,5) |
<0,05 |
|
|
Длительность ИВЛ, мин |
685±112 |
671±134 |
>0,05 |
|
|
Креатинин после операции через |
||||
|
24 ч |
115,34±42,00 |
126,44±51,28 |
>0,05 |
|
|
48 ч |
121,89±48,98 |
135,06±74,52 |
>0,05 |
|
|
Длительность пребывания в ОРИТ, ч |
20±2 |
19±3 |
>0,05 |
В настоящее время существует обоснованное мнение, что повышенный уровень натрийуретического пептида В-типа (BNP) и концевого фрагмента его предшественника (NTpro-BNP) в послеоперационном периоде является предиктором развития сердечной недостаточности, повышенной потребности в использовании кардиотонических препаратов, а также коррелирует с частотой развития инфарктов миокарда и «сердечной» смерти в течение нескольких лет после кардиохирургических вмешательств и некардиальных операций [15–20].
Больные обеих групп были сопоставимы по предоперационным концентрациям NTpro-BNP, которые, однако, оказались несколько выше так называемой точки ветвления [15] (353,11±335,93 пг/мл в группе ИИПА и 287,27±222,12 пг/мл в группе ТВА, р >0,05).
На всех этапах исследования в группе ИИПА не отмечено значимых колебаний концентрации NTpro-BNP (рис. 1). И, хотя его уровень в этой группе несколько возрос к исходу первых суток после операции (567,11±500,97 пг/мл, р >0,05), через 48 ч после вмешательства он приблизился к дооперационным значениям (484,61±391,45 пг/мл; р >0,05). Напротив, в группе ТВА прогрессивно нарастала концентрация NTpro-BNP на всех этапах исследования. Так, через 24 ч его уровень повысился до 1 105,45±661,42 пг/мл (р <0,05), а через 48 ч составлял уже 1 402,91±1 139,71 пг/мл (р <0,05). Как видно, уровень NTpro-BNP в группе ТВА превосходил таковой в группе ИИПА в 2 раза к исходу первых (р <0,05) и в 2,9 раза к исходу вторых суток (р <0,05) после операции. Описанное можно объяснить предотвращением нарушений сократимости миокарда после искусственного кровообращения вследствие АПК севофлураном и отсутствием такого эффекта при ТВА на основе пропофола и фентанила.
Сходные данные представлены коллективом во главе с К. Julier [21], которые инсуффлировали севофлуран в дозе 4 об.% в оксигенатор аппарата искусственного кровообра- щения за 10 мин до пережатия аорты. Даже несмотря на то что в этой работе в группе исследования индукцию и поддержание анестезии осуществляли пропофолом, авторы продемонстрировали значительно меньшую, по сравнению с контрольной группой, концентрацию NTpro-BNP через 24 и 48 ч после операции.
Подтвердить эту мысль можно на основании сравнения групп по количеству больных, которым в послеоперационном периоде потребовалось введение кардиотонических препаратов. Несмотря на то что потребность в кардиотонической поддержке в первые сутки после операции отмечалась у больных обеих групп, таковых было почти в 2 раза больше в группе ТВА (р <0,05) (табл. 2). Таким образом, ИИПА на основе севофлурана, вероятно вследствие феномена АПК, сохраняет функциональные резервы миокарда после искусственного кровообращения в значительно большей степени, чем ТВА на основе пропофола и фентанила. Аналогичные данные приводят S.G. De’Hert и коллеги [3]. В отличие от нашей работы, авторы этого исследования поддерживали одинаковую концентрацию севофлурана на протяжении всей операции, даже на этапе перфузии. Несмотря на то что в обеих группах индукцию анестезии осуществляли пропофолом, такая методика анестезии привела к снижению в 3 раза числа больных, требовавших инотропной поддержки в послеоперационном периоде, по сравнению с контрольной группой. Вполне вероятно, что, если бы в нашей работе помимо моделирования АПК перед наложением зажима на аорту севоф-луран в составе газовой смеси подавался в оксигенатор АИК на этапе перфузии, результаты были бы еще более впечатляющими.
У всех больных в нашем исследовании предоперационная концентрация тропонина Т находилась в пределах нормы (<0,1 нг/мл). Через сутки после операции уровень этого белка значимо повысился в обеих группах (рис. 2), причем его уровень в группе ТВА в 2 раза превосходил
Рис. 1.
Динамика концентрации NTpro-BNP в группах больных в послеоперационном периоде. р <0,05 значимые различия в сравнении с: * группой ИИПА; + предыдущим этапом в той же группе.

ИИПА
ТВА
Рис. 2.
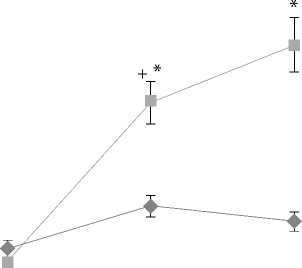
Mежгрупповые различия по суммарному клиническому баллу по шкале MMSE и концентрации тропонина Т до и после операции. * р <0,01 значимые различия в сравнении с группой ИИПА.
Интубация 24 ч 48 ч
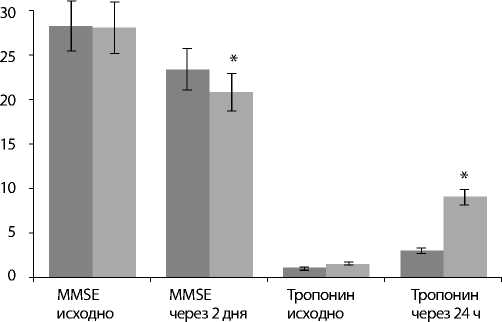
■ ИИПА
■ ТВА
таковой в группе ИИПА (0,61 и 0,29 нг/мл, р <0,05). Таким образом, АПК севофлураном обеспечивает более выраженную защиту миокарда от ишемического и реперфузионного повреждения, чем ТВА на основе пропофола и фентанила. Сходные данные представлены в уже упомянутом исследовании S.G. De’Hert и коллег [3]. Авторы определяли концентрацию тропонина I через 36 ч после операции и обнаружили, что его уровень был значительно больше в группе, где севофлуран не применялся.
Согласно литературным данным, глиальный белок S100B является маркером повреждения нервной ткани и на основании динамики его концентрации можно оценить эффективность анестетической защиты центральной нервной системы, а также прогнозировать риск развития послеоперационного делирия [22].
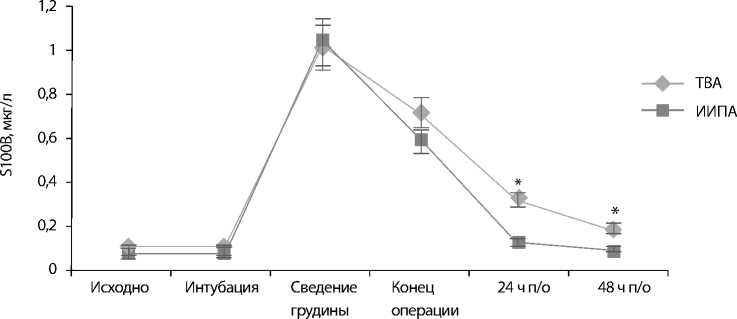
Значимых различий между группами по концентрациям белка S100В до операции в нашем исследовании не было (рис. 3). Отмечено значительное повышение концентрации белка к моменту сведения грудины, также сопоставимое между группами (1,03±0,72 мкг/л в группе ИИПА и 1,01±0,42 мкг/л в группе ТВА, р >0,05). В дальнейшем на всех этапах исследования уровень белка в обеих группах прогрессивно снижался, но достоверные различия обнару- жены лишь в послеоперационном периоде. Так, через 24 ч после вмешательства концентрация S100В в группе ТВА была 2,5 раза больше, чем в группе ИИПА (р <0,05), а через 48 ч – в 2 раза (р <0,05).
Высокая плазменная концентрация белка S100B на этапе сведения грудины не отражает поражение только нейронов и астроглии. По данным H. Jonsson и коллег [23], а также коллектива во главе с R. Anderson [24], очень высокая концентрация этого белка определяется в крови, взятой из операционной раны, а его источниками, вероятнее всего, служат жир, кожа и костный мозг. В то же время повышенная концентрация S100В в плазме крови через 24 и 48 ч после операции является, по-видимому, следствием повреждения нейронов ЦНС [25].
Быстрое снижение плазменной концентрации белка S100B в обеих группах нашего исследования к концу операции и через 24 ч после нее вызвано, вероятно, коротким периодом его полураспада – всего 25 мин. В свою очередь, описанные межгрупповые различия по концентрации белка в первые и вторые послеоперационные сутки, вполне возможно, отражают именно нейропротекторные эффекты анестезии и АПК севофлураном.
Таблица 3
Концентрация белка S100B и показатели церебральной оксигенации в группах
Рис. 3.
Динамика концентрации белка S100B в группах.
* р <0,05 значимые различия в сравнении с группой ИИПА.
|
Концентрация белка S100В, мкг/л |
ИИПА |
ТВА |
||
|
без снижения церебральной оксигенации (n = 33) |
«десатурированные» (n = 12) |
без снижения церебральной оксигенации (n = 34) |
«десатурированные» (n = 11) |
|
|
Через 24 ч |
0,13±0,05* |
0,13±0,04** |
0,33±0,32 |
0,29±0,12 |
|
Через 48 ч |
0,10±0,02* |
0,10±0,02** |
0,18±0,08 |
0,21±0,08 |
* р <0,05 между подгруппами без снижения церебральной оксигенации на одном этапе исследования в группах ИИПА и ТВА; ** р <0,05 между подгруппами «десатурированных» больных на одном этапе исследования в группах ИИПА и ТВА
В обеих группах нашего исследования наблюдалось сопоставимое количество пациентов с эпизодами снижения rSO2 во время искусственного кровообращения (табл. 3). В то же время при сопоставлении данных церебральной оксигенации и динамики белка S100B в каждой из исследуемых групп становится очевидно, что снижение rSO2 в группе ИИПА никак не повлияло на концентрацию белка в послеоперационном периоде – она все равно была меньше, чем в группе ТВА, даже при сравнении подгрупп «десатурированных» больных. По-видимому, это также отражает эффективность АПК севофлураном в отношении центральной нервной системы.
Согласно существующему мнению, во время обратимой гипоксии поражение глии наступает раньше и проявляется в большей степени, чем в нейронах коры. Кроме того, клеток глии значительно больше, они занимают весь объем между сосудами и нейронами, образуя третий слой гематоэнцефалического барьера (ГЭБ) и первыми принимают на себя удар во время искусственного кровообращения (системный воспалительный ответ, нейтрофильная инфильтрация) [26–28]. Гипоксия же становится неизбежным спутником ИК и также вносит вклад в развитие повреждения клеток глии и нейронов [29]. Таким образом, реакция астроцитов, вероятно, является не только более выраженной, но и длительной, поскольку постгипоксические репаративные процессы, связанные с ликвидацией лишней жидкости из паренхимы мозга и восстановлением целостности ГЭБ, протекают длительно и зависят от многих факторов. Этим, на наш взгляд, и объясняется более дли- тельное повышение концентрации белка S100B в группе тотальной внутривенной анестезии.
Несмотря на то что тест MMSE дает общую ориентировочную оценку состояния высших мозговых функций, он широко используется в клинических исследованиях эффективности нейропротективных методов. Исследование когнитивных функций пациентов групп ИИПА и ТВА не выявило значимых различий до операции, но на вторые сутки после вмешательства показало значимое снижение суммарного клинического балла (СКБ) по шкале MMSE в обеих группах, что говорит о возникновении нейропсихологического дефицита у этих больных после операции. В то же время СКБ в группе ТВА был значительно меньше, чем в группе ИИПА (20,84±3,73 и 23,36±4,34 балла, р <0,05), т. е. степень ухудшения когнитивных функций в группе ТВА была достоверно больше, что также, вероятно, подтверждает нейропротекторный эффект АПК севофлураном.
Полученная разница между группами по СКБ также подтверждает более благоприятный исход кардиохирургического вмешательства у пациентов группы ИИПА еще и по причине равного количества больных с эпизодами значительного снижения rSO2. Другими словами, несмотря на все интенсивные лечебные мероприятия, факт гипоксии был зарегистрирован у сопоставимого количества больных в обеих группах, но он оказался менее значим с точки зрения нейропсихических функций для больных группы ИИПА. На наш взгляд, это вполне можно обосновать ней-ропротекторными свойствами севофлурана при моделировании АПК.
Использованная нами методика ИИПА севофлу-раном способствует более выраженному сохранению функциональных резервов миокарда и его структурной целостности у больных после АКШ в условиях ИК, о чем свидетельствуют более низкие концентрации NTpro-BNP, тропонина Т и потребность в кардиотонической поддержке, чем у больных, которым выполнена ТВА на основе пропофола и фентанила. Примененный в данном исследовании способ дозирования севофлурана не влияет на частоту снижения церебральной оксигенации во время ИК, но в большей степени препятствует повышению концентрации белка S100B и снижению СКБ по шкале MMSE в послеоперационном периоде, чем анестезия на основе пропофола и фентанила.


