Картирование эпитопа на белке Erbb-2, узнаваемого моноклональным антителом 4b8, с помощью технологии фагового дисплея
Автор: Боргоякова М.Б., Ильичев А.А.
Журнал: Сибирский онкологический журнал @siboncoj
Рубрика: Лабораторные и экспериментальные исследования
Статья в выпуске: 4 (58), 2013 года.
Бесплатный доступ
Представлены результаты идентификации и локализации эпитопа в составе белка Erbb-2, с которым связывается моноклональное антитело 4b8, предназначенное для использования при проведении иммуногистохимического анализа с целью оценки уровня продукции белка Erbb-2. Эпитоп был идентифицирован с помощью биопеннинга фаговой пептидной библиотеки на основе нитчатого фага, его локализация выявлена с помощью программы ClustalW, анализ специфичности произведен с помощью иммуноферментного анализа. Полученный эпитоп также оказался схож с последовательностью, расположенной в тирозинкиназном домене рецептора, что говорит о возможном взаимодействии данного участка с МКА 4b8.
Фаговый дисплей, картирование эпитопа
Короткий адрес: https://sciup.org/14056349
IDR: 14056349 | УДК: 616-006.66:557-29
Mapping of an epitope of Erbb-2 for recognizing by monoclonal antibody 4b8 using phage display technology
This article presents identification and mapping of an epitope in the protein Erbb-2 which binds to the monoclonal antibody 4b8 intended for use in immunochemistry to estimate the level of Erbb-2 production. Epitope was identified by biopanning of phage display library based on filamentous phage. Location of the epitope was revealed in ClustalW program, analysis of specificity was carried out by ELISA. The epitope is also similar to the sequence on tyrosine kinase domain. It suggests a possible interaction of this site with 4b8.
Текст научной статьи Картирование эпитопа на белке Erbb-2, узнаваемого моноклональным антителом 4b8, с помощью технологии фагового дисплея
Белок ЕrbB-2 (НЕR-2, neu, p185) – член семейства тирозинкиназных рецепторов эпидермального фактора роста (ЭФР), которое включает ещё 3 рецептора (EGFR, ErbB-3 и -4) [5]. Они обладают сходной структурой, имеют общие лиганды и играют большую роль в процессах развития и дифференцировки тканей эпителиального, мезенхимального и нейрального происхождения [3]. Неактивные тирозинкиназные рецепторы ЭФР находятся в «закрытом» состоянии, после связывания с лигандом их конформация меняется, они димеризуются и в результате аутофосфорилирования запускают каскад реакций митогенного характера. ErbB-2 отличается от остальных членов семейства отсутствием необходимости в лиганде и, соответственно, находится в постоянно «открытой» конформации [4, 7].
За счёт спонтанной полисомии 17-й хромосомы или амплификации гена, кодирующего белок ErbB-2, происходит гиперпродукция последнего, что приводит к его спонтанной активации. Запускаемый неконтролируемый каскад реакций вызывает гиперплазию ткани с последующей ма-лигнизацией [1, 11].
Для эффективного иммунотерапевтического лечения рака молочной железы (РМЖ) необходимо предварительно оценить уровень продукции белка HER-2 (HER-2 статус) в каждом конкретном случае, так как принято считать, что гиперпродукция этого рецептора связана с более агрессивным течением заболевания. С этой целью в первую очередь проводят дешёвый иммуногистохимический анализ (ИГХ) опухолевой ткани с использованием поли- или моноклональных антител. Поскольку оценка зависит от выбранного антитела, метода фиксации и приготовления срезов, а также способа интерпретации полученной информации, результат получается довольно грубым [10]. В случае, когда ИГХ анализ не позволяет с достаточной точностью оценить HER-2-статус пациента, исследуют уровень амплификации гена c-Еrb-2 с помощью флуоресцентной гибридизации in situ . Соответственно полученной информации о наличии гиперпродукции белка ErbB-2 назначают определённые схемы терапии. Этот подход является более точным, но и более дорогостоящим и трудоёмким [9].
Как было указано выше, первичная оценка HER-2-статуса производится с использованием различных антител. Исследуемое моноклональное антитело (МКАТ) 4B8, используемое для ИГХ, связывается с N-концом белка ErbB-2. Технология фагового дисплея в настоящее время является наиболее простым подходом к изучению белок-белковых взаимодействий, в том числе взаимодействия антиген-антитело. Нитчатые бактериофаги не имеют тропности к тканям млекопитающих, поэтому взаимодействие мишени с фагами из комбинаторной библиотеки обеспечивается исключительно за счет пептидных встроек. Последовательность такой встройки легко определить секвенированием, поскольку у нитчатых фагов существует прямая физическая связь между генотипом и фенотипом.
Целью исследования являлись картирование эпитопа, к которому специфично моноклональное антитело 4B8, с помощью биопеннинга фаговой пептидной библиотеки и проверка специфичности связывания отобранных мимотопов в ИФА.
Материал и методы
Антитела. Моноклональные антитела производства фирмы Abnova, использованные в данной работе, были получены с помощью гибридомной технологии. Клон 4B8 был отобран после иммунизации мышей синтетическим пептидом, яв- ляющимся полным гомологом участка 22-122 а.о. человеческого ErbB-2. Для ИФА использовались анти-М13 антитела, конъюгированные с пероксидазой хрена (GE Healthcare).
Фаговая пептидная библиотека. В работе использовали штамм Escherichia coli ER2738 и фаговую пептидную библиотеку Ph.D.-7TM фирмы New England Biolabs, Inc. 7-мерная фаговая пептидная библиотека содержит все возможные варианты последовательностей пептидов, экспонированных на поверхности бактериофагов в составе минорного белка pIII. Каждый клон в библиотеке представлен ~1000 копий.
Среды и растворы. Использовали следующие среды: LB, 1,5 % агар, 0,6 % агар (на основе LB). Растворы: IPTG/Xgal, тетрациклина (методики приготовления описаны в инструкции к набору библиотеки), преципитирующий (20 % ПЭГ-6000, 2,5 М NaCl). Буферы: блокирующий (0,1 М NaH-CO3, pH 8,6, 0,5 % БСА, 0,02 % NaN3), TBS (50 мМ Трис-HCl, pH 7,5, 150 мМ NaCl), йодный (10 мМ Трис-HCl, pH 8,0, 1 мМ ЭДТА, 4 М NaI).
Аффинная селекция пептидов, специфически взаимодействующих с МКАТ 4B8, проводилась по схеме, указанной в инструкции, с модификациями. Для проведения всех трёх раундов селекции в лунки иммунологических планшетов вносили по 100 мкл раствора МКА 4B8 в концентрации 29 мкг/ мл в 0,1 М NaHCO3 (pH 8,6) и продолжали сорбцию в течение ночи при 4°С. Для первого раунда использовали 10 лунок, для второго и третьего – по 1 лунке. Тщательно удалив раствор антитела из лунок, в них вносили блокирующий буфер для предотвращения неспецифической сорбции фагов на пластик, инкубировали в течение 1 ч при 4°С. Затем проводили шестикратную отмывку в TBS, содержащем 0,1 % Твин-20 (для 2-го и 3-го раундов использовался 0,5 % Твин-20), и добавляли в лунки по 100 мкл разведённой в TBST фаговой пептидной библиотеки (~1011 БОЕ/мл). Инкубировали библиотеку в течение часа при комнатной температуре. Несвязавшиеся фаги удаляли, десятикратно промывая лунки TBS+Твин, а связавшиеся фаги элюировали по следующей методике: добавляли в каждую лунку по 100 мкл 0,2 М глицинового буфера с HCl (pH 2,2), 0,1 % БСА, через 10 мин нейтрализовали буфер 15 мкл 1 М Трис-HCl (pH 9,1). Для увеличения количества фагов элюат амплифицировали в 20 мл разведённой 1:100
ErbE-2 1-60 immunogen 10 12 11 15 21 01 29 23 27 19 09 33 17
HE LAAL CRUGL L LAL L P P GAASTQVCTGTDHKLRL PAS PETHLDHLRHLYQ GC QWQ GNL ---------------------STQVCTGTDHKLRLPAS PETHLDHLRHLYQ GC QWQ GNL ---------------------------TTDHKLR-------------------------- ---------------------------TTDTKLR-------------------------- ---------------------------ITDTKLR-------------------------- ---------------------------ATDSKLR-------------------------- ---------------------------YFDGKLR-------------------------- ---------------------------YLDHKVR-------------------------- ---------------------------GLDLKLR-------------------------- ---------------------------VQDPKLR-------------------------- ---------------------------HHDAKLR-------------------------- ---------------------------IADFKLR-------------------------- ---------------------------SPDAKHR-------------------------- ---------------------------TTDVKKR-------------------------- ---------------------------ITDYKHR--------------------------
Рис. 1. Часть выравнивания белка ErbB-2, иммуногена для наработки 4B8 и пептидов, отобранных в нашем исследовании с помощью фагового дисплея. Выравнивание осуществлялось на базе программы ClustalW ночной культуры ER2738 в течение 4,5 ч на термошейкере при 37°С. Амплифицированный элюат очищали и использовали для следующего раунда. Элюат третьего раунда не амплифицировали. Для изоляции отдельных фагов его титровали на чувствительной культуре и переносили индивидуальные негативные колонии фаговых клонов в пробирки с 1 мл среды LB, содержащей разведенную 1:100 ночную культуру ER2738. Проводили раздельную амплификацию фаговых клонов в течение 4,5 ч на термошейкере при 37°С. Дважды центрифугировали и переносили по 500 мкл супернатанта в новые пробирки. Очищали фаговую ДНК с использованием йодного буфера.
Таблица
|
№ клона |
Последовательность |
Количество клонов |
|
01 |
YLDMKVR |
1 |
|
09 |
SPDAKMR |
1 |
|
10 |
TTDMKLR |
1 |
|
11 |
ITDTKLR |
1 |
|
12 |
TTDTKLR |
1 |
|
15 |
ATDSKLR |
1 |
|
17 |
SVDWKLR |
7 |
|
19 |
IADFKLR |
1 |
|
21 |
YFDGKLR |
12 |
|
23 |
VQDPKLR |
1 |
|
27 |
HMDAKLR |
1 |
|
29 |
GLDLKLR |
1 |
|
33 |
TTDVKMR |
1 |
Секвенирование ДНК потомков одного фагового клона для определения последовательностей встроек проводили на автоматическом капиллярном секвенаторе в ЦКП СО РАН «Геномика». Обработка результатов секвенирования производилась в программах Seaview, ClustalW.
Иммуноферментный анализ для оценки специфичности связывания отобранных фагов с иммобилизованным МКА 4B8 был выполнен на 96-луночных планшетах, лунки которых были покрыты антигеном в концентрации 2 мкг/мл после ночной инкубации при 4°С (для разведения использовался 0,1М NaHCO3, pH 8,6). После инкубации с блокирующим буфером для уменьшения возможности неспецифического связывания и 6-кратной отмывки в TBST в лунки были добавлены фаговые клоны в концентрации 1010 БОЕ/мл, инкубация проводилась 1 ч при комнатной температуре. После отмывки были добавлены конъюгированные с пероксидазой анти-М13 антитела, разведенные 1:5000. Результат проявляли хромогеном TMB, регистрация сигнала проводилась при длине волны 450 нм. Было проведено четыре независимых ИФА.
Результаты и обсуждение
После трёх раундов аффинной селекции из не-амплифицированного элюата последнего раунда были отобраны 30 фаговых клонов, в которых была определена последовательность встройки (таблица).
Все пептиды выравниваются, обнаруживая три консенсусных аминокислотных остатка (а.о.): D – аспарагиновая кислота, K – лизин, R – аргинин.
ErbB-2 951-1010 VYMIHVKCWMIDSECRPRERELVSEFSRMARDPQRFWIUHEDLGPASPLDSTFYRSLLE
10 TTDHKLR------------------------------------------
12 TTDTKLR------------------------------------------
И ITDTKLR------------------------------------------
19 IADFKLR------------------------------------------
23 VQDPKLR------------------------------------------
27 HMDAKLR------------------------------------------
33 TIDVKMR------------------------------------------
17 ITDYKMR------------------------------------------
09 5PDAKMR------------------------------------------
21 YFDGKLR------------------------------------------
01 YLDMKVR------------------------------------------
29 GLDLKLR------------------------------------------
15 ATDSKLR------------------------------------------
Рис. 2. Взаимодействие отобранных фаговых клонов и фага mp9 на фоне бесфагового контроля (к). На оси ординат указаны значения оптической плотности (OD 450)
0,900
0,800
0,700
0,600
0,500
0,400
0,300
0,200
0,100
0,000
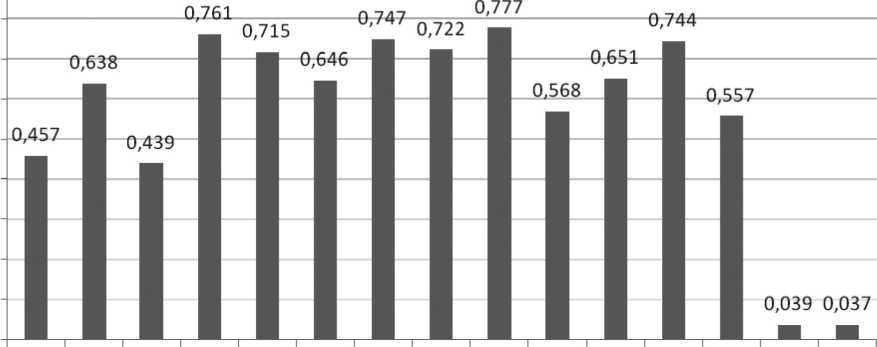
1 9 10 11 12 15 17 19 21 23 27 29 33 mp9 к
Рис. 3. Выравнивание участка тирозинкиназного домена и пептидов, отобранных в нашем исследовании, осуществлялось на базе программы ClustalW
Считается, что именно заряженные а.о. оказывают наибольшее влияние на связывание антител [6], поэтому кажется понятным, почему именно эти аминокислоты оказались в составе консенсусного мотива.
От производителя известно, что иммуноген, который использовали для наработки антитела 4B8, являлся синтетическим полипептидом, идентичным по аминокислотной последовательности участку 22–122 а.о. белка ErbB-2. Выравнивание полученных пептидов с иммуногеном и N-концом ErbB-2 позволило выявить локализацию указанных а.о. (рис. 1). Основываясь на этих результатах, с большой вероятностью мы можем предположить, что Asp-30, Lys-32, Arg-34 составляют линейный эпитоп, с которым связывается МКАТ 4B8. Стоит отметить также значимость а.о. в 33-й позиции: во всех клонах на этом месте расположены али- фатические а.о., имеющие примерно одинаковый размер бокового радикала (Leu, Met, Val). По всей видимости, эта позиция также важна для связывания антитела.
Известно, что обнаруженный мотив в нативном ErbB-2 находится между β-складкой (25–27 а.о.) и α-спиралью (39–50 а.о.), то есть участок 30–34 а.о. имеет свободную конформацию и подходит для формирования эпитопа и взаимодействия с антителом (база данных Pubmed).
Результаты иммуноферментного анализа при наличии отрицательного контроля в виде фага mp9, не имеющего встроек, показывают высокую специфичность связывания отобранных фагов с исследуемым антителом (рис. 2).
Интересно, что полученный мотив в некоторой степени гомологичен участку, расположенному в тирозинкиназном домене ErbB-2 в позиции
964–968 а.о. (ECRPR). Аспарагиновая кислота на этом участке заменена на глутаминовую, а лизин – на аргинин (рис. 3).
Поскольку считается, что в этих парах (D-E, K-R) аминокислоты иммунологически тождественны в значительной степени, а аминокислота пролин (P) является алифатической с небольшим боковым радикалом, есть вероятность, что МКАТ 4B8 связывается также и с указанным участком, то есть, возможно, позволяет выявить гиперпродукцию С-концевого фрагмента ErbB-2 (C-terminal fragment, CTF) [8]. Существуют данные, указывающие на значимость увеличения количества тирозинкиназного домена внутри клетки в развитии опухоли. Новообразования, характеризующиеся повышенной продукцией CTF, оказываются устойчивы к определённым видам терапии, поэтому важно во время анализа ткани РМЖ также выявить наличие в цитоплазме и/или ядре CTF [2]. Исследуемое нами антитело 4B8, вероятно, может позволить в некоторой степени оценить наличие данной аномалии в ходе первичного анализа HER-2 статуса.
Таким образом, впервые нами был идентифицирован и локализован линейный эпитоп рецептора HER-2, с которым связывается МКА 4B8. Он представляет собой последовательность DMKLR, в которой ключевые позиции для связывания антитела занимают заряженные аминокислотные остатки: аспарагиновая кислота, лизин и аргинин. Также была выявлена последовательность в составе тирозинкиназного домена, которая, вероятно, может связывать МКА 4B8, поскольку содержит иммунологически тождественные указанным аминокислотные остатки. Следует отметить, что полученные данные подтверждают возможность использования МКА 4B8 для оценки HER-2 ста- туса, а также дают возможность предположить, что оно может быть использовано для оценки продукции CTF. Результаты данного исследования могут быть интересны разработчикам различных методов диагностики (ИФА, ИГХ и др.), а также могут быть использованы при разработке вакцин нового поколения, например полиэпитопных вакцин или вакцин на основе дендритных клеток, нагруженных антигенами.


