Каталитические реакции на поверхности мезопористых плёнок диоксида титана с иммобилизованной гидрогеназой
Автор: Горенберг А.А., Костров А.Н., Саркисов О.М., Надточенко В.А., Никандров В.В.
Журнал: Труды Московского физико-технического института @trudy-mipt
Рубрика: Оригинальные статьи
Статья в выпуске: 1 т.1, 2009 года.
Бесплатный доступ
Короткий адрес: https://sciup.org/142185565
IDR: 142185565
Текст статьи Каталитические реакции на поверхности мезопористых плёнок диоксида титана с иммобилизованной гидрогеназой
Сопряжение наночастиц неорганических полупроводников с ферментами и/или фотоферментами открывает новые возможности для использования фото- и электрохимически генерированных в полупроводнике зарядов в многоэлектронных ферментативных каталитических реакциях или для сенсибилизированной инжекции электрона из возбуждённого фотофермента в зону проводимости полупроводника. Этот подход позволяет создавать каталитические системы нового типа, способные селективно вести многоэлектронные каталитические реакции, разрабатывать сенсоры и преобразователи света в химическую энергию и электричество [1–3].
В настоящей работе сообщается о разработке новой системы на основе фермента гидрогеназы, иммобилизованного в ме-зопористую плёнку TiO 2 . Фермент гидрогеназа способен катализировать реакцию окисления молекулярного водорода, а также реакцию восстановления протонов до водорода:
H2 ↔ 2H+ + 2e-.
Интерес к исследованию систем, основанных на ферменте гидрогеназы, связан с тем, что молекулярный водород считается сегодня наиболее перспективным химическим топливом, в частности, для топливных ячеек. Таким образом, ферментативный катализ на основе фермента гидрогеназы является одним из перспективных способов получения молекулярного водорода.
Выбор мезопористых плёнок диоксида титана в качестве подложки для иммобилизации фермента был обусловлен тем, что за счёт пористости диоксида титана достигается высокая площадь поверхности, многократно ( ∼ 1000 ) превышающая геометрическую площадь [4]. Эта большая поверхность с порами размеров, схожих с размером молекул фермента, позволяет адсорбировать большое количество фермента без потери его структурных свойств и активности.
Ключевыми вопросами в работе таких систем являются возможность иммобилизации фермента на полупроводник без потери структуры и активности фермента, а также возможность эффективного переноса заряда с полупроводника на активный центр фермента.
Целью данной работы является исследование электрохимическими методами нанобиокатализаторов на основе мезо- пористых плёнок из нанокристаллов TiO2 с иммобилизованными белковыми глобулами фермента гидрогеназы из бактерий Thiocapsa roseopersicina.
-
II. Экспериментальная часть
-
II.1. Материалы
-
В работе использовалась гидрогеназа из пурпурных бактерий Thiocapsa roseopersicina, штамм BBS (молекулярный вес 63 Кда, состоит из двух субъединиц, содержит два редокс-центра: кластер Fe 4 S 4 и Ni-центр).
-
II.2. Приготовление мезопористых плёнок TiO2
Для получения мезопористых плёнок TiO 2 использовали промышленный порошок окиси титана: Aeroxide P25 (Degussa, Германия). Данный порошок, представляющий собой кристаллическую фазу, на 85% состоит из анатаза, на 15% из рутила. Средний размер частиц порошка 25 нм, удельная поверхность около 50 м 2 / г.
Приготовление плёнок TiO 2 включает в себя следующие стадии.
-
1. Приготовление пасты: порошок окиси титана смешивали с полиэтилен гликолем (молекулярная масса 20 000) и ацетил-ацетоном C 5 H 8 O 2 ( 1 • 10 ~ 8 моль / л) на основе 0 , 25% водного раствора ПАВ (Triton X-100). Массовая доля окиси титана в пасте составляла 40% . В качестве порообразующего агента использовали полиэтилен гликоль PEG 20 000, в количестве 10% от массы TiO 2 . Ацетилацетон брали в количестве 3% от массы TiO 2 .
-
2. Ультразвуковое диспергирование: приготовленную пасту подвергали ультразвуковому диспергированию в течение 1 часа.
-
3. Нанесение пасты: полученную пасту наносили на проводящее стекло ITO методом наката.
-
4. Отжиг плёнок: для предотвращения растрескивания плёнок высушивали их на воздухе в течение 5–15 минут. Затем для удаления органических примесей плёнки отжигали в муфельной печи при 450 ° C в течение 1 часа.
Таким образом, были получены полупрозрачные плёнки TiO 2 толщиной около 8 мкм (рис. 1, 2).
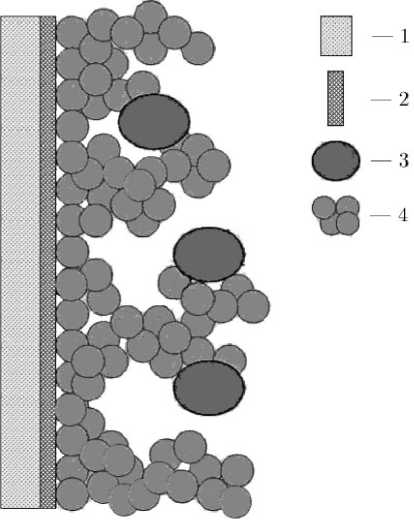
Рис. 1. Схема рабочего электрода с иммобилизованной гидрогеназой: 1 — стекло, 2 — проводящее покрытие ITO, 3 — фермент, 4 — ме-зопористая плёнка диоксида титана

Рис. 2. Морфология мезопористых плёнок диоксида титана. Снято на сканирующем электронном микроскопе JSM35C (JEOL). Длина маркера на фотографии — 1 мкм
Далее на полученные плёнки адсорбировалась гидрогеназа. Адсорбция происходила при выдерживании плёнки в растворе гидрогеназы в течение 2–4 суток при температуре 4 ° C .
-
II.3. Электрохимическая ячейка
Используемая в работе электрохимическая ячейка представляет собой стеклянный сосуд, закрытый от падающего света металлической фольгой, герметично закрытый резиновой крышкой и заполненный электролитом. В качестве раствора электролита во всех проведённых экспериментах использовался раствор pH = 7,2, содержащий 0,1 М KCl и трис-буфер. Часть экспериментов была проведена с добавлением в раствор дополнительного переносчика зарядов метилвиологена МВ2+. Концентрация метилвиологена в растворе составляла 10-3 М.
-
III. Результаты и их обсуждение
-
III.1. Электрохимические измерения
Все эксперименты в работе были проведены по трёхэлектродной схеме, где в качестве рабочих электродов использовались мезопористые плёнки диоксида титана, приготовленные, как описано выше, с иммобилизованной на них гидрогеназой, а также мезопористая плёнка диоксида титана без иммобилизованной гидрогеназы. В качестве электрода сравнения нами был использован каломельный электрод ЭСр-10101, потенциал которого составлял 202 ± 3 мВ относительно нормального водородного электрода. Все окислительновосстановительные потенциалы в работе представлены относительно каломельного электрода ЭСр-10101. В качестве противо-электрода использовалась платиновая сетка. Внутри ячейки в течение опыта, благодаря непрерывному продуву, поддерживалась водородная или аргоновая атмосфера в зависимости от эксперимента. Все эксперименты были проведены при комнатной температуре. Электрохимические измерения проводились при помощи потенциостата PS-7.
-
Основной задачей электрохимических измерений в работе было получение циклических вольт-амперных характеристик при разных скоростях развёртки потенциала в аргоновой или водородной атмосферах.
-
III.2. Эксперименты с использованием метилвиологена в качестве дополнительного переносчика заряда
Предварительно нами была измерена активность нашего рабочего электрода. Активность измеряли по восстановлению метилвиологена водородом в реакции, катализируемой гидрогеназой, на поверхности рабочего электрода при продуве ячейки водородом. В контрольном эксперименте нами было показано, что метилвиоло-ген не восстанавливается водородом в отсутствие активной гидрогеназы. В реальном времени измеряли спектры поглощения раствора, и по кинетике окрашивания раствора вычислялась скорость реакции, А = 610 нм. Скорость реакции восстановления метилвиологена составила 7,25 • 10~10 моль/с • см2 • л.
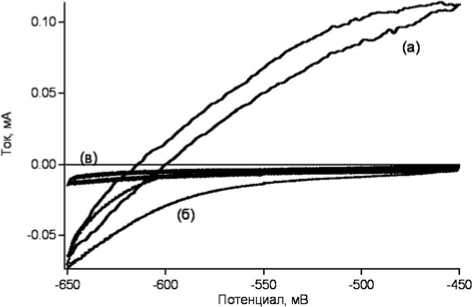
Рис. 3. Циклические вольт-амперометрические характеристики, снятые на электроде с иммобилизованной гидрогеназой в присутствии метилвиологена: (а) — в атмосфере водорода; (б) — в атмосфере аргона; (в) — циклическая вольт-амперная характеристика электрода без иммобилизованной гидрогеназы. Все потенциалы даны относительно каломельного электрода, pH раствора составлял 7 , 2
На рис. 3 изображены характерные циклические вольт-амперные характеристики электродов диоксида титана с иммобилизованной гидрогеназой, снятые в аргоновой (рис. 3б) и в водородной (рис. 3а) атмосферах, а также циклическая вольт-амперная характеристика плёнки диоксида титана в водородной атмосфере (рис. 3в), при скорости развёртки потенциала 2 мВ/с. Как видно из этой картинки, иммобилизация фермента приводит к существенному изменению тока в системе, что свидетельствует о каталитическом окислении/восстановлении (при соответствующем потенциале) водо-рода/протонов на электроде при катализе на гидрогеназе. Как видно из рис. 3, как в аргоновой, так и в водородной атмосфере наблюдается появление катодного тока, который свидетельствует о каталитической реакции восстановления протонов водной среды. Из рис. 3 видно, что присутствие в эксперименте водорода существенно изменяет вид характеристики для электрода с ферментом. Наблюдается появление анодного тока в области от -600 мВ до -450 мВ относительно каломельного электрода. В этом диапазоне потенциалов в эксперименте, проведённом в аргоновой атмосфере, анодный ток не наблюдается. Анодный ток, зафиксированный в эксперименте в атмосфере водорода, хорошо согласуется с полученными для различных подложек каталитическими токами окисления водорода гидрогеназой [5]. Таким образом, можно сделать вывод, что регистрируемый анодный ток характеризует реакцию окисления водорода ферментом гидрогеназой на поверхности нашего электрода в присутствии метилвиологена в растворе. То есть, в этом эксперименте зафиксирован каталитический ток окисления водорода на поверхности мезопористой плёнки диоксида титана с иммобилизованной гидрогеназой в присутствии метилвиологе-на, который выступает в качестве переносчика электрона между электродом и ферментом. По плотности тока, зарегистрированного в эксперименте, нами была оценена скорость реакции окисления водорода. Она составила 6,25 · 10-10 моль/с · см2 · л. Этот результат хорошо согласуется с результатом, полученным для реакции восстановления метилвиологена.
Одним из основных параметров, характеризующих кинетические возможности электрода, является ток обмена. Этот параметр характеризует равенство скоростей реакции в прямом и обратном направлениях и отображается силой тока, отнесённой к единице поверхности (плотностью тока). Анализ был проведён в рамках исследования таффелевской зависимости. Была построена зависимость ln I кат от сдвига потенциала по отношению к равновесному согласно уравнению
Iкат = I0 exp(αnF η/RT),
ln Iкат =lnI0 + αnF η/RT, где η = Ep - E — сдвиг потенциала электрода по отношению к его равновесному значению, α — эмпирическая постоянная, называемая коэффициентом переноса (0 С а С 1), T — абсолютная температура, F — постоянная Фарадея, R — газовая постоянная.
Ток обмена был рассчитан по экстраполяции таффелевского сегмента этой зависимости и составил I 0 = 78 мкА / см 2 . Известные из литературы токи обмена для электродов на основе угольных электродов с иммобилизованной гидрогеназой из пурпурных бактерий Thiocapsa roseopersicina составляют порядка 40 мкА / см 2 электрода [5].
-
III.3. Эксперименты без использования дополнительного переносчика заряда
На рис. 4 представлена циклическая вольт-амперная характеристика электрода с ферментом в водородной атмосфере, однако этот эксперимент был проведён без метилвиологена. На этом рисунке видно, что нам также удалось зафиксировать как ток окисления водорода, так и ток восстановления протонов среды. Отличие от предыдущего эксперимента состоит лишь в значениях полученных сил токов. По сравнению с предыдущим экспериментом значения сил токов упали в 2–3 раза. Этот результат имеет принципиальное значение, так как в этом опыте зафиксирован прямой перенос электрона от твёрдого тела — полупроводника TiO 2 — к активному каталитическому центру гидрогеназы.
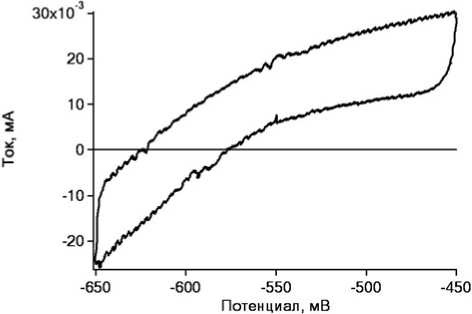
Рис. 4. Циклические вольт-амперометрические характеристики, снятые на электроде с иммобилизованной гидрогеназой в атмосфере водорода в отсутсвие метилвиологена
-
III.4. Повторная активация электрода
Как известно, фермент может терять свою активность при окислении активного центра кислородом воздуха [6]. Этот вопрос имеет важное значение для исполь- зования гидрогеназы в технических приложениях. Поэтому интересным представлялся также вопрос о возможной повторной его активации при воспроизводимости активности фермента. Нами был проведён эксперимент, когда после снятия циклических вольт-амперных характеристик электрод оставлялся на воздухе на сутки, происходила его дезактивация, затем электрод помещался в водородную атмосферу на три часа, после чего вновь проводился эксперимент. Как видно на рис. 5, в течение трёх дней нам удавалось реактивировать электрод без потери его активности.
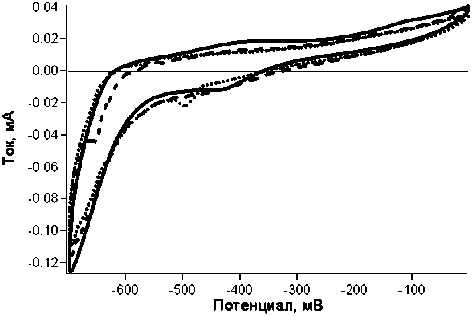
Рис. 5. Циклические вольт-амперометриче- ские характеристики, снятые на электроде с иммобилизованной гидрогеназой в атмосфере водорода, 1-й день — сплошная линия, 2-й день — точки, 3-й день — пунктир
-
IV. Выводы
В настоящей работе впервые электрохимическими методами показано, что гидрогеназа из пурпурных бактерий Thiocapsa roseopersicina, иммобилизованная на мезопористую плёнку диоксида титана, проявляет каталитическую активность. Продемонстрирована каталитическая реакция восстановления протонов среды до водорода, которая протекает как в атмосфере аргона, так и в атмосфере водорода, то есть водород как продукт реакции не подавляет активность гидрогеназы из пурпурных бактерий Thiocapsa roseopersicina по отношению к реакции восстановления. Показана реакция окисления молекулярного водорода при потенциалах более положительных по сравнению с равновесным потенциалом H + / H 2 .
Установлено, что при использовании метилвиологена в качестве переносчика электронов, ток обмена составляет 78 мкА / см 2 .
Показано, что происходит реакция прямого переноса электрона от твёрдого тела — полупроводника TiO2 — к активному каталитическому центру гидрогеназы из пурпурных бактерий Thiocapsa roseopersicina.


