Каталитическое окисление серосодержащих соединений
Автор: Батоева Агния Александровна, Цыбикова Бэлэгма Амоголоновна, Будаев Саян Львович
Журнал: Вестник Бурятского государственного университета. Философия @vestnik-bsu
Рубрика: Химия
Статья в выпуске: 3, 2011 года.
Бесплатный доступ
Изучены основные закономерности каталитического окисления тиоцианатов и тиосульфатов пероксидом водорода в присутствии ионов Fe3+ и Cu2+. Представлены результаты по обезвреживанию реальных технологических растворов од- ной из золотоизвлекательных фабрик.
Цианиды, тиоцианаты, тиосульфаты, окисление
Короткий адрес: https://sciup.org/148180227
IDR: 148180227 | УДК: 66.074.3:
Catalytic oxidation of sulfur-containing compounds
The synergistic combined effect of Fe3+ and Cu2+ on catalytic destruction of thiocyanates and thiosulfates by hydrogen peroxide was revealed. The results on dehydration of real technological solutions of one of the gold extraction plants were shown.
Текст научной статьи Каталитическое окисление серосодержащих соединений
Высокие концентрации тиоцианатов, как правило, наблюдаются при цианидном выщелачивании упорных золотосодержащих сульфидных руд или флотоконцентратов [1]. Тиоцианаты (SCN-) образуются при проведении процессов цианидного выщелачивания золота как продукт реакции между цианид-ионами (CN-) и соединениями серы, включая элементарную серу [2]:
S0 + CN- → SCN- (1)
-
S2- + CN- + H 2 O + ½ O 2 → SCN- + 2OH- (2) S 2 O 3 2- + CN- → SO 3 2- + SCN- (3)
В зависимости от содержания серы и количества оборотных циклов концентрация тиоцианатов в технологических растворах (сточных или оборотных водах) может составлять от нескольких миллиграммов до нескольких граммов на 1 л. Образование тиоцианатов приводит к увеличению расхода NaCN при цианировании и негативно влияет на процессы сорбционного выщелачивания золота [3]. Для обезвреживания цианидсодержащих технологических растворов золотоизвлекающих фабрик (ЗИФ) широко применяются: обработка активным хлором, кислородом в присутствии солей меди, так называемый INKO-процесс, озонирование, обработка солями железа с целью перевода токсичных цианидов в устойчивые нерастворимые соединения, а также их различные комбинации [4-9]. Особенностью тиоцианатов является их токсичность для аквасистем и устойчивость к разложению большинством методов, применяемых для обезвреживания цианидов. Поэтому проблема глубокой доочистки сточных или оборотных растворов от тиоцианатов является актуальной.
В последние годы определилось принципиально новое направление в практике очистки сточных вод комбинированными окислительными методами «Advanced Oxidation Processes», получившее название АОР–методы [10], суть которых заключается в жидкофазном окислении примесей высокореакционными частицами – формами активного кислорода, в первую очередь ОН–радикалами. Из комбинированных методов для практической реализации весьма привлекательной и перспективной является окислительная деструкция пероксидом водорода, поскольку при его восстановлении получаются кислород и вода, а в присутствии катализаторов – металлов переменной валентности (Fe3+, Cu2+) – реализуются условия для проведения редокс-каталитических процессов окисления тиоцианатов [11]. С учетом того, что примерно 50% цианида безвозвратно теряется за счет образования тиоцианатов, проблема регенерации цианида из тиоцианатных растворов носит не только экологический, но и экономический характер [12].
При взаимодействии тиоцианатов с пероксидом водорода в зависимости от рН среды и концентрации пероксида водорода возможно их окисление как до цианид-, так и до цианат-ионов [13-15]. Известно, что при рН>4 разложение тиоцианат ионов SCN- идет с получением цианид- и сульфат-ионов [16]. При дальнейшем окислении образующийся цианат-ион постепенно гидролизуется по уравнению:
CNO- + 2H 2 O → CO 3 2- + NH 4 +, (4)
либо может быть окислен далее до элементарного азота и диоксида углерода [13]. При низких же значениях рН<4 окисление SCN- идет c образованием цианистоводородой кислоты, которая в значительно меньшей степени подвергается дальнейшему гидролизу до цианат-иона:
SCN- + 3H 2 O 2 → HSO 4 2- + HCN + + 2H 2 O. (5)
Ранее на модельных и реальных тиоцианатсодержащих технологических растворах было показано, что окислительная деструкция SCN- наиболее эффективна при рН<3 и позволяет вернуть в производство дополнительное количество цианида [17-19].
Целью настоящей работы являлось исследование влияния серосодержащих соединений, поскольку они являются продуктом окисления сульфидов и сопутствующим поллютантом сточных и оборотных вод ЗИФ при добыче драгметаллов из упорных сульфидных руд, в частности тиосульфатов, на окисление тиоцианатов пероксидом водорода с использованием катализаторов (Fe3+, Cu2+) и обезвреживание реальных технологических растворов одной из золотоизвлекательных фабрик.
Экспериментальная часть
Для экспериментов с модельными растворами использовали реактивы марки «хч». Окисление тиоцианатов проводили при начальных концентрациях [SCN-]=17 ммоль ⋅ л-1 (1000 мг/л) и [S2O32-]=4.5 ммоль ⋅ л-1 (500 мг/л) при стехиометрически необходимой концентрации окислителя [H 2 O 2 ] 0 =51 ммоль ⋅ л-1. Состав реальной оборотной воды ЗИФ из наливного хвостохранилища ОАО «Березитовый рудник» представлен в таблице 1.
Концентрации тиоцианатов определяли фотометрированием соответствующего комплекса [20], цианидов – фотометрическим методом с пиридином и барбитуровой кислотой [21], а тиосульфатов – йодометрическим методом [22]. Атомно-абсорбционное определение ионов тяжелых металлов проводили на приборе ААS Perkin Elmer 3110. Для контроля значений рН и температуры использовали иономер рН 150-М. Для исследования полноты улавливания образующихся цианидов проводили количественный анализ на массовое содержание цианидов в поглотительном растворе [21]. Каталити- ческое окисление тиоцианатов проводили в стеклянном реакторе в статических условиях с непрерывным барботажем воздуха. В качестве катализаторов использовали растворы соответствующих солей Fe3+ и Cu2+ .
Таблица 1
Состав оборотной воды ЗИФ
|
№ п/п |
Параметры |
С, мг/л |
|
1 |
рН |
11.3 ± 0.2 |
|
2 |
Тиоцианаты |
752.0 ± 97.8 |
|
3 |
Цианиды |
272.6 ± 43.6 |
|
4 |
Тиосульфаты |
655.2 ± 98.3 |
|
5 |
Железо |
33.4 ± 7.7 |
|
6 |
Медь |
262 ± 65 |
|
7 |
Цинк |
48.3 ± 9.7 |
|
8 |
Никель |
0.620 ± 0.105 |
|
9 |
Свинец |
не обн. |
|
10 |
Хром |
0.034 ± 0.009 |
|
11 |
Кобальт |
0.628 ± 0.126 |
|
12 |
Кадмий |
0.043 ± 0.011 |
|
13 |
Кальций |
133 ± 13 |
Результаты и обсуждение
Механизм превращения SCN- достаточно сложен. Прямое окисление SCN- пероксидом водорода протекает довольно медленно, и чтобы ускорить процесс получения HCN, требуется введение в систему катализатора [23]. Изменение концентрации катализатора существенным образом сказывается на глубине и скорости реакции окисления тиоцианатов (рис. 1, табл. 2). Ранее были установлены оптимальные условия полной конверсии тиоцианатов до стадии образования цианистоводородой кислоты в присутствии ионов Fe3+: рН 2.8, мольные соотношения [H 2 O 2 ]: [SCN-]:[Fe3+]=3:1:0.2 [24]. Полная конверсия тиоцианатов наблюдается при концентрации [Fe3+]=3.6 ммоль/л. Однако аналогичного результата можно добиться при меньшей концентрации железа с использованием каталитической системы {Fe3+ + Cu2+} (рис. 1, табл. 2).
Подобный эффект можно объяснить тем, что при каталитическом окислении тиоцианатов в присутствии ионов железа небольшие добавки ионов меди генерируют гидроксильные и супероксидные радикалы по дополнительным маршрутам. В присутствии же тиосульфатов скорость и полнота реакции значительно изменяются (рис. 2): тиосульфат–ионы оказывают негативное влияние на процесс деструкции тиоцианатов, которое проявляется как за счет расходования окислителя, так и нецелевого расходования катализатора. При подкислении до рН≤3 раствора, содержащего тиоцианаты и тиосульфаты, появляется небольшое количество белого осадка. Тиосульфаты медленно разлагаются с образованием элементарной серы и сульфитов в соответствии с реакцией диспропорционирования [25]:
S2O32- + H+ = S0 + HSO3-(6)
При добавлении в раствор ионов металлов (Cu2+ или Fe3+) имеет место более быстрое, конкурирующее с тиоцианатами, окисление тиосульфатов по реакциям:
Cu2+ + S2O32- → CuS2O3 + S2O32- = S4O62-+ Cu+(7)
2Fe3+ + 2 S2O32- → 2FeS2O3+ = S4O62- + 2Fe2+(8)
и практически на 100% продуктом окисления S 2 O 3 2- являются тетратионаты S 4 O 6 2- [11, 25-26]. При этом эффективность деструкции SCN- не превышает 80% даже через 60 мин обработки, в то время как степень конверсии самих тиосульфатов достигает 93% уже в течение первых пяти минут.
Поскольку тиосульфаты в присутствии ионов Fe3+ и Cu2+ окисляются с высокой скоростью и достаточно полно, можно утверждать, что лимитирующей стадией в данной системе{(SCN- + S 2 O 3 2-) + H 2 O 2 }, как было определено и в ранее рассмотренной цианидсодержащей – {(SCN- + CN-) + H 2 O 2 } [17], является реакция окисления тиоцианатов. Полного и достаточно быстрого окисления SCN- в растворе, содержащем S2O32-, можно добиться, увеличивая концентрацию ионов Fe3+ в реакционной смеси (табл. 3).
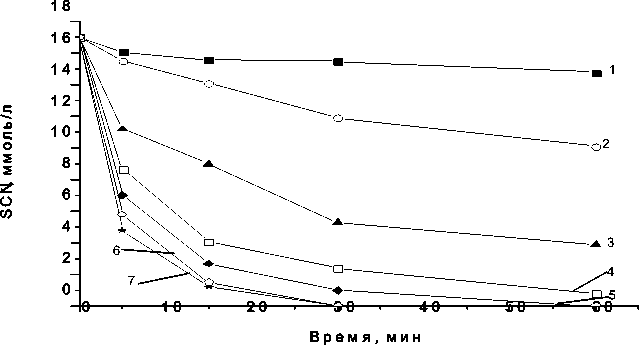
Рис. 1. Влияние концентрации ионов Fe3+ на процесс окисления SCN- пероксидом водорода: рH 2.8, [SCN-] 0 =17.2 ммоль ⋅ л-1, [H 2 O 2 ] 0 =51 ммоль ⋅ л-1, [Fe3+], ммоль ⋅ л-1 соответственно: 1 – 0.0, 2 – 0.45, 3 – 0.9, 4 – 1.8, 5 – 2.7, 6 – 2.7 (в присутствии [Cu2+]=0.78 ммоль ⋅ л-1), 7 – 3.6
Таблица 2
Зависимость начальной скорости реакции и эффективности окисления SCN- от концентрации Fe3+
|
Условия |
Fe3+, ммоль ⋅ л-1 |
W0,ммоль ⋅ л-1 ⋅ мин-1 |
Эффективность окисления, % |
|
[SCN-] o = 17.2ммоль ⋅ л-1 |
0 |
0.2 |
9.5 |
|
pH = 2.8 |
0.9 |
1.2 |
69.1 |
|
1.8 |
1.7 |
85.9 |
|
|
2.7 |
1.8 |
94.5 |
|
|
*[Cu2+]= 0.78 ммоль·л-1 |
3.6 |
2.4 |
100 |
|
2.7* |
2.2 |
100 |
* эффективность процесса рассчитана через 30 мин обработки
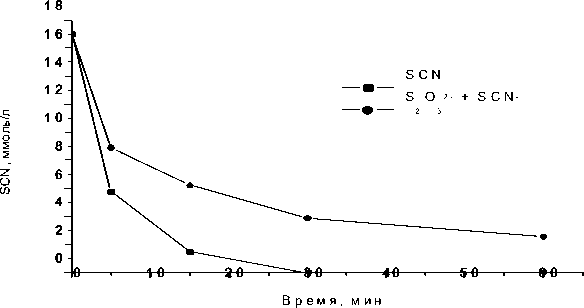
Рис. 2. Влияние S2O32- на процесс окисления SCN- пероксидом водорода в присутствии {Fe3++ Cu2+}: рH 2.8, [SCN-] 0 =17.2 ммоль ⋅ л-1, [S 2 O 3 2-] 0 =4.5 ммоль ⋅ л-1, [H 2 O 2 ] 0 =51 ммоль ⋅ л-1, [Fe3+]=2.7 ммоль ⋅ л-1, [Cu2+]=0.78 ммоль ⋅ л-1
Полученные данные свидетельствуют о том, что при [S2O32-] ≤ 4.5 ммоль/л и [Fe3+] ≥ 3.6 ммоль/л весь пероксид водорода расходуется на окисление тиоцианатов, а тиосульфаты окисляются по реакциям (7) и (8). Увеличение начальной концентрации тиосульфатов до 9.0 ммоль/л приводит к снижению W0 до 1.6 ммоль/л ⋅ мин и степени конверсии тиоцианатов до 88% за 30 мин. Очевидно, что в этом случае Н 2 О 2 расходуется и на окисление тиосульфатов по реакции:
2S 2 O 3 2- + H 2 O 2 + 2H+ = S 4 O 6 2- + 2H 2 O (9)
Таблица 3
Зависимость начальной скорости реакции и эффективности окисления SCN- в присутствии [S2O32-] от концентрации Fe +
|
Условия |
[Fe3+], ммоль - л |
W 0 , ммоль - л-1 - мин-1 |
[S 2 O 3 2-], моль - л |
Эффективность окисления, % |
|
|
SCN- |
S 2 O 3 2- |
||||
|
[SCN-] o = 17.2 ммоль - л [Cu2+]= 0.78 ммоль·л pH = 2.8 |
0 |
0.2 |
4.5 |
9.5 |
|
|
2.7 |
1.8 |
94.0 |
95.5 |
||
|
3.6 |
2.4 |
100 |
100 |
||
|
4.5 |
2.6 |
100 |
100 |
||
|
3.6 |
1.6 |
9.0 |
88 |
85.9 |
|
Примечание : эффективность процесса рассчитана через 30 мин обработки
Согласно полученным данным, оптимальными условиями можно считать: рН<3, мольные соотношения [H 2 O 2 ]:[SCN-]=3:1, [SCN-]:[Fe3+]: [Cu2+]=5:1:0.2 [27]. Сравнение процессов окисления серосодержащих соединений SCN- + S2O32- при их совместном присутствии пероксидом водорода с использованием катализаторов Fe3+, Cu2+ и каталитической системы {Fe3++ Cu2+}, а также расчет синергического индекса свидетельствуют о взаимном положительном влиянии ионов железа и меди. Так, значение синергического индекса, рассчитанного по формуле, равно 1.5÷1.7 (рис. 3):
r rf ( ПВ + Fe ( III ) + Cu ( II ))
f(Fe (III )Cu (II )) = ;---------------—-------------, rf (ПВ + Fe (III )) + rf (ПВ + Cu (II ))
где f (Fe(II)+Cu(II)) – синергические индексы; r f – конверсия тиоцианатов или тиосульфатов через 5 мин; f = 1 – аддитивность; f > 1- синергизм
В таблице 4 представлены результаты экспериментов на реальной воде ЗИФ из наливного хвосто-хранилища ОАО «Березитовый рудник» (Амурская область) (табл. 1). Отработанная технологическая вода предварительно обрабатывалась по AVR-методу (регенерационный метод), т.е. воду подкисляли до рН < 3.0, далее подвергали барботажу кислородом воздуха с целью отдувки образующейся HCN и поглощения ее раствором щелочи. Подробное описание технологии извлечения цианидов из отработанных растворов цианирования сульфидных флотоконцентратов представлено в работах [18-19, 28]. После проведения AVR-процесса вода подвергалась обработке пероксидом водорода в присутствии катализаторов.
Таблица 4
Результаты очистки модельных растворов и реальных оборотных вод ЗИФ
|
Показатели |
Модельный раствор |
Производственная вода |
||||||
|
AVR |
*Окисление H 2 O 2 |
|||||||
|
S 2 O 3 2- |
SCN" |
CN- |
S 2 O 3 2- |
SCN" |
S 2 O 3 2- |
SCN" |
||
|
Сисх, мг/л |
500 |
1000 |
272.6 |
655.2 |
752.0 |
649.4 |
735.2 |
|
|
Сост, мг/дм3 через t, мин. |
5 |
39.0 |
339.7 |
- |
- |
- |
57.4 |
373.2 |
|
15 |
37.4 |
89.12 |
- |
- |
- |
45.9 |
252.3 |
|
|
30 |
36.7 |
отс. |
- |
- |
- |
40.2 |
116.9 |
|
|
60 |
36.7 |
отс |
отс. |
649.4 |
735.2 |
40.2 |
26.7 |
|
|
Эффективность, % |
94.2 |
100 |
96 |
1.2 |
3.4 |
93.8 |
92.4 |
|
*мольные соотношения [H2O2]:[SCN-]=3:1, [SCN-]:[Fe3+]: [Cu2+]=5:1:0.2
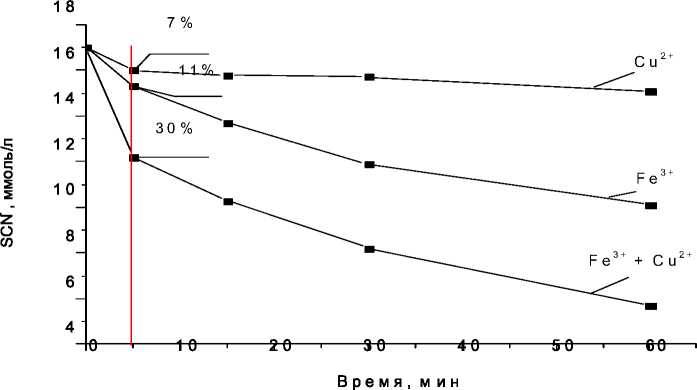
Рис. 3. Влияние ионов Fe3+ и Cu2+ на процесс окисления SCN- пероксидом водорода: рH 2.8, [SCN-]0=17.2 ммоль ⋅ л-1, [S 2 O 3 2-] 0 =4.5 ммоль ⋅ л-1, [H 2 O 2 ] 0 =51 ммоль ⋅ л-1. 1 – [Cu2+]=0.38 ммоль ⋅ л-1, 2 – [Fe3+]=0.44 ммоль ⋅ л-1, 3 – [Cu2+] + [Fe3+]
Выводы
Изучены основные закономерности каталитического окисления тиоцианатов и тиосульфатов пероксидом водорода в присутствии ионов Fe3+ и Cu2+. Лимитирующей стадией является реакция окисления тиоцианатов. Определены оптимальные мольные соотношения ионов металлов в используемой каталитической системе: [SCN-]:[Fe3+]: [Cu2+]=5:1:0.2. Выявлен синергизм совместного действия ионов металлов в каталитической системе {Fe3+ и Cu2+} при окислении тиоцианатов и тиосульфатов пероксидом водорода. Полученные результаты подтверждают перспективность применения комбинированного окислительного метода, заключающегося в обработке воды пероксидом водорода в присутствии ионов железа (III) и меди (II) для обезвреживания серосодержащих соединений сточных или оборотных вод ЗИФ.