Кинетика бейнитного превращения в малоуглеродистых сплавах железа
Автор: Мирзаев Д.А., Окишев К.Ю.
Журнал: Вестник Южно-Уральского государственного университета. Серия: Металлургия @vestnik-susu-metallurgy
Статья в выпуске: 24 (124), 2008 года.
Бесплатный доступ
Работа поддержана грантом Президента РФ МК-3549.2007.8 и грантом НШ-5965.2006.3.
Короткий адрес: https://sciup.org/147156590
IDR: 147156590 | УДК: 669.017.3
Текст научной статьи Кинетика бейнитного превращения в малоуглеродистых сплавах железа
В работе [1] было показано, что специфические особенности строения пакетного мартенсита -иерархической структуры, где отдельные кристаллы рейки группируются в блоки и далее в пакеты -должны оказывать влияние на кинетику аустенит—>мартенситного превращения. Бейнит, особенно в сплавах с низким содержанием углерода, также представляет собой сложно организованную пакетную структуру, поэтому можно ожидать, что подобные особенности должны наблюдаться и для него.
Кинетику превращения в мы описывали при помощи уравнения Аврами
/ = 1-ехрН&”), (1) где / - доля превращения, t - время изотермической выдержки, а К и и -коэффициенты. Как показано в [1], для иерархической пакетной структуры показатель и должен уменьшаться в ходе превращения от 2 или 3 до 1.
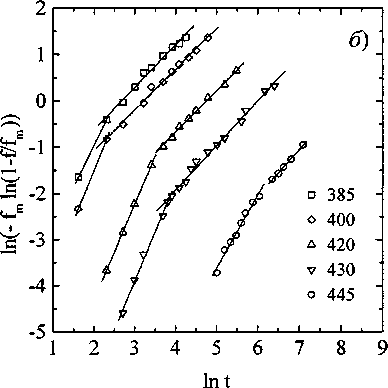
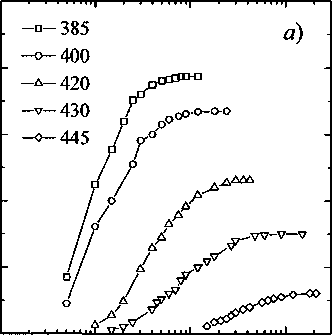
На рис. 1, а приведены кинетические кривые образования бейнита в сплаве Fe-9 % Сг, содержащем 0,09 % С (09X9) [2]. На рис. 1, б они, аналогично [1], представлены в двойном логарифмическом масштабе, что позволяет найти коэффициенты и и К:
In -A in
= 1п£+и1пГ
(здесь А - предельная доля превращения при данной температуре). На графиках действительно наблюдается изменение наклона; значения коэффициентов пи К приведены в таблице.
В отличие от мартенситного, при бейнитном превращении скорость роста отдельного реечного кристалла имеет конечную величину. Тогда, например, для и=2 параметр К будет равен
к=Ш,
1,0
0,8
0,6
0,4
0,2
0,0
1 10 100 1000
t, с
Рис. 1. Кинетические кривые образования бейнита в сплаве 09X9: а - в линейном масштабе; б - в двойном логарифмическом масштабе. Температуры превращения (в °C) указаны на рисунке
Таблица 1
Значения предельной доли превращения fm и коэффициентов п и In К для сплава 09X9 при различных температурах
|
Температура, °C |
А |
Значения коэффициентов в выражениях |
|||
|
(2) |
(18) |
||||
|
п |
1пХ |
п |
In Л" |
||
|
385 |
0,775 |
1,81/0,91 |
—4,57/—2,44 |
2,20/1,00 |
—4,95/—2,40 |
|
400 |
0,67 |
2,19/0,88 |
—5,86/—2,82 |
2,19/1,00 |
—5,86/—3,04 |
|
420 |
0,462 |
2,08/0,90 |
—8,46/—4,27 |
2,08/1,00 |
-8,46М,61 |
|
430 |
0,30 |
2,13/0,97 |
—10,3/-5,81 |
2,13/1,00 |
-10,3/—5,91 |
|
445 |
0,122 |
1,59/1,01 |
—11,6/-8,10 |
2,00/1,00 |
-13,5/-8,01 |
Примечание: в числителе указаны значения на первом этапе превращения, в знаменателе - на втором этапе.
если автокаталитическое зарождение является более медленным процессом, чем рост рейки, и
К = кг1н<Вр1р (4)
в противном случае. Здесь /н - скорость независимого зарождения первых реек пакета; 7а - скорость автокаталитического зарождения элементов пакета; Гор - скорость роста реечного кристалла в длину; /р и Кр - его средняя длина и объем. Через кх и кг обозначены численные коэффициенты.
По поводу соотношения процессов зарождения и роста при бейнитном превращении в литературе встречаются разные мнения. По мнению Хиллерта [3], хотя рейки в макрокристалле и объединены автокаталитическим зарождением, но лимитирующим процессом является все же рост. Бхадешиа [4], напротив, полагает, что рост субъединиц происходит с большой скоростью, а кинетика превращения аустенит—>бейнит лимитируется зарождением. Авторы данной работы считают, что обе точки зрения можно примирить, если, во-первых, для кинетического коэффициента К использовать формулу (3), отражающую эффект автокаталитического зарождения субъединиц бей-нитной пластины [5, 6], а во-вторых, в гипотезе Бхадешиа учесть, что скорость зарождения зависит от вероятности перехода атома через межфазную границу (Р+-Р_), где Р+ - вероятность присоединения атома к растущему зародышу, а Р_ - вероятность обратного перехода [7]. Добавление атома к зародышу на площади с? вызывает увеличение объема на с^, то есть продвижение фронта превращения вперед на расстояние d, чему соответствует скорость
®=d(P+-P_), (5)
где d примерно равно межатомному расстоянию. Так как вероятность (Р+-Р-) пропорциональна скорости роста, то скорость независимого и автокаталитического зарождения также должна быть пропорциональна скорости роста. Мы будем определять их следующим выражением:
IH4Njd>ex^-W[RTV (6, а)
Ia = (Njd^exp^W-E^/RT^, (6, б)
где NH и Na - количество соответствующих потенциальных мест зарождения в единице объема, Ж -энергия активации зарождения, а величина Е учитывает автокаталитический эффект.
Энергетический барьер зарождения в рамках теории Кауфмана-Коэна [8] можно записать как
W = WO-^^G = Ф-^^G-^GSY д^
где AG - изменение свободной энергии при образовании новой фазы, a AGS - термодинамический стимул превращения при Т=Т# который отражает необходимость энергетических затрат для начала превращения. Хиллерт [9], приняв во внимание возможность обратных переходов атомов через границу, предложил заменить в (6) множитель
/ / dti л Г Ф kG—AG ехр(-Ж/7?Г) на Вехр ——--L- v RT) RT
Бейнитный феррит, образующийся в сталях, имеет, как правило, концентрацию углерода х“ более низкую, чем у исходного аустенита Хс=х0, причем х“<х^«1, а содержание элементов замещения (например, хрома) в у- и a-фазах остается неизменным. Изменение свободной энергии при образовании зародыша феррита в бинарном сплаве Fe-C определяется выражением
AG=x“^-p“)+(l-x“)(^-p“e), (8) где ц - химические потенциалы углерода и железа в у- и a-фазе, которое в [3] было преобразовано к виду
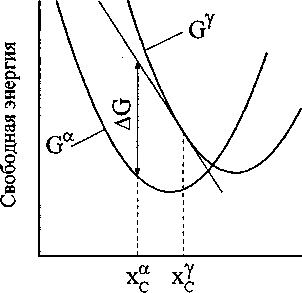
AG = О' (x^-G*(х“)-(х* -Хс )^- (9) Геометрический смысл выражения (9) иллюстрирует рис. 2. Все необходимые термодинамические данные для расчета AG приведены в [10].
Концентрация углерода
Рис. 2. Изменение молярной свободной энергии при зарождении a-фазы, концентрация которой отлична от концентрации у-фазы (схема)
Рассчитанные зависимости свободной энергии зарождения a-фазы от концентрации углерода в а-зародыше имеют максимум, который соответствует очень низкой концентрации углерода. Во многих работах [11, 12] предполагается, что зародыш ос-фазы имеет состав, отвечающий этому максимуму. Тогда bG«bG;;acr-RTx0. (io)
Согласно гипотезе Хиллерта, зарождение а-фазы может произойти, если AG>AGS- Если мы предполагаем, что в основе бейнитного превращения в стали лежит мартенситное превращение в безугле-родистом сплаве [13], то значение AGS должно быть таким же, как и при мартенситном превращении в основе. Верхняя температурная граница образования бейнита Ts определяется условием AG = AGS. Но если начало превращения в стали оценивается по разности свободных энергий у- и сс-фаз безуглеродистого сплава, то (AGFe.Cr) =EGs+RTsx0. Это выражение фактически означает, что верхняя температурная граница бейнитного превращения линейно снижается по мере роста концентрации углерода, что экспериментально показано в [10]. Помимо сомножителя, связанного с энергетическим барьером зарождения, скорость зарождения, по нашему предположению, зависит от скорости роста через вероятность перехода атомов через межфазную границу (6).
Проблема диффузионного роста кристаллов a-фазы из аустенита была рассмотрена Б.Я. Любо-вым [7]. Образование феррита включает перестройку кристаллической решетки, которую формально можно описать как переход атомов железа через межфазную поверхность под влиянием разности химических потенциалов железа в двух фазах, и диффузионный отвод атомов углерода от границы раздела фаз:
dt RTX 5е Ре где р - радиус кривизны растущего кристалла; Кх - коэффициент подвижности межфазной границы, а величина AGS включает энергию искажений и энергию поверхности раздела.
С другой стороны, по Хиллерту, если скорость роста определяется диффузионным потоком углерода от межфазной границы в глубь аустенита в условиях локального равновесия атомов углерода на самой границе, то
= (12)
8aKFe х0-х^
где Д, = Doexp(-Gc/7?7’) - коэффициент диффузии углерода в у-фазе; ст - межфазная поверхностная энергия; у^ - парциальный молярный объем железа в сплавах Fe-C.
Выравнивание скоростей роста, определенных соотношениями (11) и (12), происходит, на наш взгляд, благодаря установлению на межфазной границе таких поверхностных концентраций х^а и x“h, при которых величина ^pYe-p“e-AGs) в уравнении (11) оказывается малой. Мы примем ее равной нулю. Для сильно разбавленных растворов
14 = °14+ЯГ1п(1-ху/“)« “цк-ДГх^;
14 = °ц“е+ДПп(1-х^)« °ц“е -RTx^. (13) Следовательно, в нашем приближении
YHa _~ rr/a _24z!14z^4 J^?"^ , (14) с с с RT RT где AGY'a - разность свободных энергий у- и а-фаз чистого железа, которую следует заменить на AGF~aCr для сплава Fe-9 % Сг. Учет AGS приводит к уменьшению х^а по сравнению с равновесным значением; соответственно уменьшается и x“/Y. Если подставить выражение (14) в (12), то в числителе возникнет величина
Знаменатель формулы (12) зависит от разности х0-х^н. Когда х0^х“/у, скорость роста должна неограниченно возрастать. Однако эксперименты с быстрым охлаждением сплавов Fe-9%Cr [14] свидетельствуют о том, что снижение концентрации углерода от 6,09 до 0,007 % С еще не приводит к резкому увеличению критической скорости охлаждения, определяющейся скоростью роста, то есть для исследуемого сплава х0» х“/у.
Тогда с учетом (14)
Do (AG-AGJ2 ( Uc
—=2—2-----—-ехр -
8стКРех0 RT ( RT
В сущности, полученная формула отличается от аналогичной формулы для бездиффузионного роста степенью (AG - AGS).
Скорости зарождения (6) равны тогда с учетом поправки Хиллерта:
r NRD0 (EG-EGA3 ( Ф+UA , г =— нН о -------Д'-exp--^ , (16, а)
МоУВеха (КГ? ( RT )
r NRD0 (AG-AGJ3 ( Ф+и-Е} _ 1 =—^-2—5-----д'—exp-----^— - (16,6)
а &кУЕех0 (RT) I RT )
Обратим внимание на то, что третья степень свободной энергии возникла в выражениях (16) как произведение (AG-AGS)2, входящего в выражение для скорости диффузионного роста (а точнее, вероятности перехода атомов через межфазную границу), и (AG-AGS), входящего в энергетический барьер зарождения. Барьер зарождения при сдвиговых превращениях существенно зависит от плотности дефектов кристаллического строения и упругих напряжений в исходной фазе. Однако движущая сила диффузионного роста, по-видимому, не зависит (или зависит лишь в малой степени) от состояния превращающейся фазы. На это указывает хотя бы тот факт, что образование феррита, в отличие от бейнита и мартенсита, обычно доходит до конца, то есть до/= 1. Поэтому в более общем виде в выражениях (16) следует заменить (AG-AGS)3 на произведение (AG-AGg)E (AG-AG°)3~E, где AGg - термодинамический стимул начала превращения, который, как мы предполагаем, не зависит от количества накопленной фазы, а AGS - тер модинамический стимул зарождения, возрастающий с ростом / так что (AG-AGS) определяется формулой (17). В рассмотренном выше случае 8=1.
В [1] было сделано предположение, что термодинамический стимул AGS возрастает в ходе превращения, так что разность (AG-AGg) уменьшается с ростом степени превращения / и обращается в ноль при / = Уй • Подстановка этого выражения в формулы (6) позволяет найти взаимосвязь/и t; при еп Ф1
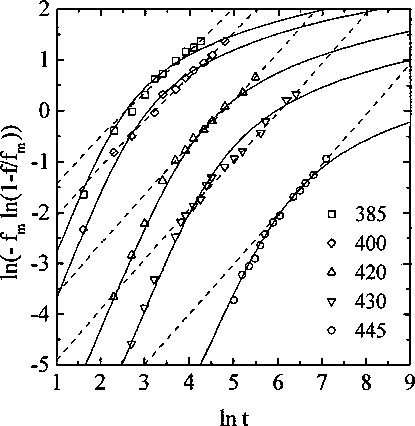
Рис. 3. Сравнение экспериментальных и рассчитанных по уравнениям (18) кинетических кривых образования бейнита. Сплошные линии - при п » 2, пунктирные линии - при л к 1
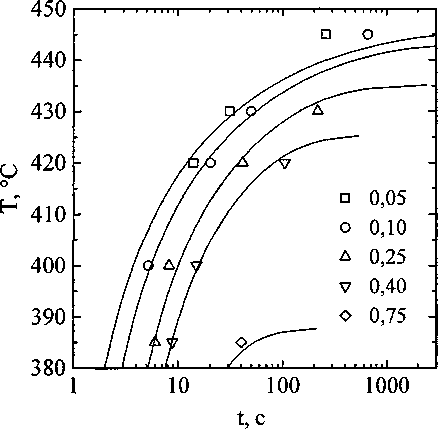
Рис. 4. С-образная диаграмма образования бейнита, рассчитанная по уравнениям (18), в сравнении с экспериментальными данными. Доли превращения указаны на графике
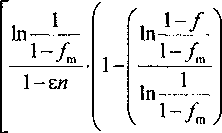
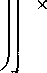
(18, а)
а при еи=1
t = k- ln(l-/m) ln 1--х
(rtV
X(ag-ags°)3
•exp
(18,6)
где Q - суммарная энергия активации превращения; kt - постоянный коэффициент. Формулы (18)
определяют развитие превращения во времени для любой фиксированной температуры.
На рис. 3 рассчитанные по уравнениям (18) кинетические кривые сравниваются с экспериментальными данными (при этом значения п и К были слегка скорректированы для улучшения согласия -см. таблицу).
Интересно, что теоретические кривые при п«2 хорошо согласуются с экспериментом и для тех значений/ для которых мы видели второй участок си»1 на рис. 1, б, то есть эффект уменьшения термодинамического стимула должен приводить к такому же кажущемуся уменьшению п.
Отложив значения 1п(к''" (RTf/(AG-AG°)3) в зависимости от обратной температуры, можно определить по наклону графика энергию актива- ции превращения Q. Найденная таким образом по значениям К из таблицы величина Q составила 85,3 кДж/моль.
Выражения (18) фактически описывают кинетическую диаграмму образования бейнита. На рис. 4 рассчитанная по (18) диаграмма сравнивается с экспериментальной (использованы следующие значения параметров: кр^ЛД6 с; е=1; и=2; 2=85,3 кДж/моль). Как видно, их согласие достаточно хорошее.
Таким образом, можно заключить, что подход, который мы предложили ранее для описания кинетики образования пакетного мартенсита, может быть использован и для бейнитного превращения.
Работа поддержана грантом Президента РФ МК-3549.2007.8 и грантом НШ-5965.2006.3.
Список литературы Кинетика бейнитного превращения в малоуглеродистых сплавах железа
- Мирзаев, Д.А. Кинетическая теория образования пакетного мартенсита/Д.А. Мирзаев, К.Ю. Окишев//Вестник ЮУрГУ. Серия «Металлургия». 2007. Вып. 9. № 21. С. 9-14.
- Кинетика образования бейнита и пакетного мартенсита. III. Бейнитное превращение в сплаве Fe-9% Сr/Д.А. Мирзаев, К.Ю. Окишев, В.М. Счастливцев, И.Л. Яковлева//ФММ. 2000. Т. 90, вып. 6. С. 72-82.
- Hillert, M. Diffusion and Interface Control of Reactions in Alloys/M. Hillert//Met. Trans. 1975. V.6A, N 1. P. 5-19.
- Bhadeshia, H.K.D.H. Bainite in Steels/H.K.D.H. Bhadeshia. London: The Institute of Materials, 1992. 468 p.
- Purdy, G.R. On the Nature of the Bainite Transformation in Steels/G.R. Purdy, M. Hillert//Acta Met. 1984. V. 32, N 6. P. 823-828.
- Formation of Bainite in Ferrous and Nonferrous Alloys Through Sympathetic Nucleation and Ledgewise Growth Mechanism/H.-S. Fang, J.-J. Wang, Z.-G. Yang et al.//Met. and Mat. Trans. 1996. V. 27A, N 6. P. 1535-1545.
- Любов, Б.Я. Кинетическая теория фазовых превращений/Б.Я. Любов. М.: Металлургия, 1969.-264 с.
- Кауфман, Л. Термодинамика и кинетика мартенситных превращений/Л. Кауфман, М. Коэн//Успехи физики металлов. М.: Металлургиздат, 1961. Вып. IV. С. 192-289.
- Borgenstam, A. Activation Energy for Isothermal Martensite in Iron Alloys/A. Borgenstam, M. Hillert//Acta Mat. 1997. V. 45, N 2. P. 651-662.
- Особенности мартенситного и бейнитного превращения в хромистых сталях/Д.А. Мирзаев, С.Е. Карзунов, В.М. Счастливцев и др.//ФММ. 1986. Т. 62, вып. 2. С. 318-327.
- Bhadeshia, H.K.D.H. Thermodynamic Analysis of Isothermal Transformation Diagrams/H.K.D.H. Bhadeshia//Metal Science. 1982. V. 16, N 3. P. 159-165.
- Hsu, T.Y. Thermodynamics of the Bainitic Transformation in Fe-C Alloys/T.Y. Hsu, Y. Мои//Acta Met. 1984. V. 32, N 9. P. 1469-1481.
- Счастливцев, В.М. Структура термически обработанной стали/В.М. Счастливцев, Д.А. Мирзаев, И.Л. Яковлева. М.: Металлургия, 1994. 288 с.
- Гамма→альфа превращение в низкоуглеродистых сплавах Fe-Cr/Д.А. Мирзаев, С.Е. Карзунов, В.М. Счастливцев и др.//ФММ. 1986. Т. 61, вып. 2. С. 331-338.