Кинетика реакции диоксида хлора с остаточным лигнином лиственной сульфатной целлюлозы
Автор: Липин И.В., Демин В.А.
Журнал: Известия Коми научного центра УрО РАН @izvestia-komisc
Рубрика: Химические науки
Статья в выпуске: 4 (16), 2013 года.
Бесплатный доступ
Определены кинетические параметры реакции диоксида хлора с остаточным лигнином различных целлюлоз после обработки на производстве - константы скоростей расходования ClO 2 в водной суспензии сульфатной целлюлозы по реакциям первого и второго порядков. Установлено, что по мере делигнифи-кации лиственной сульфатной целлюлозы реакционная способность остаточного лигнина по отношению к ClO 2 уменьшается.
Потенциометрия, окислительно-восстановительный потенциал, сульфатная целлюлоза, остаточный лигнин, диоксид хлора, кинетика реакции
Короткий адрес: https://sciup.org/14992637
IDR: 14992637 | УДК: 661.432:541.13
Kinetics of reaction of chlorine dioxide with residual lignin of hardwood sulphate pulp
The kinetic parameters of the reaction of chlorine dioxide with residual lignin pulps after industrial processing - ClO 2 flow rate constants in aqueous suspension of sulphate cellulose on reactions of the first and second order - are defined. It is established that with delignification of hardwood kraft pulp lignin the reactivity of residual lignin against ClO 2 decreases.
Текст научной статьи Кинетика реакции диоксида хлора с остаточным лигнином лиственной сульфатной целлюлозы
Основным методом изучения реакционной способности лигнина, в том числе кинетических параметров процессов варки и отбелки, является метод, основанный на определении содержания лигнина в лигноцеллюлозных материалах после окислительных обработок, проводимый, как правило, по кинетическим моделям первого порядка. При этом собственно определение изменений содержания лигнина при отбелке целлюлозы возможно только косвенными методами с довольно большими погрешностями и допусками.
Представляется интересным и актуальным оценить кинетику процесса делигнификации с использованием современной приборной базы на основе прямых потенциометрических измерений величин, связанных с концентрацией растворов диоксида хлора.
Предлагаемый в данной работе метод потенциометрии позволяет изучать целый комплекс гетерогенных реакций лигнина с кислородными соединениями хлора как на основе их прямой потенциометрии, так и с элементами формально-кинетического подхода для изучения и расчета реакций второго порядка.
Цель работы . Отработать методику определения кинетических параметров реакции диоксида хлора с остаточным лигнином – констант скоростей расходования ClO 2 в водной суспензии сульфатной целлюлозы по реакциям первого и второго порядков.
Материал и методы
Исходным сырьем служила лиственная сульфатная небеленая целлюлоза, отобранная после варки, а также после кислородно-щелочной обработки (КЩО) с ОАО «Монди Сыктывкарский ЛПК».
Образцы лиственной сульфатной небеленой целлюлозы были дополнительно промыты и дека-тионированы. Навеску воздушно сухой целлюлозы ( к сух = 0,950) массой 0,1000 : 0,5000 г, взвешенной с точностью до ± 0,0001 г , смачивали водой, размешивали до однородной массы, помещали в установку с притертой крышкой вместимостью 150 см3 и перемешивали суспензию целлюлозы до полного ее роспуска на магнитной мешалке, затем добавляли воду до общего объема 100 см3 и закрепляли измерительные электроды. В работе использованы многоканальный прибор «Мультитест ИПЛ-103» и компьютерная программа, позволяющая одновременно накапливать в виртуальном журнале данные по температуре, рН и величине окислительновосстановительного потенциала (ОВП) φ с интервалом в 1 с. [1].
Основные условия опытов I серии и расчетные данные для образца лиственной сульфатной небеленой целлюлозы с жесткостью 15,9 ед. Каппа приведены в табл. 1. Опыты 1 и 2 являются параллельными. Для расчета концентрации остаточного
Таблица 1
Условия опытов I серии и расчетные данные
|
№ опыта |
Масса навески лиственной сульфатной небеленой целлюлозы, г в.с.ц |
Расчетная начальная концентрация остаточного лигнина в растворе |
|
1,2 |
0,1501 |
1,86·10-4 М |
|
3 |
0,2002 |
2,47·10-4 М |
|
4 |
0,2500 |
3,07·10-4 М |
Примечание: T = 23,0 °С. Перед проведением опытов исходный раствор ClO 2 разбавляли в 10 раз (9:1) и дозировали микропипеткой по 0,60 мл. Концентрация диоксида хлора в растворе для всех опытов составляла 6,3x10 -5 М.
лигнина использованы следующие принятые в химии древесины допущения: коэффициент перевода числа Каппа в процентное содержание лигнина для сульфатных целлюлоз равен 0,15, среднечисловая молекулярная масса фенилпропановой единицы – 182,5 г/моль [2].
Известно, что с изменением величины pH водных растворов диоксида хлора изменяется величина ОВП (рис. 1) [3].
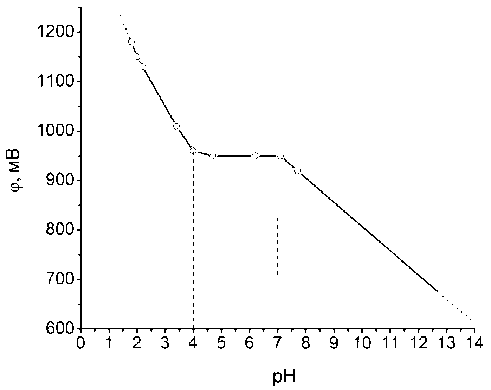
Рис. 1. Зависимость ф от pH в растворе диоксида хлора. Значения потенциала приведены относительно нормального водородного электрода.
Потенциал пары ClO 2 /ClO 2 - в интервале pH 4-7 не изменяется (рис. 1), и таким образом, для одноэлектронного перехода уравнение Нернста имеет вид [4]:
0 a ClO 2
ф = ф ClO 2 /ClO - + RT ' ln „ a cio -
Следовательно, величина потенциала в данном случае может быть использована для оценки константы скорости реакции первого порядка по тангенсу наклона графика « ф - т».
Результаты и обсуждение
В экспериментальной части работы проведено изучение изменений величины ОВП на платиновом индикаторном электроде относительно хлорсе- ребряного электрода в процессе обработки лиственной сульфатной небеленой целлюлозы диоксидом хлора.
Общий вид кривой ОВП, снятой при обработке суспензии лиственной сульфатной небеленой целлюлозы диоксидом хлора, приведен на рис. 2. Наблюдаемые в некоторых опытах в начальные мгновения более высокие начальные значения ф можно объяснить наличием в растворе незначительного количества молекулярного хлора, всегда присутствующего в промышленных растворах диоксида хлора. Нормальный потенциал редокс пары Cl 2 /2Cl– существенно выше. В силу малого количества примеси молекулярного хлора он расходуется практически сразу же, а диоксид хлора сравнительно медленно, и соответствующие потенциалу пары «диоксид хлора – хлорит-ион» линейные участки легко выделить на экспериментальной кривой в области +680 + 740 мВ (отн. хлорсеребряного электрода).
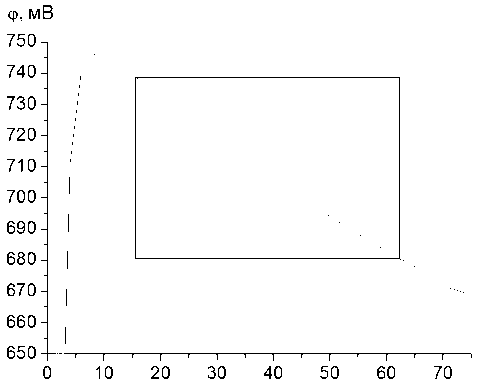
г, с
Рис. 2. Общий вид кривой φ , снятой при обработке суспензии лиственной сульфатной целлюлозы диоксидом хлора при 23,0 °С.
Линейный участок зависимости φ от времени – это полулогарифмическая анаморфоза кинетической кривой расходования диоксида хлора, поскольку величина ОВП прямо пропорциональна натуральному логарифму концентрации диоксида хлора. Тангенс угла является константой скорости реакции первого порядка по диоксиду хлора. Аппроксимация участков 740 + 660 мВ кривой «ф - т» уравнением прямой типа Y = A + B x во всех опытах характеризуется очень высоким коэффициентом корреляции – около 0,999. С помощью метода наименьших квадратов, рассчитываем значения коэффициентов уравнения линеаризации, погрешность: А ± ДА, -В ± ДВ , величину к эфф(1) , с-1 (табл. 2). В зависимости от скорости падения ОВП, т.е. скорости расходования диоксида хлора, для статистической обработки взято различное количество точек измерений (рис. 3). Данные, полученные в 1 и 2 опытах, на рис. 3 были усреднены и представлены одной кривой.
Таблица 2
Результаты статистической обработки потенциометрических измерений
|
№ |
Участок линеаризации |
А |
± ΔA |
-B = k эфф(I) с -1 |
± ΔB |
|
|
φ н , мВ |
φ к , мВ |
|||||
|
1 |
720 |
680 |
720,1 |
0,1 |
0,35 |
0,01 |
|
2 |
721 |
693 |
721,1 |
0,1 |
0,36 |
0,01 |
|
3 |
726 |
669 |
726,3 |
0,2 |
0,98 |
0,01 |
|
4 |
725 |
662 |
725,4 |
0,3 |
1,82 |
0,01 |
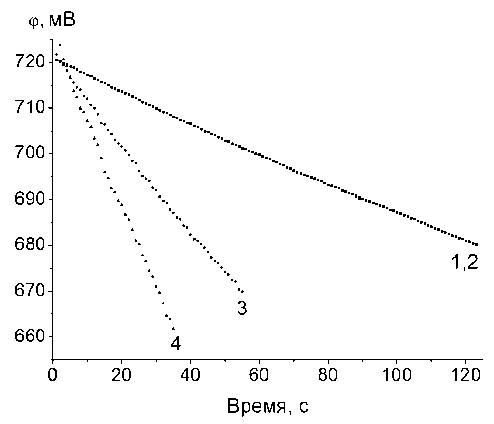
Рис. 3. Экспериментальные точки на линейных участках кривой φ (до статистической обработки). Номера 1-4 – в соответствии с табл. 1.
Как видно из табл. 2, значения эффективных констант скорости первого порядка k эфф(I) находятся в диапазоне от 0,33 до 1,82 с-1 .
Уравнение скорости реакции диоксида хлора с лигнином L :
V= k эфф(II) ∙[ClO 2 ]∙[L], где k эфф(II) – константа скорости реакции второго порядка.
В этом уравнении два реагента и предварительная литературная и экспериментальная информация позволяют считать, что реакция имеет второй порядок, поскольку процесс делигнификации в отдельности по лигнину и диоксиду хлора протекает по первому порядку, что суммарно по двум компонентам дает второй порядок [5].
При изучении кинетики реакций второго порядка один из реагентов берут в большом избытке и экспериментально получают значения эффективных констант первого порядка k эфф(I) [6]. При этом в константу k эфф(I) входит начальная концентрация избыточного реагента [ L o ]:
k эфф(I) = k эфф(II) ·[L 0 ].
Путем варьирования этой начальной концентрации остаточного лигнина (за счет изменения концентрации суспензии небеленой сульфатной целлюлозы) была найдена зависимость k эфф(I) от [ L o ] и по тангенсу угла наклона рассчитано значение константы второго порядка (рис. 4).
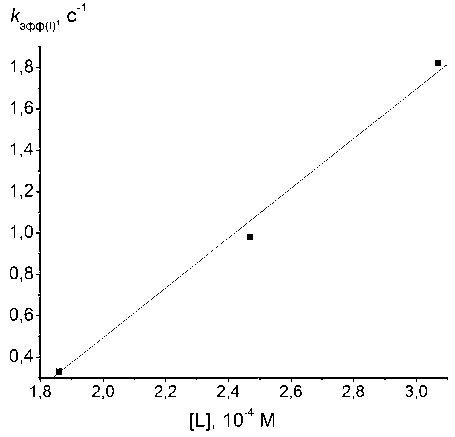
Рис. 4. Зависимость эффективной константы первого порядка K эфф(I) от концентрации остаточного лигнина [L] в суспензии целлюлозы.
k эфф(I) = A 0 + k эфф(II) ∙ [L] = – (2,0 ± 0,2) + (12270,9 ± ±656,0) с-1
k эфф(II) ≈ 12250 ± 650 М-1с-1.
Аналогичным образом была проведена статистическая обработка экспериментальных данных, полученных при поглощении диоксида хлора остаточным лигнином сульфатных целлюлоз после варки жесткостью 14,6 и 17,0 ед. Κ , а также сульфатной целлюлозы после КЩО жесткостью 8,5 ед. Κ (табл. 3).
Таблица 3
Значения константы скорости второго порядка для разных образцов целлюлозы
|
№ |
Жесткость лиственной сульфатной целлюлозы, ед. Κ |
k эфф(II) , М -1 с -1 |
R |
|
I |
15,9 |
12250 ± 650 |
0,997 |
|
II |
17,0 |
12700 ± 450 |
0,997 |
|
III |
14,6 |
10350 ± 300 |
0,998 |
|
IV |
8,5 |
7250 ± 350 |
0,998 |
Примечание : образцы 1-3 - после варки, 4 - после КЩО
На рис. 5 представлены зависимости эффективной константы первого порядка k эфф(I) от концентрации остаточного лигнина в суспензии целлюлозы для всех обработанных образцов.
На основании проведенных исследований можно заключить следующее. Установлено, что по мере уменьшения содержания остаточного лигнина в лиственной сульфатной целлюлозе его реакционная способность по отношению к ClO 2 снижается. Путем варьирования концентрации остаточного лигнина, взятого в большом избытке относительно диоксида хлора, по значениям эффективных констант первого порядка определены значения констант второго порядка v = k ∙[ClO 2 ]∙[L] , которые для
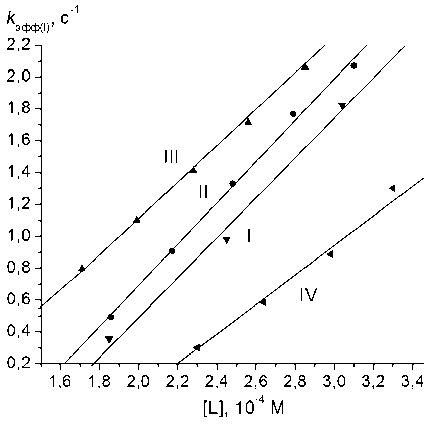
Рис. 5. Зависимости эффективной константы первого порядка k эфф(I) от концентрации остаточного лигнина в суспензии целлюлозы для обработанных образцов (номера соотв. табл.3)
реакции ClO 2 с остаточным лигнином целлюлозы, отобранной после сульфатной варки, находятся в пределах 10350 ^ 12700 ± 650 М-1с-1 и существенно убывают по мере снижения содержания лигнина в небеленой целлюлозе, после КЩО до 7250 ± 350 М-1с-1.
Выводы
-
1. Исследование изменений величины потенциала окислительно-восстановительной пары ClO 2 / ClO 2 - позволяет определить значения частной константы скорости первого порядка (по диоксиду хлора) для процесса окисления остаточного лигнина, т.е. количественно охарактеризовать реакционную способность остаточного лигнина сульфатной целлюлозы.
-
2. Определены значения констант второго порядка для реакции ClO 2 с остаточным лигнином целлюлозы после сульфатной варки и после КЩО.
-
3. Установлено, что по мере делигнификации лиственной сульфатной целлюлозы реакционная способность остаточного лигнина по отношению к ClO 2 уменьшается.
Работа выполнена в рамках Программы Президиума РАН «Создание и совершенствование методов химического анализа и исследования структуры веществ и материалов» (проект №12–П–З–1024).
Список литературы Кинетика реакции диоксида хлора с остаточным лигнином лиственной сульфатной целлюлозы
- Липин И.В. Кинетика гипохлоритного окисления остаточного лигнина//Лесной журнал. 2012. №1. С. 103-106.
- Карманов А.П. Самоорганизация и структурная организация лигнина. Екатеринбург: УрО РАН, 2004. 269 с.
- Туманова Т.А. Физико-химические основы отбелки целлюлозы. М.: Лесн. пром., 1984. 216 с.
- Флис И.Е. Электрохимия окислительно-восстановительных процессов в отбельных растворах и в некоторых других системах//Труды ЛТИ ЦБП. Ленинград: ЛТИ ЦБП, 1964. Вып. XII. С. 50-64.
- Удоратина Е.В., Демин В.А. Исследование полихронной кинетики процесса делигнификации сульфатной целлюлозы в среде водного диоксана//Тез. докл. 21-го Всероссийского симпозиума молодых ученых по химической кинетике. М.: МГУ, 2003. С.25.
- Горбачев С.В. Практикум по физической химии. М.: Высшая школа. 1974. 496 с.


