Кинетика выщелачивания молибдата кальция раствором карбоната натрия
Автор: Алешин Дмитрий Сергеевич, Крашенинин Алексей Геннадьевич, Гаврилов Алексей Сергеевич, Танутров Игорь Николаевич
Журнал: Вестник Южно-Уральского государственного университета. Серия: Металлургия @vestnik-susu-metallurgy
Рубрика: Металлургия чёрных, цветных и редких металлов
Статья в выпуске: 4 т.21, 2021 года.
Бесплатный доступ
Молибдат кальция CaMoO4 (повеллит) является главным продуктом при окислительном обжиге сульфидных молибденовых концентратов и молибденового сырья с кальцийсодержащими добавками. Далее огарок перерабатывают гидрометаллургическим способом. Одним из основных способов извлечения молибдена из огарка является выщелачивание раствором карбоната натрия. С целью определения оптимальных параметров извлечения Мо необходимо исследовать кинетику выщелачивания CaMoO4 водным раствором Na2CO3, определить зависимости скорости процесса извлечения молибдена в раствор от основных технологических параметров: температуры, концентрации реагентов, установить лимитирующую стадию процесса. В качестве исходных материалов применяли СаМоО4 и Na2CO3 квалификации ХЧ. Растворение СаМоО4 в Na2CO3 изучали в пределах концентрации соды СNa2CO3 = 100, 150, 200, 250, 300 г/дм3, в температурном интервале от 20 до 90 °С, отношение Т : Ж = 1 : 2, 1 : 4, 1 : 6, 1 : 8, 1 : 10, продолжительностью от 30 до 300 мин. Изучена зависимость скорости выщелачивания CaMoO4 от интенсивности перемешивания. Определены кажущийся порядок реакции в интервале концентрации Na2CO3 = 100…250 г/дм3 и кажущаяся энергия активации в интервале температур от 60 до 90 °С. Установлено, что оптимальными параметрами выщелачивания СаМоО4 является: Т : Ж = 1 : 6, Т = 90 °С, СNa2CO3 = 200…250 г/дм3, интенсивности перемешивания более 500 мин-1, при данных параметрах процесс протекает в кинетическом режиме. Показано, что при концентрации Na2CO3 более 250 г/дм3 процесс протекает с образованием карбонатов натрия-кальция, в этом случае лимитирующей стадией процесса является внутренняя диффузия. Также формирование карбонатов натрия-кальция приводит к увеличению расходу Na2CO3.
Молибден, кинетика выщелачивания, молибдат кальция, карбонат натрия, энергия активации
Короткий адрес: https://sciup.org/147236539
IDR: 147236539 | УДК: 669.283 | DOI: 10.14529/met210402
Kinetics of calcium molybdate leaching with sodium carbonate solution
Calcium molybdate CaMoO4 is the main product in the oxidative roasting of sulphide molybdenum concentrates and molybdenum raw materials with calcium-containing additives. After that, the cinder is processed hydrometallurgically. One of the main methods for extracting molybdenum from cinder is leaching with sodium carbonate solution. In order to determine the optimal parameters of Mo extraction, it is necessary to study the kinetics of CaMoO4 leaching with an aqueous solution of Na2CO3, to determine the dependences of the rate of the process of extracting molybdenum into solution on the main technological parameters: temperature, concentration of reagents, and to establish the limiting stage of the process. As starting materials, we used Reagent grade CaMoO4 and Na2CO3. The dissolution of CaMoO4 in Na2CO3 was studied within the concentration of soda СNa2CO3 = 100, 150, 200, 250, 300 g/dm3, in the temperature range from 20 to 90 °C, the ratio S : L = 1 : 2, 1 : 4, 1 : 6, 1 : 8, 1 : 10, duration from 30 to 300 minutes. The dependence of the CaMoO4 leaching rate on the mixing intensity has been studied. The apparent order of the reaction in the concentration range of Na2CO3 = 100…250 g/dm3 and the apparent activation energy in the temperature range from 60 to 90 °C have been determined. It was found that the optimal parameters of CaMoO4 leaching are: S : L = 1 : 6, T = 90 °C, СNa2CO3 = 200…250 g/dm3, stirring intensity is more than 500 min-1, with these parameters the process proceeds in a kinetic mode. It is shown, that at a Na2CO3 concentration of more than 250 g/dm3, the process proceeds with the formation of sodium-calcium carbonates; in this case, the limiting stage of the process is internal diffusion. In addition, the formation of sodium-calcium carbonates leads to an increase in the consumption of Na2CO3.
Текст научной статьи Кинетика выщелачивания молибдата кальция раствором карбоната натрия
Молибдат кальция CaMoO4 (повеллит) является одним из основных молибденсодержащих минералов. Также он является важным промежуточным звеном в некоторых гидрометаллургических и пирометаллургических технологиях переработки молибденовых концентратов. Авторами работ [1–6] были предложены технологии окислительного обжига молибденового сырья в присутствии соединений кальция в интервале температур 500–700 °С с образованием молибдата кальция, что позволяет значительно снизить выброс сернистого ангидрида в атмосферу при окислительном обжиге сульфидных молибденовых концентратов.
В Институте металлургии УрО РАН продолжаются исследования по поиску экологи- чески чистой технологии производства молибдена и рения из сульфидных концентратов путем обжига концентратов с кальцийсодержащей добавкой и последующей гидрометаллургической переработкой огарка [7, 8].
Целью работы является исследование кинетики выщелачивания CaMoO 4 водным раствором Na2CO3, определение зависимости скорости процесса извлечения молибдена в раствор от основных технологических параметров: температуры, концентрации реагентов, лимитирующей стадии процесса.
Оборудование и методы исследования
В рамках работы использовали синтезированный СаМоО4 и Na2CO3 квалификации ХЧ. Выщелачивание молибдата кальция в со- довом растворе проводили в термобане, точность поддержания температуры ±0,1 °С, в комбинации с перемешивающим устройством ПЭ-8100. Для фильтрации пульпы использовали вакуумный нутч-фильтр. Процесс проходил следующим образом: в сосуд объемом 400 мл с раствором Na2CO3, нагретым до заданной температуры, при постоянном перемешивании вводили навеску СаМоО4. Отбор проб для анализа раствора проводили каждые 30 мин. Полученный после выщелачивания кек сушили в сушильном шкафу (Nabertherm P330) при температуре 150–200 °С. Степень перехода молибдена из молибдата кальция в раствор определяли по сопоставлению результатов химического анализа раствора и кека. Анализ растворов проводили на атомно-абсорбционном спектрофотометре. Кек подвергался рентгенофазовому анализу.
Экспериментальная часть
Растворение СаМоО 4 в Na 2 CO 3 изучали в пределах концентрации соды С Na CO = 100, 150, 200, 250, 300 г/дм3 в температурном интервале от 20 до 90 °С, отношение Т : Ж = 1 : 2, 1 :4, 1 : 6, 1 : 8, 1 : 10, продолжительность процесса составляла от 30 до 300 мин.
Взаимодействие СаМоО 4 с Na 2 CO 3 протекает согласно уравнению
CaMoO 4(т) + Na 2 CO 3(р) →
→ NaMoO4(р) + CaCO3(т). (1)
Известно, что кинетика взаимодействия такого типа состоит из нескольких этапов: перенос реагента из объема раствора к поверхности твердой фазы через пограничный слой жидкости; диффузия реагента через слой твердого продукта (слой СаСО3 на частице СаМоО4); химическое взаимодействие на поверхности СаМоО4 и перенос продукта ( МоО24- ) в объем раствора.
Результаты изучения степени выщелачивания молибдена из молибдата кальция при Т = 90°С, С Na CO = 200 г/дм3 от продолжительности при различных скоростях вращения мешалки представлены на рис. 1. Обороты импеллера перемешивающего устройства варьировали от 3,3 до 10 с–1. После того как экспериментально установили и построили график зависимости степени выщелачивания молибдена от продолжительности при различных скоростях вращения мешалки, определяли начальные скорости выщелачивания и строили зависимости d α/ d τ от корня квадратного от оборотов мешалки ω [9].
Начальный прямолинейный участок кривой при оборотах от 3,3 до 5 с–1 соответствует внешнедиффузионному режиму, затем идет область переходного режима, а при увеличении числа оборотов с 8,3–1 (500 мин–1) начальная скорость выщелачивания становится постоянной, процесс переходит в кинетическую область. Из чего следует, что, оптимальным параметром скорости вращения перемешивающего устройства предпочтительно выбрать 8,3 с–1 (500 мин–1), так как при данном значении процесс проходит в устойчивый кинетический режим. Дальнейшие исследования проводились при данном параметре.
Влияние отношения твердого к жидкому при выщелачивании молибдата кальция в водном растворе кальцинированной соды проводили при концентрации С Na CO = 150 г/дм3,
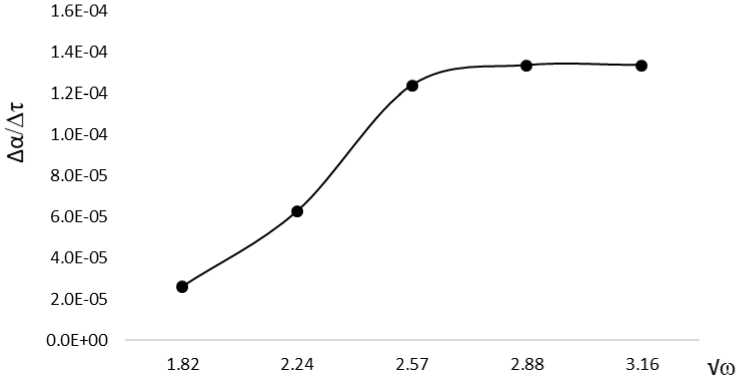
Рис. 1. Зависимость скорости выщелачивания от корня квадратного оборотов мешалки
Металлургия чёрных, цветных и редких металлов
Т = 90 °С, с постоянным перемешиванием n = 8,3 с–1. Отношение Т : Ж варьировали от 1 : 2 до 1 : 10. Результаты приведены на рис. 2.
В результате эксперимента установили, что соотношения Т : Ж = 1 : 4 не достаточно, максимальное извлечение молибдена в раствор наблюдалось при соотношение Т : Ж = 1 : 6, при данном соотношение в раствор перешло 79,9 % Мо. Также в рамках эксперимента было установлено, что оптимальной продолжительностью выщелачивания является 120–150 мин. Дальнейшее увеличение продолжительности не приводит к значительному увеличению перехода молибдена в раствор, а даже наоборот после 150-й минуты наблюдается снижение концентрации молибдена в растворе, это связано с образованием соединения Na2MoO4·2H2O, которое переходит в осадок, аналогичный процесс наблюдали авторы работы [10, 11], также при увеличении соотношения Т : Ж свыше 1 : 6 возможно интенсивное выделение представленной фазы.
Исследования по влиянию исходной концентрации Na 2 CO 3 на степень выщелачивания СaMoO 4 при следующих параметрах: Т = 90 °С, Т : Ж = 1: 6, τ = 120 мин, С Na CO = 100, 150, 200, 250, 300 г/дм3. Результаты представлены на рис. 3.
С повышением концентрации Na 2 CO 3 в растворе от 100 до 200 г/дм3 степень перехода молибдена в раствор увеличивается, но дальнейший рост концентрации соды в растворе
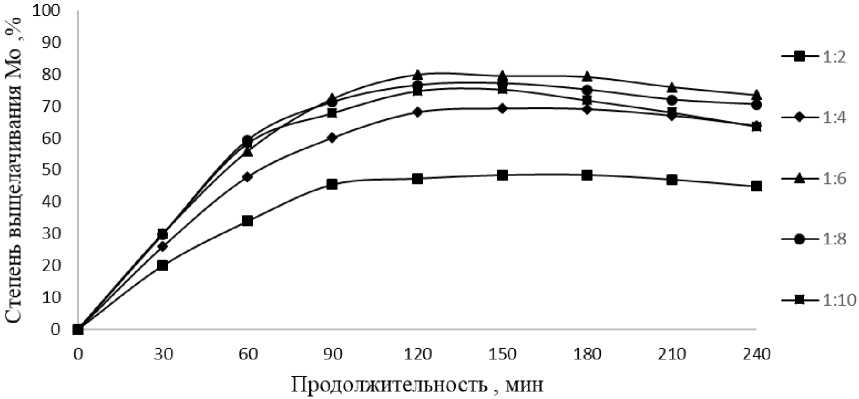
Рис. 2. Зависимость степени выщелачивания молибдена от соотношения Т : Ж
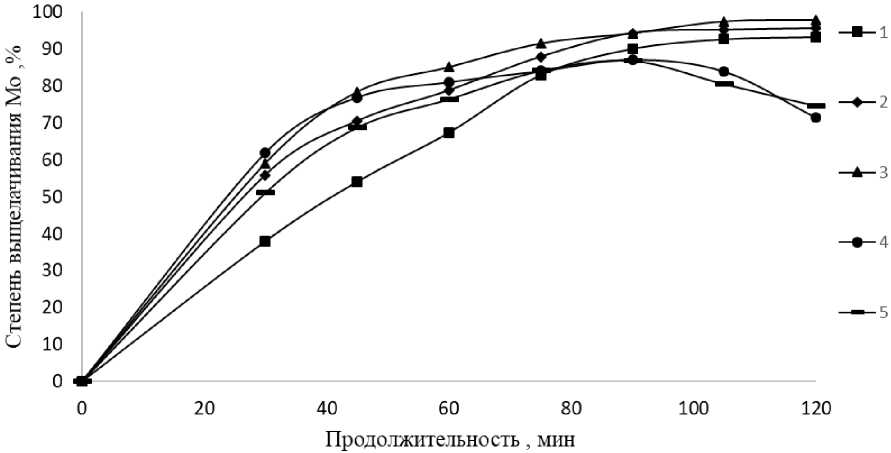
Рис. 3. Зависимость извлечения молибдена в раствор от продолжительности выщелачивания при СNa CO , г/дм3: 1 – 100, 2 – 150, 3 – 200, 4 – 250, 5 – 300
с 250 до 300 г/дм3 не приводит к изменению интенсификации процесса. Наилучшие показатели степени перехода молибдена в раствор в количестве 97,9 отн. % достигнуты при концентрации Na 2 CO 3 в растворе 200 г/дм3. В рамках этого эксперимента установлено, что при увеличение концентрации соды в выщелачивающем растворе с 250 до 300 г/дм3 снижается степень растворения молибдена. Это возможно из-за формирования двойных карбонатов натрия-кальция в виде безводной соли Na 2 Ca(CO 3 ) 2 или формирования кристаллогидратов с переменным числом молекул Na 2 Ca(CO 3 ) 2 ·2H 2 O [12, 13]. Результаты рентгенофазового анализа кека представлены на рис. 4.
Согласно полученным данным, в осадке содержится CaMoO4, две модификации СаСО3 – ватерит и кальцит, также присутствует безводная соль Na2Ca(CO3)2. Это позволяет сделать вывод, что формирование кальцита происходит через образование его менее устойчивой модификации ватерита. Возможно, безводная соль получается через взаимодействие ватерита с карбонатом натрия. Полученные результаты не противоречат литературным данным [14].
На рис. 5 представлены данные в координатах lg v – lg C , где скорость реакции v рассчитана с учетом линейности участков как отношение Δα/Δτ (α – степень растворения, доли единицы; τ – время, мин).
Кажущийся порядок процесса по реагенту n , рассчитанный как угловой коэффициент прямой в координатах lg v – lg C , составляет 0,49 ± 0,02, это означает, что в интервале кон-
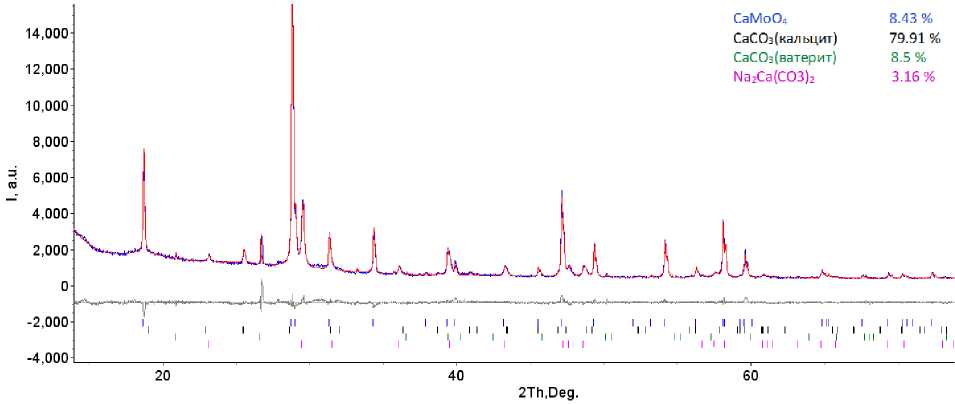
Рис. 4. Рентгенограмма остатка после выщелачивания при С = 300 г/дм3,
Т = 90 °С, Т : Ж = 1 : 6, т = 120 мин на дифрактометре D8 ADVANCE
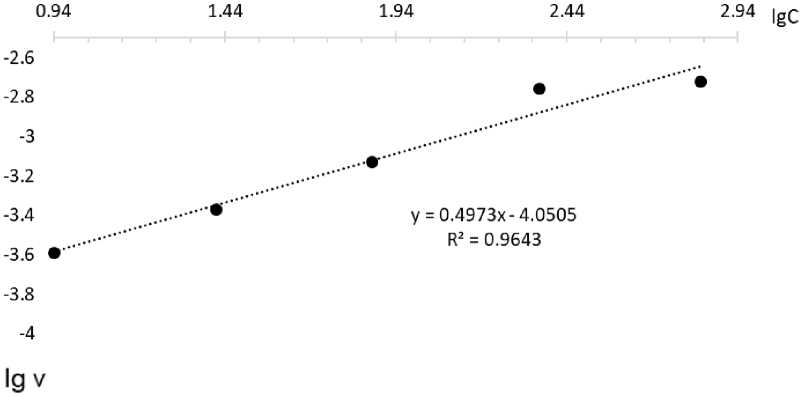
Рис. 5. Зависимость скорости выщелачивания СаМоО 4 от исходной концентрации Na 2 CO 3 , Т = 90 °С
Металлургия чёрных, цветных и редких металлов центраций 100–250 г/дм3 процесс протекает в кинетической области. Константа скорости в этом концентрационном интервале Na2CO3 при температуре 90 °С равна 4,1·10–2 моль/с.
Полученные результаты позволяют предположить, что в системе с ростом концентрации соды выше 250 г/дм3 растворение СаМоО4 сопровождается взаимодействием получаемого СаСО 3 (ватерита) с содой по уравнению
CaCO 3 + 2Na + + CO 2- = Na 2 Ca(CO 3 ) 2 (2) с образованием плотной оболочки двойных карбонатов. В этом случае лимитирующей стадией процесса будет внутренняя диффузия молибдат-иона от фронта реакции в раствор через твердую оболочку из СаСО 3 и двойной соли [15].
Влияние температуры на скорость процесса изучали в интервале температур 60–90 °С, при концентрации Na 2 CO 3 = 200 г/дм3, Т : Ж = = 1 : 6, τ = 120 мин. На основании данных, полученных авторами работы [10], исследования при температуре менее 60 °С проводить не целесообразно. Установлено, что скорость растворения молибдата кальция заметно увеличивается с ростом температуры, наибольшие значения её достигается при температуре 90 °С (рис. 6).
В интервалах температур от 80 до 90 °С при достижение степени выщелачивания молибдата кальция более 50 % скорость уменьшается, что указывает на рост внутридиф-фузионного сопротивления. Возможно, это связано с тем, что при температурах более
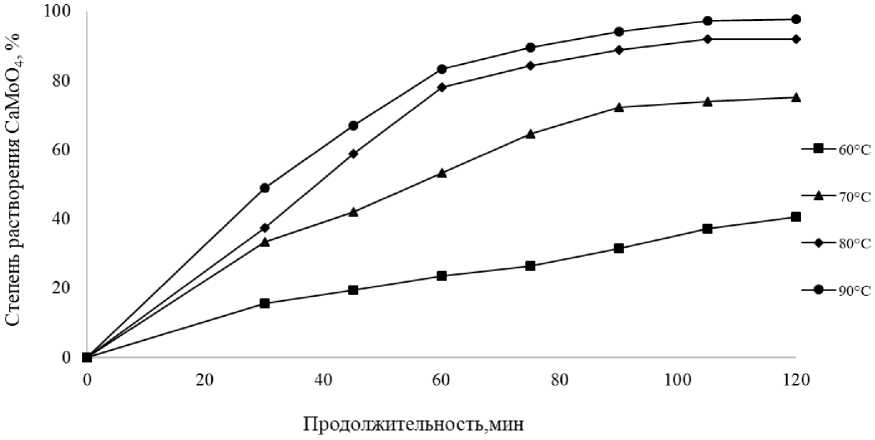
Рис. 6. Зависимость степени выщелачивания СаМоО 4 от температуры
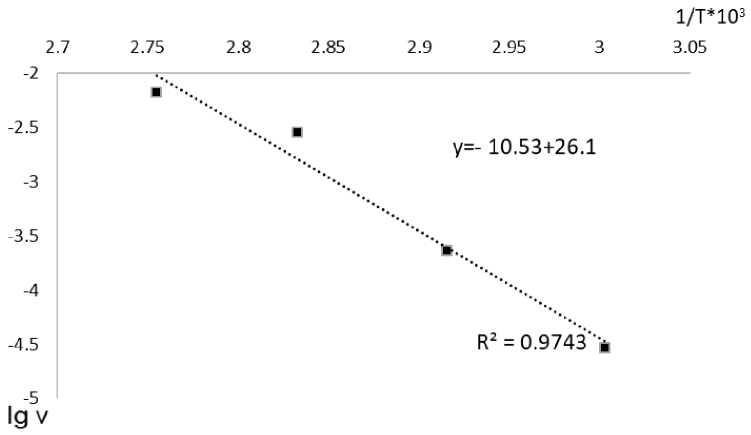
Рис. 7. Определение энергии активации по зависимости скорости реакции от температуры
80 °С в состав твердой оболочки продуктов входит двойной карбонат натрия-кальция большей плотности, что объясняет падение скорости выщелачивания молибдена при достижении степени выщелачивания более 50 %.
Энергию активации определяли методом начальных скоростей. Этот метод основан на определение начальных скоростей реакции при разных температурах, но с фиксированными начальными концентрациями реагентов.
На рис. 7 данные представлены в координатах lg v – 1/ Т ·103, где скорость реакции v рассчитана с учетом линейности участков как отношение Δα/Δτ (α – степень растворения, доли единицы; τ – время, мин). Кажущаяся энергия активации, рассчитанная как угловой коэффициент прямой в выбранных координатах, составляет 87,5 ± 2 кДж/моль.
Вывод
Изучена кинетика выщелачивания молибдата кальция в растворах карбоната натрия. Установлено, что скорость растворения
СаМоО 4 зависит от интенсивности перемешивания, оптимальная скорость мешалки более 400 мин–1. Скорость выщелачивания СаМоО4 в водном растворе карбоната натрия при концентрации 100–250 г/дм3 зависит от концентрации реагента. Кажущейся порядок по реагенту составляет 0,49 ± 0,02, величина кажущейся энергии активации равна 87,5 ± 2 кДж/моль. При интенсивном перемешивание (более 400 мин–1) и постоянной температуре 90 °С в указанном интервале концентраций соды процесс выщелачивания протекает в кинетическом режиме. Увеличение концентрации Na2CO3 приводит к образованию двойных карбонатов и к дополнительному расходу соды. Лимитирующей стадией процесса может являться внутренняя диффузия молибдат-иона через плотною оболочку продуктов.
Работа выполнена по государственному заданию ИМЕТ УрО РАН в рамках программы фундаментальных исследований государственных академий № госрегистрации: 0396-2019-0005.
Список литературы Кинетика выщелачивания молибдата кальция раствором карбоната натрия
- Зеликман, А.Н. Металлургия тугоплавких редких металлов / А.Н. Зеликман. – М.: Металлургия, 1986. – 440 с.
- Lasheen, T.A. Molybdenum Metallurgy Review: hydrometallurgical routes to recovery of molybdenum from ores and mineral raw materials / T.A. Lasheen, M.E. El-Ahmady, H.B. Hassib // Mineral Processing and Extractive Metallurgy Review. – 2015. – Vol. 36, no. 3. – P. 145–173. DOI: 10.1080/08827508.2013.868347
- Extraction of molybdenum from high-impurity ferromolybdenum by roasting with Na2CO3 and CaO and leaching with water / Lihua Shi, Xue-Wen Wang, Ming-Yu Wang et al. // Hydrometallurgy. – 2011. – Vol. 108, iss. 3-4. – P. 214–219. DOI: 10.1016/j.hydromet.2011.04.009
- A Novel Self-Heated Roasting Technology for Molybdenum Concentrate / Wang Lianyong, Wen-qiang Sun, Zhang Jingfan, Cai Jiuju // Rare Metal Materials and Engineering. – 2015. – Vol. 44 (11). – P. 2618–2622. DOI: 10.1016/S1875-5372(16)60005-X
- Wang, M. A novel technology of molybdenum extraction from low grade Ni-Mo ore / M. Wang, X. Wang, W. Liu // Hydrometallurgy. – 2009. – Vol. 97 (1-2). – P. 126–130. DOI: 10.1016/j.hydromet.2008.12.004
- Обжиг молибденового концентрата с добавкой Са(ОН)2 / Д.С. Алешин, А.Г. Крашенинин, Д.С. Реутов, И.Н. Танутров // Вестник Иркутского государственного технического университета. – 2020. – № 4. – С. 876–885. DOI: 10.21285/1814-3520-2020-4-876-886
- Харин, Е.И. Разработка экологически чистой комплексной технологии переработки молибденового концентрата Южно-Шамейского месторождения / Е.И. Харин, Б.Д. Халезов, Е.А. Зеленин // Известия высших учебных заведений. Горный журнал. – 2015. – № 5. – С. 129–134.
- Поиск экологически чистой технологии переработки молибденовых концентратов / Н.А. Ватолин, Б.Д. Халезов, Е.И. Харин, Е.А. Зеленин // Химическая технология. – 2012. – Т. 13, № 4. – С. 229–232.
- Вольдман, Г.М. Теория гидрометаллургических процессов / Г.М. Вольдман, А.Н. Зеликман. – М.: Интермет Инжиниринг, 2003. – 464 с.
- Рейнгольд, Б.М. О взаимодействии молибдатов кальция меди и железа с раствором карбоната натрия / Б.М. Рейнгольд // Добыча и обработка руд редких, цветных и благородных металлов: сб. тр. Иргиредмета. – 1965. – Вып. 13. – С. 398–406.
- Rodriguez-Blanco, J.D. The kinetics and mechanisms of amorphous calcium carbonate crystallization to calcite, viavaterite / J.D. Rodriguez-Blanco, S. Shaw, L.G. Benning // Nanoscale. – 2011. – No. 3. – P. 265–271. DOI: 10.1039/c0nr00589d
- Киндряков, П.С. Равновесие системы CaMoO4 + Na2CO3 ↔ Na2MoO4 + CaCO3 и некоторых других систем / П.С. Киндряков // Редкие металлы. – 1934. – № 4. – С. 48–51.
- Зеликман, А.Н. Исследование реакций взаимодействия молибдатов кальция, меди и железа / А.Н. Зеликман, Л.В. Беляевская // Журнал прикладной химии. – 1956. – № 1. – С. 11–17.
- Chang, R. Calcium Carbonate Precipitation for CO2 Storage and Utilization: A Review of the Carbonate Crystallization and Polymorphism / R. Chang, S. Kim, S. Lee // Frontiers in Energy Re-search. – 2017. – Vol. 5. – P. 1–12. DOI: 10.3389/fenrg.2017.00017
- Соколова, Ю.В. Исследование кинетики выщелачивания молибдата кальция растворами карбоната натрия / Ю.В. Соколова, Е.В. Богатырева // Цветные металлы. – 2021. – № 1. – С. 40–46. DOI: 10.17580/tms.2021.01.04


