Кислотно-основные свойства поверхности оксидных материалов
Автор: Рязанов М.А.
Журнал: Известия Коми научного центра УрО РАН @izvestia-komisc
Рубрика: Химические науки
Статья в выпуске: 2 (6), 2011 года.
Бесплатный доступ
Составлена и решена система уравнений, соответствующая 4рК модели ки- слотно-основных свойств поверхности оксидных материалов. Показано, что при уменьшении концентрации фонового электролита точка нулевого заряда протонов этой поверхности сдвигается в сторону более низких значений рН в случае специфической адсорбции катионов и в сторону более высоких рН в случае специфической адсорбции анионов. Представлено обоснование метода рК-спектроскопии. На основе полученных данных построен рК-спектр, соот- ветствующий данной модели; он состоит из двух полос, положение которых зависит от концентрации фонового электролита.
Адсорбция, адсорбенты, катализ, кислотно-основные свойства, 4рк-модель, анатаз, рк-спектры, рк-спектроскопия
Короткий адрес: https://sciup.org/14992449
IDR: 14992449 | УДК: 541.18.537
Acid-base properties of the surface of oxide materials
The system of equations corresponding to 4pK model of acid-base surface properties of oxide materials is composed and solved. It is shown that with decreasing of concentration of supporting electrolyte the point of zero charge of the protons of the surface is shifted toward lower pH values in case of specific adsorption of cations and toward higher pH in case of specific adsorption of anions. Substantiation of pK spectroscopy method is given. Basing on the data obtained pKspectrum is constructed corresponding to this model, it consists of two bands, which position depends on the concentration of background electrolyte.
Текст научной статьи Кислотно-основные свойства поверхности оксидных материалов
Кислотно-основные свойства различных материалов давно и интенсивно изучаются, главным образом, в связи с их адсорбционными и каталитическими свойствами [1 – 4].
В частности, кислотно-основной характер активных центров на поверхности оксидных минералов во многом определяет их поведение в природной среде, взаимодействие с поровым раствором, является причиной образования геохимических барьеров и существенно связан с комплемен-тарностью поверхности в отношении к простейшим биомолекулам в концепции генобиоза [5].
Наиболее распространенным методом изучения кислотно-основных свойств (в рамках концепции Бренстеда) оксидных материалов является потенциометрическое титрование их суспензий в водной среде. Использование неводных растворителей перспективно в отношении изучения кислотноосновных свойств в рамках концепции Льюиса. Обычно титрование проводится из кислой области в щелочную (и наоборот) добавлением к суспензии, содержащей известную концентрацию свободной сильной кислоты cHA , последовательных порций сильной щелочи с концентрацией c и измере-
BOH
нием при этом рН раствора.
Кислотно-основные свойства изучаемого материала удобно охарактеризовать соответствующим рК-спектром [2, 3], представляющим собой гистограмму, площадь отдельных полос которой равна вероятности того, что характеризующая данный кислотно-основной центр величина рK i лежит в интервале между pK i и pK i + A pK. Расчет рК-спектров проводится на основании экспериментальной кривой титрования, выражающей зависимость Гиббсо-вой адсорбции ионов водорода на изучаемой поверхности от рН раствора (в расчете на 1 г изучаемого образца):
c u д V o — c roh V — [H ] " ( V o + V ) i \
Г н (pH) = HA 0 —BOH--------- 0----, ммоль/г. (1)
m
Здесь V0 – объем суспензии, взятой для титрования, концентрация одноосновной сильной кислоты в которой равна cHA , V – объем добавлен- ной щелочи с концентрацией cBOH , m – масса твердой фазы суспензии (г) во взятом образце. Концентрация ионов водорода в уравнении (1) рассчитывается из рН раствора по уравнению [H + ] = 10 - pH.
Интерпретация кислотно-основных свойств оксидных материалов обычно проводится в рамках концепции Дэвиса – Джеймса – Лекки [1] на основе так называемых 2рК и 4рК- моделей.
В 2рК-модели предполагается, что заряд по- верхности появляется в результате ионизации поверхностных амфотерных групп ─SOH по следующим реакциям и описывается соответствующими им уравнениями закона действующих масс:
+ + [-SOH] • [H + ]
-SOH 2+ ^ -SOH + H+ ( K ), K =
1 1 [-SOH + ]
+ [-SO-] • [H + ]
-SOH ^ -SO- + H+ ( K ,). K, = .
2 2 [-SOH]
Здесь индекс ─S используется для обозначения поверхности изучаемого образца. Константы равновесия K 1 и K2 характеризуют силу рассматриваемых кислотно-основных центров и постоянны при проведении эксперимента в условиях постоянной концентрации фонового электролита.
В кислой области (рН<=6) наблюдается равновесие (2), а в щелочной (рН>=9) – равновесие (3).
В тех случаях, когда константы K 1 и K 2
оказываются зависящими от концентрации фонового электролита, вместо модели 2рК используется модель 4рК. 2рК-модель – частный случай 4рК-модели, которая допускает возможность частичной нейтрализации поверхностного заряда ионами индифферентного электролита (например, NaCl), т.е. образованием на поверхности ионных пар:
+ + [SOH] • [H + ] • [Cl-]
SOH%Cl< > SOH+H + +Cl( K. ), K, =
3 3 [SOH + Cl-]
SOH+Na + ^ SO Na + +H + ( K 4 ), K 4 =
[SO-Na + ] • [H + ] [SOH] • [Na + ] .
Очевидно, большие значения констант K 3 и
K 4 соответствуют специфической адсорбции катионов, а малые значения – специфической адсорбции анионов.
Вообще говоря, зависимость констант K 1 и
K 2 от концентрации фонового электролита можно объяснить не только образованием ионных пар по реакциям (4) и (5), но и изменением коэффициентов активности реагирующих ионов, как это обычно делается при изучении комплексообразования в растворах.
Решая теперь систему уравнений законов действующих масс для равновесий (2), (3), (4), (5) и уравнений, выражающих условие электронейтральности раствора:
[SOH 2 +] + [H+] + [Na+] – [SO-] – [Cl-] = 0, условие баланса ионов Na+ и Cl- в системе (считая, что в качестве фонового электролита используется NaCl):
[NaCl] = [Na+] + [SONa], и
[NaCl] + [HCl] = [Cl-] + [SOH 2 Cl], получаем следующее уравнение для расчета величины F H(pH) :
c - [H ]
Гн (pH) = -HC =
H B
( K 3 / K 1 + [NaCl]) [H + ]2 - K 3 K 4[NaCl]- K 2 K 3
( K 3 / K 1 + [NaCl]) [H + ]2 + K 3 [H + ] + K 3 K 4[NaCl}^ K 2 K 3
При решении предполагалось, что [NaCl] = [Na+] = [Cl-], что справедливо при достаточно малых количествах твердой фазы и сравнительно высоких концентрациях фонового электролита. На рис. 1 представлен график зависимости ^(pH) для случая, когда рК 1 = 3.2, рК 2 = 8.7, рК 3 = 4.0, рК 4 = 7.0 (анатаз [6]) и при различных концентрациях NaCl. C ростом концентрации фонового электролита кривая в данном случае смещается в сторону более меньших значений рН в области положительных величин r H(pH) и в сторону более высоких значений рН в области отрицательных значений ^(pH) .
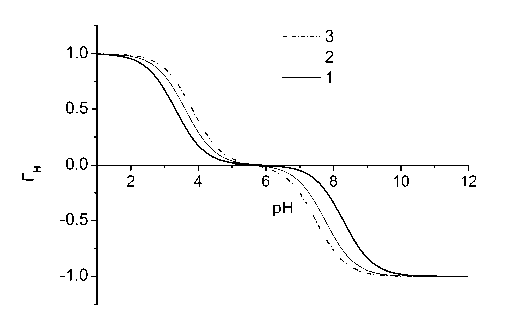
Рис. 1. Зависимость ^(pH) при различных концентрациях фонового электролита: 1 – 0.05 М, 2 – 0.25 М, 3 – 0.5 М NaCl.
Полученная зависимость ^(pH) может быть использована для построения соответствующего рК-спектра. Полная адсорбция ионов водорода на поверхности изучаемого сорбента, очевидно, равна:
N_ N_ I r H ( pH ) +Г 0 = 5r H i = ^r i pH-pK. ■ (7)
i i 1 + wp p 1
Суммирование в уравнении (7) проводится по всем ионам водорода или числу кислотно-основных центров N , находящихся на поверхности данного образца. Г , - полная обменная емкость i - го кислотно-основного центра, pK i – показатель константы диссоциации этого центра (отрицательный десятичный логарифм константы диссоциации). Г 0 — количество адсорбированных ионов водорода на изучаемой поверхности, не зависящее от рН раствора и соответствующее точке нулевого заряда протонов этой поверхности. Эту величину можно рассматривать как количество «не титруемых» в условиях проведения эксперимента ионов водорода, например, ионы водорода, входящие в состав OH-групп на поверхности изучаемого адсорбента, когда pK , ^- го . Величины Г н ( pH ) и Г ) могут быть как положительными, так и отрицательными в зависимости от положения разделяющей поверхности, которая обычно соответствует поверхности образца.
Сложность решения уравнения (7) относительно величин Г, обусловлена тем, что общее число N кислотно-основных центров заранее неизвестно.
Таким образом, каждое уравнение системы (7) линейно зависит от Г ) и N величин r i , а также нелинейно от N величин pK i . Общее число неизвестных равно 2 N +1. Для решения такой системы уравнений следует составить по меньшей мере 2 N +1 уравнений, что возможно, если экспериментальную кривую титрования аппроксимировать каким-либо сглаживающим сплайном и использовать этот сплайн для расчета величин Г н ( pH ) при заданных значениях рН. Очевидно, стандартный метод наименьших квадратов в данном случае не подходит, тем более, что заранее известно, что величины Г, положительны.
Поскольку величины Г i являются однозначными функциями дискретного множества величин pK i , уравнение (7) можно переписать в виде: rH ( pH ) = -r0 + N HpK ’- 5 ( pK - pK i )-- - pK .
I = 1 -го 1 + 10p p
Здесь d ( pK - pK i ) - дельта-функция. Число уравнений вида (8) равно числу величин Г н ( pH ) , соответствующих дискретным значениям рН и определяемых с помощью выше упомянутого сплайна.
Если значения величин pKi лежат в интер- вале pKmin < pKi < pKmax, то уравнение (8) можно представить в виде:
Гн^-Г )
N pKmax
+ Z j r(pK)- 5(pK-pp)-i=1pK ■ min dpK i+iopH"pK.
Разбивая область интегрирования на интервалы шириной ApK, представим каждый интеграл уравнения (9) в виде суммы: pKmax
HK)* - pK, )- »pK = pKmin 1 + 10 , (10)
l pK y +A pK
= Z j г( pK ) -6 ( pK - pK , ) . > pK
J = 0 pK ,. 1 + 10
где l = ( pKmax - pKmin ) / A pK-1 - равно числу интервалов шириной A pK . В результате уравнение (10) принимает вид:
Г ( pH ) = -f 0 +
Nl
+ z z i = 1 j = 0
= -Г0 + lN
+z z j=0 i=1
pK j +A pK
J r ( pK ) .S ( pK - pK , ) . —L pK j
PK j +A pK J V
J* ) -8( pK - pK , ) - 1 + 1" pH - pK .
pK j
Выполняя интегрирование и суммирование по i в последнем уравнении, получаем:
Г н ( pH ) = -Г 0 + z aj , J =0 J
где а равно либо 0, либо Г ,-- H - p ,
1 + 10p p i если pKi попадает в интервал pKmin + jApK < "K < pKmin + (j + 1)apK - в ре-mn mn зультате чего pKi можно аппроксимировать вели- чиной pK j = pKmin + jApK , положив
{Г, | i = 1...N} ■ {Гj | j = 0.J}. Окончательно урав- нение (11) принимает вид:
l 1
гн ( pH ) = г, - ( - 1 ) +У г, ----———,
H\r / 0 \ j 1 + 10"H -(pKmin+ jApK) , где
г , =1
; > 0 , если
_pKmin + jApK < "Ki < pKmin + (j + 1)ApK.
Таким образом, нахождение набора чисел
{ Г j\ j = 0.. l } , включающего набор чисел
{Г, | i = 1...N}, можно выполнить обычным методом наименьших квадратов с ограничением на положительные значения корней (алгоритм NNLS [7]), если предполагается, что Г, и Г0 > 0, на основе экспе- риментальной зависимости Гн (pH). Неопределенность найденных таким образом величин pKi характеризуется шагом ApK изменения pK и может быть снижена уменьшением этого шага и, соответственно, возрастанием числа членов l суммы по j в уравнении (12), если экспериментальную зависимость Гн (pH) интерполировать соответствующим сплайном. Величину ApK можно рассматривать как доверительный интервал для найденной таким образом величины pKi . Данная задача относится к числу некорректных задач [8], и при ее решении необходимо принимать во внимание погрешность экспериментальных данных.
Результаты решения задачи удобно представлять в виде гистограммы зависимости чисел l qj =Гj £ Г от соответствующих им величин J Л i=0
pK j . Число полос на такой гистограмме будет равно числу индивидуальных равновесий, описывающих изучаемую диаграмму состав – свойство. Сама гистограмма может быть названа рК-спектром изучаемой системы. Надежный рК-спектр, очевидно, может быть получен лишь при минимально возможной погрешности экспериментальных данных. В данном случае возникает своеобразный принцип неопределенности , согласно которому неопределенность рК-спектра является следствием неопределенности ошибки эксперимента.
На рис. 2 представлен рK-спектр (для A pK=0.1), построенный по данным рис. 1, из которого видно, что найденные этим методом величины рК i близки к заданным при построении рис. 1. По оси ординат здесь отложена относительная мольная доля соответствующего кислотно-основного центра от общего их числа ( q ).
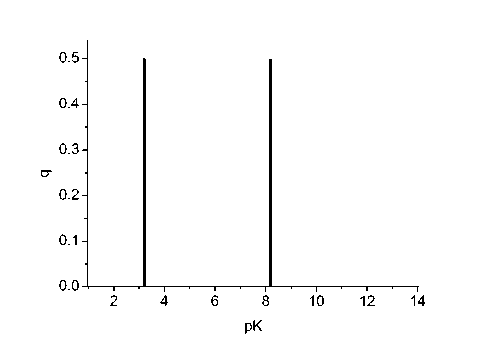
Рис. 2. рК-спектр анатаза при [NaCl]=0.
Уравнение (6) перепишем в виде:
Г H(pH) =
[H + ]2 - K‘K 2
[H + ]2 + K ‘ [H + ] + K 1 K 2
в котором штрихованные константы соответствуют величинам рК i , получаемым при использовании фонового электролита:
K 1 =
K 1 • K 3 _
K 3 + K 1[NaCl] ’
и
K 2 = K 4[NaCl] + K 2 .
При этом K1 и K 2 соответствуют, очевидно, предельным значениям штрихованных констант при нулевой концентрации фонового электролита. Если константы K1 и K2 найдены в условиях очень низкой (практически нулевой) концентрации фонового электролита, то уравнения (14) и (15) позволяют определить константы K3 и K4 при условии, что штрихованные константы определены из рК-спектров, соответствующих заданной концентрации фонового электролита.
Из полученных уравнений следует, что при увеличении концентрации фонового электролита полоса, соответствующая величине pK, должна сдвигаться в сторону более высоких значений, а полоса, соответствующая величине pK^, в сторону более низких значений. Положение точки нулевого заряда протонов pznpc (Гн (pH) = 0) определяется выражением:
pznpc = I (pK 1 + pK^) =
^(pK1 + pK2) - ^g
K 3( K 2 + K 4[NaCl]) ’ K 2( K 3 + K 1[NaCl])
и в пределе очень большой концентрации фоново- го электролита стремится к величине
2"(pKg + pK4). При специфической адсорбции катионов фона на изучаемой поверхности точка нулевого зарядов протонов сдвигается в область более низких значений рН, а при специфической адсорбции анионов – в сторону более высоких значений рН. При достаточно высоком сродстве поверхности к присутствующим в растворе катионам можно ожидать, что величина Гн (pH) во всей изучаемой области рН окажется отрицательной.
Список литературы Кислотно-основные свойства поверхности оксидных материалов
- Davis J.A., James R.O., Leckie J.O.//J. Colloid and Interface Sci. 1978. Vol. 61. No. 3. P. 480.
- Рязанов М.А., Дудкин Б.Н.//Коллоид. журн. 2003. Т. 65. № 6. С. 831.
- Ryazanov M.A., Dudkin B.N. Rus. Journal of Phys. Chem. A. 2009. Vol. 83. No. 13. P. 2318.
- Танабе К. Твердые кислоты и основания. М.: Мир, 1973.
- Юшкин Н.П. Минеральный мир и биосфера: минеральный организмобиоз, биоминеральные взаимодействия, коэволюция//Матер. IV Международного семинара «Минералогия и жизнь: Происхождение биосферы и коэволюция минерального и биологического миров». Сыктывкар. Геопринт, 2007. С. 5.
- Huertas F.J., Chou Lei, Wollast R.//Geochim. et Cosmochim. Acta. 1998. Vol. 62. Nо. 3. P. 417.
- Лоусон Ч., Хенсон Д. Численное решение задач метода наименьших квадратов. М.: Наука, 1986. 230 с.
- Тихонов А.Н., Гончарский А.В., Степанов В.В., Ягола А.Г. Численные методы решения некорректных задач. М.: Наука, 1990. 230 с.


