Классификация, частота и клинико-морфофункциональные типы повторных внутристентовых рестенозов
Автор: Шевченко Ю.Л., Чотчаев Ш.А., Ермаков Д.Ю.
Журнал: Вестник Национального медико-хирургического центра им. Н.И. Пирогова @vestnik-pirogov-center
Рубрика: Редакционные статьи
Статья в выпуске: 1 т.21, 2026 года.
Бесплатный доступ
В настоящее время проблема повторного внутристентового рестеноза (ВСР) коронарных артерий (КА) остается основным лимитирующим фактором ЧКВ в отдаленном периоде наблюдения. Цель. Разработать комплексную клинико-морфофункциональную классификацию и оценить частоту, структуру и клинически значимые варианты повторных внутристентовых рестенозов. Материалы и методы. В исследование на ретроспективной основе включено 168 пациентов с рецидивом рестеноза КА, которые перенесли эндоваскулярную реваскуляризациию в Клинике грудной и сердечно-сосудистой хирургии имени Святого Георгия ФГБУ «НМХЦ им. Н.И. Пирогова» Минздрава России. Результаты. На основании полученных данных рестенозы были классифицированы следующим образом: 1. Клиническая стратификация: бессимптомный (43,5%), стабильный (47,6%), ОКС-ассоциированный (8,9%); 2. Хронологическая: ранний (25,6%), поздний (36,3%), отдаленный (38,1%); 3. Анатомическая: локальный (35,5%), диффузный (27,3%), пролиферативный (27,1%), окклюзивный (10,1%); 4. Этиологическая: мальпозиция (74,4%), отсутствие мальпозиции (25,6%); 5. Анамнестическая: рецидив после БЛП (42,3%), после имплантации стента (33,3%), резидуальный рестеноз (24,4%). Заключение. Разработанная клинико-морфофункциональная классификация повторных внутристентовых рестенозов позволяет объективно описать структуру, частоту и особенности клинического течения
Ишемическая болезнь сердца, внутристентовый рестеноз, рецидив ишемии миокарда, чрескожное коронарное вмешательство
Короткий адрес: https://sciup.org/140314173
IDR: 140314173 | DOI: 10.25881/20728255_2026_21_1_4
Classification, Frequency, and Clinical and Morphofunctional Types of Repeated In-Stent Restenoses
Currently, the problem of repeat in-stent restenosis (ISR) of coronary arteries (CA) remains the main limiting factor for PCI in the long-term follow-up period. Objective. To develop a comprehensive clinical and morphofunctional classification and evaluate the frequency, structure, and clinically significant types of repeat in-stent restenoses. Materials and methods. This retrospective study included 168 patients with recurrent coronary restenosis who underwent endovascular revascularization at the St. George Thoracic and Cardiovascular Surgery Clinic of the N. I. Pirogov National Medical Surgical Center of the Ministry of Health of the Russian Federation. Results. Based on the obtained data, restenoses were classified as follows: 1. Clinical stratification: asymptomatic (43.5%), stable (47.6%), ACS-associated (8.9%); 2. Chronological: early (25.6%), late (36.3%), distant (38.1%); 3. Anatomical: local (35.5%), diffuse (27.3%), proliferative (27.1%), occlusive (10.1%); 4. Etiologic: malposition (74.4%), no malposition (25.6%); 5. Anamnestic: recurrence after BLP (42.3%), after stent implantation (33.3%), residual restenosis (24.4%). Conclusion. The developed clinical and morphofunctional classification of repeated in-stent restenoses allows for an objective description of the structure, frequency and characteristics of the clinical course.
Текст научной статьи Классификация, частота и клинико-морфофункциональные типы повторных внутристентовых рестенозов
В последние десятилетия достижения в эндоваскулярной хирургии существенно расширили возможности лечения пациентов с ИБС [1]. Однако, несмотря на революционное снижение частоты рестенозов с внедрением стентов с лекарственным покрытием (СЛП), проблема повторного внутристентового рестеноза (ВСР) продолжает сохранять особую актуальность. По данным крупных регистров суммарная частота ВСР, несмотря на технический прогресс, достигает 10–15% даже в наиболее благоприятных клинических и морфологических группах, тогда как при наличии фоновых факторов риска (сахарный диабет, малый диаметр сосуда, диффузные и бифуркационные поражения) достигает 30% и выше [2–7].
ВСР напрямую ассоциирован с ухудшением долгосрочного прогноза, потребностью в повторных вмеша- тельствах, тяжелыми рецидивами стенокардии, высокой частотой острого коронарного синдрома и инфаркта миокарда [8]. При этом фундаментальные механизмы и отличия патогенеза повторного рестеноза по-прежнему активно изучаются, что требует создания современной многоуровневой классификации, учитывающей как клинические, так и морфофункциональные параметры, возможности внутрисосудистой визуализации [9; 10].
На сегодняшний день большинство существующих классификаций рестенозов базируется или на хронологических (временных), или анатомических признаках поражений, однако для правильного выбора тактики лечения и прогнозирования течения заболевания клиницисту необходим многоуровневый системный инструмент, объединяющий объектные и субъективные признаки, данные инструментальной верификации, морфологиче-

ские детали поражения и анализ эффективности предшествующих вмешательств.
Первые описания феномена рестеноза появились с момента активного распространения баллонной ангиопластики, когда частота клинических рецидивов стенокардии достигала 30–50% в течение первого года после процедуры [11]. Уже на этом этапе были предложены критерии «раннего» и «позднего» рестеноза в зависимости от сроков дебюта стеноза после вмешательства, а также выделены клинические и морфологические варианты, ассоциированные с рецидивом болезни [12].
С внедрением металлических и, позднее, лекарственных стентов, рестеноз в значительной степени эволюционировал: современная морфологическая картина характеризуется развитием неоинтимальной гиперплазии, формированием неоатеросклероза, а также особенностями ремоделирования сосудистой стенки – фиброз, кальцификация. Особое внимание уделяется техническим причинами рестеноза: мальпозиция стента, неадекватная длительность его раскрытия, переломы стентов, некачественная подготовка поражения и постдилатация [13].
Вопрос унифицированного подхода к классификации повторных ВСР и анализа их клинико-морфофункциональных характеристик имеет ключевое значение для выбора оптимальной тактики лечения и прогнозирования исходов.
Цель исследования
Разработать комплексную клинико-морфофункциональную классификацию и оценить частоту, структуру и клинически значимые варианты повторных внутристен-товых рестенозов у 168 пациентов, включая подгруппу с поражениями аутовенозных шунтов.
Материалы и методы
В исследование включено 168 пациентов, перенесших повторные внутристентовые рестенозы, в том числе 15 больных с рестенозами в стентах аутовенозных шунтов. 125 (81,7%) мужчин и 28 (18,3%) женщин, средний возраст – 57±10,5 лет, находившихся на лечении в Клинике грудной и сердечно-сосудистой хирургии имени Святого Георгия ФГБУ «НМХЦ им. Н.И. Пирогова» Минздрава России.
Диагностика основана на комплексной оценке: оценка клинического состояния пациента, результатов функционального тестирования на ишемию миокарда (сцинтиграфия миокарда с нагрузкой, стресс-ЭхоКГ), стандартная коронарная ангиография, внутрисосудистое ультразвуковое исследование (ВСУЗИ).
Внутристентовым стенозом считали значимое уменьшение диаметра просвета в стентированном сегменте коронарной артерии более 50%, или на расстоянии 5 мм проксимальнее или дистальнее стента, подтвержденное результатами коронарной ангиографии или внутрисосудистой визуализации – ВСУЗИ.
Повторным (рецидивирующим) внутристентовым стенозом считали повторное развитие гемодинамически значимого сужения (≥50%) в том же сегменте коронарной артерии после успешного вмешательства по поводу предыдущего внутристентового рестеноза (баллонная ангиопластика, повторное стентирование).
Пациенты стратифицировались по следующим признакам:
-
• клинический (бессимптомный, стабильный, ОКС-ассоциированный),
-
• хронологический (ранний, поздний, отдалённый),
-
• анатомический (адаптация классификации R. Mehran),
-
• ультразвуковой (наличие мальпозиции стента),
-
• по эффективности предыдущих вмешательств (рецидив после баллона/стента, остаточный рестеноз).
Результаты
Классификация и частота различных типов повторного рестеноза
Все пациенты с повторными рестенозами (n = 168) были стратифицированы по многоуровневой системе. Структура представлена в таблице 1.
Распределение по подгруппам
Среди небифуркационных поражений наиболее часто встречались локальные (35,5%) и диффузные (27,3%) формы, что затрудняет повторную реваскуляризацию за счет протяженности поражения.
Табл. 1. Клинико-морфофункциональные типы повторных рестенозов
|
Признак |
Все пациенты c повторными рестенозами (n = 168) |
|
1. Клиническая стратификация |
|
|
А. Бессимптомный |
73 (43,5%) |
|
Б. Стабильный |
80 (47,6%) |
|
В. ОКС-ассоциированный |
15 (8,9%) |
2. Хронологическая стратификация
|
А. Ранний (<6 мес.) |
43 (25,6%) |
|
Б. Поздний (6–12 мес.) |
61 (36,3%) |
|
В. Отдаленный (более 12 мес.) |
64 (38,1%) |
|
3. Анатомическая стратификация рестеноза небифуркационного поражения, n = 110 (65,5%) |
|
Б. Краевой рестеноз (рестеноз в пределах
Г. Мультифокальный рестеноз. |
39 (35,5%) |
|
II. Диффузный в пределах стентов (рестеноз >10 мм, но в пределах стентов) |
30 (27,3%) |
|
III. Пролиферативный (распространенный за пределы стентов) |
29 (27,1%) |
|
IV. Окклюзивный рестеноз |
12 (10,1%) |

Табл. 1. Клинико-морфофункциональные типы повторных рестенозов (продолжение)
|
Признак |
Все пациенты c повторными рестенозами (n = 168) |
|
3. Анатомическая стратификация рестеноза бифуркационного поражения, n = 43 (25,6%) |
|
Б. Локальный дистальный рестеноз (рестеноз в основной ветви дистальнее бифуркации)
Г. Локальный рестеноз в области бифуркации (рестеноз основной и боковой ветвей) |
15 (34,9%) |
|
II. Диффузный рестеноз в пределах стентов (распространенное поражение основной и боковой ветвей) |
15 (34,9%) |
|
III. Пролиферативный (распространенный за пределы стентов) |
10 (23,3%) |
|
IV. Окклюзивный рестеноз |
3 (6,9%) |
|
3. Анатомическая стратификация рестеноза аутовенозных шунтов, n = 15 (8,9%) |
|
|
I. Локальный |
3 (20%) |
|
II. Диффузный рестеноз в пределах стентов |
6 (40%) |
|
III. Пролиферативный (распространенный за пределы стентов) |
5 (33,3%) |
|
IV. Окклюзивный рестеноз |
1 (6,7%) |
|
1. Внутрисосудистая ультразвуковая стратификация рестеноза |
|
|
А. Мальпозиция стента |
125 (74,4%) |
|
Б. Внутристентовый рестеноз без мальпозиции стента |
43 (25,6%) |
|
2. Стратификация рестеноза согласно эффективности предыдущего ЧКВ (второй операции) |
|
|
А. Рецидив после БЛП (лекарственного баллона) |
71 (42,3%) |
|
Б. Рестеноз после повторного стентирования |
56 (33,3%) |
|
В. Остаточный рестеноз после множественных неудачные ЧКВ |
41 (24,4%) |
Рестенозы после стентирования артерии

IA. Локальный рестеноз в местах наложения стентов или промежутках между ними
IБ. Краевой рестеноз (в пределах 5 мм от края стентов)

IГ. Мультифокальный рестеноз
IB. Локальный рестеноз в пределах стентов (ограниченный участок внутри стентов, <10 мм)

II. Диффузный рестеноз в пределах стента (р естеноз более 10 мм, но в пределах стентов)

III. Пролиферативный рестеноз (распространенный за пределы стентов)

IV. Окклюзивный рестеноз
Рис. 1. Адаптированная анатомическая классификация ВСР при небифуркационных поражениях.
Рестенозы после бифуркационного стентирования
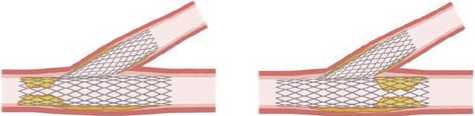
IA. Локальный проксимальный рестеноз IБ. Локальный дистальный рестеноз
(в основной ветви проксимальнее бифуркации) (в основной ветви дистальнее бифуркации)

Пролиферативные (27,1%) и окклюзивные (10,1%) рестенозы были связаны с наихудшими клиническими исходами.
В группе бифуркационных поражений доля локальных и диффузных типов примерно одинакова, но на 6,9% случаев приходится окклюзивный тип – осложнения вмешательств в области бифуркаций наиболее неблагоприятны.
В разделе поражений аутовенозных шунтов диффузные (40%) и пролиферативные (33,3%) формы превалировали, что связано с особенностями структуры венозной стенки и более выраженным пролиферативновоспалительным ответом.
Стратификация по технике и результату предыдущего вмешательства
Высокая доля (42,3%) рецидивов отмечалась после баллонной ангиопластики с лекарственным покрытием;
IB. Локальный рестеноз боковой ветви IГ. Локальный pестеноз бифуркации
(в устье или в другом сегменте боковой ветви) (в основной и боковой ветвях)
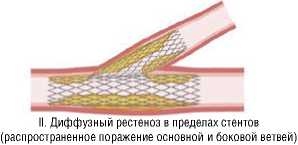
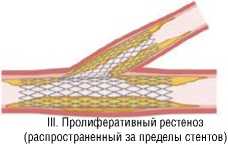
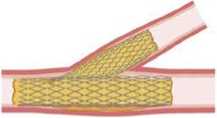
IV. Окклюзивный рестеноз
Рис. 2. Адаптированная анатомическая классификация ВСР при бифуркационных поражениях.

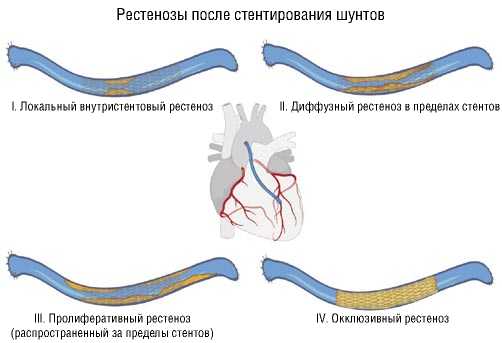
Рис. 3. Адаптированная анатомическая классификация ВСР шунтов.
33,3% после повторного стентирования. 74,4% всех повторных рестенозов ассоциированы с выявленной маль-позицией стента при внутрисосудистом исследовании – что отражает ключевую роль технических факторов.
Обсуждение
Анализ комплекса клинических, инструментальных и морфологических факторов указывает на чрезвычайную гетерогенность как клинического течения ВСР, так и его морфологических вариантов. Представленные результаты подтверждают данные мировых регистров: большинство рестенозов имеют бессимптомное или стабильное течение, но не менее 9% сопровождаются острыми коронарными событиями, требующими немедленной повторной реваскуляризации [14–16].
Особое значение следует уделять техническим дефектам имплантации: мальпозиция стента, выявленная в нашем исследовании в 74,4% случаев, несомненно, является важнейшей причиной рецидива рестеноза. Применение ВСУЗИ позволяет не только верифицировать наличие мальпозиции, но и точно оценивать форму и протяжённость гиперплазии неоинтимы, степень неоатеросклероза и прогнозировать риск повторных событий [17].
Результаты исследования демонстрируют, что анатомическое распределение поражений существенно влияет на дальнейшую стратегию лечения: диффузные и пролиферативные типы рестенозов гораздо хуже поддаются повторным эндоваскулярным вмешательствам и требуют индивидуального подхода, тогда как локальные поражения в ряде случаев могут быть эффективно купированы лечением с использованием лекарственных баллонов или применением новых поколений стентов.
Повторные рестенозы по-прежнему требуют строгой индивидуализации на всех этапах лечения: выбор схемы вмешательства с учётом клинической стратификации (в т.ч. вид рестеноза, наличие мальпозиции или тотальной окклюзии), морфофункциональных особенностей и анамнеза эффективности предыдущих процедур [18].
Комплексная стратификация пациентов чрезвычайно важна в организации вторичной профилактики, формирования индивидуальных программ динамического наблюдения и своевременного выявления показаний к повторным вмешательствам.
Результаты и других исследований подчеркивают необходимость индивидуального подхода к ведению пациентов после коронарного стентирования, учитывающего весь спектр клинических, ангиографических и процедурных факторов риска [19].
Заключение
Разработанная клинико-морфофункциональная классификация повторных ВСР позволила объективно описать структуру, частоту и особенности клинического течения осложнения у 168 пациентов. Высокая частота мальпозиции стента как патогенетического механизма, а также превалирование диффузных и пролиферативных форм при бифуркационных поражениях и поражениях шунтов – важные аспекты при эндоваскулярной реваскуляризации.
Предлагаемый подход открывает перспективы для дальнейшей стратификации риска, эффективной персонализации терапии и улучшения долгосрочного прогноза у больных с повторными рестенозами.


