Классификация эмболизирующих агентов
Автор: Боломатов Н.В.
Журнал: Вестник Национального медико-хирургического центра им. Н.И. Пирогова @vestnik-pirogov-center
Рубрика: Обзоры литературы
Статья в выпуске: 3-2 т.15, 2020 года.
Бесплатный доступ
Катерная эмболизация в последние годы стала широко использоваться в клинической практике. Разработка новых эмболизирующих агентов и технологий позволила выполнять большое количество клинических задач. Существует ряд классификаций, которые позволяют подразделять эмболизационные материалы по различным признакам. Приводится анализ ранее разработанных классификаций эмболизирующих материалов, а также новый вариант классификации эмболизирующих материалов с учётом следующих признаков: способность к резорбции, механизм влияния на сосудистую стенку, физических и химических свойств.
Эмболизирующие агенты, эмболизирующие материалы, катетерная эмболизация, внутрисосудистая эмболизация, окклюзия
Короткий адрес: https://sciup.org/140260118
IDR: 140260118 | DOI: 10.25881/BPNMSC.2020.85.96.024
Classification of embolizing agents
In recent years, cutter embolization has become widely used in clinical practice. The development of new embolizing agents and technologies has made it possible to perform a large number of clinical tasks. There are a number of classifications that allow you to subdivide embolization materials according to various criteria. An analysis of the previously developed classifications of embolizing materials is given, as well as a new version of the classification of embolizing materials, taking into account the following features: the ability to resorption, the mechanism of influence on the vascular wall, physical and chemical properties.
Текст обзорной статьи Классификация эмболизирующих агентов
Эмболизация — мининвазивная внутрисосудистая операция, заключающаяся в избирательной окклюзии кровеносных сосудов при помощи специально введенного эмболизирующего материала (ЭМ). Согласно доступным данным, первая эмболизация была выполнена в 1904 г. R. Dawbarn, который окклюзировал артерии опухоли шеи парафином и вазелином через пункцию наружной сонной артерии [1]. Спустя 26 лет, в 1930 г., B. Brooks сообщил об окклюзии сонной артерии фрагментированной мышцей и серебряной клипсой у пациента с каротидно-кавернозным соустьем, операция проводилась под рентгеновским контролем [2]. В 1964 г. для лечения этой же патологии Speakman T.J. применил гемостатическую желатиновую губку [3]. Однако эти операции проводились методом прямой пункции артерии или через разрез в ней. Впервые катетерную или эндоваскулярную эмболизацию (ЭЭ) провел Чарльз Доттер в 1970 г., он выполнил эмболизацию правой желудочно-сальниковой артерии с целью остановки острого желудочного кровотечения. В качестве ЭМ применялись аутосвертки крови. Эта операция была проведена в силу невозможности оперировать пациента открытым способом [4]. Благодаря разработкам выдающегося отечественного нейрохирурга Ф.А. Сербиненко в 1971 г. был применен новый тип ЭМ — отделяемые баллоны [5]. В 1974 г. Tadavarthy et al. сообщили о первом применении синтетического полимера, поливинил алкоголя (ПВА) в качестве ЭМ [6]. В 1975 г. Gianturco C. et al. сообщили о разработке и использовании первых спиралей: устройство «cotton-tail» (ватный хвост), состоящее из восьми хлопковых нитей, прикрепленных к 3-мм стальному корпусу, и устройство «wool-tail» (шерстяной хвост), состоящее из четырех волокон шерсти, прикрепленных к пятисантиметровому проводнику [7]. Конструкция устройства в конечном итоге трансформировалась в спираль из нержавеющей стали в 1976 г., а шерстяные волокна были заменены синтетическими [8]. Со временем были разработаны и внедрены в клиническую практику различные клеевые композиции, сферы с радиофармпрепаратом (РФП), окклюдеры и другие ЭМ [9–14]. Также существуют ЭМ, которые не нашли широкого применения в клинической практики, используются в экспериментальных работах или находятся в стадии разработки [15–20].
В процессе совершенствования инструментов и накопления клинического опыта внутрисососудистые катетерные эмболизации получают все большее распространение в клинической практике. Это связано с малой травматичностью, небольшой частотой осложнений по сравнению с открытыми операциями, возможностью многократного применения. Широкое применение эти технологии нашли при остановке кровотечений, лечении опухолей, аневризм и ангиодисплазий. Ключевую роль при планировании и проведении ЭЭ занимает правильный подбор эмболизирующих агентов.
ЭМ были классифицированы по нескольким направлениям: физическим характеристикам (жидкий, твердый); продолжительности окклюзии сосудов (временная или постоянная); уровню окклюзии (проксимальная или дистальная); типу патологии, которую лечат; техники доставки; стоимости и многим другим признакам. Необходимо принять во внимание, что не все ЭМ доступны из-за ограничений по стоимости, а также из-за проблем маркетинга, традиций и законодательного регулирования. Доступность различных ЭМ для обеспечения надлежащего выполнения эмболизации по различным показаниям

является требованием для любого эндоваскулярного хирурга и стационара, выполняющих ЭЭ.
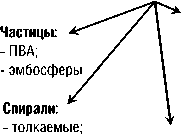
Наиболее распространенный способ классификации ЭМ заключается в том, чтобы определить их как временные или постоянные (Рис. 1) [21]. Это полезно при выборе материала, потому что для некоторых ЭЭ, таких как предоперационная эмболизация, химиоэмболизация или лечение кровотечений при травмах, может потребоваться использование временного ЭМ, тогда как для других клинических ситуаций постоянный эмболизирующий агент будет более подходящим. В настоящее время разработаны и внедрены в клиническую практику новые ЭМ такие как Phil микрочастицы с РФП, которые также не вошли в классификацию. Обращает на себя внимание отсутствие в градации по механизмам действия ЭМ, что очень важно учитывать при планировании операции.
В качестве признака классификации можно использовать физические свойства ЭМ: 1. Механические или твердые: спиральные эмболы, оделяемые баллоны; частицы (аутогемосгустки, ПВА, желатиновая губка, микросферы). 2. Жидкие: склерозирующие (спирт, натрия тетра-дицилсульфат), склеивающие (N-бутил-2-цианокрилат, этиблок) [22]. Эта классификация имеет также достаточно достоинств, такие как выделение в отдельный подкласс склерозирующих веществ. Однако не учитывается постоянный или временный характер окклюзии, не описываются ранее разработанные или применяемые ЭМ, а также нет современных эмболизирующих агентов, таких как неадгезивные композиты, что делает эту классификацию не полной.
В литературе встречается также классификация, подразделяющая ЭВ на два типа: механические агенты и поток-направляемые (табл. 1) [23; 24]. Данная классификация учитывает отношение агентов к потоку крови, также авторы включили в классификацию типы патологий, при которых можно их использовать. Среди недостатков классификации можно выделить отсутствие упоминания склонности к резорбции, малое количество ЭМ, которые вошли в классификацию, а также не учитываются материалы, которые недавно разработаны, в настоящее время не имеют широкого распространения или не применяются, это в свою очередь делает классификацию неполной.
Существует также классификация медицинских изделий, утверждённая приказом Минздрава России от 06.06.2012 г. N 4н (ред. от 07.07.2020 г.), в которую входят ЭМ. Она включает в себя все виды медицинских изделий, в том числе и ЭМ с номенклатурой и градацией по степени потенциального риска их применения для здоровья пациента [25]. Данную классификацию удобно применять при работе с органами власти, в административной и правовой работе, т.к. она является официально утвержденным документом. Однако, её неудобно применять в лечебной и исследовательской практике, т.к. даны только общие понятия о ЭМ.
Опыт практической и преподавательской деятельности позволяет сделать вывод о несовершенстве ранее
Эмболизирующие материалы
Временные:

Постоянные
- денатурированный коллаген;
- оксицеллюлоза;
- аутогемосгустки
Жидкие агенты:
- клей;
- onix©;
- этиловыспирт;
- Calcium alginate gel (ALGEL).
-
- спирали направляемые потоком;
-
- инекционне;
-
- отделяемые;
Другие устройства:
-
- окклюдеры;
-
- Grifka-Gianturco (GGVOD);
-
- отделяемые баллоны
- гидрогелевые
Рис. 1. Классификация ЭМ.
Табл. 1. Классификация ЭМ по отношению к току крови
-
1. Резорбирующиеся ЭМ (со временем подвергаются рассасыванию — резорбции):
-
– аутогемосгустки;
-
– денатурированный коллаген (гемостатическая желатиновая губка, Gelfoam);
-
– оксицеллюлоза (Oxycel, Surgicel, Becton Dickinson, Franklin Lakes);
– масляные вещества (липиодола ультра-флюид, вазелиновое масло).
-
2. Нерезорбирующиеся ЭМ (материалы, которые со временем не подвергаются резорбции):

-
А. Партикулярные (относящиеся к частицам):
-
– аутомышца;
-
– микрочастицы или микросферы (ПВА, три-акрил желатин и гидрогелевые сферы, микрочастицы с гидрогелем);
-
– микрочастицы с лекарственными препаратами;
-
– микрочастицы с ферромагнетиками;
-
– металлические шарики;
-
– микрочастицы с РФП.
Б. Непартикулярные (не относящиеся к частицам):
-
– спирали;
-
– фетр медицинский (ЭМ изготовленные из полимера 4-фторопласта).
-
– шовный материал;
-
– отделяемые баллонные катетеры;
-
– окклюдеры;
-
– стент-графты и стенты.
-
В . Жидкие:
-
– адгезивные клеевые композиты (ЭМ содержащие n-бутил-2-цианоакрилат);
-
– неадгезивные клеевые композиты или неадгезивные композиты (ЭМ содержащие полимер этилвинилового спирта: Onyx, Squid; или полимеры соединений поли-лактид-гликогена и полгидроксиэтилметакрилата: Phil);
-
– этиблок.
-
3. Склерозирующие ЭМ:
-
– этиловый спирт 96%;
-
– тетрадецилсульфат натрия (Сотрадекол, Тромбо-вар, Облитерол, Тергитол-4);
-
– полидокапол (Этоксисклерол);
-
– глюкоза 40% и большей концентрации.
-
4. Перспективные ЭМ.
(к этой группе ЭМ относятся вещества, составы, устройства, технологии, которые находятся в стадии разработки, доклинических испытаний). Предложенная классификация включает максимальное количество ЭВ как редко применяемые, так и недавно разработанных.
Автор заявляет об отсутствии конфликта интересов (The author declare no conflict of interest).
Список литературы Классификация эмболизирующих агентов
- Dawbarn R. The starvation operation for malignancy in the external carotid area. JAMA. 1904;43:792-795. Doi: 10,1001 / jama.1904.92500120002g.
- Brooks B. The treatment of traumatic arterio-venous fistula. South Med J. 1930;23:100-106.
- Speakman TJ. Internal occlusion of a carotid-cavernous fistula. J Neuro-surg. 1964;21:303-315.
- Dick R. Therapeutic angiographic embolization. Br. J. Radiol. 1977;50:2-41-242. Doi: 10.1259/0007-1285-50-592-241.
- Сербиненко Ф.А. Катетеризация и окклюзия больших церебральных сосудов и перспективы развития сосудистой нейрохирургии // Вопросы нейрохирургии. — 1971. — Т. 35. — №5. — С. 17-27. [Serbinenko FA. Kateterizatsiya i okklyuziya bol'shikh tserebral'nykh sosudov i perspektivy razvitiya sosudistoi neirokhirurgii. Voprosy neirokhirurgii. 1971;35(5):17-27. (In Russ).]
- Tadavarthy SM, Knight L, Ovitt TW, et al. Therapeutic transcatheter arterial embolization. Radiology. 1974;111:13-16.
- Gianturco C, Anderson JH, Wallace S. Mechanical devices for arterial occlusion. Am J Roentgenol Radium Ther Nucl Med. 1975;124:428-438.
- Rose SC. Mechanical devices for arterial occlusion and therapeutic vascular occlusion utilizing steel coil technique: clinical applications. AJR Am J Roentgenol. 2009;192:321-324. Doi: 10.2214/AJR.08.1610.
- Guimaraes M, Wooster M. Onyx (ethylene-vinyl alcohol copolymer) in peripheral applications. Semin Intervent Radiol. 2011;28:350-356. Doi:10.1055/s-0031-1284462.
- Laurent A, Beaujeux R, Wassef M, et al. Trisacryl gelatin microspheres for therapeutic embolization, I: development and in vitro evaluation. AJNR Am J Neuroradiol. 1996;17:533-540.
- Lewis AL, Gonzalez MV, Lloyd AW, et al. DC Bead: in-vitro characterization of a drug-delivery device for transarterial chemoembolization. J Vasc Interv Radiol. 2006;17:335-342. Doi:10.1097/01.RVI.0000195323.46152.B3.
- Yan ZP, Lin G, Zhao HY, et al. An experimental study and clinical pilot trials on yttrium-90 glass microspheres through the hepatic artery for treatment of primary liver cancer. Cancer. 1993;72:3210-3215. Doi: 10.1002/1097-0142(19931201)72:11-3210::aid-cncr2820721113-3.0.co;2-6.
- Weng L, Rostambeigi N, Zantek ND, et al. An in situ forming biodegradable hydrogel-based embolic agent for interventional therapies. Acta Biomater. 2013;9:8182-8191. Doi: 10.1016/j.actbio.2013.06.020.
- Owen RJ, Nation PN, Polakowski R, et al. A preclinical study of the safety and efficacy of Occlusin 500 artificial embolization device in sheep. Ca-rdiovasc Intervent Radiol. 2012;35:636-644. Doi: 10.1007/s00270-011-0218-7.
- Карелин М. И. Обоснование рентгеноэндоваскулярной ферромагнитной эмболизации и локальной ВЧ-гипертермии при почечно-кле-точном раке IV стадии. Экспериментальные исследования и клинические наблюдения. Дис. ... д-ра мед. наук. — СПб., 1998. [Karelin MI. Obosnovanie rentgenoendovaskulyarnoi ferromagnitnoi embolizatsii i lokal'noi VCh-gipertermii pri pochechno-kletochnom rake IVstadii. Eksperimental'nye issledovaniya iklinicheskie nablyudeniya. [dissertation] Saint Petersburg; 1998. (In Russ).]
- Rizk G, Atallah N, Bridi G. Renal arteriovenous fistula treated by catheter embolization. Br. J. Radiol. 1973;46:222-224. Doi: 10.1259 / 0007-128546-543-222.
- Dubois J, Sebag G, De Prost Y, et al. The treatment of soft tissue venous malformation in children: percutaneous sclerotherapy with Ethibloc. Radiology. 1991;180:195-198. Doi: 10.1148 / radiology.180.1.2052693.
- Lang E. Transcatheter embolization of pelvic vessels for control of intractable hemorrhage. Radiology. 1981;140(2):331-339. Doi: 10.1148 / radiology.140.2.7196055.
- Nguyen M, Lee D. Injectable biodegradable hydrogels. Macromol. Biosci. 2010;10:563-579. Doi: 10.1002/mabi.200900402.
- Andrews R, Binkert C. Relative rates of blood flow reduction during transcatheter arterial embolization with tris-acryl gelatin microspheres or polyvinyl alcohol: quantitative comparison in a swine model. J Vasc Interv Radiol. 2003;14:1311-131. Doi: 10.1097/01.rvi.0000092903.31640.70.
- Vaidya S, Tozer KR, Chen J. An overview of embolic agents. Semin Intervent Radiol. 2008;25(3):204-215. Doi: 10.1055/s-0028-1085930.
- Волков О.В. Основы ангиографии. — 20 с. [Volkov OV. Osnovy angio-grafii. 20 p. (In Russ).] Доступно по: http://grekov-clinic.ru/filesattached/ newslib/cookangio/cookangio.pdf.
- Hoshino J, Ubara Y, Suwabe T, et al. Intravascular embolization therapy in patients with enlarged polycystic liver. Am J Kidney Dis. 2014;63(6):937-944. Doi: 10.1053/j.ajkd.2014.01.422.
- Guimaraes M, Lencioni R, Gary P. Embolization Therapy: Principles and Clinical Applications. Wolters Kluwer Health; 2015.
- Приказ Минздрава России № 4н от 6.06.2012 «Об утверждении номенклатурной классификации медицинских изделий». [Order of the Ministry of Health of the Russian Federation N 4-n "Ob utverzhdenii nomenklaturnoi klassifikatsii meditsinskikh izdelii" dated 06 June 2012. (In Russ).] Доступно по https://legalacts.ru/doc/prikaz-minzdrava-rossii-ot-06062012-n-4n/.


