Кластеризация белковых молекул в водно-солевых растворах лизоцима
Автор: Рожков Сергей Павлович, Горюнов Андрей Сергеевич
Журнал: Ученые записки Петрозаводского государственного университета @uchzap-petrsu
Рубрика: Биология
Статья в выпуске: 4 (125), 2012 года.
Бесплатный доступ
Методом электронного парамагнитного резонанса показано, что среднее расстояние между спин-мечеными молекулами лизоцима (35 мг/мл) немонотонно и обратимо изменяется в зависимости от концентраций NaCl в диапазоне от 0 до 3 моль/л параллельно с изменениями гетерогенности раствора. Полученные результаты интерпретируются на основе представления о непрерывных закритических фазовых переходах и формировании различных типов белковых кластеров.
Дипольное взаимодействие спин-меток, кластеры белка, фазовая диаграмма
Короткий адрес: https://sciup.org/14750147
IDR: 14750147 | УДК: 577.322
Clusterization of protein molecules in water-salt lisozyme solutions
Electron paramagnetic resonance technique was employed to reveal the nonmonotonous and reversible alterations of the average distance between spin-labeled lysozyme molecules (35 mg/mL.). The changes depend on the NaCl concentration within the range of 0 to 3 mol/L and are parallel to the variations in the solution heterogeneity. The obtained results are interpreted based on the idea of continuous overcritical phase transitions and different types of protein clusters’ development.
Текст научной статьи Кластеризация белковых молекул в водно-солевых растворах лизоцима
В последние годы в связи с развитием прецизионных структурных методов исследования сложных микрогетерогенных биологических дисперсий все большее внимание уделяется проблеме возникновения в растворах глобулярных белков надмолекулярных структур – белковых кластеров различного типа. К ним относятся перманентные кластеры белковых макромолекул – олигомеры [31], динамические [25] и мезоскопические кластеры размерами в десятки и сотни нанометров [15], [24], [33], кинетические агрегаты размером в сотни и более нанометров [12], а также плотные жидкие фазы микроскопических размеров с концентрацией белка, на порядок большей, чем средняя по объему [10], [14], [20], зародыши кристаллической фазы, микрокристаллы и, наконец, гель [12]. Изучение таких белковых образований необходимо для решения ряда важных проблем биотехнологии, биологии и медицины, в числе которых кристаллизация белка [21], патогенез заболеваний, связанных с конденсацией белка [18], устойчивость белковых препаратов медицинского назначения [8], [23], регуляция осмотического гомеостаза висцеральных жидкостей [6], [7].
Ярким примером конденсации белка в водной среде является кристаллизации лизоцима в присутствии NaCl. Водно-солевые растворы этого белка подробно изучались разнообразными методами, в том числе с помощью теоретических моделей, с целью выяснить механизмы зародышеобразования и роста кристаллов [10], [12], [14], [20], [31]. При этом были построены фазовые диаграммы растворимости и разработаны экспериментальные и теоретические подходы, позволяющие установить соответствие между разными типами белковых ассоциатов в растворе и участками фазовой диаграммы, где они воз- никают. Это способствовало значительно более глубокому пониманию явления фазового перехода типа жидкость – жидкость и перманентных белковых кластеров размером до 10 нм [31].
Однако результаты, полученные разными методами, не позволяют дать однозначный ответ на самый общий вопрос о том, чем же являются обнаруженные концентрационные неоднородности [17], [22], [24], [31], [33]. Ряд авторов считают их статическими (перманентными, равновесными) кластерами [13], [31]. В то же время другие исследователи считают их динамическими [26], [30]. Поэтому актуальность привлечения дополнительных экспериментальных физических методов исследования концентрационных неоднородностей в белковых растворах, а также дальнейшего анализа данных, получаемых с помощью этих методов, на основе фазовых диаграмм сохраняется, несмотря на прогресс в решении ряда методических проблем, возникающих при изучении явлений кластеризации белков [32].
Уширение линий спектра ЭПР, обусловленное диполь-дипольным взаимодействием спин-меток, связанных с молекулой белка, нередко используют для оценки расстояния между парамагнитными центрами [2], [4], [18], [19]. Уширение можно зарегистрировать в спектрах ЭПР застеклованных матриц белков, если расстояние между парамагнитными центрами не превышает 6–8 нм [2]. Поскольку среднее расстояние между молекулами белка в плотной фазе (или в кластере) составляет 0,6–1 нм [24], то образование кластеров должно приводить к уширению спектров ЭПР спиновых меток. В настоящей работе ставилась задача зарегистрировать надмолекулярные формирования – от белковых кластеров до геля – путем оценки относительных изменений среднего расстояния между макромолекулами методом ЭПР спин-метки. Важной
задачей также было обсуждение полученных результатов на основе представления о разных типах белковых кластеров, возникающих в за-критической области фазовой диаграммы тройной системы вода – белок – соль.
МЕТОДЫ И МАТЕРИАЛЫ
Конъюгацию спиновой метки 4-(2-io-doacetamido)-2,2,6,6-tetramethylpiperidine 1-oxyl (Takeda Chemical Industries) с лизоцимом из белка куриных яиц (Sigma) проводили, следуя методике Лихтенштейна и др. [5]. При этом происходит избирательная модификация остатка аминокислоты гистидина-15 молекулы лизоцима (коэффициент посадки – 0,8) [5]. Для получения растворов с различной ионной силой в исходный раствор белка, приготовленного на основе 0,01 М фосфатного буфера, рН 6,4, добавлялись разные количества NaCl. Конечная концентрация белка в образцах составляла 35 мг/мл. Спектры ЭПР регистрировались с помощью радиоспектрометра Bruker EMX 6/1 (модуляция 100 кГц, амплитуда 1 Гс). Перед снятием спектров образцы выдерживали 6–8 часов при 20 °C для формирования возможной структурной организации раствора. При температуре 20 °C оценивали времена корреляции τ с вращения метки, связанной с белком, для разных концентраций соли на основе модели быстрого вращения радикала [4], используя отношение амплитуд низкопольной и центральной линии спектра, а также ширину центральной линии.
Уширение линий спектра ЭПР, обусловленное диполь-дипольным взаимодействием спиновых меток, исследовалось в замороженных (77 К) растворах спин-меченого белка. Температура 77 К в образце устанавливалась после мгновенного помещения кюветы в наполненный жидким азотом сосуд дьюара резонатора. Показано [34], что концентрационные неоднородности в растворах макромолекул сохраняются при мгновенном замораживании, поскольку лимитирующим фактором их сохранения является трансляционная диффузия молекул, сопряженная с преодолением достаточно больших потенциальных барьеров.
Амплитуду крайних компонент спектра d1 и центральной компоненты d и их отношение определяли для образцов с разным содержанием соли при 77 К в зависимости от СВЧ-мощности. Параметр d1/d, чувствительный к диполь-дипольному взаимодействию нитроксильных радикалов, может быть использован при концентрациях нитроксильных радикалов более 7 х 10-3 М для характеристики изменений среднего расстояния между спин-метками [4] и, соответственно, между спин-мечеными молекулами белков в условиях одного центра посадки спин-метки на белке. При понижении концентрации нитроксильных радикалов параметр d1/d стано- вится слабо чувствителен к расстоянию между ними [2], поэтому при концентрации радикалов менее 7 х 10-3 М для оценки их взаимодействия может быть использована форма кривой насыщения СВЧ-сигнала [4].
РЕЗУЛЬТАТЫ
Зависимости амплитуды центральной линии спектра ЭПР спин-меченого лизоцима от мощности СВЧ поля, представленные на рис. 1 для разных концентраций NaCl при 77, позволяют разбить рассматриваемый диапазон концентрации соли m3 (М/л) на три части по характеру насыщения сигнала: (1) 0 < m3< 0,15 М/л; (2) 0,3 М/л < m3< 1,5 М/л; (3) m3 > 1,5 М/л. При малых концентрациях соли (1) кривая насыщения менее пологая, чем в контроле (растворе белка без NaCl), при средних концентрациях (2) – более пологая, чем в контроле, в условиях высаливания (3) – снова менее пологая. Более пологие кривые насыщения отвечают и более близкому расположению спиновых меток [4]. Это позволяет использовать форму кривой насыщения для контроля изменений среднего расстояния взаимодействия между спиновыми метками l . Следовательно, можно полагать, что в 1-й части диапазона концентрации соли среднее расстояние l между спин-метками больше, чем в контроле, во 2-й – меньше, в 3-й – снова больше.
Увеличение СВЧ-мощности приводит к изменению параметров сигнала ЭПР и позволяет выявить различия между величинами d1/d для растворов спин-меченого лизоцима с разной концентрацией соли при 77 К. Если в условиях без насыщения (0,63 мВт) зависимость d1/d от концентрации соли проявляется слабо, то в условиях умеренного насыщения (12,4 мВт) зависимость становится более выраженной (рис. 2). Поскольку d1/d ~ l -1, то данные, представленные на рис. 1 и 2, указывают, что с ростом концентрации соли до 0,15 М среднее расстояние l между связанными с белком спиновыми метками увеличивается, затем уменьшается и вновь возрастает по достижении концентрации NaCl 3 М, которая является высаливающей.
Эти результаты, а также тот факт, что при общей концентрации спин-меток (и спин-мече-ного белка) 2,5 х 10-3 М параметр d 1 /d сохраняет чувствительность к изменению условий и СВЧ-мощности, свидетельствуют о том, что в растворе лизоцима образуются концентрационные неоднородности, в составе которых локальная концентрация превышает 7 х 10-3 М.
Образование вязкого белого геля в условиях высаливания лизоцима – известный эффект [12], [20], который наблюдали и мы еще до погружения образца в жидкий азот. Образец белка при добавлении 3 М NaCl мгновенно превращался в гель и оставался в состоянии геля белого цвета в течение 4 суток при 20 °С. Образцы белка,
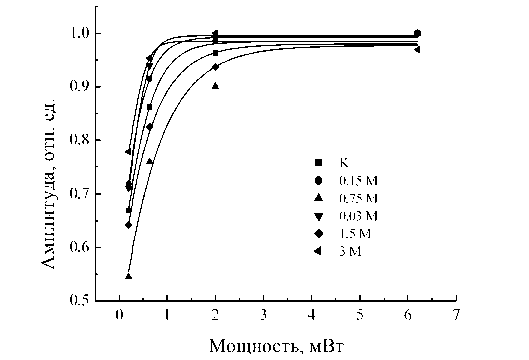
Рис. 1. Нормированные значения амплитуд центральной компоненты спектра ЭПР спин-меченого лизоцима в зависимости от насыщающей СВЧ-мощности при разных концентрациях NaCl в растворе белка
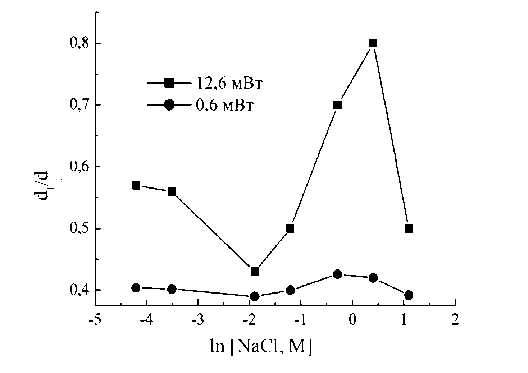
Рис. 2. Зависимость параметра d1/d от концентрации NaCl (М) как ln(NaCl) при значении СВЧ-мощности 12,6 мВт – (1) и 0,6 мВт – (2). Размер символа соответствует стандартной погрешности содержавшие менее 0,3 М NaCl, сохраняли прозрачность. В изначально прозрачных образцах, содержавших от 0,3 до 1,5 М NaCl, через 4 суток наблюдалась выраженная опалесценция, которая была тем более заметна, чем выше исходная концентрация NaCl. Постепенное уменьшение расстояния между молекулами белка в диапазоне 0,3–1,5 М NaCl, выявляемое на основе анализа спектров ЭПР спин-меченого лизоцима, можно связать с проявлением сильного взаимодействия белок – белок, которое, как предполагается, в этих условиях может приводить к формированию различных агрегатов, кластеров плотной фазы и даже зародышей кристаллической фазы [12], [14], [20]. Однако поскольку зародыши новой фазы обычно появляются лишь через несколько суток, следует предположить, что обнаруженное по спектрам ЭПР через 6–8 часов уменьшение расстояния в диапазоне 0,3– 0,8 М NaCl, поначалу не сопровождающееся визуально наблюдаемой опалесценцией, обусловлено формированием белковых кластеров и/или агрегатов вследствие потери системой термодинамической устойчивости.
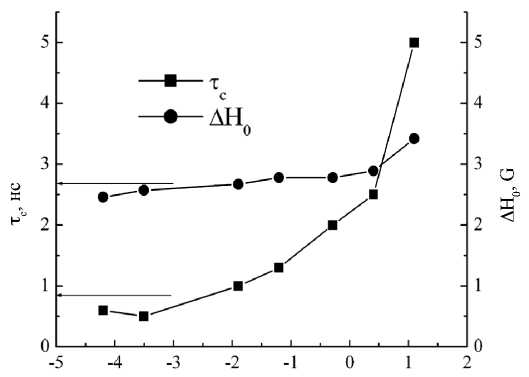
На рис. 3 эффективное время корреляции вращения спиновой метки, определяющееся отношением амплитуд линий спектра ЭПР [4], представлено в зависимости от концентрации соли при 20 °С. Как время корреляции, так и ширина центральной линии спектра монотонно возрастают во всем рассматриваемом диапазоне солей. Однако в растворе без соли время корреляции (горизонтальная линия на рис. 3) больше, чем в низкосолевых растворах. Поскольку в спектрах ЭПР в первую очередь проявляется наиболее быстрый тип подвижности спиновой метки, эти изменения времени корреляции отражают изменения микровязкости белковой глобулы в области локализации метки.
ln [NaCl, M]
Рис. 3. Зависимости изменения времени корреляции ( τ с) спин-метки, связанной с молекулой лизоцима, и ширины центральной компоненты ( Δ H0) спектра ЭПР спин-метки от концентрации NaCl. Горизонтальными отрезками показаны уровни τ с и Δ H0 в растворе белка без соли.
Размер символа соответствует стандартной погрешности
Первые две точки обеих зависимостей рис. 3 лежат ниже уровня значений, соответствующих раствору белка без соли (пунктир). Благодаря этому можно сделать вывод, что при концентрациях менее 0,05 М NaCl имеет место некоторое снижение микровязкости в области спин-метки, которое может быть связано с разрыхлением структуры белковой глобулы в этих условиях. Однако в дальнейшем значения обоих параметров возрастают и превышают уровень бессолевого раствора, что указывает на постепенную солью индуцируемую стабилизацию структуры белка в области спин-метки. Весьма вероятно, эти изменения сопряжены в том числе с усилением взаимодействия между молекулами белка при образовании высокосолевых мезоскопических кластеров, а впоследствии и при формировании зародышей кристаллической фазы.
Вблизи верхней границы рассматриваемого диапазона – при 3 М NaCl в условиях высали- вания при 20 °С в спектре ЭПР спин-меченого лизоцима – появляется широкая линия, и время корреляции существенно увеличивается. Это может указывать на сильное увеличение вязкости в системе, поскольку аналогичная линия наблюдается, например, в растворе 35 % сахарозы [3]. Однако среднее расстояние между спиновыми метками и молекулами белка при этом не уменьшается, как можно было бы ожидать, а остается на том же уровне, что и при физиологических концентрациях соли (рис. 2). Это говорит об отсутствии кристаллической фазы в геле и о том, что гель является целлюлярной, достаточно рыхлой структурой.
ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ
На рис. 4 представлена фазовая диаграмма раствора лизоцима, которая наряду с линиями бинодалей (1–3), полученными ранее экспериментально для фиксированных концентраций соли [20], содержит предлагаемую нами линию бинодали для концентрации 3 М NaCl (кривая 4). С увеличением концентрации соли критическая точка бинодали и спинодали (рис. 4) смещается все выше по оси температур, и область, ранее являвшаяся однофазной, оказывается на границе бинодали. При этом происходит фазовый переход типа жидкость – жидкость, связанный с образованием плотной и разбавленной фаз [20]. Соответственно, в растворах лизоцима при малых концентрациях NaCl бинодаль окажется в области низких температур, а с ростом концентрации соли до 1,5 М при содержании белка 35 мг/мл она сдвинется к 20 °С. При дальнейшем повышении концентрации соли до 3 М NaCl в результате быстрого кинетического процесса спинодального распада [14] вместо концентрированной, но прозрачной фазы (или микрокапель плотной фазы) образуется вязкий гель (см. рис. 1 в работе [12]).
Обычно в присутствии высоких концентраций солей раствор белка теряет термодинамическую устойчивость. Переход в устойчивое состояние может приводить к образованию зародышей кристаллической фазы или вязкого геля, установление равновесия в котором требует значительного времени. Образование вязкого геля белого цвета сопровождается сильной иммобилизацией спиновой метки относительно белка, которая приводит к появлению второй (широкой) линии в спектре ЭПР и к резкому возрастанию времени корреляции (рис. 3). Однако сохраняющееся сравнительно большое расстояние между молекулами белка (рис. 1 и 2) позволяет предположить, что пространственная сетка геля при этом формируется в виде ячеистой фрактальной структуры из белковых кластеров за счет межмолекулярных взаимодействий различной природы [14]. Возможно, часть кластеров появляется в результате некоторого разворачивания структуры белковой молекулы.
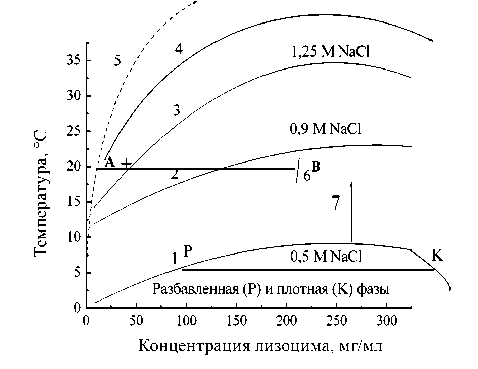
Рис. 4. Схематическая фазовая диаграмма раствора лизоцима: 1–3 – экспериментальные бинодали как линии равновесия фаз при соответствующей концентрации NaCl согласно [20]; 4 – предполагаемое положение бинодали при концентрации соли 3 М NaCl; 5 – линия растворимости белка при 0,5 М NaCl согласно [20]; 6 – предполагаемая линия гелеобразования при 3М NaCl. А и В – концентрация белка в разбавленной фазе и в геле соответственно;
7 – предполагаемая квазиспинодаль для кривой 1. Критической точке соответствует около 270 мг/мл белка.
Состояние исследуемого раствора лизоцима на фазовой диаграмме показано крестиком
В области физиологических концентраций соли фазовое разделение в наших экспериментах не обнаруживается. Следовательно, экспериментальная точка, соответствующая 20 ºС и 35 мг/мл лизоцима, располагается выше линии бинодали. При этом изменения концентрации соли во всем диапазоне ее низких значений, включая физиологические, заметно сказываются на диполь-ди-польном взаимодействии между спин-метками и, таким образом, на среднем расстоянии между молекулами белка. Это, вероятно, связано с существованием концентрационных неоднородностей. Они обнаруживаются и другими методами: светорассеяния, МУРР и МУНР – также в заведомо однофазной области – в окрестности линии растворимости, то есть выше и линии би-нодали, и температуры критической точки [24], [31], и интерпретируются как белковые кластеры. Мы предполагаем, что добавление NaCl вызывает постепенное замещение одних кластеров (1-го типа с размерами до 10 нм), которые доминируют в растворах без соли [31], другими кластерами (2-го типа с размерами около 100 нм), появляющимися при добавлении солей [24].
Данные рис. 3 позволяют предположить, что такой переход от одних кластеров к другим должен сопровождаться постепенным переходом белковой глобулы к более рыхлой структуре с повышенной гибкостью. Это может быть обусловлено тем, что по мере роста концентрации NaCl взаимодействие ионов Cl- с центрами сорбции белковой глобулы усиливается, а в связи с этим увеличивается осмотическое давление в водно-белковой матрице, способствующее ее разрыхлению из-за снижения удельной поверхностной энергии. Считается, что анионы хлора, помимо участия в экранировке положительно заряженных групп, также активно сорбируются специфическими неполярными участками молекул лизоцима и других белков благодаря устройству своей электронной оболочки и способности к поляризации [11]. Число таких адсорбированных анионов хлора может достигать десятка [27]. Однако при больших концентрациях соли, когда центры адсорбции насыщены, увеличение концентрации солей ведет к росту удельной поверхностной энергии вследствие эффектов предпочтительной гидратации [9].
Зависимость критической температуры системы вода – белок – соль от критического состава – соотношения молярных концентраций белка m2 и соли m3(X = (m2/m3)кр) (рис. 5) показывает, что и в области закритических состояний могут возникать условия для фазового перехода типа жидкость – жидкость [28], [29], который реализуется как флуктуационное мезофазное состояние. Это означает, что максимальные флуктуации концентрации будут иметь место в области квазиспинодали фазовой диаграммы в закритической области, то есть там, где и обнаруживаются экспериментально метастабильные мезоскопические кластеры белков [24].
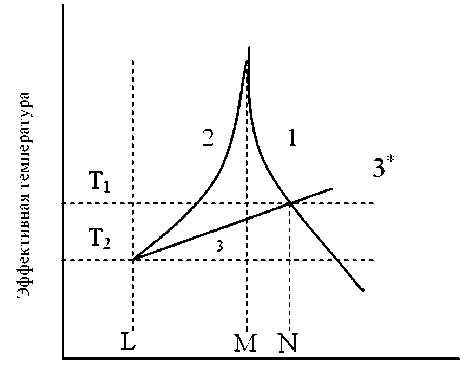
X = (m2/m3)кр
Рис. 5. Линии критических точек, устанавливающих соответствие критического состава X = (m2/m3)кр и эффективной температуры Т. Кривые 1 и 2 построены для концентраций соли, при которых производная от коэффициента активности соли по концентрации отрицательна и положительна соответственно.
При (m2/m3) > N квазиспинодаль (кривая 3*) выходит в закритическую область фазовой диаграммы.
При (m2/m3) < N кривая 3 может характеризовать положение линии бинодали [29]. Температуре T2 соответствует тройная точка, где (m2/m3) = L = 2/ ν и ν – число адсорбированных на белке анионов электролита
В соответствии с закономерностями термодинамики непрерывных фазовых переходов в закритической области система в целом является однородной, но при этом она постепенно теряет свойства двухфазной системы [1]. Эта трансформация может занимать значительную область фазовой диаграммы вдоль квазиспи-нодали и представлять собой область закрити-ческих фазовых переходов, захватывая линию растворимости. В этом случае флуктуирующая смесь кластеров белка является остаточным явлением низкотемпературного двухфазного состояния системы и представляет собой особое макроскопически однородное мезофазное состояние.
С другой стороны, если есть квазиспинодаль, то, вероятно, существует и квазибинодаль [1], то есть возможны такие условия, при которых во внешне однородных растворах будут существовать метастабильные белковые кластеры. Можно предположить, что кластеры – олигомеры лизоцима размерами до 10 нм являются гелеподобными квазичастицами [24], а мезоскопические кластеры – частью фрактальных агрегатов гелевой фазы. Поскольку гель образуется мгновенно после добавления избытка соли, естественно предположить, что еще до момента гелеобразования в растворе уже существует некоторая динамическая структура, имеющая отношение к мезоскопической кластерной организации. В области квазиспинодали в некотором диапазоне температур кластеры двух типов могут существовать одновременно, хотя и не находиться при этом в равновесии.
ЗАКЛЮЧЕНИЕ
Таким образом, наблюдаемые методом спиновой метки при комнатных температурах солью индуцированные изменения среднего расстояния между молекулами лизоцима в области физиологических концентраций NaCl, сопровождаемые увеличением гибкости молекул белка, могут быть обусловлены прохождением системы вода – белок – электролит области квазиспино-дали ее фазовой диаграммы. В этом состоянии пониженной термодинамической устойчивости система при макроскопической однородности будет представлять собой особое мезофазное состояние – смесь флуктуационных кластеров обеих граничных фаз – золя и геля. При концентрациях соли выше физиологических в растворе белка развивается термодинамическая неустойчивость, приводящая к формированию различных неустойчивых надмолекулярных структур типа фрактальных кластеров белка и зародышей кристаллической фазы. В области «высаливающих» концентраций соли имеет место фазовый переход золь – гель, приводящий систему к термодинамически устойчивому состоянию геля.
Список литературы Кластеризация белковых молекул в водно-солевых растворах лизоцима
- Базаров И. П. Термодинамика. М.: Высш. шк., 1983. 344 с.
- Вассерман А. М., Коварский А. Л. Спиновые метки и зонды в физикохимии полимеров. М.: Наука, 1986. 246 с.
- Кяйвяряйнен А. И., Рожков С. П. Сравнительный анализ времен корреляции молекул лизоцима и лизоцима в комплексе с ингибитором в области физиологических температур методом спиновой метки//Биофизика. 1987. Т. 32. № 1. С. 22-25.
- Лихтенштейн Г. И. Метод спиновых меток в молекулярной биологии. М.: Наука, 1974. 256 с.
- Лихтенштейн Г. И., Ахмедов Ю. Д., Иванов Л. В., Криницкая Л. А., Коханов Ю. В. Изучение молекул лизоцима методом спиновых меток//Молекулярная биология. 1974. T. 8. № 1. C. 48-57.
- Рожков С. П. Трехкомпонентная система вода-биополимер-ионы как модель молекулярных механизмов осмотического гомеостаза//Биофизика. 2001. Т. 46. № 1. С. 53-59.
- Рожков С. П. Критические явления, фазовые равновесия и структурно-температурный оптимум гомеостаза в модельной системе вода-биополимер-электролит//Биофизика. 2005. Т. 50. № 2. С. 115-122.
- Семенченко В. К. Избранные главы теоретической физики. М.: Просвещение, 1966. 396 с.
- Ahrer K., Buchacer A., Iberer G., Jungbauer A. Thermodynamic stability and formation of aggregates of human immunoglobulin G characterized by differential scanning alorimetry and dynamic light scattering//J. Biochem. Biophys. Methods. 2006. Vol. 66. № 1-3. P. 73-86.
- Arakawa T., Timasheff S. N. Mechanism of protein salting in and salting out by divalent salts: balance between hydration and salt binding//Biochemistry. 1984. Vol. 23. № 25. P. 5912-5923.
- Asherie N. Protein crystallization and phase diagrams//Methods. 2004. Vol. 34. № 3. P 266-272.
- Bostrom M., Williams D. R. M., Ninham B. W. Specific ion effects: why the properties of lysozyme in salt solutions follow a Hofmeister series//Biophys. J. 2003. Vol. 85. № 2. P. 686-694.
- Dumetz A. C., Chockla A. M., Kaler E. W., Lenhoff A. M. Protein phase behavior in aqueous solutions: crystallization, liquid-liquid phase separation, gels, and aggregates//Biophys. J. 2008. Vol. 94. № 2. P. 570-583.
- Fukasawa T., Sato T. Versatile application of indirect Fourier transformation to structure factor analysis: from X-ray diffraction of molecular liquids to small angle scattering of protein solutions//Phys. Chem. Chem. Phys. 2011. Vol. 13. № 8. P. 3187-3196.
- Georgalis Y., Umbach P., Soumpasis D. M., Saenger W. Dynamic and microstructure formation during nucleation of lysozyme solutions//J. Am. Chem. Soc. 1998. Vol. 120. № 22. P. 5539-5548.
- Glico O., Pan W., Katsonis P., Neumaier N., Galkin O., Weinkauf S., Vekilov P. G. Metastable liquid clusters in super and undersaturated protein solutions//J. Phys. Chem. B. 2007. Vol. 111. № 12. P. 3106-3114.
- Hill S. E., Robinson J., Matthews G., Musсhol M. Amyloid protofibrils of lysozyme nucleate and grow via oligomer fusion//Biophys. J. 2009. Vol. 96. № 9. P. 3781-3790.
- Igarashi K., Azuma M., Kato J., Ooshima H. The initial stage of crystallization of lysozyme: a differential scanning calorimetric (DSC) study//J. Cryst. Growth. 1999. Vol. 204. № 1-2. P. 191-200.
- Ionita P., Caragheorgheopol A., Gilbert B. C., Chechik V. Dipole-dipole interactions in spin-labeled Au nanoparticles as a measure of interspin distances//J. Phys. Chem. B. 2005. Vol. 109. № 9. P. 3734-3742.
- Mevorat-Kaplan K., Veiner L., Sheves M. Spin-labeling of Natronomonas pharaonis halorodopsin: Probing the cysteine residues environment//J. Phys. Chem. B. 2006. Vol. 110. № 17. P. 8825-8831.
- Muschol M., Rozenberger F. Liquid-liquid phase separation in supersaturated lysozyme solutions and associated precipitate formation/crystallization//J. Chem. Phys. 1997. Vol. 107. № 6. P. 1953-1962.
- Nanev C. N. On slow protein crystal nucleation: cluster-cluster aggregation on diffusional encounters//Cryst. Res. Technol. 2009. Vol. 44. № 1. P. 7-12.
- Niimura N., Minezaki Y., Ataka M., Katsura T. Aggregation in supersaturated lysozyme solution studied by time-resolved small angle neutron scattering//J. Cryst. Growth. 1995. Vol. 154. № 1-2. P. 136-144.
- Nishi H., Miyajima M., Nakagami H., Noda M., Uchiyama S., Fukui K. Phase separation of an IgG1 antibody solution under a low ionic strength condition//Pharm. Res. 2010. Vol. 27. № 7. P. 1348-1360.
- Pan W., Vekilov P. G., Lubchenko V. Anomalous mesoscopic phases in protein solutions//J. Phys. Chem. B. 2010. Vol. 114. № 22. P. 7620-7630.
- Piazza R. Protein interacton and association: an open challenge for colloid science//Curr. Opin. Colloid Interface Sci. 2004. Vol. 8. № 6. P 515-522.
- Porcar L., Falus P., Chen W.-R., Faraone A., Fratini E., Hong K., Baglioni P., Liu Y. Formation of the dynamic clusters in concentrated lysozyme protein solutions//J. Phys. Chem. Lett. 2010. Vol. 1. № 1. P. 126-129.
- Retailleau P., Ries-Kautt M., Ducruix A. No salting in of lysozyme chloride observed at low ionic strength over a large range of pH//Biophys. J. 1997. Vol. 73. № 4. P. 2156-2163.
- Rozhkov S. P. Phase transitions and precrystallization processes in a water-protein-electrolyte system//J. Cryst. Growth. 2004. Vol. 273. № 1-2. P. 266-279.
- Rozhkov S. P., Goryunov A. S. Effects of inorganic salts on the structural heterogeneity of serum albumin solutions//Eur. Biophys. J. 2000. Vol. 28. № 8. P. 639-645.
- Rozhkov S. P., Goryunov A. S. Thermodynamic study of protein phases formation and clustering in model water-protein-salt solutions//Biophys. Chem. 2010. Vol. 151. № 1-2. P. 22-28.
- Shukla A., Mylonas E., Di Cola E., Finet S., Timmins P., Narayanan T., Svergun D. I. Absence of equilibrium cluster phase in concentrated lysozyme solutions//Proc. Natl. Acad. Sci. USA. 2008. Vol. 105. № 13. P. 50755080.
- Stradner A., Cardinaux F., Schurtenberger P. A small-angle scattering study on equilibrium clusters in lysozyme solutions//J. Phys. Chem. B. 2006. Vol. 110. № 42. P. 21222-21231.
- Trewhella J. The different views from small angles//Proc. Natl. Acad. Sci. USA. 2008. Vol. 105. № 13. P. 4967-4968.
- Vekilov P. G. Metastable mesoscopic phases in concentrated protein solutions//Ann. N. Y. Acad. Sci. 2009. Vol. 1161. № 4. P. 377-386.
- Weber S., Wolff T., von Bunau G. Molecular mobility in liquid and in frozen micellar solutions. EPR spectroscopy of nitroxide free radicals//J. Colloid Interface Sci. 1996. Vol. 184. № 1. P. 163-169.


