Клеточные кооперации в разные сроки COVID-19 пневмонии
Автор: Тодоров Сергей Сергеевич, Тодоров Сергей сергеевич мЛ., Казьмин Андрей Сергеевич
Журнал: Волгоградский научно-медицинский журнал @bulletin-volgmed
Статья в выпуске: 3 т.20, 2023 года.
Бесплатный доступ
Цель работы: оценить степень выраженности воспалительной клеточной инфильтрации и экспрессии белков CD3, CD45, CD15, CD68 в разные сроки COVID-19 пневмонии. Материал для выполнения морфологического и иммуногистохимического исследования был получен во время выполнения вскрытий 80 умерших. Непосредственной причиной смерти больных при COVID-19 были острый респираторный дистресс-синдром (45 %), тромбоз ветвей легочной артерии (30 %), полиорганная недостаточность (25 %). Использована компьютерная морфометрия, определение коэффициента площади окрашивания с последующим статистическим анализом. Выполненное морфоиммуногистохимическое исследование легких при COVID-19 свидетельствует о существенном нарушении клеточной кооперации иммунокомпетентных клеток (CD3, CD45) с преобладанием макрофагов (CD68) в поздние сроки развития заболевания (22-40 суток). Вероятно, активация макрофального звена иммунитета может в дальнейшем инициировать развитие пневмофиброза и неоангиогенеза.
Covid-19 пневмония, клеточные кооперации, cd68+ макрофаги, сроки заболевания, ремоделирование
Короткий адрес: https://sciup.org/142238794
IDR: 142238794 | УДК: 616-091.8
Cellular cooperations at different times of COVID-19 pneumonia
Objective: to assess the severity of inflammatory cell infiltration and expression of CD3, CD45, CD15, CD68 proteins at different times of COVID-19 pneumonia. Material for morphological and immunohistochemical studies was obtained during autopsy of 80 deceased. The immediate cause of death in patients with COVID-19 was acute respiratory distress syndrome (45 %), thrombosis of the branches of the pulmonary artery (30 %), multiple organ failure (25 %). Computer morphometry was used, the staining area coefficient was determined, followed by statistical analysis. The role of immunocompetent cells at different stages of the development of COVID-19 pneumonia has been little studied. The performed morphoimmunohistochemical study of the lungs with COVID-19 indicates a significant disruption of cellular cooperation of immunocompetent cells (CD3, CD45) with a predominance of macrophages (CD68) in the late stages of the disease development (2240 days). Probably, activation of the macrophage link of immunity can further initiate the development of pneumofibrosis and neoangio-genesis.
Текст научной статьи Клеточные кооперации в разные сроки COVID-19 пневмонии
Новая коронавирусная инфекция, вызванная РНК-вирусом SARS-CoV-2, объявленная ВОЗ в марте 2020 г. пандемией, относится к особо опасным инфекциям с поражением легких и внутренних органов. Особое значение в патогенезе заболевания, которое носит название COVID-19, придают патологическим процессам в иммунной системе и кровеносных сосудах [1–3].
В отдельных отечественных патологоанатомических работах было показано значение различных иммуннокомпетентных клеток CD4, CD8, CD20 при
COVID-19 пневмонии [4]. По мнению авторов, преобладание CD8+ Т-лимфоцитов-супрессоров над CD4+ Т-лимфоцитами-хелперами рассматривается как признак аутоиммунного поражения, а повышенная экспрессия CD68+, CD31 в макрофагах может свидетельствовать о неблагоприятном прогнозе заболевания [5, 6].
В работе А. В. Смирнова и соавт. (2021) были выделены факторы неблагоприятного прогноза COVID-19 пневмонии: макрофагальная инфильтрация, генерализованное поражение микроциркуляторного русла с развитием тромбоэмболических осложнений, фиброз паренхимы легких, присоединение вторичной бактериальной инфекции [5]. Однако до настоящего времени работ, посвященных сравнительному изучению морфологических изменений в легких в динамике COVID-19 пневмонии, недостаточно [7–10].
ЦЕЛЬ РАБОТЫ
Оценить степень выраженности воспалительной клеточной инфильтрации и экспрессии белков CD3, CD45, CD15, CD68 в разные сроки COVID-19 пневмонии.
МЕТОДИКА ИССЛЕДОВАНИЯ
Материал для выполнения морфологического и иммуногистохимического исследования был получен во время выполнения вскрытий 80 умерших в разных стационарах Ростова-на-Дону. Участки легочной ткани (плотные, лаковые, отечные, резко полнокровные) иссекались в виде кусочков размерами не менее 2 × 2 см. Отдельно забирался материал для выполнения посмертного ПЦР-исследования с последующим обнаружением вируса SARS-CoV-2.
Среди умерших было 42 мужчины, 38 женщин, средний возраст которых составил 69 лет. Анализ историй болезни умерших пациентов с COVID-19 пневмонией выявил наличие коморбидной патологии: сахарный диабет (32,2 %), артериальная гипертензия (86,4 %), ожирение (33,4 %). Во всех наблюдениях COVID-19 пневмония была основным заболеванием в клиническом и патологоанатомическом диагнозах.
В зависимости от длительности развития заболевания, с учетом клинических данных COVID-19
пневмонии, нами были выделены хронологические группы: 1) 0–14 суток; 2) 15–21 суток; 3) 22–40 суток. Была использована компьютерная программа ImageJ (US National Institutes of Health, США) морфометрии, определение коэффициента площади окрашивания (КПО) (Славинский А. А., 2020) с последующим статистическим анализом.
Микроскопия и фотографирование полученных гистологических препаратов осуществлялась с помощью микроскопа Leica 1000DM c пакетом программного обеспечения (Германия).
Статистическую обработку полученных результатов осуществляли на персональном компьютере с применением статистических инструментов программы MedCalc Statistical Software version 19.1.3. Значения всех выборок подвергли проверке на характер распределения с помощью W-критерия Шапиро – Уилка. Поскольку распределение отличалось от нормального, для характеристики вариационных рядов использовали медиану, первый и третий квартили (Me [Q1; Q3]). Достоверность различия выборочных значений оценивали с помощью критерия Манна – Уитни. Нулевую гипотезу отвергали при пороговом значении p < 0,05.
Иммуногистохимическое исследование сосудов легких при COVID-19 пневмонии проводилось с использованием антител к CD3, CD45, CD15, CD68 (табл. 1).
Непосредственной причиной смерти больных при COVID-19 были острый респираторный дистресс-синдром (45 %), тромбоз ветвей легочной артерии (30 %), полиорганная недостаточность (25 %).
Таблица 1
|
Название антитела |
Прозводитель (фирма) |
Клон |
Происхождение антитела |
Разведение |
|
CD3 |
Cell Marque, США |
MRQ-39 |
rabbit monoclonal antibody |
1:200 |
|
CD45 |
Cell Marque, США |
LCA2811&PD7128 |
mouse monoclonal antibody |
1:200 |
|
CD15 |
Cell Marque, США |
MMA |
mouse monoclonal antibody |
rtu |
|
CD68 |
Cell Marque, США |
Kp-1 |
rabbit monoclonal antibody |
1:200 |
Антитела, используемые в исследовании
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ И ИХ ОБСУЖДЕНИЕ
В течение первых двух недель от начала COVID-19 пневмонии в стенках альвеол имелись белковые эозинофильные преципитаты с формированием гиалиновых мембран, в их просветах – лизированные эритроциты, нейтрофилы, макрофаги (рис. 1). В эти сроки отмечалась умеренная экспрессия CD3+, CD45+, CD15+ с периваскулярной локализацией, в то время как CD68+ обнаруживались внутриальвеолярно (рис. 2). В сроки 15–21 сутки COVID-19 пневмонии в просветах альвеол легких отмечалась резко выраженная нейтрофильная клеточная инфильтрация с участками деструкции межальвеолярных перегородок, скоплением гиалиновых мембран. Просветы мелких и средних артерий легких были резко эктазирова-ны, полнокровны. Экспрессия белков CD45+, CD3+ по сравнению с CD15+ и CD68+ была снижена. Отмечалось преобладание CD15+, CD68+ клеточной инфильтрации в просветах альвеол и периваскулярно.
Спустя 22–40 дней от начала развития COVID-19 пневмонии в паренхиме легочной ткани формировались фиброзные узелки, состоящие из фибробластов, макрофагов, лимфоцитов, вокруг которых имелись мелкие кровеносные сосуды с признаками резкого полнокровия и периваскулярными диапедезными кровоизлияниями. Фиброзные узелки были представлены CD68+ макрофагами с формированием веерообразных клеточных структур (рис. 3). Проведенная компьютерная морфометрия и статистическая обработка полученных данных позволила получить следующие результаты распределения воспалительных клеточных элементов (CD3, CD45, CD15, CD68) в легких при COVID-19 в динамике развития заболевания (рис. 4).
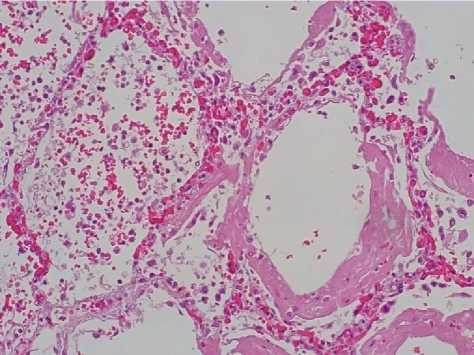
Рис. 1. В стенках альвеол – гиалиновые мембраны с резким утолщением. В просветах альвеол – лизированные эритроциты, нейтрофилы, макрофаги. Окраска гематоксилином-эозином. Увеличение ×200
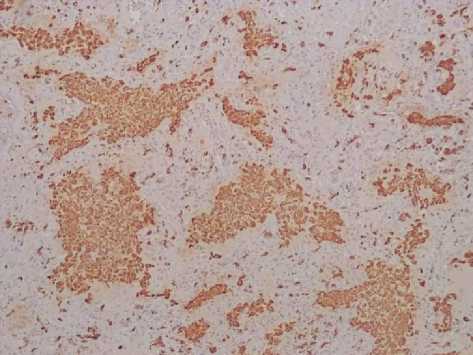
Рис. 2. Выраженная цитоплазматическая экспрессия CD68+ макрофагов с преимущественной внутриальвеолярной локализацией при COVID-19. Иммуногистохимическая реакция к CD68. Увеличение ×200
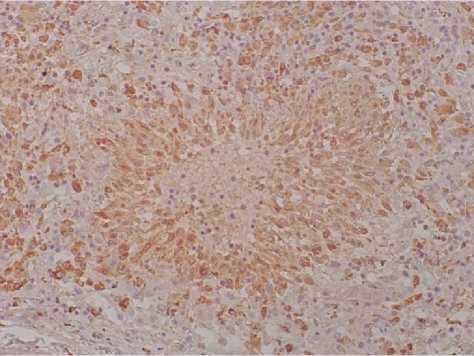
Рис. 3. Яркая экспрессия белка CD68+ в фиброзных узелках при COVID-19. Иммуногистохимическое исследование с антителом к CD68. Увеличение ×200
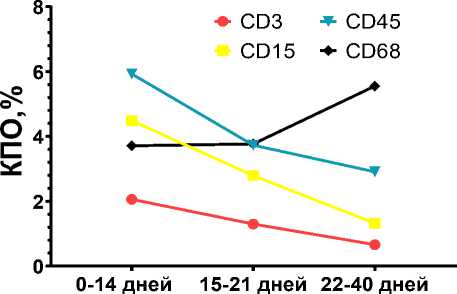
Рис. 4. Соотношения CD3, CD15, CD45, CD68
в разные сроки COVID-19 (КПО – коэффициент площади окрашивания, %)
Нами показано, что в первые две недели заболевания COVID-19 КПО экспрессии белков CD68, CD15 составляла 3,71; 4,49 %, CD3, CD45 2,06; 5,93 % соответственно. Спустя 15–21 дней COVID-19 пневмонии КПО экспрессии белков CD68, CD15 со- ставили 3,77; 2,79 %, CD3, CD45 – 1,3; 3,73 % соответственно.
Через 22–40 суток заболевания КПО экспрессии белков CD68, CD15 составили 5,55; 1,32 %, CD3, CD45 – 0,66; 2,91 % соответственно (табл. 2).
Таблица 2
КПО CD3, CD45, CD15, CD68 в разные сроки COVID-19 пневмонии
|
Срок |
CD3 |
CD15 |
CD45 |
CD68 |
|
КПО, % |
КПО, % |
КПО, % |
КПО, % |
|
|
0–14 |
2,06 |
4,49 |
5,93 |
3,71 |
|
15–21 |
1,3 |
2,79 |
3,73 |
3,77 |
|
22–40 |
0,66 |
1,32 |
2,91 |
5,55 |
Примечание. Нулевую гипотезу отвергали при пороговом значении p < 0,05.
ЗАКЛЮЧЕНИЕ
COVID-19 пневмония представляет собой острое инфекционное заболевание, вызываемое вирусом SARS-CoV-2, имеющее ряд патоморфологических и иммуногистохимических особенностей в динамике развития патологического процесса.
Работ, посвященных изучению данной проблемы в отечественной и зарубежной литературе, нам не встретилось. Отдельные работы отечественных исследователей указывают на важность участия клеток иммунокомпетентной системы в разные сроки заболевания. Однако компьютерная морфометрия с последующим выполнением статистического анализа клеточных коопераций при COVID-19 пневмонии на секционном материале в работах не был представлен.
В своем исследовании мы выделили наиболее значимые временные интервалы развития патологического процесса (до 14 суток, 15–21 суток, 22–40 суток), в течение которых наступал летальный исход пациентов в ковидных госпиталях.
На основании проведенного исследования нами было установлено, что в течение двух недель развития COVID-19 пневмонии в паренхиме легких наблюдались признаки острого дистресс-синдрома.
В клеточном воспалительном инфильтрате преобладало количество CD15 (4,49 %), CD45 (5,93 %) по сравнению с CD3 (2,06 %), CD68 (3,71 %), что вероятно указывало на нарушение клеточной кооперации.
Через 15–21 сутки развития COVID-19 пневмонии в просветах альвеол имелись гиалиновые мембраны, выраженная нейтрофильная инфильтрация с участками деструкции альвеолярных перегородок. В клеточном воспалительном инфильтрате отмечалась тенденция к снижению количества CD45 (3,73 %), CD15 (2,79 %), CD3 (1,3 %) c незначительным повышением CD68 (3,77 %). Данные изменения могут указывать на депрессию клеточного звена иммунитета за счет Т-лимфоцитов, моноцитов.
Через 22–40 суток развития COVID-19 пневмонии возникали пролиферативные и фибротические процессы, которые характеризовались развитием интерстициального фиброза, фиброзно-макрофагальных узелков.
В клеточном воспалительном инфильтрате отмечалось дальнейшее уменьшение количества CD45 (2,91 %), CD15 (1,32 %), CD3 (0,66 %) с одновременным увеличением количества CD68 (5,55 %), что возможно обусловлено незавершенным фагоцитозом вирусных частиц с последующим развитием фиброза. Полученные данные представлены на рис. 4.
Морфоиммуногистохимическое исследование легких при COVID-19 свидетельствует о существенном нарушении клеточной кооперации иммунокомпетентных клеток (CD3, CD45) с преобладанием макрофагов (CD68) в поздние сроки развития заболевания (22–40 суток).
Вероятно, активация макрофагального звена иммунитета может в дальнейшем инициировать развитие пневмофиброза и неоангиогенеза, что отмечается в некоторых исследованиях [11].
Список литературы Клеточные кооперации в разные сроки COVID-19 пневмонии
- Забозлаев Ф. Г., Кравченко Э. В., Галлямова А. Р., Летуновский Н. Н. Патологическая анатомия легких при новой коронавирусной инфекции (COVID-19). Предварительный анализ аутопсийных исследований. Клиническая практика. 2020;11(2):21–37.
- Рыбакова М. Г., Карев В. Е., Кузнецова И. А. Патологическая анатомия новой коронавирусной инфекции COVID-19. Первые впечатления. Архив патологии. 2020;82(5):5–15.
- Самсонова М. В., Михалева Л. М., Зайратьянц О. В. и др. Патология легких при COVID-19 в Москве. Архив патологии. 2020;82(4):32–40.
- Ackermann M., Verleden S. E., Kuehnel M. et al. Pulmonary Vascular Endothelialitis, Thrombosis, and Angiogenesis in Covid-19. N Engl J Med. 2020;383(2):120–128.
- Смирнов А. В., Бисинбекова А. И., Григорьева Н. В. и др. Патологическая анатомия коронавирусной инфекции в современных условиях. Волгоградский научно-медицинский журнал. 2021;4:5–12.
- Libby P., Lüscher T. COVID-19 is, in the end, an endothelial disease. Eur Heart J. 2020;41(32):3038–3044.
- Brasier A. R., Recinos A. 3rd, Eledrisi M. S. Vascular in-flammation and the renin-angiotensin system. Arterioscler Thromb Vasc Biol. 2002; 22(8):1257–1266.
- Gómez-Moreno D., Adrover J. M., Hidalgo A. Neutrophils as effectors of vascular inflammation. Eur J Clin Invest. 2018;48(2):e12940.
- Тодоров С. С., Казьмин А. С., Тодоров, С. С. (мл.) Эндотелиопатия сосудов легких в динамике развития COVID-19. Волгоградский научно-медицинский журнал. 2022;19(2):18–22.
- Ермилов В. В., Смирнов А. В., Дорофеев Н. А. и др. COVID-19 у молодых пациентов с коморбидной патологией на фоне иммуносупрессии (случай из практики). Вестник Волгоградского государственного медицинского университета. 2021;1(77):84–88.
- Mauad T., Duarte-Neto A. N., da Silva L. F. F. [et al.] Tracking the time course of pathological patterns of lung injury in severe COVID-19. Respir Res. 2021;22(1):32.


