Клиническая анатомия целиако-мезентериального бассейна, перспективы эндоваскулярной эмболизации при желудочно-кишечных кровотечениях
Автор: Хитарьян А.Г., Бондаренко И.В., Андреев Е.В., Чепурная И.А., Адизов С.А., Амегнину М.Ж. К., Богомолова К.Р., Ляпина В.А.
Журнал: Московский хирургический журнал @mossj
Рубрика: Сосудистая хирургия
Статья в выпуске: 1 (75), 2021 года.
Бесплатный доступ
Введение. Цель исследования. Представить данные о кровоснабжении желудка и двенадцатиперстной кишки (ДПК), актуальные для использования эндоваскулярного гемостаза.Материал и методы. 117 мультиспиральных компьютерных томограмм с болюсным контрастированием артериальной фазы.Результаты. Обычное строение чревного ствола установлено в 88,89%, печеночно-селезеночный ствол выявлен в 0,85%, печеночно-желудочной ствол - в 0,85%, желудочно-селезеночный ствол - в 1,71%, печеночно-брыжеечный ствол - в 5,13%, чревно-ободочный ствол - в 1,71% случаев. Кровоснабжение желудка в 54,70% осуществлялось преимущественно правой желудочной артерией (ПЖА) и правой желудочно-сальниковой артерией (ПЖСА), в 15,34% - левой желудочной артерией (ЛЖА) и левой желудочно-сальниковой артерией. Анастомоз между ЛЖА и ПЖА, в виде единого сосуда имелся в 55,55%. Общая печеночная артерия явилась источником ПЖА в 67,52%. Обычное строение панкретодуоденальных артерий установлено в 82,2%, в 91,45% бассейны чревного ствола и верхней брыжеечной артерии анастомозировали вдоль ДПК.Заключение. При локализации источника кровотечения в области малой кривизны, либо в антральном отделе желудка целесообразна эмболизация ЛЖА. При локализации источника кровотечения в области большой кривизны желудка целесообразна селективная эмболизация ПЖСА. При локализации источника в пилорическом отделе желудка либо в луковице ДПК необходимо последовательно эмболизировать устья верхней поджелудочно-двенадцатиперстной артерии и желудочно-двенадцатиперстной артерии. При локализации кровотечения в ДПК дистальнее луковицы необходима селективная эмболизация бассейна верхней передней поджелудочно-двенадцатиперстной артерии, при неэффективности гемостаза необходимо эмболизировать устье нижней передней поджелудочно-двенадцатиперстной артерии. Разработаны рекомендации по алгоритму эмболизации сосудов целиако-мезентериального бассейна при различных локализациях источников язвенных желудочно-кишечных кровотечений.
Анатомия, чревный ствол, желудочно-кишечное кровотечение, гемостаз, эндоваскулярная эмболизация
Короткий адрес: https://sciup.org/142230020
IDR: 142230020 | УДК: 616.33-005.1 | DOI: 10.17238/issn2072-3180.2021.1.77-90
Clinical anatomy of the celiac mesenteric trunk, perspectives of endovascular embolization in case of gastrointestinal bleeding
Purpose of study. Provide Systematized data on the blood supply of the stomach and duodenum, relevant for endovascular methods of homeostasis.Material and methods. 117 multispiral computed tomograms with bolus contrast enhancement of the arterial phase.Results. The normal structure of the celiac trunk is established in 88.89% of cases, hepatosplenic trunk identified in 0.85% of cases, hepatogastric trunk - in 0.85% of cases, gastrosplenic trunk - in 1.71% of cases, hepato mesenteric trunk - in 5.13% of cases, celiac colon trunk - in 1.71% of cases. Stomach blood supply in 54.70% of cases was carried out mainly by the right gastric artery and the right gastroepiploic artery, in 15.34% of cases by the left gastric artery and the left gastroepiploic artery. Anastomosis between the right gastric artery and the left gastric artery, as a single vessel had a 55.55% of cases. The common hepatic artery is the source of right gastric artery in 67.52% of cases. Normal structure of hepatoduodenale arteries established in 82.2% of cases. In 91.45% of cases the celiac trunk and superior mesenteric artery combined along the duodenum by anastomosis. Conclusion. When the source of bleeding is localized in the lesser curvature or in the antrum embolisation of the left gastric artery is advisable. When the source of bleeding is localized in the greater curvature, selective embolisation of the right gastroepiploic artery is advisable. When the source is localized in the pylorus of the stomach or in the duodenum bulb it’s necessary to embolize sequentially ostia superior pancreaticoduodenal artery and gastroduodenal artery. When the source of bleeding is localized distal to the duodenum bulb required selective embolisation superior anterior pancreaticoduodenal artery, if hemostasis is ineffective, it is necessary to embolize the ostia of the inferior anterior pancreatic-duodenal artery.
Текст научной статьи Клиническая анатомия целиако-мезентериального бассейна, перспективы эндоваскулярной эмболизации при желудочно-кишечных кровотечениях
В XXI веке язвенная болезнь желудка (ЯБЖ) остается одним из распространенных заболеваний желудочно-кишечного тракта. В последние десятилетия произошли изменения структуры острых хирургических заболеваний, однако желудочно-кишечные кровотечения (ЖКК) по-прежнему остаются на 4-м месте по частоте — 8,8%, и являются частым показанием для экстренной госпитализации [1, 2, 3, 4, 5, 6]. В течение жизни от 11,0% до 14,0% мужчин и от 8,0% до 11,0% женщин могут заболеть ЯБЖ [5, 7, 8], отмечается тенденция роста распространенности язвенных ЖКК [5, 9]. Частота язвенных ЖКК характеризуется географическим разнообразием от 48 до 160 случаев на 100 тыс. населения [6, 11]. По данным отечественных обсервационных исследований, установлено увеличение числа пациентов с язвенными ЖКК с 42,8±2,05 случаев на 100 тыс. населения в 1996–2000 гг. до 49±5,47 случаев на 100 тыс. населения в 2011–2015 гг. [5], в ряде регионов более 50 случаев на 100 тыс. населения [6]. В последние два десятилетия сократилось число плановых операций в связи с ЯБЖ [4, 5, 10, 12], с 2000 г. в РФ общее количество операций при ЖКК, осложнивших ЯБЖ, сократилось на 31,4% [6], при этом увеличилось абсолютное число ежегодно умирающих пациентов с осложнениями ЯБЖ, летальность при язвенных ЖКК варьирует от 3,7% до 9,0% [5, 6]. Широкомасштабным национальным исследованием установлено, что летальность от язвенных ЖКК среди неоперированных пациентов варьирует от 3,9% до 8,2%, у оперированных — от 17,4% до 36,9% [4, 7]. Использование эндоваскулярного гемостаза, а также применение этапного алгоритма оказания помощи являются путями снижения летальности и улучшения результатов лечения больных с язвенными ЖКК и высоким операционным риском [13, 14]. По мере внедрения эндоваскулярных технологий в практическое здравоохранение повышается интерес к хирургической анатомии вариантов строения висцеральных ветвей брюшной аорты (БА) [15]. Представленные данные демонстрируют перспективу использования эндоваскулярных методов гемостаза при язвенных ЖКК. Для практического применения эндоваскулярной эмболизации при язвенных ЖКК необходимы углубленные знания в области клинической анатомии целиако-мезентериального бассейна (ЦМБ).
Цель исследования: представить систематизированные данные о кровоснабжении желудка и двенадцатиперстной кишки (ДПК), актуальные для использования эндоваскулярных методов гемостаза в ЦМБ при лечении пациентов с язвенными ЖКК.
Материал и методы исследования
Изучены данные архивов компьютерной томографии МБУЗ «Городская больница скорой медицинской помощи г. Ростов-на-Дону» и ЧУЗ Клиническая больница «РЖД-Медицина» г. Ростов-на-Дону, всего 117 мультиспиральных компьютерных томограмм с болюсным контрастированием артериальной фазы (МСКТА) органов брюшной полости.
Критерии включения в исследование:
-
— Мужской и женский пол, все возрастные периоды.
Критерии исключения из исследования:
— Опухоль гепатопанкреатодуоденальной зоны.
-
— Операция в гепатопанкреатодуоденальной зоне (кроме холецистэктомии).
-
— Портальная гипертензия, синдром Мэлори-Вейса.
Среди МСКТА пациентов, включённых в исследование, 53,84% (63 из 117) составили мужчины, 46,16% (54 из 117) — женщины. Средний возраст мужчин — 61 (48,5; 68), 57,32±1,60, 54,13–60,0 лет, женщин — 58,5 (48,25; 67), 55,54±1,97, 51,59–59,48 лет. Гендерное и возрастное распределение наблюдений были сопоставимыми (φ от 0,199 до 1,025; p> 0,05) (табл. 1).
Таблица 1
Характеристика лиц, включенных в исследование
|
Возраст ( годы ) |
Женщины (n, %) |
Мужчины (n, %) |
φ |
|
Моложе 30 |
4 (3,42%) |
2 (1,71%) |
0,834 |
|
31–40 |
7 (5,98%) |
6 (5,13%) |
0,298 |
|
41–50 |
7 (5,98%) |
9 (7,69%) |
0,512 |
|
51–60 |
12 (10,26%) |
13 (11,11%) |
0,199 |
|
61–70 |
19 (16,24%) |
25 (21,37%) |
1,025 |
|
Старше 70 |
5 (4,27%) |
8 (6,83%) |
0,841 |
МСКТА выполнены на аппаратах General Electric Optima CT 360 (AOMTL, RUS) и Siemens Somatom Perspective 128 (Siemens AG, GER) с применением программы трек-болюса, а также автоматических двухголовчатых инъек-торов MEDTRONAG (Medtron, GER) и MEDRAD Salient CT (Medrad, Imaxion, USA). МСКТА брюшной полости начинали с нативного исследования при стандартной укладке пациента, толщина среза 0,9 мм, pitch 0,9, 120 кВ,
220 мАс, ширина окна W/С 360–1000/60–120, коллимация 64 × 0,625, область сканирования — от купола диафрагмы до лонных костей. Инъектором в локтевую вену вводили 100 мл неионного низкоосмолярного контрастного вещества с содержанием йода 350 мг/мл со скоростью 4–5 мл/с, сразу после инъекции контрастного препарата вводили 50 мл 0,9% раствора натрия хлорида со скоростью 4 мл/с. Начало сканирования соответствовало триггерному сигналу достижения заданного уровня плотности в нисходящей аорте над диафрагмой. Время задержки сканирования рассчитывалось от времени достижения порога плотности 100 ед. Н. Время начала сканирования ранней артериальной фазы составляло от 8 до 10 с. Постпроцессорная обработка включала мультипланарную и 3D-реконструкцию изображений PACS DICOM программой RadiAnt DICOM Viewer 2020.2 ( Medixant ). Определяли варианты анатомии артерий ЦМБ, скелетотопию устьев, угол отхождения, диаметр, длину и клинически значимые анастомозы. Тип ангиоархитектоники чревного ствола (ЧС) и его ветвей 1-го порядка определяли по схемам Coco D ., Leanza S . 2019 [16], ангиоархитектонику сосудов ЦМБ 2-го порядка, в аспекте кровоснабжения ДПК, классифицировали по схемам Song S.Y., Chung J.W., Yin Y.H., et al. (2010) [17], и Sanampudi S., Raissi D. (2019) [18].
Методы статистической обработки
В формате Microsoft Exel 2017 была сформирована база данных, анализ проведен программами Statistica 10 и Microsoft Exel 2017. Нормальность выборки определяли критериями Колмогорова–Смирнова (n>50) и Шапиро–Уилка (n<50). Для показателей, выраженных абсолютными значениями, вычисляли среднюю величину (М), стандартную ошибку средней арифметической (m), медиану (Ме), нижний (LQ) и верхний (UQ) квартили, а также 95% доверительный интервал (95% ДИ), данные представлены записью: Ме (LQ; UQ), М±m, 95% ДИ. При сравнении показателей, выраженных абсолютными значениями, использовали t-критерий Стьюдента (распределение близкое к нормальному) и U-критерий Манна–Уитни (распределение отличное от нормального). Сравнение показателей, выраженных относительными значениями, проводили по угловому преобразованию Фишера (φ). Уровень значимости 5,0% (p<0,05).
Результаты
Распределение типов ангиоархитектоники ЧС, его ветвей 1-го порядка и их морфологическая характеристика по Coco D ., Leanza S . (2019) [16] представлены в таблице 2.
Тип I деления ЧС и его ветвей 1-го порядка установлен в 88,89% (104 из 117) случаев (рис. 1). Тип II (a), при котором ЧС делился на общую печеночную артерию (ОПА) и селезеночную артерию (СА), левая желудочная артерия (ЛЖА) ответвлялась от БА самостоятельным стволом, встретился в 0,85% (1 из 117) случаев (рис. 2). Тип II (b), при котором СА отходил от БА ветвью 1-го порядка, печеночно-желудочный ствол делился на ОПА и ЛЖА, установлен у 0,85% (1 из 117) (рис. 3). Тип II (c), характеризующийся тем, что общая ОПА отходит от БА ветвью 1-го порядка, желудочно-селезеночный ствол делится на ЛЖА и СА, был установлен в 1,71% (2 из 117) (рис. 4). В 0,85% (1 из 117) случаях ЧС отсутствовал, его ветви 1-го порядка начинались от БА — тип деления III (рис. 5). Тип IV (b) ЧС, отличающийся тем, что ОПА и верхняя брыжеечная артерия (ВБА) отходят от БА общим устьем, также совместным устьем от БА отходят СА и ЛЖА, встретился у 5,13 % (6 из 117) (рис. 6). Тип V, при котором ЧС отдает 3 ветви аналогичные ветвям ЧС 1-го порядка и ВБА, выявлен в 1,71% (2 из 117) случаях (рис. 7). Аберрантная ЛЖА имелась у 4,27% (5 из 117) обследованных, аберрантная артерия к ДПК — у 5,13% (6 из 117) (рис. 8).
Таблица 2
Деление ЧС и его ветвей 1-го порядка по Coco D ., Leanza S . (2019) [16]
|
Тип |
Ангиоархитектоника ветвей ЧС |
n (%) |
|
I |
Обычное анатомическое строение ЧС |
88,89 % (104 из 117) |
|
II (a) |
Печеночно-селезеночный ствол |
0,85% (1 из 117) |
|
II (b) |
Печеночно-желудочной ствол |
0,85 % (1 из 117) |
|
II (c) |
Желудочно-селезеночный ствол |
1,71% (2 из 117) |
|
III |
Отсутствие ЧС |
0,85% (1 из 117) |
|
IV (b) |
Печеночно-брыжеечный ствол |
5,13 % (6 из 117) |
|
V |
Чревно-ободочный ствол |
1,71% (2 из 117) |
Проекция ответвления ЧС от БА варьировала от верхней трети ThXI до верхней трети LII, в 82,91% (97 из 117), соответствовала уровню межпозвоночного диска ThXII–LI (рис. 9), (табл. 3).
Таблица 3
Проекция устья чревного ствола аорты, (n, %)
|
Проекция устья |
Типичное деление |
Атипичное деление |
Все типы |
|
Верхняя треть ThXI– нижняя треть ThXII |
5 (4,80%) |
9 (69,23%) |
14 (11,97%) |
|
Межпозвоночный диск ThXII–LI |
96 (92,31%) |
1 (7,69%) |
97 (82,91)% |
|
Верхняя треть LI |
3 (2,88%) |
3 (23,08%) |
6 (5,13%) |
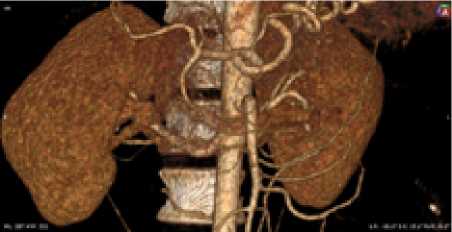
Рис. 1 . Женщина, 36 лет. Тип деления ЧС I, визуализируются ветви ЧС, ВБА 1-го порядка. Равномерный тип кровоснабжения желудка. Проекция устья ЧС – средняя треть Th12 позвонка, проекция устья ВБА – верхняя треть L1 позвонка
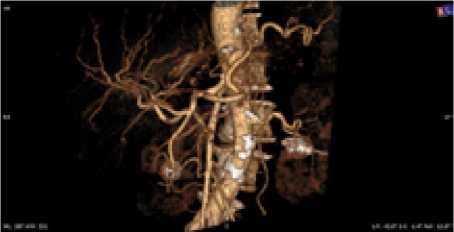
Рис. 2. Женщина, 72 года. Тип деления ЧС II (a), ЛЖА ответвляется от БА над устьем ЧС. Равномерный тип кровоснабжения желудка. Проекция устья ЧС – средняя треть Th12 позвонка, устья ВБА – нижняя треть Th12 позвонка
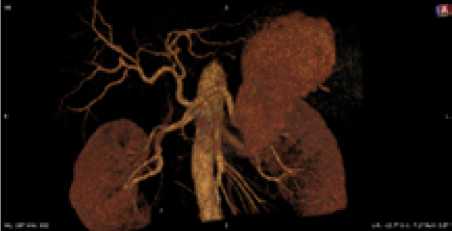
Рис. 3. Мужчина, 63 года. Тип деления ЧС II (b), кровоснабжение желудка преимущественно ветвями ОПА, аналогами ЛЖА и ПЖА, выражены ЛЖСА и ПЖСА. Равномерный тип кровоснабжения желудка
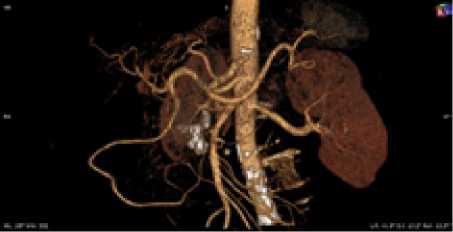
Рис. 4. Женщина, 71 год. Тип деления ЧС II (с), ВППДА выражена, ЧС ответвляется под прямым углом, ЛЖА делится на две ветви, анастомозирует с ПЖА. Равномерный тип кровоснабжения желудка
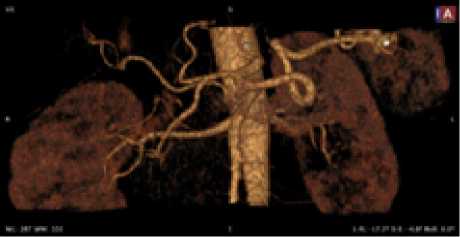
Рис. 5. Мужчина, 58 лет. Тип деления ЧС III, СА, ЛЖА и собственная печеночная артерия ответвляются от БА ветвями 1-го порядка, ПЖА и ВППДА ветви СА. Равномерный тип кровоснабжения желудка
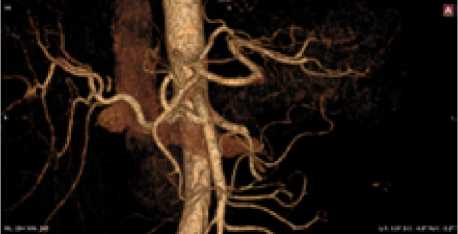
Рис. 6. Женщина, 48 лет. Тип деления ЧС IV (b), собственная печеночная артерия, ветвь ВБА, ВППДА и ПЖА отделяются общей ветвью от ЧС. Кровоснабжение большей части тела и выходного отдела желудка ПЖА и ВППДА
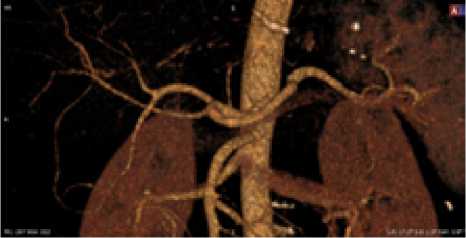
Рис. 7. Мужчина, 41 год. Тип деления ЧС V, общее устье ЧС и ВБА, ВППДА и ЛЖА выражены.
Равномерный тип кровоснабжения желудка
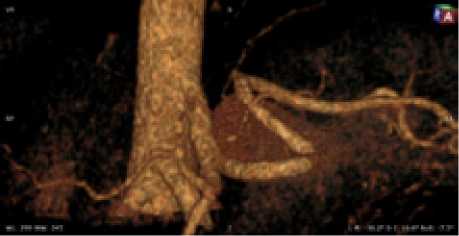
Рис. 8. Мужчина, 51 год. Тип деления ЧС I, ЧС и ВБА ответвляются от БА под углом, близким к прямому, от ЧС ответвляются две артерии, аналогичные ЛЖА. Равномерный тип кровоснабжения желудка
Проекция ответвления ЧС от БА на уровне диска ThXII–LI в 92,31% (96 из 104) отмечена при типичном делении ЧС и в 7,69% (1 из 13) при атипичном. Проекция устья ЧС БА на уровне верхней трети тела ThXI — нижней трети тела ThXII установлена в 11,97% (14 из 117), при типичном делении — 4,80% (5 из 104), при атипичном делении — 69,23% (9 из 13). У 5,13% (6 из 117) пациентов проекцией ответвления ЧС от БА являлась верхняя треть LI позвонка, из них при делении I типа — 2,86% (3 из 104), при атипичном делении — 23,08% (3 из 13).
Средний угол отхождения ЧС от БА составил 58,0° (80,0°; 45,0°), 59,30±2,11°, 55,13–63,47°, при типичном делении — 55,0° (43,5°; 80,0°) 59,32±2,26°, 54,83–63,81°, при атипичном делении — 59,15° (50,0°; 72,0°), 59,15±5,83°, 46,44–71,87° (р=0,978) (рис 10). Наименьший угол ответвления ЧС встретился при атипичном делении — 10,0°, при типичном делении — 15,0°, наибольший угол ответвления ЧС от БА наблюдался при типичном делении — 100,0°, при атипичном делении тупой угол отхождения не встречался, наибольший угол отхождения составил 85,0°.
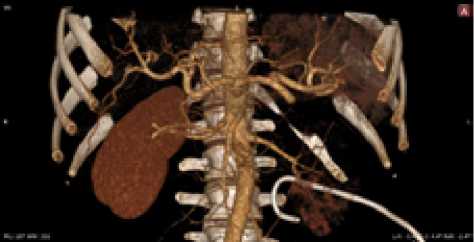
Рис. 9. Женщина, 43 года. Тип деления ЧС I. Равномерный тип кровоснабжения желудка. Проекция устья ЧС – диск ThXII– LI, проекция устья ВБА – верхняя треть LI позвонка
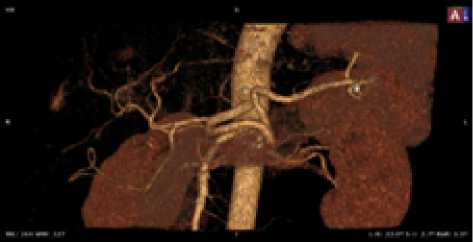
Рис. 10. Мужчина, 41 год. Тип деления ЧС I, ЧС и ВБА ответвляются от аорты под углами, близкими к 60°, ВППДА выражена. Равномерный тип кровоснабжения желудка
Угол ответвления ЧС менее 40°, при проекции устья на верхнюю треть ThXI — нижнюю треть ThXII встречался в 2,56% (3 из 117), при проекции на межпозвоночный диск ThXII–LI — в 14,53% (17 из 117), при проекции на верхнюю треть LI — в 1,71% (2 из 117) случаев. Угол ответвления ЧС от БА 40–79° при проекции устья на верхнюю треть ThXI — нижнюю треть ThXII встречался у 8,55% (10 из 117), при проекции на межпозвоночный диск ThXII–LI — у 41,89% (49 из 117), при проекции на верхнюю треть LI — в 4,27% (5 из 117). Ответвление ЧС от БА под углом 80–94,0° при проекции устья на верхнюю треть ThXI — нижнюю треть ThXII встречалось в 1,71% (2 из 117) случаев, при проекции на межпозвоночный диск ThXII–LI — в 17,95% (21 из 117). Угол ответвления ЧС более 95° установлен при проекции на межпозвоночный диск ThXII–LI в 6,84% (8 из 117) (табл. 4).
Угол ответвления ЧС от БА менее 40,0° при всех типах ангиоархитектоники установлен в 18,80% (22 из 117), с одинаковой частотой при типичном — 19,23% (20 из 104) и атипичном — 15,38% (2 из 13) (ф=0,34; р>0,05) делении. Угол ответвления ЧС от БА 40–79° при всех типах деления встречался в 54,70% (64 из 117), при типичном делении — 52,88% (55 из 104), при атипичном делении ЧС — 69,23% (9 из 13) (φ=1,142; р>0,05). Угол ответвления ЧС от БА 80–94° при всех типах деления встречался в 19,66% (23 из 117) случаев, при типичном делении — 20,19% (21 из 104), при атипичном — 15,3 8% (2 из 13) (ф=0,495; р>0,05). Угол отхождения ЧС от БА более 95° встречался только при типичном делении — 7,69% (8 из 104). Данные об угле (°)
ответвления ЧС от БА, типе деления и скелетотопии устья представлены в таблице 5.
Таблица 4
Проекция устья и угол ответвления чревного ствола от аорты (°), (n, %)
|
Проекция устья |
Менее 40° |
40–79° |
80–94° |
95–115° |
|
Верхняя треть ThXI– нижняя треть ThXII |
3 (2,56%) |
10 (8,55%) |
2 (1,71%) |
- |
|
Межпозвоночный диск ThXII–LI |
17 (14,53%) |
49 (41,89%) |
21 (17,95%) |
8 (6,84%) |
|
Верхняя треть LI |
2 (1,71%) |
5 (4,27%) |
— |
— |
При проекции устья ЧС на верхнюю третьThXI — нижнюю третьThXII при типичном делении угол отхождения ЧС от БА составил 38,2±8,51°, рис. 11, при атипичном делении — 66,4±4,81° (р=0,014). При проекции устья ЧС на межпозвоночный диск ThXII–LI и I типе его деления средний угол ответвления составил 61,55±2,35°, при атипичном делении ЧС на протяжении непосредственно прилежал к БА, угол 10,0±0,0° (р=0,0). При проекции устья ЧС на верхнюю треть LI при его типичном делении угол ответвления от БА составил 38,4±4,19°, при атипичном делении — 47,5±2,5° (p=0,136) (рис. 12).
Таблица 5
Проекция и угол (°) отхождения чревного ствола, Me (UQ; LQ), M ± m
|
Проекция устья |
Типичное деление |
Атипичное деление |
Все типы |
|
Верхняя треть ThXI– нижняя треть ThXII |
50,0 (20,0; 52,0), 38,2±8,51 |
67,5 (62,5; 73,5), 66,4±4,81 |
62,0 (51,0; 71,0), 57±5,43 |
|
Межпозвоночный диск ThXII–LI |
63,5 (45,0; 81,5), 61,55±2,35 |
10,0 (10,0; 10,0), 10±0,0 |
62,0 (44,5; 81,0), 61,01±2,38 |
|
Верхняя треть LI |
45,0 (32,0; 45,0), 38,4±4,19 |
47,5 (46,25; 48,75), 47,5±2,5 |
45,0 (38,5; 45,0), 41,0±3,38 |
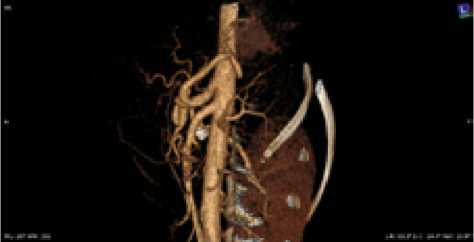
Рис. 11. Мужчина, 35 лет. Тип деления ЧС I, ЧС и ВБА ответвляются от БА под острым углом, визуализируется ВППДА. Направление сосудов ЦМБ вверх под острыми углами. Равномерный тип кровоснабжения желудка
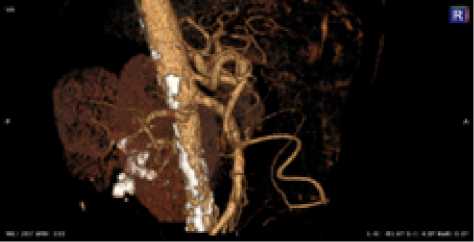
Рис. 12. Женщина, 67 лет. Тип деления ЧС II (c), собственная печеночная артерия отделяется от БА самостоятельно под острым углом, кровоснабжение тела и дна желудка ЛЖА. Равномерный тип кровоснабжения желудка
Установлено, что наименьшая длина ЧС при I типе деления составила 0,6 см, при некоторых типах ангиоархитектоники ЧС отсутствовал — тип деления III. Наибольшая длина ЧС при всех типах деления — 3,2 см, при атипичном делении — 3,0 см. При всех типах ангиоархитектоники ветвей ЦМБ 1-го порядка длина ЧС составила 2,4 (1,4; 2,6), 2,05±0,07 см, при типичном делении — 2,4 (1,4; 2,6), 2,05±0,07 см, при атипичном делении — 2,2 (1,7; 2,8), 2,0±0,26,1,43-2,57 см (p=0,850). Данные о длине ЧС в зависимости от скелетотопии его устья представлены в таблице 6.
Из данных таблицы 6 следует, что средняя длина ЧС при проекции его устья на верхнюю треть ThXI — нижнюю треть ThXII, при I типe деления составляла 2,8±0,0 см, при атипичном делении — 2,14±0,27 см (p=0,016). Длина ЧС при проекции его устья на межпозвоночный диск ThXII–LI при его типичном делении — 1,98±0,07 см, при атипичном делении ЧС мог отсутствовать. Длина ЧС при проекции устья ЧС на верхнюю треть LI при типичном делении составляла 2,93±0,13 см, при атипичном делении — 1,53±0,71 см (p=0,054).
Основной ЧС отсутствовал либо первая ветвь 1-го порядка отходила непосредственно у устья в 5,12% (6 из 117) случаев. Длина ЧС меньше 1 см при всех типах деления установлена в 11,97% (14 из 117), при типичном делении — 12,5% (13 из 104), при атипичном делении — 7,69% (1 из
-
13) (φ=0,547, p> 0,05). Длина ЧС от 1 до 3 см установлена в 81,20% (95 из 117), при типичном делении — 86,54% (90 из 104), при атипичном делении — 38,46% (5 из 13) (φ=3,099, p<0,01). Длина ЧС более 3 см при всех типах деления встречалась у 1,71% (2 из 117), при типичном делении — 0,96% (1 из 104), при атипичном делении — 7,69% (1 из 13) (φ=1,231, p>0,05) (табл. 7).
Таблица 6
Длина (см ) чревного ствола, скелетотопия устья, Me (UQ; LQ), M ± m
|
Проекция устья |
Типичное деление |
Атипичное деление |
Все типы |
|
Верхняя треть ThXI – нижняя треть ThXII |
2,8 (2,8; 2,8), 2,8±0 |
2,3 (1,9; 2,725), 2,14±0,27 |
2,8 (2,2; 2,8), 2,36±0,197 |
|
Межпозвоночный диск ThXII–LI |
2,2 (1,4; 2,6), 1,98±0,07 |
— |
2,2 (1,4; 2,6), 1,98±0,07 |
|
Верхняя треть LI |
2,8 (2,8; 3), 2,93±0,13 |
1,2 (0,85; 2,05), 1,53±0,71 |
2,8 (1,6; 2,875), 2,23±0,45 |
Таблица 7
Длина чревного ствола либо его аналога, тип деления (см ), (n, %)
|
Длина основного ствола |
Типичное деление |
Атипичное деление |
Все типы |
|
Отсутствует |
0 (0,0%) |
6 (46,15%) |
6 (5,12%) |
|
Меньше 1 см |
13 (12,5%) |
1 (7,69%) |
14 (11,97%) |
|
От 1 до 3 см |
90 (86,54%) |
5 (38,46%) |
95 (81,20%) |
|
Более 3 см |
1 (0,96%) |
1 (7,69%) |
2 (1,71%) |
Проекция устья ЧС короче 1 см соответствовала межпозвоночному диску ThXII–LI в 11,11% (13 из 117), верхней трети LI позвонка — 0,86% (1 из 117). ЧС от 1 до 3 см встречался преимущественно при проекции устья на межпозвоночный диск ThXII-LI — 66,67% (78 из 117), реже при проекции устья от верхней трети тела ThXI до нижней трети тела ThXII — 11,11% (13 из 117) и на верхнюю треть тела LI — 3,42% (4 из 117). Длина ЧС более 3 см отмечена при проекции устья от верхней трети тела ThXI до нижней трети тела ThXII, а также на верхнюю треть тела LI — 0,86% (1 из 117) (табл. 8).
Таблица 8
Длина (см ) чревного ствола, скелетотопия устья
|
Проекция устья |
Меньше 1 см |
От 1 до 3 см |
Более 3 см |
|
Верхняя треть ThXI – нижняя треть ThXII |
— |
13 (11,11%) |
1 (0,86%) |
|
Межпозвоночный диск ThXII–LI |
13 (11,11%) |
78 (66,67%) |
— |
|
Верхняя треть LI |
1 (0,86%) |
4 (3,42%) |
1 (0,86%) |
Наименьший диаметр устья ЧС при типичном делении составил 4,5 мм и, соответственно, отсутствовал при III типе. Наибольший диаметр при всех типах деления составил 8,0 мм, при делении I типа — 6,0 мм. При всех типах ангиоархитектоники ветвей ЦМБ 1-го порядка средний диаметр ЧС составил 4,8 (4,6; 5,5), 5,07±0,07, 4,93–5,22 мм, при типичном делении — 4,6 (4,6; 5,5), 5,0±0,05, 4,90-5,10 мм, при атипичном делении — 6,0 (6,0; 6,0), 5,69±5,0, 4,61-6,78 мм (p=0,168). Диаметр устья ЧС при его проекции на уровень верхней трети ThXI — нижней трети ThXII и типичном делении составил 6,0±0,0 мм, при атипичном делении — 5,4±0,6 мм (p=0,319). Средний диаметр устья ЧС при его проекции на межпозвоночный диск ThXII–LI в сочетании с типичной ангиоархитектоникой составил 4,91±0,04 мм, при атипичном делении в крайних случаях ЧС отсутствовал, либо непосредственно у устья отдавал ветвь 1-го порядка, обычно ЛЖА. Диаметр устья ответвления ЧС при проекции устья на верхнюю треть LI при типичном делении составил 6,0±0,0 мм, при атипичном делении — 6,66±0,66 мм (p=0,319) (табл. 9).
Таблица 9
Диаметр (мм) устья чревного ствола от аорты, Me (UQ; LQ), M±m
|
Проекция устья |
Типичное деление |
Атипичное деление |
Все типы |
|
Верхняя треть ThXI – нижняя треть ThXII |
6,0 (6; 6), 6±0 |
6,0 (6,0; 6,0), 5,4±0,6 |
6,0 (6,0; 6,0), 5,6±0,4 |
|
Межпозвоночный диск ThXII–LI |
4,6 (4,6; 5,28), 4,91±0,04 |
— |
4,6 (4,6; 5,28), 4,91±0,04 |
|
Верхняя треть LI |
6,0 (6,0; 6,0), 6,0±0,0 |
6,0 (6,0; 7,0), 6,66±0,66 |
6,0 (6,0; 6,0), 6,33±0,33 |
Наименьший диаметр устьев ЛЖА, правой желудочной артерии (ПЖА) и правой желудочно-сальниковой артерии (ПЖСА) составил 1 мм, устья левой желудочно-сальниковой артерии (ЛЖСА) — 0,5 мм. Наибольший диаметр устья ЛЖА — 2,0 мм, ПЖА и ПЖСА — 3 мм, устья ЛЖСА – 1,5 мм. Средний диаметр устья ЛЖА – 2,0 (2,0; 2,0), 1,85±0,03, 1,78–1,91 мм, ПЖА — 2,0 (2,0; 2,0) 1,97±0,03, 1,92–2,03 мм, ЛЖСА — 1,5 (1,0; 1,5), 1,21±0,03, 1,15–1,28 мм, ПЖСА — 2,0 (2,0; 2,0), 2,0±0,04, 1,92–2,08 мм. Средняя длина артерий, непосредственно кровоснабжающих желудок, до деления на терминальные ветви, либо общая длина соответствующей анастомотической дуги варьировала: ЛЖА от 9,0 до 15,0 см — 12,0 (10,0; 14,0), 12,07±0,19, 11,68–12,45 см, ПЖА от 2,0 до 5,0 см — 4,0 (3,0; 4,0), 3,55±0,09, 3,37–3,73 см, ЛЖСА от 6,0 до 20,0 см — 15,0 (14,0; 16,0), 14,79±0,29, 14,22–15,37 см, ПЖСА от 20,0 до 26,0 см — 24,0 (20,0; 26,0), 23,26±0,23, 22,80–23,63 см.
Учитывая вариабельность ангиоархитектоники артерий ЦМБ, изучена частота ответвления ЛЖА от различных источников (табл. 10).
Установлено, что ЛЖА являлась ветвью ЧС 1-го порядка в 95,73% (112 из 117), БА — в 2,56% (3 из 117) и левого печеночно-желудочного ствола — в 1,71% (2 из 117) случаев. В 4,27% (5 из 117) имелись аберрантные артериальные сосуды, аналогичные ЛЖА (рис. 13). В 29,91% (35 из 112) ЛЖА ответвлялась от ЧС непосредственно у его устья либо в проксимальной трети (рис. 14), в 57,26% (67 из 117) — в средней трети (рис. 15), в 12,82% (15 из 117) — непосредственно перед бифуркацией на ОПА и СА либо их аналоги (рис. 16).
Таблица 10
Источники левой желудочной артерии, (n, %)
|
Источник |
1 ствол |
2 и более |
Всего |
|
Чревный ствол |
106 (90,60%) |
— |
106 (90,60%) |
|
Аорта |
3 (2,56%) |
— |
3 (2,56%) |
|
Левый печеночно-желудочный ствол |
2 (1,71%) |
1 (0,85%) |
3 (2,56%) |
|
Желудочно-селезеночный ствол |
1 (0,85%) |
2 (1,71%) |
3 (2,56%) |
|
Общая печеночная артерия |
0 (0,0%) |
2 (1,71%) |
2 (1,71%) |
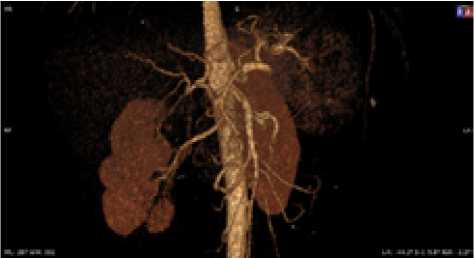
Рис. 13. Женщина, 42 года. Тип деления ЧС IV (b), общий ствол ОПА и ВБА, а также СА ответвляются от БА под тупым углом, ВППДА, ЛЖА и ПЖА выражены. Аберрантная ЛЖА – ветвь ОПА. Кровоснабжение желудка ветвями ОПА и ВППДА – ветви ЧС 1-го порядка
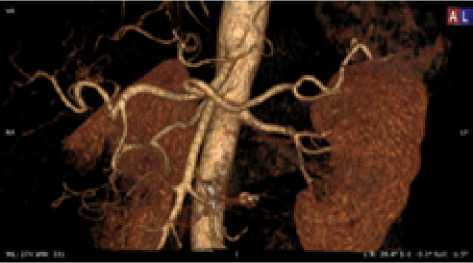
Рис. 14. Мужчина, 48 лет. Тип деления ЧС I, ЧС и ВБА ответвляются от БА под острым углом, ПНДА, ЛНДА, ЛЖА и ПЖА последовательно ответвляются от ЧС в проксимальной трети. Равномерный тип кровоснабжения желудка
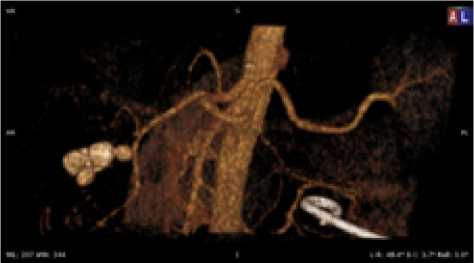
Рис. 15. Женщина, 59 лет. Тип деления ЧС I, ЧС и ВБА ответвляются от БА под острым углом, ЛЖА ответвляется от ЧС в средней трети. Равномерный тип кровоснабжения желудка
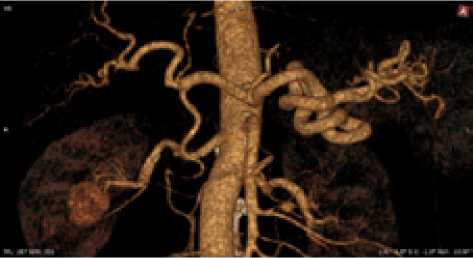
Рис. 16. Женщина, 66 лет. Тип деления ЧС I, ЛЖА ответвляется от ЧС непосредственно перед его бифуркацией на ОПА и СА.
Кровоснабжение желудка преимущественно ЛЖА и ЛЖСА
К стенке желудка ЛЖА подходила одним стволом в 70,1% (82 из 117) (рис. 17). Одним стволом до бифуркации к кардиальному отделу ЛЖА подходила в 74,39% (61 из 82), к малой кривизне в 25,61% (21 из 82) (φ=6,531, p<0,01) (рис. 18). После бифуркации ЛЖА подходила к стенке желудка в 29,9% (35 из 117) (φ=6,325, p<0,01) (рис. 19). К кардиальному отделу желудка, после бифуркации, ЛЖА подходила в 62,86% (22 из 35), к малой кривизне — в 37,14% (13 из 35) (φ=2,184, 0,05>p>0,01) (рис. 20).
Кардиальный отдел являлся проекцией перехода ЛЖА на желудок одним стволом в 74,39% (61 из 82) наблюдений, двумя стволами — в 62,86% (22 из 35). Левая треть малой кри- визны являлась проекцией перехода ЛЖА на желудок одним стволом в 25,61% (21 из 82), двумя стволами — в 37,14% (13 из 35) (φ=1,233, p>0,05). Восходящая ветвь ЛЖА на задней стенке кардиального отдела желудка установлена в 35,04% (41 из 117) наблюдений, при проекции перехода ЛЖА на уровне кардиального отдела желудка — 65,85% (27 из 41), при переходе в левой трети малой кривизны — 41,18% (14 из 41) (φ=2,929, р<0,01). Анастомоз между ЛЖА и ПЖА, в виде единого сосуда с равномерным диаметром, установлен в 55,55% (65 из 117), при переходе в области кардиального отдела — в 47,46% (49 из 65), при переходе на левой тре- ти малой кривизны желудка — 24,61% (16 из 65) (φ=6,077, р<0,01). Сочетание восходящей ветви ЛЖА с анастомозом с ПЖА наблюдалось в 9,40% (11 из 117), при переходе в об- ласти кардиального отдела желудка — 63,64% (7 из 11), при переходе на левую треть малой кривизны желудка — 36,36% (4 из 11) (φ=1,292, р>0,05).
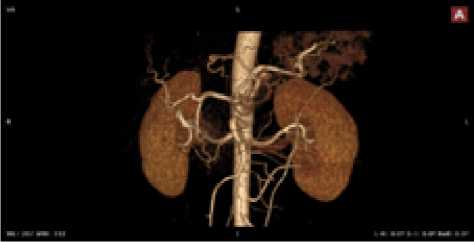
Рис. 17. Женщина, 28 лет. Тип деления ЧС I, ЧС и ВБА ответвляются от БА под прямым углом, ПЖА не выражена, большая часть желудка кровоснабжается ветвями ЛЖА
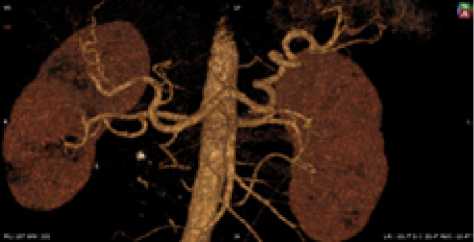
Рис. 18. Женщина, 44 года. Тип деления ЧС I, анастомозы между ветвями ЧС и ВБА 1-го порядка не выражены. Равномерный тип кровоснабжения желудка
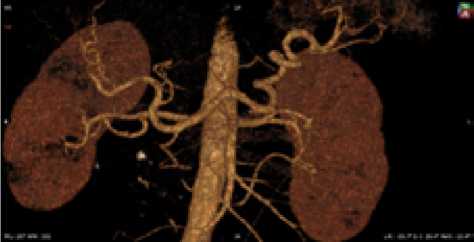
Рис. 19. Женщина, 44 года. Тип деления ЧС I, видны все значимые ветви ЧС и ВБА. Кровоснабжение желудка преимущественно ЛЖА и ЛЖСА
ОПА явилась источником ПЖА в 67,52% (79 из 117), последняя анастомозировала с ЛЖА в 56,96% (45 из 79) посредством 1–4 ветвей, образуя анастомотическую дугу. Собственная печеночная артерия явилась источником ПЖА в 20,51% (24 из 117), анастомозирующей с ЛЖА в 50,0% (12 из 24). Желудочно-двенадцатиперстная артерия (ЖДА) являлась источником ПЖА в 11,11% (13 из 117), анастомозирующей с ЛЖА в 53,85% (7 из 13). Левая печеночная артерия явилась источником ПЖА, анастомозирующей с ЛЖА, в 0,85% (1 из 117). Средняя длина ОПА до устья ПЖА составила 3,68±0,11 см, диаметр устья ПЖА — 2,01±0,03 мм. Собственно печеночная артерия имела длину 3,46±0,2 см, диаметр устья ПЖА — 1,92±0,06 мм. ЖДА как источник ПЖА характеризовалась длиной ствола 2,85±0,15 см, диаметр устья ПЖА — 1,92±0,08 мм. Левая печеночная артерия имела длину 4,0±0 см, диаметр устья ПЖА — 2,0±0 мм.
СА явилась источником ЛЖСА в 76,07% (89 из 117), последняя анастомозировала с ПЖСА в 32,48% (38 из 89). Нижняя ветвь СА явилась источником ЛЖСА в 20,51% (24 из 117), анастомоз с ПЖСА установлен в 45,83% (11 из 24). Ветви СА в воротах явились источником ЛЖСА в 3,42% (4 из 117), в этом случае ЛЖСА и ПЖСА анастомозировали
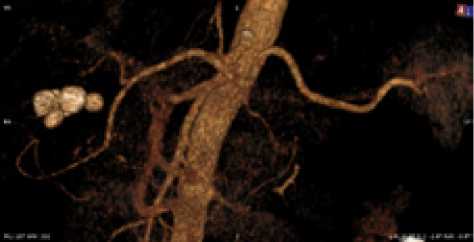
Рис. 20. Мужчина, 47 лет. Тип деления ЧС I, видны значимые ветви ЧС и ВБА, анастомозы не выражены. Равномерный тип кровоснабжения желудка между собой в 25,0% (1 из 4). ЛЖСА ответвлялась от СА в среднем на расстоянии 6,36±0,04 см от ее устья, диаметр устья ЛЖСА составлял 2,61±0,03 мм. ЛЖСА отходила от нижней ветви СА на расстоянии 2,58±0,05 см от ее устья, диаметр — 1,85±0,01 мм. ЛЖСА отходила от терминальных ветвей СА в воротах селезенки на расстоянии 2,8±0,04 см от их устьев, диаметр — 1,75±0,01 мм.
ЖДА явилась источником ПЖСА в 96,58% (113 из 117), анастомозировавшей с ЛЖСА в 44,25% (50 из 113). Селезеночнодвенадцатиперстный ствол был источником ПЖСА в 3,42% (4 из 117), желудочно-сальниковые артерии не анастомозировали между собой (φ=18,356, р>0,01). ЖДА как источник ПЖСА имела длину 5,45±0,04 см, диаметр устья ПЖСА составлял 3,31±0,05 мм. В тех случаях, когда источником ПЖСА являлся селезеночно-двенадцатиперстный ствол, последний имел среднюю длину до отхождения ЖДА 2,9±0,03 см, диаметр устья ЖДА — 3,4±0,04 мм.
Ретропанкреатический отдел СА являлся основным источником коротких артерий желудка в 71,79% (84 из 117) (φ=6,899, р>0,01), анастомозировавших с ЛЖСА в 45,24% (38 из 84). Терминальный отдел СА в воротах являлся источником коротких артерий желудка в 28,21% (33 из 117), анастомозировавших с ЛЖСА в 36,36% (12 из 33).
Ретропанкреатический отдел СА до ответвления коротких артерий желудка имел среднюю длину 4,29±0,06 см, диаметр — 2,53±0,05 мм. СА при ответвлении коротких артерий желудка в воротах имела длину 6,09±0,11 см до их ответвления устьями диаметром 1,97±0,03 мм.
Кровоснабжение желудка в 54,70% (64 из 117) осуществлялось преимущественно ПЖА и ПЖСА. Кровоснабжение желудка преимущественно ЛЖА и ЛЖСА установлено в 15,34% (18 из 117). Равномерный тип кровоснабжения желудка наблюдался на 29,91% (35 из 117) изученных МСКТА. При типичном отхождении ЛЖА от ЧС в 55,36% (62 из 112) желудок кровоснабжался за счет ПЖА и ПЖСА, в 14,28% (16 из 112) — преимущественно за счет ЛЖА и ЛЖСА. В 30,36% (34 из 112) желудок кровоснаб-жался равномерно. При отхождении ЛЖА от БА в 66,67% (2 из 3) кровоснабжение желудка осуществлялось преимущественно ЛЖА и ЛЖСА, в 33,33% (1 из 3), установлен равномерный тип кровоснабжения. При отхождении ЛЖА от левого печеночножелудочного ствола в 100% (2 из 2) желудок кровоснабжался преимущественно ЛЖА и ЛЖСА.
При типичном отхождении ПЖА от ОПА в 50,63% (40 из 79) желудок кровоснабжался преимущественно ПЖА и ПЖСА и в 11,39% (9 из 79) — ЛЖА и ЛЖСА. В 37,98% (30 из 79) желудок кровоснабжался равномерно. При отхождении ПЖА от собственной печеночной артерии в 87,5% (21 из 24) желудок кровоснабжался из бассейнов ПЖА и ПЖСА. В 8,33% (2 из 24) желудок кровоснабжался равномерно. В 4,17% (1 из 24) желудок кровоснабжался преимущественно ветвями ЛЖА и ЛЖСА. При отхождении ПЖА от ЖДА в 53,85% (7 из 13) кровоснабжение желудка осуществлялось преимущественно ЛЖА и ЛЖСА, в 23,08% (3 из 13) кровоснабжение желудка было равномерным, в 23,08% (3 из 13) — ПЖА и ПЖСА.
Вдоль ДПК во всех случаях имелась анастомотическая артериальная дуга. Верхняя поджелудочно-двенадцатиперстная артерия в 87,18% (102 из 117) ответвлялась от ЖДА одним стволом, после бифуркации верхняя передняя поджелудочнодвенадцатиперстная артерия (ВППДА) во всех случаях была более выраженной, в 12,82% (15 из 117) случаев присутствовала только ВППДА. Нижние поджелудочно-двенадцатиперстные артерии ответвлялись от ВБА общим стволом в 35,89% (42 из 117). Нижняя задняя поджелудочно-двенадцатиперстная артерия (НЗПДА) отсутствовала у 4,27% (5 из 117). В 18,80% (22 из 117) нижняя передняя поджелудочно-двенадцатиперстная артерия (НППДА) отходила от ВБА совместно с НЗПДА и тонкокишечной ветвью. Наименьшая длина основного ствола ВППДА составляла 23,0 мм, НППДА — 18,0 мм, ВЗПДА — 22,0 мм и НЗПДА — 32,0 мм. Наибольшая длина ВППДА составляла 27,0 мм, НППДА — 22,0 мм, ВЗПДА — 25,0 мм, НЗПДА — 34,0 мм. Средняя длина ВППДА — 25,0 (24,0; 27,0), 25,27±0,12, 25,03–25,55 мм, НППДА — 20,0 (18,0; 22,0), 20,03±0,15, 19,74–20,33 мм, ВЗПДА — 23,0 (22,0; 24,0), 22,64±0,16,
22,33–22,95 мм, НЗПДА — 32,0 (32,0; 34,0), 32,32±0,13, 32,06– 32,59 мм. Наименьший диаметр устья ВППДА составлял 1,7 мм, НППДА — 1,5 мм, ВЗПДА и НЗПДА имели минимальный диаметр устья 1,4 мм. Наибольший диаметр устья у ВППДА — 2,0 мм, НППДА и ВЗПДА — 1,8 мм, у НЗПДА — 1,6 мм. Средний диаметр ВППДА — 1,8 (1,7; 2,0), 1,85±0,01, 1,82–1,87 мм, НППДА — 1,7 (1,7; 1,8), 1,71±0,01, 1,69–1,73 мм, ВЗПДА — 1,5 (1,5; 1,6), 1,57±0,01, 1,54–1,59 мм, НЗПДА — 1,5 (1,4; 1,6), 1,5±0,01, 1,48–1,51 мм.
Обычное анатомическое строение ветвей ЧС 2-го порядка по Song S.Y., Chung J.W., Yin Y.H., et al. (2010), и Sanampudi S., Raissi D. (2019) [17, 18] установлено в 82,2% (95 из 117). Анастомоз печеночно-мезентериального ствола и желудочно-селезеночного ствола встречался в 10,26% (12 из 117). Анастомоз печеночно-мезентериального ствола, СА, ЛЖА с печеночножелудочно-селезеночным стволом, ВБА отмечен в 3,42% (4 из 117). Анастомоз печеночно-селезеночно-мезентериального ствола, ЛЖА с чревно-мезентериальным стволом установлен у 1,71% (2 из 117). Чревно-мезентериальный ствол при обычном анатомическом строении ЧС наблюдался в 2,56% (3 из 117). Аберрантная панкреатодуоденальная артерия в виде панкреато-дуоденально-печеночного ствола встретилась в 0,85% (1 из 117).
Обычная ангиоархитектоника ветвей ЦМБ 2-го порядка сочеталось с I типом ангиоархитектоники ветвей 1-го порядка в 92,63% (88 из 95), с типом II (b) — 1,05% (1 из 95), с типом II (c) — 1,05% (1 из 95), с типом IV (b) — 3,16 % (3 из 95), с типом V — 2,11 % (2 из 95). Обычное анатомическое строение, анастомоз печеночно-мезентериального ствола и желудочно-селезеночного ствола установлен в 58,33% (7 из 12) при I типе ангиоархитектоники ветвей ЧС 1-го порядка, по 8,33% (1 из 12) при типах II (c) и III, при IV (b) типе — 25,0% (3 из 12). Среди МСКТА, на которых имелся анастомоз печеночномезентериального ствола, СА, ЛЖА с печеночно-желудочноселезеночным стволом, I тип ангиоархитектоники ветвей ЧС 1-го порядка встретился в 75,0% (3 из 4) случаев, тип II (a) — 25,0% (1 из 4). Анастомоз печеночно-селезеночно-мезентериального ствола, ЛЖА с чревно-мезентериальным стволом; обычное анатомическое строение, чревно-мезентериальный ствол, а также аберрантная панкреатодуоденальная артерия, панкреато-дуоденально-печеночный ствол всегда встречались при ангиоархитектонике ветвей 1-го порядка I типа. На 91,45% (107 из 117) МСКТА бассейны ЧС и ВБА объединялись вдоль двенадцатиперстной кишки анастомозом, обычно передней верхней панкреатодуоденальной артерий либо ее аналогом.
Обсуждение
Обычное анатомическое строение ЧС установлено в 88,89% (104 из 117), печеночно-селезеночный ствол выявлен в 0,85% (1 из 117), печеночно-желудочной ствол в 0,85% (1 из 117), желудочно-селезеночный ствол в 1,71% (2 из 117), печеночно- брыжеечный ствол в 5,13 % (6 из 117), чревно-ободочный ствол в 1,71% (2 из 117) случаев, ЛЖА, СА и ОПА являлись ветвями БА в 0,85% (1 из 117). Аберрантная ЛЖА имелась в 4,27% (5 из 117), аберрантная ветвь к ДПК в 5,13% (6 из 117) исследованных случаев. Кровоснабжение желудка в 54,70% (64 из 117) осуществлялось преимущественно ПЖА и ПЖСА, в 15,34% (18 из 117) — ЛЖА и ЛЖСА, равномерный тип кровоснабжения желудка наблюдался на 29,91% (35 из 117) изученных МСКТА. Установлено, что кроме локализации источника ЖКК в бассейне ЛЖСА, в большинстве случаев возможна селективная эмболизация устья, приносящего сосуда. При эмболизации устья ЛЖА необходимо учитывать, что ЛЖА является ветвью ЧС 1-го порядка в 95,73% (112 из 117), в 2,56% (3 из 117) БА и левого печеночно-желудочного ствола в 1,71% (2 из 117) случаев. В 4,27% (5 из 117) имелись аберрантные артериальные сосуды аналогичные ЛЖА. В 29,91% (35 из 112) ЛЖА ответвлялась от ЧС у его устья либо в проксимальной трети, в 57,26% (67 из 117) — в средней трети, в 12,82% (15 из 117) — непосредственно перед бифуркацией. Восходящая ветвь ЛЖА на задней стенке кардиального отдела желудка установлена в 35,04% (41 из 117) наблюдений, в этих случаях эмболизация основного ствола у устья целесообразна после контрастирования СА. Анастомоз между ЛЖА и ПЖА, в виде единого сосуда с равномерным диаметром, установлен в 55,55% (65 из 117), при локализации источника ЖКК в данном сегменте гемостаз может быть достигнут при эмболизации устьев ЛЖА и ПЖА. В 9,40% (11 из 117) при сочетании восходящей ветви ЛЖА с анастомозом с ПЖА для гемостаза в бассейне ветвей ЛЖА может потребоваться эмболизация ПЖА — при переходе ЛЖА на стенку желудка в области кардиального отдела в 63,64% (7 из 11), при переходе в проекции левой трети малой кривизны желудка — в 36,36% (4 из 11). ОПА явилась источником ПЖА в 67,52% (79 из 117), последняя анастомозировала с ЛЖА в 56,96% (45 из 79) посредством 1–4 ветвей, образуя анастомотическую дугу, эмболизация данных сосудов целесообразна на протяжении. Эмболизация устья ЛЖСА потенциально сопряжена с риском ишемии селезенки — СА источник ЛЖСА в 76,07% (89 из 117), однако данная процедура может потребоваться лишь при наличии восходящей ветви ЛЖА на задней стенке кардиального отдела желудка либо при выраженном анастомозе с ПЖСА — 32,48% (38 из 89). При ответвлении ЛЖСА от ствола СА диаметр устья ЛЖСА составляет 2,61±0,03 мм, длина приносящего сосуда — 6,36±0,04 см, таким образом, устье ЛЖСА доступно селективной эмболизации. ПЖСА практически всегда доступна селективной эмболизации устья. ЖДА, как источник ПЖСА, имела длину 5,45±0,04 см, диаметр устья ПЖСА — 3,31±0,05 мм. Если ПЖСА являлась ветвью селезеночно-двенадцатиперстного ствола, последний имел среднюю длину до ответвления ЖДА 2,9±0,03 см, диаметр устья ЖДА — 3,4±0,04 мм. Обычное анатомическое строение в бассейне панкретодуоденальных артерий установлено в 82,2% (95 из 117), на 91,45% (107 из 117) МСКТА бассейны ЧС и ВБА объединялись вдоль ДПК анастомозом, преимущественно за счет ПВПДА. Учитывая выраженность анастомозов и аберрантных панкреатодуоденальных артерий, эмболизация ветвей и устьев панкретодуоденальных артерий не сопряжена с риском ишемии стенки ДПК.
Выводы
При локализации источника язвенного ЖКК в области малой кривизны, либо в антральном отделе желудка целесообразна эмболизация бассейна ЛЖА, при диаметре ЛЖА менее 2 мм возможна эмболизация устья ЛЖА, при неэффективности гемостаза следует эмболизировать бассейн ПЖА. При эмболизации устья ЛЖА следует учитывать, что она является ветвью ЧС 1-го прядка в 95,73%, в 2,56% — ветвью БА, и левого печеночно-желудочного ствола в 1,71% случаев.
При локализации источника ЖКК в области большой кривизны желудка для гемостаза необходимо эмболизиро-вать ПЖСА, целесообразна селективная эмболизация, при неэффективности гемостаза необходимо эмболизировать устье ЛЖСА.
При локализации источника ЖКК в пилорическом отделе желудка либо в луковице ДПК возможен гемостаз последовательной эмболизацией устьев верхней панкреатодуоденальной артерии и ЖДА, учитывая выраженную коллатеральную сеть целесообразна эмболизация в непосредственной близости от бифуркации ЖДА, на расстоянии 0,5–1,0 см от ее ответвления от ОПА.
При локализации источника ЖКК в ДПК дистальнее луковицы для достижения гемостаза необходима селективная эмболизация в бассейне верхней передней поджелудочнодвенадцатиперстной артерии, при неэффективности гемостаза необходимо эмболизировать устье нижней передней поджелудочно-двенадцатиперстной артерии.
Список литературы Клиническая анатомия целиако-мезентериального бассейна, перспективы эндоваскулярной эмболизации при желудочно-кишечных кровотечениях
- Сажин В.П., Кутакова Е.С., Климов Д.Е., Сажин И.В., Савельев В.М., Грыженко С.В. Профилактика и лечение язвенных гастродуоденальных кровотечений. Хирургия. Журнал им. Н.И. Пирогова, 2011. № 11. С. 20–25.
- Тимербулатов В.М., Кунафин М.С., Тимербулатов М.В., Смыр Р.А. Экстренная абдоминальная хирургия в регионе Российской Федерации: анализ за 40 лет. Вестник хирургии им. И.И. Грекова, 2013. № 6. С. 89–92.
- Черноусов А.Ф., Хоробрых Т.В., Богопольский П.М. Хирургия язвенной болезни желудка и двенадцатиперстной кишки. М.: Практическая медицина, 2016. 352 с.
- Кубышкин В.А., Сажин В.П., Федоров А.В., Кривцов Г.А., Сажин И.В. Организация и результаты хирургической помощи при язвенном гастродуоденальном кровотечении в стационарах Центрального федерального округа. Хирургия. Журнал им. Н.И. Пирогова, 2017. № 2. С. 4–9. https://doi.org/10.17116/hirurgia201724-9
- Марийко В.А., Романова Н.Н., Кремянский М.А., Третьяков В.О., Марийко А.В. Анализ современного состояния плановой хирургии язвенной болезни. Хирургия. Журнал им. Н.И. Пирогова, 2019. № 4. С. 24–29. https://doi.org/1017116/hirurgia201904124
- Ревишвили А.Ш., Федоров А.В., Сажин В.П., Оловянный В.Е. Состояние экстренной хирургической помощи в Российской Федерации. Хирургия. Журнал им. Н.И. Пирогова, 2019. № 3(1). С. 88–97. https://doi.org/10.17116/hirurgia201903188
- Тарасов Е.Е., Багин В.А., Нишневич Е.В., Астафьева М.Н., Руднов В.А., Прудков М.И. Эпидемиология и факторы риска неблагоприятного исхода при неварикозных кровотечениях из верхних отделов желудочно-кишечного тракта. Хирургия. Журнал им. Н.И. Пирогова, 2019. № 5. С. 31–37. https://doi.org/10.17116/ hirurgia201905131
- Gastroenterologie systematisch (Hrsg. B. Göke, Ch. Beglinger). Bremen – London – Boston, 2 Auflage, 2007, рр. 150–170. (In German).
- Кульчиев А.А., Морозов А.А., Тeдеев С.У., Галачиев С.М., Дзбоев Д.М. Хирургическое лечение рубцово-язвенного стеноза пилородуоденального канала. Вестник хирургической гастроэнтерологии, 2015. № 3–4. С. 62–70.
- Лобанков В.М. Хирургия язвенной болезни на рубеже XXI века. Хирургия. Журнал им. Н.И. Пирогова, 2005. № 1. С. 58–64.
- Di Saverio S., Bassi M., Smerieri N., Masetti M., Ferrara F., Fabbri C., Ansaloni L., Ghersi S., Serenari M., Coccolini F., Naidoo N., Sartelli M., Tugnoli G., Catena F., Cennamo V., Jovine E. Diagnosis and treatment of perforated or bleeding peptic ulcers: 2013 WSES position paper. World J. Emerg. Surg., 2014, No. 45 (9), рр. 2–15. https://doi.org/10.1186/1749-7922-9-45
- Крылов Н.Н. Helicobacter pylori — причина язвенной болезни? Вестник хирургической гастроэнтерологии, 2014. № 1–2. С. 75–86.
- Цуркан В.А., Араблинский А.В., Шиков Д.В. Рентгенэндоваскулярные технологии в лечении пациентов с желудочно-кишечными кровотечениями. Альманах Института хирургии им. А.В. Вишневского, 2020. № 1. С. 114–115.
- Щеголев А.А., Аль-Сабунчи О.А., Павлычев А.В., Вакурова Е.С. Стандарты и рекомендации в лечении больных с язвенными гастродуоденальными кровотечениями. Альманах Института хирургии им. А.В. Вишневского, 2020. № 1. С. 384.
- Хитарьян А.Г., Мизиев И.А., Глумов Е.Э., Мурлычёв А.С., Провоторов М.Е., Ковалев C.A. Особенности эндоваскулярной ангиоархитектоники ветвей нижней брыжеечной артерии и их значимость для хирургической колопроктологии. Анналы хирургии, 2013. № 6. С. 38–42.
- Coco D., Leanza S. Celiac Trunk and Hepatic Artery Variants in Pancreatic and Liver Resection Anatomy and Implications in Surgical Practice. Open Access Maced J. Med. Sci., 2019, No. 7(15), pp. 2563–2568. https://doi.org/10.3889/oamjms.2019.328
- Song S.Y., Chung J.W., Yin Y.H., Jae H.J., Kim H.C., Jeon U.B., Cho B.H., So Y.H., Park J.H. Celiac axis and common hepatic artery variations in 5002 patients: systemetic analisis with spiral CT and DSA, Radiology, 2010, No. 255 (1), pp. 278–288. https://doi.org/radiology.rsna.org/lookup /suppl/ doi:10.1148/radiol.09090389/-/DC1
- Sanampudi S., Raissi D. Aberrant Inferior Pancreaticoduodenal Artery During Upper Gastrointestinal Bleed Embolization, Cureus, 2019, No. 11 (1). https://doi.org/10.7759/cureus.3945


