Клинические и морфологические особенности панникулита и узловатой эритемы
Автор: Усачева М.Н., Черкасова Е.Г., Бабаева А.Р.
Журнал: Волгоградский научно-медицинский журнал @bulletin-volgmed
Рубрика: Случай из практики
Статья в выпуске: 1 (53), 2017 года.
Бесплатный доступ
В статье приведено клиническое наблюдение, наглядно иллюстрирующее возникающие в реальной терапевтической практике трудности дифференциальной диагностики воспалительных поражений подкожно-жировой клетчатки и кожи, которые могут иметь системный характер с тяжелым, фульминантным течением и развитием септических осложнений, полиорганной недостаточности.
Панникулит, условатая эритема, клинический случай
Короткий адрес: https://sciup.org/142149215
IDR: 142149215 | УДК: 616-003.826:616.511
Clinical and morphological features of erythema nodosum and panniculitis
The article presents a clinical case that illustrated the difficulties faced in the course of differential diagnosis of inflammatory lesions of subcutaneous fat and skin which can be systemic with a severe and fulminant course and involve the development of septic complications and multiple organ failure in real therapeutic practice.
Текст научной статьи Клинические и морфологические особенности панникулита и узловатой эритемы
Панникулит (П) и узловатая эритема (УЭ) относятся к воспалительным поражениям подкожно-жировой клетчатки и включены в класс ХIII МКБ10 – «Болезни костно-мышечной системы и соединительной ткани», при этом несмотря на наличие соответствующего раздела «Болезни мягких тканей» (М60-М79), такая форма как спонтанный панникулит (СП) включена в раздел «Системные поражения соединительной ткани» (М 35.6).
Под панникулитами понимают группу разнородных по этиологии и клиникоморфологической картине заболеваний, основным проявлением которых является воспаление подкожно-жировой клетчатки (ПЖК) с образованием подкожных узлов. В редких случаях в воспалительный процесс вовлекается висцеральная жировая ткань, что приводит к более тяжелому течению заболевания с развитием фатальных осложнений. Впервые «синдром очаговой дистрофии ПЖК» был описан еще в 1892 году Пфейфером (V. Pfeifer), термин «панникулит» был предложен J. Salin в 1911 году. Однако единого представления об этиологии и патогенезе заболевания до настоящего времени нет. Определенную роль отводят инфекционным агентам (вирусам, бактериям), а также травмам, гормональным и иммунным нарушениям, злокачественным новообразованиям и др. [1, 4]. Основным механизмом разви- тия неспецифического воспаления является нарушение процессов перекисного окисления липидов с накоплением высокоактивных промежуточных продуктов окисления, которые приводят к дегенерации клеточных структур и цитолизу.
УЭ является наиболее частой формой поражения ПЖК и кожи и также характеризуется появлением болезненных узлов в коже и ПЖК. Заболеваемость УЭ по усредненным данным составляет 1–5 случаев на 100 тыс. населения. Встречается чаще у женщин фертильного возраста, пик заболеваемости приходится на возраст 20–30 лет. Это заболевание характеризуется симметричностью поражения, преимущественной локализацией узлов на передней поверхности голеней, реже бедер, благоприятным течением, хотя возможно образование новых узлов в течение 2–6 недель. Однако процесс разрешается самостоятельно в течение 2 месяцев, не оставляя атрофии ПЖК и рубцов на коже. Иногда на месте узла остается гипрепигмен-тация, которая с течением времени полностью проходит. Особенностью УЭ является отсутствие изъязвлений и вскрытия узлов, что может иметь место при панникулитах. В настоящее время зарубежные специалисты рассматривают УЭ как одну из форм П, характеризующуюся морфологически поражением междольковых перегородок (септальный П). В противоположность этой кон- цепции отечественные ревматологи рассматривают УЭ как форму глубокого кожного ангиита нижних слоев дермы и ПЖК [2, 6].
Согласно современной морфологической классификации П подразделяют на септальные (преимущественная локализация воспалительного процесса в соединительно-тканных перегородках между жировыми дольками) и лобулярные (с поражением преимущественно самих жировых долек). Оба варианта заболевания могут также протекать с развитием клиникоморфологической картины васкулита или без него. Наряду с этим существуют различия и по характеру воспалительной клеточной инфильтрации при различных вариантах П, в том числе при УЭ. Так, для УЭ помимо инфильтративного васкулита характерна лимфоцитарно-плазмоцитарная и гистиоцитарная инфильтрация тканей без развития некрозов и формирования абсцессов [3, 6].
Что касается П, то гистологическая картина может быть разной: как отмечалось выше, возможно развитие септального П, лобулярного П либо сочетанной формы П. Для лобулярного П характерно развитие некрозов жировой ткани, тогда как септальный П протекает более благоприятно, без морфологических признаков некроза. По характеру воспалительной клеточной инфильтрации выделяют преимущественно лимфоцитарный, гистиоцитарный (гранулематозный), нейтрофильный и эозинофильный варианты П. Такое разделение имеет важное клиническое значение, т. к. определенные клинические формы П ассоциированы с тем или иным гистологическим вариантом поражения. Так, в частности, базофильный некроз с образованием массивного базофильного детрита характерен для инфекционного П. Особый интерес представляет и морфологическая оценка поражения сосудистой стенки при П, которое может быть представлено лейкоцитокластическим либо некротизирующим васкулитом, а также тромбангиитом. Как правило, тяжелые формы сосудистых поражений (некротизирующий васкулит, тромботическая васкулопатия) чаще наблюдаются при нейтрофильных П, ассоциированных с инфекцией [5].
Основными клиническими признаками П является образование в ПЖК верхних и нижних конечностей, реже в области груди и живота множественных узлов различной окраски (от телесной до синюшно-розовой) и размеров (от 0,5–1,0 см до 5–7 см в диаметре). Нередко происходит сливание узлов с образованием обширных конгломератов и бляшек с неровными контурами и бугристой поверхностью. Постепенно узлы претерпевают развитие и рассасываются с образованием очагов атрофии и запа- дения кожи, но могут иногда подвергаться вскрытию с выделением маслянисто-пенистой массы и формированием плохо заживающих язв с последующим рубцеванием тканей. Развитие сливного инфильтративного поражения ПЖК с некрозом узлов характерно для лобулярного варианта заболевания, при септальном варианте воспалительный процесс носит, как правило, ограниченный характер с образованием нескольких узлов без изъязвления.
Одной из клинически значимых форм панникулитов является спонтанный панникулит (СП), или идиопатический лобулярный П (панникулит Вебера-Крисчена). При этом варианте заболевания образуются мягкие, умеренно болезненные узлы диаметром более 2,0 см, расположенные в ПЖК нижних и верхних конечностей, реже в области ягодиц, живота и груди. По форме узлов СП подразделяется на узловой, бляшечный, инфильтративный и смешанный варианты. В зависимости от глубины залегания узлов и конгломератов окраска кожи варьирует от нормальной до ярко-красной. Иногда конгломераты узлов распространяются на всю поверхность голени, бедер и плеч, что приводит к выраженному отеку и болезненности в данной области. При инфильтративном варианте в месте поражения зачастую определяется флюктуация, что напоминает флегмону или даже абсцесс, но при вскрытии очага выделяется желтая маслянистая масса без признаков нагноения, после вскрытия вышеуказанных конгломератов и инфильтратов образуются плохо заживающие изъязвления. Чаще в клинике встречается вариант с поэтапным образованием узлов, инфильтратов и конгломератов – так называемая смешанная форма [3].
Как показывает анализ литературы, преобладают кожные формы П, однако имеются клинические наблюдения, описывающие изменения висцеральной жировой ткани, морфологически сходные с таковыми в ПЖК [3, 5]. Системные варианты П встречаются в клинической практике гораздо реже, при этом в патологический процесс вовлекается жировая клетчатка забрюшинного пространства, сальника, паранефрия и др. органов, характерно развитие гепатоспленомегалии, признаков панкреатита, нефропатии. В этом случае заболевание протекает с ярко выраженной системной воспалительной реакцией в виде лихорадки, полиартралгий, миалгий, острофазовых лабораторных показателей. По степени клинико-лабораторной выраженности воспалительного процесса можно косвенно судить об активности системного П. Важно подчеркнуть, что системный П представляет собой жизнеугрожающее заболевание состояние с высокой летальностью [1, 4]. Прижиз- ненная диагностика поражения висцеральной жировой ткани затруднена в связи с отсутствием простых и доступных методов визуализации этой патологии, а также недостаточной информированностью врачей о такой форме некротизирующего П. Иногда поражение внутренних органов может протекать при отсутствии кожной симптоматики или со скудными ее проявлениями.
Чрезвычайно важным представляется установление возможной причины П и УЭ, т. к. воспалительные поражения мягких тканей часто являются вторичными как следствие инфекционных, онкологических, аутоиммунных процессов. В реальной клинической практике самыми частыми пусковыми факторами УЭ являются стрептококковая инфекция (стрептококковый фарингит, тонзиллит – 28–48 %), туберкулезная инфекция, саркоидоз, хроническая вирусная инфекция, лимфопролиферативные заболевания (Т-клеточная лимфома), лекарственная болезнь, системные заболевания соединительной ткани. Однако примерно в половине случаев УЭ рассматривается как идиопатический процесс [2, 6].
Что касается П, то в случае нейтрофильного лобулярного П чаще имеет место бактериальная природа заболевания. Реже встречаются П ассоциированные с поражением поджелудочной железы, дефицитом альфа-трипсина, введением химических агентов в кожу и подкожную клетчатку (facticial panniculitis), а также особая подкожная форма синдрома Свита (subcutaneous Sweet syndrome), которая характеризуется вовлечением в процесс наряду с ПЖК фасций и мышц [7]. СП Вебера-Крисчена характеризуется лифоцитарной, лимфоплазмоцитарной либо гистиоцитарной инфильтрацией тканей в очагах поражения, что типично для системных ревматологических процессов аутоиммунной природы. В связи с этим гистологическое исследование вносит важный вклад в трактовку механизма развития П, его возможной причины. Так, преимущественно лифоци-тарная воспалительная реакция свидетельствует об аутоиммунном механизме воспаления, тогда как резко выраженная лейкоцитарная инфильтрация более характерна для инфекционной этиологии поражения ПЖК [5].
Успех в клинической диагностике и дифференциальной диагностике П зависит в первую очередь от тщательного сбора анамнеза с анализом перенесенных инфекционных заболеваний, принимаемых лекарственных препаратов, оценки фоновой патологии, а также от адекватной оценки клинической симптоматики и выявления типичных морфологических изменений в тканях при гистологическом исследовании.
Многообразие форм и вариантов течения заболевания требует своевременного клинико-лабораторного и инструментального обследования пациента с целью более ранней верификации диагноза и проведения адекватной терапии.
Приводим наблюдение из практики. Представленный клинический случай отражает всю сложность диагностики системного панникулита.
Пациентка М., 1939 г. р., пенсионерка, инвалид II группы, поступала в терапевтическое отделение ГУЗ «Клиническая больница № 12» Волгограда 7 сентября 2016 г. с направительным диагнозом: Узловатая эритема. Жалобы при поступлении: на боли в верхних и нижних конечностях, скованность в суставах, резко болезненные узловые образования в области голеней, стоп, бедер, плеч, общую слабость, сухость во рту. Заболела за 3 недели до госпитализации, когда после возвращения из другой области, где находилась в течение 2 месяцев, появилась резкая слабость, болезненность и скованность в суставах, отмечались уплотнения в подкожной клетчатке нижних конечностей, а затем узлы: сначала – на стопах и голенях, затем, через 2 недели, – на бедрах, плечах, животе. Кожа над узлами сначала была красного цвета, затем темнела до синюшно-буроватого, отмечалось вскрытие узлов на стопах и в области голеностопных суставов с выделением желтоватой жидкости без запаха.
Обратились в поликлинику по месту жительства, выполнено исследование: ОАК, биохимический анализ крови, консультирована ревматологом 01.09.2016 г., выставлен диагноз: Узловатая эритема с суставным синдромом. Были даны рекомендации проводить лечение: ГКС парентерально, трентал, НПВС, направлена на госпитализацию, однако в экстренной госпитализации в профильное отделение было отказано, в связи с чем пациентку госпитализировали в общетерапевтическое отделение по месту жительства.
Из анамнеза жизни: перенесла ОНМК в 1998 г., имеются последствия в виде левостороннего гемипареза. Страдает СД 2-го типа более 10 лет, принимала глидиаб МВ 30 мг 1 таблетку утром, глюкофаж 1 000 мг /сут., у эндокринолога регулярно не наблюдалась, контроль гликемии не осуществляла, дома глюкометр отсутствует. Примерно с этого же времени диагностирована ИБС. Стенокардия напряжения. ФК II. ГБ 3-й стадии, риск 4. Проводилась терапия: кардиомагнил – 75 мг, бисопролол – 5 мг, периндоприл – 5 мг, амлодипин – 5–10 мг по уровню АД, индапамид – 2,5 мг. Перенесенные операции: холецистэктомия более 15 лет назад, экстирпация матки с придатками по поводу миомы более 10 лет назад.
Объективно при поступлении: состояние средней тяжести, температура тела 36,6°. Дома не лихорадило. Сознание ясное, положение лежа на каталке (перестала самостоятельно ходить, присаживалась в постели только с посторонней помощью в течение последних 3 недель). Эритематозные пятна и узлы – диаметром около 2,0– 2,5 см на стопах и голенях, плотные, спаянные с ПЖК, резко болезненные при пальпации в области бедер и плеч, в области голеней и стоп буроватого цвета, в области плеч и живота – ярко красные, местами сливные, кожа над сливными конгломератами в области плеч бугристая, ярко-красного цвета (рис. 1).
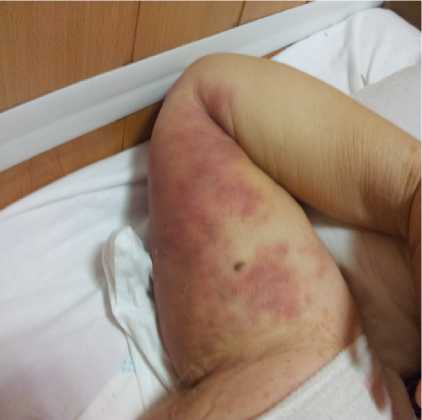
Рис. 1. Участок кожи на плече с конгломератом узлов в ПЖК
В области стоп узлы вскрылись самостоятельно с серозным мутноватым отделяемым. Подмышечные лимфоузлы с обеих сторон увеличены до 1,0–1,5 см, безболезненны, подчелюстные л/у увеличены до 1,0 см, плотные, безболезненные. Щитовидная железа не увеличена, пальпация шеи в данной области безболезненна. Коленные суставы деформированы за счет пролиферативных изменений (остеоартроз). Снижение силы в левой руке и ноге (гемипарез). Дыхание в легких везикулярное, ослаблено в нижних отделах, хрипов нет, ЧД – 18 в мин. Сердечные тоны ритмичные, приглушены, систолический шум на верхушке, ЧСС 80 в мин, АД 140/80 мм рт. ст. Язык сухой, покрыт беловато-желтым налетом. Живот мягкий, не вздут, безболезненный. Печень не увеличена, безболезненна. Селезенка не пальпируется. Мочеиспускание свободное, безболезненное, учащенное. Стул нерегулярен (хронические запоры), обычный, без патологических примесей. Периферических отеков нет.
ЭКГ – синусовый ритм, ЭОС влево, ГЛЖ, ГЛП, диффузные изменения в миокарде.
ОАК – лейкоцитоз 17,5, Нв – 108 г/л, эрит-роц – 3,8, нормохромия эритроцитов, п/я – 25, сегм – 60, моноц – 3, лимф – 10, эоз – 2, тромбоциты 403 тыс.
Глюкоза плазмы (суточная гликемия): 26,3–26,0–25,0–14,5 мм/л.
СРБ – отрицат. Сывороточное железо – 31,3 мкм/л.
На основании имеющихся клинических данных, несмотря на наличие деструктивных изменений в узлах с отделением мутной жидкости, был поставлен предварительный диагноз: Узловатая эритема с суставным синдромом. СД 2-го типа, декомпенсация углеводного обмена, диабетическая нефропатия, ХБП 3а, макроангиопатия (ИБС, ЦВБ), дистальная полинейропатия, целевой HbA1c < 7,5 %. ДЭ 2 ст. последствия ОНМК (1998 г). ИБС. Стенокардия напряжения. ФК II (клин). ХСН IIа. ФК II. Гипертоническая болезнь III стадии, степень 1, риск 4.
Назначено обследование: общепринятое лабораторное обследование, ЭКГ в динамике, УЗИ ОБП и почек, ЭГДС (онкопоиск), (ректороманоскопию временно было выполнить невозможно, ввиду неспособности пациентки принять вынужденное положение во время исследования), в проведении ирригографии без предшествующей ректороманоскопии отказано. Назначена консультация ревматолога в динамике.
Проводили терапию ИКД перед приемами пищи и по уровню гликемии, инфузионная терапия, ГКС 60 мг/сут. с последующим уменьшением дозы до 30 мг /сут., антибиотики (цефотаксим 2,0 г в/в), пентоксифиллин в/в кап., НПВП, омепразол, антиангинальная, гипотензивная, антиагрегантная терапия.
На фоне проводимого лечения в течение первых двух недель отмечалось уменьшение болевого синдрома в области узловатых образований, уменьшилась скованность в суставах нижних конечностей, температура тела не повышалась. С 20.09 ухудшение состояния в виде нарастания болевых ощущений в области плеч, сливание узлов в болезненный конгломерат, горячие на ощупь, стали нарастать явления системной воспалительной реакции с прогрессированием поли-органных нарушений, электролитными расстройствами, присоединением вторичной пневмонии. Проводилась пункция узлового образования дважды – 15.09 в области стопы – получено мутносерозное содержимое, микроскопия по Граму единичные гр + кокки, посев роста не дал. 21.09 – пункция в области левого плеча, микроскопия – флоры не обнаружено, посев роста не дал. Отправлен участок ткани на гистологическое исследование: бесструктурный детрит, материал не информативен.
Повторно осмотрена ревматологом 20.09.16 г.: несмотря на прогрессирование деструктивного поражения ПЖК и кожи, диагноз УЭ не был пересмотрен, было рекомендовано продолжить лечение с усилением антибактериальной терапии, провести дообследование с целью онкопоиска, рентгенографию стоп, посев из узла и кровь на стерильность. Кровь на стерильность и гемокультуру – роста нет. В ОАК – на фоне нормального уровня лейкоцитов нарастал сдвиг лейкоформулы влево: палочкоядерный сдвиг вплоть до миелоцитов. ЭГДС – смешанный гастрит. УЗДГ вен н/к – без патологии. УЗИ ОБП и почек: дилатация холедоха компенсаторная ПХЭС, диффузные изменения поджелудочной железы, печень и селезенка б/о. Кальцинаты почек. Рентгенография стоп – остеоартроз 1 ПФС обеих стоп.
Несмотря на усиление противовоспалительной и антибактериальной терапии у пациентки продолжали нарастать явления полиор-ганной недостаточности, электролитные расстройства, угнетение сознания. Пациентка по тяжести состояния была переведена в ПИТ АРО, получала меропенем – 3 г/сут. ванкомицин – 2 г/сут., затем линезолид – 1,2 г/сут. Несмотря на проводимое лечение, нарастала тяжесть состояния, и, вследствие прогрессирующей полиорганной недостаточности, 02.10.2016 г. наступил летальный исход.
Заключительный диагноз
Основной: Острый бактериальный панникулит узловато-инфильтративная форма.
Конкурирующий: Возможный инфекционный эндокардит аортального клапана. Септико-пиемические очаги ПЖК.
Фон: СД 2-го типа, диабетическая нефропатия, ХБП 3а, макроангиопатия (ИБС, ЦВБ), дистальная полинейропатия, целевой HbA1c < 7,5 %.
Осложнения: Сепсис, полиорганная недостаточность, респираторный дистресс-синдром, отек легких, отек головного мозга.
Сопутствующий: ИБС. Стенокардия напряжения. ФК II (клин). ХСН IIа. ФК II. Гипертоническая болезнь III стадии, степень 1, риск 4. Дисциркуляторная энцефалопатия 2 ст. смешанного генеза. Последствия ОНМК.
Патолого-анатомический диагноз
Основное заболевание: Спонтанный панникулит с поражением подкожной жировой клетчатки (правой и левой нижних конечностей, левой верхней конечности), висцеральный панникулит (брыжейки тонкой и толстой кишок, сальниковой сумки, переднего средостения, забрюшинного пространства).
Фоновое заболевание: СД 2-го типа (глюкоза до 29,9 ммоль/л, склероз, липоматоз, атрофия поджелудочной железы).
Осложнения основного заболевания: Сеп- сис: миелоидная метаплазия селезенки, гиперплазия костного мозга, интерстициальный гепатит, некронефроз, эрозивный эзофагогастроэн-терит. Отек легких. Отек головного мозга.
Сопутствующие заболевания: ИБС, диффузный мелкоочаговый кардиосклероз, атеросклероз коронарных артерий (стадия IV, степень 2, стеноз 35 %). Последствия инфаркта в правом полушарии головного мозга в области базальных ядер (множественные мелкие кисты).
При патологоанатомическом исследовании были обнаружены следующие типичные для системного П изменения:
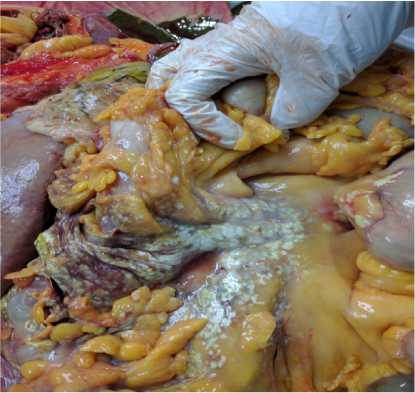
Брыжейка тонкой и толстой кишки с обилием бляшек светло-желтого цвета диаметром до 2,5 см; брыжейка – в жировой ткани обширные очаги стеатонекрозов с перифокальной лейкоцитарной инфильтрацией, очаговой лимфоидной инфильтрацией (рис. 2).
А
Б
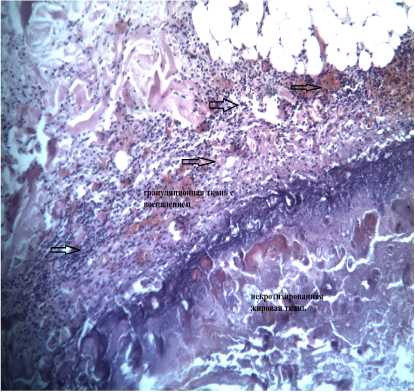
Рис. 2. А – брыжейка тонкой кишки с обилием бляшек светло-желтого цвета, Б – лимфоцитарная инфильтрация с некрозом адипоцитов
В паранефральной клетчатке справа поля стеатонекрозов с кровоизлияниями, занимающими 8х6х4 см; под капсулой почки поля стеато-некрозов с кровоизлияниями, представленными гемолизированными эритроцитами, со слабой перифокальной лейкоцитарной инфильтрацией с наличием обломков лейкоцитов (рис. 3).
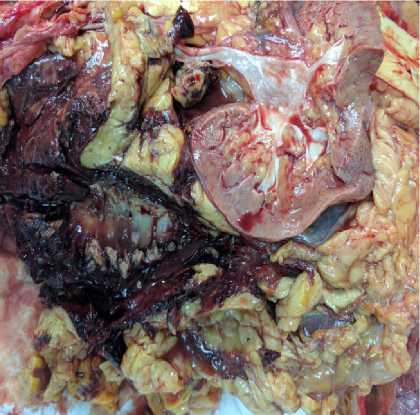
Рис. 3. Стеатонекрозы с кровоизлияниями в паранефральной клетчатке
Селезенка: 10х6х2,5 см, масса 170 г, консистенция дряблая. Печень – очаговая жировая и зернистая дистрофия гепатоцитов, полнокровие центральных вен с кровоизлиянием в центры долек, рассеянная лейкоцитарная инфильтрация интерстиция, отложение бурого пигмента пери-нуклеарно, умеренный перипортальный фиброз со слабой лимфоцитарной инфильтрацией.
Поджелудочная железа: стеатонекрозы, липоматоз стромы, перидуктальный склероз, лимфоидная инфильтрация, атрофия островков Лангерганса, кальцинаты.
Миокард: полнокровие сосудов микроцир-куляторного русла, зернистая дистрофия кардиомиоцитов, гипертрофия кардиомиоцитов, периваскулярный, мелкоочаговый кардиосклероз, фрагментация мышечных волокон, отложение липофусцина перинуклеарно.
Кожа: в подкожной жировой клетчатке сте-атонекрозы с лейкоцитарной инфильтрацией.
Следует подчеркнуть, что у пациентки имела место морфологическая картина преимущественно нейтрофильного лобулярного системного П с массивным некротическим поражением ПЖК и висцеральной жировой ткани, что, с учетом обнаружения кокковой флоры в прижизненном пунктате п/к узла, резким палочкоядерным сдвигом, отрицательным СРП, не дает возможности полностью исключить первичную бактериальную природу П. Вместе с тем представленные морфологические дока- зательства послужили основанием для заключения о том, что у больной имел место спонтанный панникулит с поражением подкожной жировой клетчатки и висцеральной жировой ткани, осложнившийся развитием сепсиса, который и явился непосредственной причиной смерти. Предрасполагающими факторами развития фатальных осложнений следует считать пожилой возраст, неконтролируемый СД 2-го типа, ХБП, предшествующую сердечнососудистую патологию. Проводимое лечение с включение высоких доз ГКС, комбинированной антибактериальной терапии оказалось неэффективным. Тем не менее имела место недостаточно полная оценка клинической картины заболевания и тяжести состояния больной в дебюте заболевания, что отразилось в первичном диагнозе «узловатая эритема», которая, как известно, имеет благоприятный прогноз, не дает некротических поражений и лимитирована исключительно поражением кожи и ПЖК.
Тогда как некротизирующий панникулит, в том числе спонтанный, представляет собой тяжелое системное заболевание с высокой частотой неблагоприятных исходов.
В заключение следует отметить, что приведенное клиническое наблюдение наглядно иллюстрирует возникающие в реальной терапевтической практике трудности при проведении дифференциальной диагностики воспалительных поражений ПЖК и кожи, которые могут иметь тяжелое, фульминантное течение с развитием септических осложнений, полиорганной недостаточности и фатальным исходом.
Список литературы Клинические и морфологические особенности панникулита и узловатой эритемы
- Белов Б. С., Егорова О. Н., Савушкина Н. М., Раденска-Лоповок С. Г. Панникулиты в практике интерниста//Т ер. Архив. -2014. -№ 5. -С. 88-93.
- Белов Б. С/, Егорова О. Н., Раденска-Лоповок С. Г. и др. Узловатая эритема: васкулит или панникулит?//Современная ревматология. -2009. -№ 3. -С. 45-49.
- Егорова О. Н., Белов Б. С., Гпухова С. И., Раденска-Лоповок С. Г., Карпова Ю. Л. Идиопатический панникулит Вебера-Крисчена: клинические аспекты//Современная ревматология. -2016. -№ 1. -С. 15-20.
- Егорова О. Н., Белов Б. С., Карпова Ю. А. Спонтанный панникулит: современные подходы к лечению//Научно-практическая ревматология. -2012. -№ 5. -С. 110-114.
- Chan M. P. Neutrophilic panniculitis//Arch Pathol Lab Med. -2014. -Vol. 138. -P. 1337-1343.
- Schwartz R. A., Nervi S. J. Erythema nodosum: a sign of systemic disease//Am. Fam. Fhysician. -2007. -Vol. 75 (5). -P. 695-700.
- Roshet N. M., Chavan R. N., et al. Sweet syndrome//J Am Acad Dermatol. -2013. -Vol. 69 (4). -P. 557-564.


