Клинические особенности BRCA-позитивного рака яичников
Автор: Максимов С.Я., Имянитов Е.Н., Гусейнов К.Д., Городнова Т.В.
Журнал: Сибирский онкологический журнал @siboncoj
Рубрика: Клинические исследования
Статья в выпуске: 6 (60), 2013 года.
Бесплатный доступ
Роведена оценка клинической значимости носительства мутаций в геле BRCA1 в формировании ответа на химиотерапию, а также на продолжительность жизни у больных распространенным РЯ. Из архива института (с января 2000 г. по январь 2008 г.) была отобрана 21 больная распространенным РЯ с наследственной мутацией в гене BRCA1. Контрольную группу составили 42 (1:2) случая распространенного ненаследственного РЯ, сопоставимые по стадиям, гистологическому типу, возрасту и объему первичной циторедукции — известные прогностические факторы. Все BRCA-позитивные пациентки ответили на неоадъювантную платиносодержащую химиотерапию, в то время как в группе ненаследственного РЯ общий ответ был зафиксирован у 36 % (8/8 (100 %) vs 9/25 (36 %); OR 14,8; 95 % CI 1,78-100; р=0,002). По сравнению с больными контрольной группы BRCA-позитивные больные характеризовались более высокой частотой общего ответа (81 % vs 33,4 %; OR 8,50; 95 % CI 2,52- 34,89; р=0,001) на первую линию платиносодержащей химиотерапии и на вторую (62 % vs 21,4 % OR 5,96; 95 % CI 1,76-22,50; р=0,004). После третьей линии химиотерапии у BRCA-позитивных больных отмечалась выраженная тенденция к лучшим результатам (18,8 % vs 5,6 %; р=0,233). У больных с BRCA1 мутациями, по сравнению с контрольной группой, наблюдалось статистически значимое улучшение среднего значения безрецидивного периода после первой линии химиотерапии (20,05 vs 7,21 мес; р=0,005). Продолжительность жизни у BRCA-позитивных больных была значимо больше по сравнению с больными с ненаследственным РЯ (медиана 9,3 vs 3,4 года; р=0,001).
Brca-позитивные больные, платиночувствительный рак яичников, наследственные мутации в гене brca1, длительность безрецидивного периода, общая выживаемость
Короткий адрес: https://sciup.org/14056374
IDR: 14056374 | УДК: 618.11-006.6-056.7:575.113
Clinical features of BRCA-positive ovarian cancer
It has been recently proved that cells with impaired BRCA1function demonstrate high sensitivity to platinum-containing derivatives because they are not able to eliminate DNA disorders caused by these agents. Early studies showed that BRCA carriers had better odds of surviving ovarian cancer than do women without these mutations. The purpose of the study was to evaluate clinical significance of BRCA1 mutation carriage in response to chemotherapy as well as to life span in patients with advanced ovarian cancer. Treatment outcomes of 21 patients with advanced ovarian cancer with inherited BRCA1gene mutation, who were treated from January 2000 to January 2008, were analyzed. The control group consisted of 42 (1:2) cases with advanced non-inherited ovarian cancer matched by stage, histological type, age and the extent of primary cytoreductive surgery. All BRCA-positive patients responded to neoadjuvant platinum-containing chemotherapy. In non-inherited ovarian cancer patients, complete response was observed in 36 % (8/8 (100 %) vs 9/25 (36 %); OR 14,8; 95 % CI 1,78–100; p=0,002). In comparison with the control group patients, BRCA-positive patients had higher rates of complete response to the first-line platinum-containing chemotherapy (81 % vs 33,4 %; OR 8,50; 95 % СI 2,52–34,89; p=0,001) and to the second-line chemotherapy (62 % vs 21,4 %; OR 5,96; 95 % СI 1,76–22,50; p=0,004). After the third line chemotherapy, BRCA-positive patients had a tendency to better results (18,8 % vs 5,6 %; p=0,233). A statistically significant improvement in the median relapse-free survival time was observed in patients with BRCA1mutations after the first-line chemotherapy as compared to that observed in the control group patients (20,05 vs 7,21 months; p=0,005). Life span in BRCA-positive patients was significantly longer than in patients with non-inherited ovarian cancer (medium 9,3 years vs 3,4 years; p=0,001).
Текст научной статьи Клинические особенности BRCA-позитивного рака яичников
СИБИРСКИЙ ОНКОЛОГИЧЕСКИЙ ЖУРНАЛ. 2013. № 6 (60)
Семейный наследственный рак яичников (РЯ) – результат мутаций генов BRCA1 и BRCA2. Каждая седьмая больная РЯ в России – это пациентка с наследственной мутацией в гене BRCA1 [1, 2, 7]. Гены-супрессоры опухолевого роста BRCA1 и BRCA2 участвуют в регуляции пролиферации клеток и репарации молекулы ДНК посредством механизмов гомологичной рекомбинации [9, 10]. Клетки с нарушенной функцией генов BRCA1/2 не способны восстанавливать разрывы двойной цепи ДНК и демонстрируют высокую чувствительность к препаратам платины, точкой приложения которых и является молекула ДНК опухолевых клеток. Таким образом, «недостаточные» функциональные возможности систем репарации в клетке опухоли могут служить поводом для выделения группы пациентов с повышенной чувствительностью к определенной цитостатической терапии. Многочисленные работы убедительно демонстрируют, что у BRCA-позитивных больных РЯ протекал более благоприятно, это, вероятно, связано с сохраняющейся чувствительностью к препаратам платины на протяжении нескольких рецидивов заболевания [3, 4, 8].
Цель исследования – оценить клиническую значимость носительства мутаций в гене BRCA1 в формировании ответа на химиотерапию (ХТ), а также их влияние на продолжительность жизни у больных распространенным РЯ.
Материал и методы
Все больные с распространенным РЯ, наблюдавшиеся в НИИ онкологии им. Н.Н. Петрова (г. Санкт-Петербург) с января 2000 г. по январь 2008 г., были протестированы на носительство 3 мутаций в гене BRCA1. В группу BRCA-позитивного РЯ вошла 21 пациентка с распространенным РЯ, в том числе 17 (81 %) женщин с мутацией BRCA1 5382insC и 4 (19 %) – с мутациями BRCA1 4153delA. Из них 9 (43 %) пациенток имели клинические признаки наследственного рака: 5 (24 %) – отягощенный семейный онкологический анамнез, 4 (19 %) – случаи метахронного первично-множественного рака.
В контрольную группу были включены 42 (1:2) пациентки с ненаследственным распространенным РЯ, сначала по точному совпадению стадии и гистологического типа, затем по соответствию возраста на момент постановки диагноза, объему произведенной первичной циторедукции – известные прогностические факторы для РЯ. Случаи ненаследственного РЯ определяли по следующим критериям: отсут- ствие мутаций в гене BRCA1; отсутствие у больной рака молочной железы (РМЖ) и/или РМЖ и РЯ в семейном анамнезе. Преобладающим гистотипом опухоли у пациенток в обеих группах был серозный рак. Важно отметить, что в настоящее исследование включены 3 (14 %) BRCA-позитивных больных с низкодифференцированной эндометриоидной аденокарциномой; им соответствовали 3 (7 %) случая ненаследственного РЯ с аналогичным гистотипом, 2 (5 %) случая с умеренно дифференцированной и 1 (2 %) случай с высокодифференцированной эндометриоидной аденокарциномой. У 10 больных в контрольной группе был серозно-папиллярный, светлоклеточный рак, а также смешанные формы опухоли. Одной BRCA-позитивной больной с низкодифференцированным РЯ соответствовало 2 случая ненаследственного РЯ с тем же морфологическим описанием (табл. 1).
Медиана возраста на момент постановки диагноза для BRCA-позитивных больных РЯ составила 51 год (диапазон от 39 до 74 лет) и была близкой к медиане возраста в контрольной группе больных ненаследственным РЯ (медиана – 50 лет, диапазон – от 35 до 72 лет).
Все больные в составе ХТ первой линии как неоадъювантной, так и адъювантной получали препараты платины. Хирургическую стадию определяли по FIGO (International Federation of Gynecology and Obstetrics) после анализа анамнеза и данных, полученных в ходе операции и патоморфологического исследования. При оценке объема первичной циторедукции за оптимальную операцию принимали ту, при которой максимальные размеры оставшихся опухолевых образований не превышают 1 см; субоптимальной циторедукции соответствовал размер оставшейся опухоли 1–2 см. При размерах оставшихся опухолевых масс более 2 см объем операции считался неоптимальным.
Показатели эффективности лечения устанавливали по Response Evaluation Criteria In Solid Tumors (RECIST). За полный ответ принимали исчезновение всех измеряемых очагов; за неполный ответ – уменьшение на 30 % суммы наибольших диаметров измеряемых очагов; за прогрессирование заболевания – увеличение на 20 % суммы наибольших диаметров измеряемых очагов; стабилизация заболевания определялась как изменения, не соответствующие ни одному из перечисленных выше критериев. Дату рецидива заболевания определяли по первому при- знаку прогрессирования заболевания на основании данных КТ, либо МРТ, либо УЗИ, оцениваемых по шкале RECIST, а также по повышению уровня маркера СА-125.
Статистической обработке подвергались показатели ответа после предоперационной, 1, 2, 3-й линий ХТ ( χ 2), а также безрецидивный период и интервал без лечения после первой, второй, третьей линий
Таблица 1
|
Показатель |
BRCA-позитивный РЯ (n=21) |
Ненаследственный РЯ (n=42) |
|
Возраст на момент постановки диагноза, годы |
||
|
Медиана |
51 |
50 |
|
Диапазон |
39–74 |
35–72 |
|
Год постановки диагноза |
||
|
Диапазон |
2000–2008 |
2001–2008 |
|
Стадия |
||
|
IIC |
3 (14 %) |
6 (14 %) |
|
III |
10 (48 %) |
21 (50 %) |
|
IV |
8 (38 %) |
15 (36 %) |
|
Гистологический тип |
||
|
G3 серозная аденокарцинома |
9 (43 %) |
18 (43 %) |
|
G2 серозная аденокарцинома |
2 (10 %) |
4 (9,5 %) |
|
Эндометриоидная аденокарцинома |
3 (14 %) |
6 (14 %) |
|
Светлоклеточная карцинома |
1 (5 %) |
2 (5 %) |
|
Серозно-папиллярная аденокарцинома |
3 (14 %) |
6 (14 %) |
|
Смешанная, преимущественно серозная аденокарцинома |
2 (9 %) |
4 (9,5 %) |
|
Низкодифференцированная карцинома |
1 (5 %) |
2 (5 %) |
|
Объем циторедукции |
||
|
Оптимальныая циторедукция |
11 (52 %) |
20 (48 %) |
|
Субоптимальная циторедукция |
8 (38 %) |
17 (40 %) |
|
Неоптимальная циторедукция |
2 (10 %) |
4 (10 %) |
|
Без операции |
– |
1 (2 %) |
|
Мутация BRCA1 |
||
|
BRCA1 5382insC |
17 (81 %) |
– |
|
BRCA1 4153delA |
4 (19 %) |
– |
|
BRCA1 185delAG |
– |
– |
Таблица 2
общий ответ (полный ответ + частичный ответ) у больных с brCa-позитивным и ненаследственным раком яичников в зависимости от срока рецидива
ХТ (t-критерий, U-критерий), общая выживаемость (метод Каплана–Мейера). Для всех статистических анализов использовался пакет SPSS (версия 13).
Анализ мутаций в гене BRCA1 проводился методом аллель-специфической полимеразной цепной реакции в режиме реального времени (iCycler iQ5 Real Time Detection System (Bio-Rad)). Учет результатов производился при оценке графиков амплификации и кривых плавления. В качестве источника ДНК использовалась ткань из парафиновых блоков.
Результаты и обсуждение
Предоперационную платиносодержащую ХТ получали 37 % пациенток с BRCA-позитивным РЯ и 63 % – с ненаследственным РЯ. Все BRCA-позитивные пациентки ответили на неоадъювантную ХТ, тогда как в группе ненаследственного РЯ общий ответ был зафиксирован у 36 %, отличия статистически значимы (8/8 (100 %) vs 9/25 (36 %); OR 14,8; 95 % CI 1,78–100; p=0,002). В 12 % случаев ненаследственного РЯ при предоперационной платиносодержащей ХТ наблюдалось увеличение размера опухоли.
В клинической практике выбор терапии рецидивов РЯ основан на том, что общий ответ на повторное применение платиносодержащих программ четко пропорционален длительности без-рецидивного периода: при сроках <6 мес частота объективного ответа составляет около 5 %, при 6–12 мес – 26–30 %, при 12–24 мес – 30–60 %, более 24 мес – 77–80 % [5, 6]. Мы проанализировали частоту ответа на платиносодержащую ХТ при первом рецидиве заболевания в зависимости от срока возникновения рецидива. BRCA-позитивные больные характеризовались более высокой частотой общего ответа даже при сроке <6 мес: у 4 из 21 (19 %) BRCA-позитивные пациенток возникли рецидивы в этом интервале, при этом у двух из них наблюдался полный ответ на ХТ по схеме цисплатин + циклофосфан, а две другие не ответили на монохимиотерапию таксанами. В группе ненаследственного
Таблица 3
|
Химиотерапия |
Ответ на химиотерапию (ПР + ЧР) |
р |
Отношение шансов для ответа |
95 % допустимый интервал |
|
Вторая линия |
||||
|
Любая химиотерапия |
||||
|
BRCA-позитивный РЯ (n=21) |
13 (62 %) |
0,0041 |
5,96 |
1,76–22,50 |
|
Ненаследственный РЯ (n=28) |
6 (21 %) |
|||
|
Платиносодержащая химиотерапия |
||||
|
BRCA-позитивный РЯ (n=17) |
13 (76 %) |
>0,0011 |
12,35 |
3,02–62,26 |
|
Ненаследственный РЯ (n=24) |
5 (21 %) |
|||
|
Неплатиновая химиотерапия |
||||
|
BRCA-позитивный РЯ (n=4) |
– |
– |
– |
– |
|
Ненаследственный РЯ (n=4) |
1 (25 %) |
|||
|
Третья линия |
||||
|
Любая химиотерапия |
||||
|
BRCA-позитивный РЯ (n=16) |
3 (19 %) |
0,2852 |
3,46 |
0,39–74,81 |
|
Ненаследственный РЯ (n=16) |
1 (6 %) |
|||
|
Платиносодержащая химиотерапия |
||||
|
BRCA-позитивный РЯ (n=8) |
1 (12 %) |
0,7162 |
1,71 |
0,06–8,16 |
|
Ненаследственный РЯ (n=13) |
1 (8 %) |
|||
|
Неплатиновая химиотерапия |
||||
|
BRCA-позитивный РЯ (n=8) |
2 (25 %) |
– |
– |
– |
|
Ненаследственный РЯ (n=3) |
– |
|||
Примечание: 1 –критерий ( χ 2), 2 – критерий Фишера.
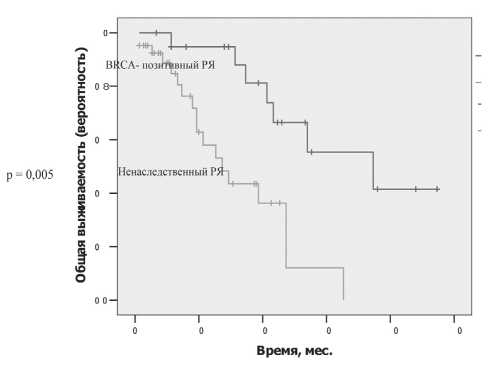
Рис. 1. Общая продолжительность жизни для BRCA-позитивных больных по сравнению с больными ненаследственным РЯ
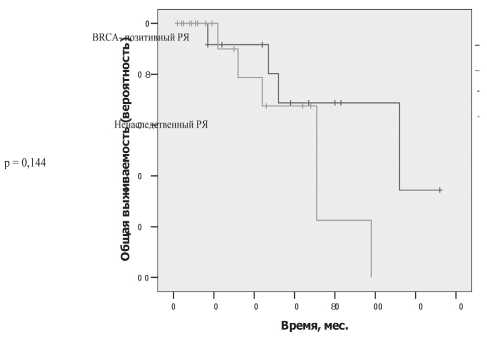
Рис. 2. Общая продолжительность жизни для BRCA-позитивных больных по сравнению с больными ненаследственным РЯ в группах только с оптимальной циторедукцией
Таблица 4
Интервал без лечения при brCa-позитивном и ненаследственном раке яичников
РЯ болезнь рецидивировала у 30 из 40 (72 %) больных при сроке <6 мес, при этом общего ответа на платиновую терапию не наблюдалось (табл. 2).
По сравнению с больными контрольной группы BRCA-позитивные больные характеризовались более высокой частотой общего ответа на первую линию платиносодержащей ХТ (81 % vs 33,4 %; OR 8,50; 95 % СI 2,52–34,89; p=0,001), а также на вторую (62 % vs 21.4 %; OR 5,96; 95 % СI 1,76–22,50; p=0,004). После третьей линии ХТ у BRCA-позитивных больных отмечалась выраженная тенденция к улучшению результатов (18,8 % vs 6,2 %; p=0,285) (табл. 3).
Сопоставление эффективности цитостатической терапии только по показателю общего ответа не вполне оправдано. При несомненном выигрыше в частоте общего ответа его продолжительность при последующих рецидивах не отличается от таковой у больных с ненаследственным РЯ. В нашем исследовании уже после второго рецидива заболевания статистически значимой разницы между группами не наблюдается – медиана интервала без лечения после завершения 3-й линии ХТ в группе BRCA-позитивных больных составила 2,5 мес против 1,1 мес (р=0,085) в группе ненаследственного РЯ (табл. 4).
У больных с BRCA1 мутациями, по сравнению с пациентками контрольной группы, наблюдалось статистически значимое улучшение среднего значения безрецидивного периода после ХТ первой линии (20,05 vs 7,21 мес; p=0,005). При анализе в группах сравнения только с оптимальной первичной циторедукцией безрецидивный период достигал больших значений у носительниц мутаций (21,5 vs 9,5 мес; p=0,083), однако значимых различий не было. Оценка выживаемости по методу Каплана–Мейера с момента постановки диагноза выявила статистически значимое улучшение показателей общей продолжительности жизни для больных с BRCA-позитивным РЯ (медиана продолжительности жизни – 9,3 года) по сравнению с больными ненаследственным РЯ (медиана продолжительности жизни – 3,4 года; p=0,001) (рис. 1). Общая продолжительность жизни в группе ненаследственного РЯ с оптимальной первичной циторедукцией была лучше, чем в общей, но в сравнении с BRCA-позитивными пациентками значимых различий не получено (медиана 9,3 vs 5,9 мес; p=0,144) (рис. 2).
Выводы
Все BRCA-позитивные пациентки ответили на неоадъювантную платиносодержащую
ХТ, в то время как в группе ненаследственного РЯ общий ответ был зафиксирован у 36 % (8/8 (100 %) vs 9/25 (36 %); OR 14,8; 95 % CI 1,78–100; p=0,002). В результате анализа групп сравнений, подобранных по гистологическому типу, стадии, возрасту, объему первичной циторедукции, было выявлено, что BRCA-позитивные больные характеризуются более высокой частотой общего ответа (81 % vs 33,4 %; OR 8,50; 95 % СI 2,52–34,89; p=0,001) на первую линию платиносодержащей ХТ и на вторую (62 % vs 21,4 %; OR 5,96; 95 % СI 1,76–22,50; p=0,004). После третьей линии ХТ у BRCA-позитивных больных отмечалась выраженная тенденция к лучшим результатам (18,8 % vs 5,6 %; p=0,233). У больных с BRCA1 мутациями, по сравнению с пациентками контрольной группы, наблюдалось статистически значимое улучшение среднего значения безрецидивного периода после первой линии ХТ (20,05 vs 7,21 мес; p=0,005). Продолжительность жизни у BRCA-позитивных больных составила 9,3 года и была достоверно больше по сравнению с больными с ненаследственным РЯ (медиана 9,3 vs 3,4 года; p=0,001).


