Клинический случай инфекционного перитонита кошек
Автор: Масалов В.Н., Малахова Н.А., Клеймнова Н.В., Пискунова О.Г., Лищук А.П., Агеева А.В., Деркач А.А.
Журнал: Вестник аграрной науки @vestnikogau
Рубрика: Сельскохозяйственные науки
Статья в выпуске: 1 (106), 2024 года.
Бесплатный доступ
В настоящей статье рассмотрено тяжелое системное инфекционное заболевание кошачьих - инфекционный перитонит, которое является одной из наиболее часто регистрируемых причин смерти от инфекционных болезней кошек. Приведены статистические данные по частоте встречаемости данной патологии. Указаны основные клинические проявления и симптомы, выявленные при данном заболевании: вялое, угнетенное состояние, снижение температуры тела, диспноэ, тусклость шерсти, желтушность кожных покровов и видимых слизистых. Описаны результаты проведения ультразвуковой диагностики, биохимического исследования крови и ПЦР-исследования. Акцентируется внимание на наличии гепатомегалии, диффузного снижения эхогенности печени с усилением визуализации гиперэхогенной ткани перипортальной области, хронического диффузного повреждения печени, свободной жидкость в брюшной полости, изменениях паренхимы почек и увеличении почек в объеме. Приведено обоснование поставленного диагноза на основании комплекса исследований: анамнеза, жалоб и данных проведенных исследований. Отмечена важность ранней и своевременной диагностики заболевания с целью предупреждения развития возможных осложнений. Особое внимание уделено методам лечения данной патологии: препаратом выбора стал Коронакэт в комбинации с патогенетической и поддерживающей терапией. Сделан акцент на то, что Коронакэт - первый препарат, содержащий GS-441524, с сертификатом GMP в Европе, применяемый для лечения вирусного перитонита кошек FIP. Описаны результаты проводимой терапии в динамике с приведением результатов осмотра, ультразвукового исследования и биохимического исследования крови. Сделан вывод о высокой эффективности выбранного препарата на основании положительной морфологической динамики выздоровления пациента и возможности рекомендации данного препарата в качестве специфического средства лечения при выпотной форме вирусного перитонита кошек.
Инфекционный перитонит, энтеральный коронавирус кошек, ультразвуковое исследование, гепатомегалия, коронакэт
Короткий адрес: https://sciup.org/147244313
IDR: 147244313 | УДК: 636.8.045: | DOI: 10.17238/issn2587-666X.2024.1.21
A clinical case of feline infectious peritonitis
This article considers serious systemic feline infectious disease - infectious peritonitis which is one of the most frequently reported reasons of death from infectious feline disease. There is statistical data presented on the incidence of pathology. The main clinical implications and symptoms that have been identified with this disease are: sluggish condition and depressed state, a decrease in body temperature, dyspnea, dull coat, yellowness of the skin and of the visible mucous membranes. The results of the ultrasound diagnosis, of the biochemical blood test and of the PCR diagnistics are given in the article. It focuses on the presence of hepatomegaly, a chronic diffusive liver hypoechogenity with more visible hyperechogenic tissue of periportal area, chronic diffuse liver damage, free fluid in the abdominal cavity, changes in kidney parenchyma and enlarged kidneys. The arguments are presented related to the diagnosis: anamnesis, complaints and research data. The importance of early and timely diagnostics for preventing the occurrence of possible complications is described. Special attention is paid to the methods of treatment of this pathology: Coronacat is a drug of choice in combination with pathogenetic and maintenance therapy. It is underlined that Coronacat is the first drug containing the GS-441524 with the GMP certificate in Europe, used to treat feline viral peritonitis. The results of the conducted therapy in the dynamics with the results of the examination, ultrasonography and biochemical blood test are given in the article. There is a conclusion about the high efficiency of the selected drug based on positive morphological dynamics of the patient’s recovery and about the possibility of recommending this drug as a specific treatment for an exatative form of feline infectious peritonitis.
Текст научной статьи Клинический случай инфекционного перитонита кошек
Введение. Инфекционный перитонит кошек Feline infectious peritonitis (FIP) – тяжелое системное особо опасное иммуноопосредованное инфекционное заболевание кошачьих, вызываемое вирусом семейства Coronaviridae [1]. Согласно данным статистики на выставках кошек выявляют до 82% кошек, зараженных коронавирусом [2]. Установлено, что вирус инфекционного перитонита кошек является мутацией вируса Feline coronavirus [3]. Мутация чаще происходит после стрессовой ситуации в жизни кошки, сопровождающейся снижением иммунного статуса организма, пиогранулематозным воспалением, прогрессирующим в течение нескольких недель или месяцев, которое всегда имеет летальный исход. Вирус инфекционного перитонита кошек поражает макрофаги, в результате чего вырабатываемые иммунной системой организма антитела не создают устойчивости и ухудшают течение болезни [4,5].
Наряду с панлейкопенией, вирусной лейкемией и иммунодефицитом кошек инфекционный перитонит является одной из наиболее часто регистрируемых причин смерти от инфекционных болезней кошек. Долгое время специфического эффективного средства лечения FIP не существовало, и исход болезни, как правило, был летальным [6].
В 2019 году в Калифорнии на симпозиуме по FIP инфекционный перитонит кошек получил статус излечимого заболевания, что связано с появлением препарата GS-441524 и его аналогов - ингибиторов протеаз группы GS для лечения кошек с инфекционным перитонитом [7,8].
Цель исследования - оценить на примере клинического случая выпотной формы вирусного перитонита у кота терапевтическую эффективность ветеринарного препарата Коронакэт.
Условия, материалы и методы. В сентябре 2022 г. на приём поступил беспородный кот в возрасте – 5 лет. Годом ранее ПЦР-диагностикой был поставлен диагноз коронавирусный энтерит кошек, лечение не назначали. Незадолго до обращения в клинику, животное перенесло длительный перелет по причине смены местожительства хозяев. Поводом для обращения в клинику послужили: прогрессирующая анорексия, депрессия, потеря веса, расстройство стула, увеличение живота в объеме.
Клиническое обследование проводили по общепринятым методикам. Материал для лабораторных исследований отправляли в ООО «Vet Union» (г. Москва) - Лицензия ВЕТ ЮНИОН, 3-4 гр. от 20.12.2007 г. (бессрочно) СЭЗ, ВЕТ ЮНИОН, 3-4 гр., от 26.04.2021 г. (до 25.04.2026г.)
Ультразвуковое исследование проводилось с использованием прибора модели Chison, датчик MC6-Е (микроконвекс), L7-Е (линейный), при частоте 7,79,0.
В качестве специфического средства лечения был апробирован препарат Коронакэт (серия 040823, производитель Филиал «Промветсервис-Альба», РФ).
Результаты и обсуждение. При клиническом осмотре отмечали вялое, угнетённое состояние, снижение температуры тела до 37,40С, диспноэ. Шерсть тусклая, плохо удерживается в волосяных фолликулах. Кожа жёлтого цвета, холодная, сухая, безболезненная, от неё исходит кислый запах. Эластичность кожи понижена, целостность не нарушена. Подкожная клетчатка развита незначительно. Также наблюдали желтушность и сухость конъюнктивы и видимых слизистых оболочек. При пальпации выявлено увеличение печени и мезентеральных лимфатических узлов.
По результатам ультразвукового исследования печень имеет неровные нечёткие контуры, притуплённые края. Капсула утолщена, под ней визуализируется свободная жидкость. Желчные протоки незначительно расширены, сосудистый рисунок стёрт. Эхоструктура паренхимы неоднородная, паренхима мелкозернистая. Наблюдается диффузное снижение эхогенности печени с усилением визуализации гиперэхогенной ткани перипортальной области.
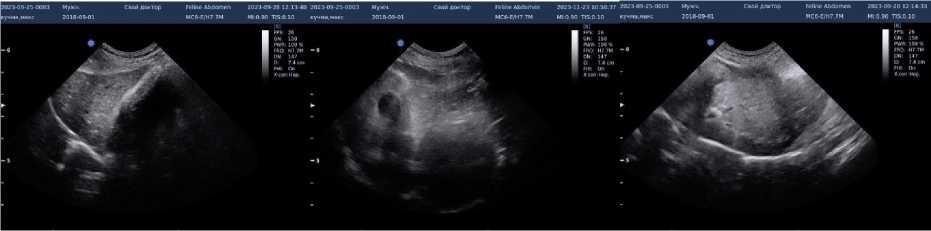
Рисунок 1 – Результаты ультразвукового исследования печени и желчного пузыря до лечения
Желчный пузырь каплевидной формы, размеры – 2,5 х 1 см, контуры ровные, чёткие, наполнен, содержимое анэхогенное, конкременты отсутствуют. Стенка утолщена до 2 мм (рис. 1).
Почки увеличены в объёме (левая – 4,72 х 2,5 см, правая – 4,69 х 2,64 см), контуры ровные, чёткие. Эхогенность коркового слоя усилена, толщина коры в левой почке 0,89 см, правой – 1 см. Кортико - медуллярная дифференциация незначительно сглажена. Почечная лоханка расширена (левой почки – до 0,67 см, правой – до 0,84 см). Включения отсутствуют (рис. 2).
Мочевой пузырь наполнен, стенка утолщена до 0,15 мм. Содержимое неоднородное, небольшое количество гиперэхогенных образований (рис.2).
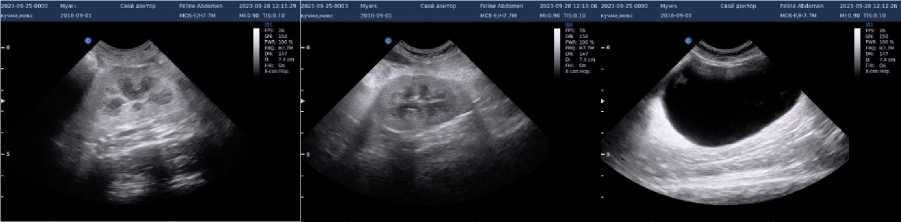
а) б) в)
Рисунок 2 – Результаты ультразвукового исследования почек и мочевого пузыря до лечения: а) левая почка; б) правая почка; в) мочевой пузырь
Таким образом, на момент исследования выявлены признаки гепатомегалии и хронического диффузного поражения печени; в мочевом пузыре умеренное количество гиперэхогенной взвеси, плотный гиперэхогенный осадок, не дающий акустической тени (скопление белковых нитей, слизь); визуализируется свободная жидкость в брюшной полости.
Результаты биохимического анализа крови представлены в таблице 1.
Таблица 1 – Результаты биохимического исследования крови до начала лечения
|
Показатели |
Результат |
Единицы измерения |
Референсные значения |
|
АлАТ |
31 |
Ед/л |
10-85 |
|
АсАТ |
159 |
Ед/л |
10-56 |
|
Альбумин |
20 |
г/л |
24-39 |
|
Альбумин/глобулин соотношение |
0,3 |
0,6-1,5 |
|
|
α-амилаза |
3253 |
Ед/л |
350-2000 |
|
Билирубин общий |
110,2 |
Мкмоль/л |
до 10,0 |
|
Билирубин прямой |
65,2 |
Мкмоль/л |
0-5 |
|
γ-ГТ |
˂4,0 |
Ед/л |
0-6 |
|
Глюкоза |
5,69 |
Ммоль/л |
3,2-7,9 |
|
Креатинкиназа |
705 |
Ед/л |
41-360 |
|
Креатинин |
52 |
Мкмоль/л |
44-160 |
|
Липаза |
34 |
Ед/л |
10-150 |
|
ЛДГ |
874 |
Ед/л |
40-350 |
|
Мочевина |
3,4 |
Ммоль/л |
3,5-12,0 |
|
Общий белок |
82 |
г/л |
66-84 |
|
Триглицериды |
4,7 |
Ммоль/л |
0,2-1,3 |
|
Холестерин |
5,08 |
Ммоль/л |
2,3-5,9 |
|
Фосфатаза щелочная |
61 |
Ед/л |
10-92 |
|
Кальций |
1,68 |
Ммоль/л |
1,9-2,6 |
|
Калий |
4,2 |
Ммоль/л |
4,0-5,5 |
|
Натрий |
130 |
Ммоль/л |
142-158 |
|
Хлор |
96 |
Ммоль/л |
108-125 |
|
Магний |
1,20 |
Ммоль/л |
0,8-1,2 |
|
Фосфор органический |
0,66 |
Ммоль/л |
0,90-2,50 |
|
Железо |
50,2 |
Мкмоль/л |
12-42 |
При биохимическом исследовании крови обнаружено изменение белкового состава крови и показателей, указывающих на печеночную недостаточность: увеличение содержания АсАТ в 15,9 раза/2,7 раза; альфа-амилазы – в 9,3 раз/1,6 раз; лактатдегидрогеназы – в 21,9 раз/2,5 раза; триглицеридов – в 23,5 раза/3,6 раза; креатинкиназы – в 17,2 раза/2 раза; железа – в 4,2/1,2 раза от нижней/верхней границы референсных значений, общего и прямого билирубина – в 11 и 13 раз от верхней границы референсных значений соответственно.
Общий белок не выходил за пределы референсных значений, но находился на верхней границе. Отмечено снижение против референсных значений: альбумин/глобулин соотношения в 2 раза/5 раз от нижней/верхней границы референсных значений, альбумина – на 16,7%/48,7%; мочевины – на 2,9/71,7%; натрия – на 8,5%/17,7%; хлора – на 11,1%/23,2% и фосфора – на 26,7%/74,0% от нижней/верхней границы референсных значений.
Кроме того, проведено исследование соскоба эпителиальных клеток слизистой прямой кишки методом полимеразной цепной реакции (ПЦР) с детекцией в режиме реального времени. В результате исследований обнаружен коронавирус кошек энтеральный (FCoV).
На основании комплексной диагностики коту был поставлен диагноз – инфекционный перитонит кошек (FIP).
В качестве специфического противовирусного средства был назначен препарат Коронакэт из расчёта 0,5 мл на 1 кг массы тела согласно инструкции. Коронакэт – первый препарат, содержащий GS-441524, с сертификатом GMP в Европе, применяемый для лечения вирусного перитонита кошек FIP (ФИП /ВПК). Был составлен дневник лечения Коронакэтом на период с 28.09.2023 по 20.12.2023 гг. Дозу Коронакэта корректировали по мере набора массы у животного с целью контроля вводимой эффективной дозы.
Также животному была назначена патогенетическая терапия: для повышения иммунного статуса организма применяли препарат Ронколейкин – по 0,5 мл п/к на 3 дня; в качестве гепатопротектора Гепатоджект – по 2 мл п/к на 5 дней, далее Гепатолюкс суспензия – по 0,5 мл внутрь 2 раза в день на 14 - 21 день; с целью предотвращения рвоты Маропиталь – 0,4 мл п/к по мере необходимости; для повышения аппетита - Нуклеопептид – 0,6 мл п/к по мере необходимости.
На вторые сутки применения препарата Коронакэт у кота появилась двигательная активность: он вставал и пытался ходить по квартире. На третьи сутки кот начал самостоятельно принимать пищу малыми порциями и проявлять интерес к окружающему миру. После двух недель применения препарата температура составила 38,40С, что соответствует физиологической норме, восстановился пищевой режим. Коронакэт продолжали вводить до 20.12.2023 г. К концу лечения масса животного увеличилась на 0,6 кг и составила 4,6 кг. На протяжении всего лечения проводился периодический контроль состояния брюшной полости методом УЗ - диагностики.
После завершения курса лечения по данным УЗ – исследования контуры печени ровные и чёткие, капсула не утолщена, паренхима гиперэхогенна, эхоструктура однородная. Сосудистый рисунок умеренно сглажен, желчные протоки не расширены. Форма желчного пузыря округлая, размеры – 0,81 х 1,04 см., не наполнен, содержимое анэхогенное, стенка не утолщена, конкрементов нет (рис. 3).
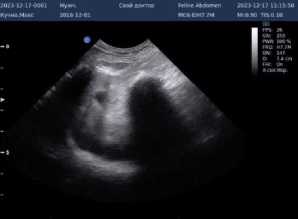
Рисунок 3 – Результаты ультразвукового исследования печени и желчного пузыря после лечения
Почки в объёме уменьшились (левая – 4,16 х 2,41, правая – 4,06 х 2,6), контуры ровные, чёткие. Эхогенность коркового слоя усилена, толщина коры в левой почке 0,49 см, правой – 0,76 см. Эхогенность мозгового слоя усилена в левой почке. Кортико-медуллярная дифференциация незначительно сглажена, почечные лоханки не расширены, включения отсутствуют. Мочевой пузырь
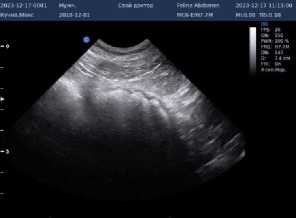
наполнен, стенка не утолщена. Содержимое анэхогенное. Имеется небольшое количество гиперэхогенных образований (рис. 4).
а)
б)
в)
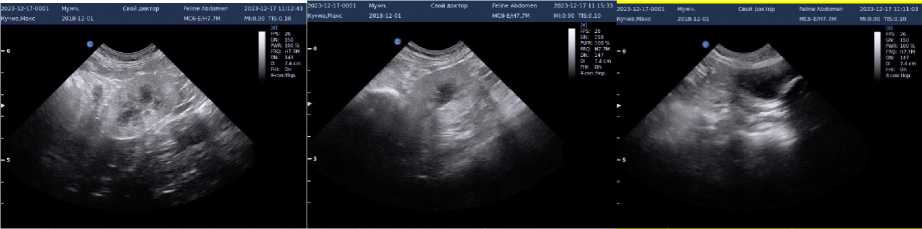
Рисунок 4 – Результаты ультразвукового исследования почек и мочевого пузыря после лечения: а) левая почка; б) правая почка; в) мочевой пузырь
Заключительное ультразвуковое исследование показало, что свободная жидкость в брюшной полости не визуализируется (рис. 5).
Рисунок 5 –Результаты ультразвукового исследования брюшной полости после лечения
Таким образом, выявлены признаки диффузного изменения паренхимы печени (гепатоз), выявлены признаки диффузного изменения почек (пиелонефрит).
Гиперэхогенная структура органа, рассматриваемая как признак воспаления, может быть следствием лечения, так как Коронакэт может оказывать побочное действие на печень и почки. Кроме того, произошло восстановление массы тела животного и жировых депо, поэтому внутренние органы визуально стали светлее (гиперэхогеннее).
Результаты биохимического исследования крови по окончании лечения (на 90 - е сутки) представлены в таблице 2.
Анализируя данные биохимического исследования крови на момент окончания лечения следует отметить, что основной показатель – альбумин/глобулиновое соотношение – повысился на 66,7% относительно его значения до начала лечения и приблизился к нижней границе референсных значений, также повысилось на 30% и вошло в пределы референсных значений содержание альбумина, снизилось на 57,4% до физиологической нормы содержание щелочной фосфатазы, содержание общего белка относительно его значения до начала лечения снизилось на 2,4%. В результате проведённого лечения показатели АсАТ снизились в 6,6 раза и общий билирубин – в 64,8 раза.
Показатель креатинина вырос по сравнению с его значением до начала лечения в 2,6 раза, мочевины – в 2,4 раза, что говорит об улучшении белкового обмена.
Таблица 2 – Биохимическое исследование крови в конце лечения
|
Показатели |
Результат |
Единицы измерения |
Референсные значения |
|
АлАТ |
63 |
Ед/л |
10-85 |
|
АсАТ |
24 |
Ед/л |
10-56 |
|
Альбумин |
26 |
г/л |
24-39 |
|
Альбумин/глобулин соотношение |
0,5 |
0,6-1,5 |
|
|
Билирубин общий |
˂1,70 |
Мкмоль/л |
до 10,0 |
|
γ-ГТ |
˂4,0 |
Ед/л |
0-6 |
|
Глюкоза |
5,12 |
Ммоль/л |
3,2-7,9 |
|
Креатинин |
133 |
Мкмоль/л |
44-160 |
|
Мочевина |
8,1 |
Ммоль/л |
3,5-12,0 |
|
Общий белок |
80 |
г/л |
66-84 |
|
Фосфатаза щелочная |
26 |
Ед/л |
10-92 |
Выводы. Препарат Коронакэт показал высокую эффективность при инфекционном перитоните кошек (FIP). Проводимое в период лечения ультразвуковое исследование позволило визуализировать положительную морфологическую динамику выздоровления. Препарат Коронакэт можно рекомендовать в качестве специфического средства лечения при выпотной форме вирусного перитонита кошек.
Список литературы Клинический случай инфекционного перитонита кошек
- Pedersen N. C. A review of feline infectious peritonitis virus infection: 1963-2008//J. Feline Med. Surg., 2009; 44, 225-258. EDN: MLMYYB
- Whittaker G.R. Coronaviridae. Fenner's Veterinary Virology. 5th ed. MacLachlan N.J. Dubovi E.J. // London, UK: Academic Press, 2017.
- Porter E. Tasker S., Day M.J., Harley R., Kipar A., SiddellS.G., Helps C.R. Amino acid changes in the spike protein of feline coronavirus correlate with systemic spread of virus from the intestine and not with feline infectious peritonitis // Veterinary research. 2014. EDN: RLLQDT
- Desmarets L MB, TheunsS., Olyslaegers D. AJ., Dedeurwaerder A. Establishment of feline intestinal epithelial cell cultures for the propagation and study of feline enteric coronaviruses // Vet Res, 2013; 44(1), 71. EDN: PRQQPE
- Kipar A, Meli M.L., Baptiste K.E., et al. Sites of feline coronaviral persistence in healthy cats// J Gen Virol, 2010; 91, 1698-1707.
- Hohdatsu T. H. Yamato, T. Ohkawa, M. Kaneko, K. Motokawa, Kusuhara H., Kaneshima T., Arai S., Koyama H. Vaccine efficacy of a cell lysate with recombinant baculovirus-expressed feline infectious peritonitis (FIP) virus nucleocapsid protein against progression of FIP // Veterinary microbiology. 2003. Р.31-44.
- Murphy B.G. Perron M., Murakami E., Bauer K., Park Y., Eckstrand C., Liepnieks M., Pedersen N.C. The nucleoside analogGS-441524 strongly inhibits feline infectious peritonitis (FIP) virusin tissue culture and experimental cat infection studies // Veterinary microbiology. 2018. Р.226-233.
- Sheahan T. P. Broad-spectrum antiviral GS-5734 inhibits both epidemic and zoonotic coronaviruses / T. P. Sheahan, А.С. Sims, R. L. Graham // Science translational medicine. 2017. V. №396. -. DOI: 10.1126/scitranslmed.aal3653


