Клинический случай проведения транскатетерной имплантации аортального клапана пациенту с критическим аортальным стенозом, фибрилляцией предсердий, эндоваскулярной окклюзией ушка левого предсердия и синдромом Маллори-Вейсса
Автор: Барковская М.К., Валиева З.С., Даренский Д.И., Терещенко А.С., Мартынюк Т.В.
Журнал: Евразийский кардиологический журнал @eurasian-cardiology-journal
Рубрика: Клинический случай
Статья в выпуске: 4, 2022 года.
Бесплатный доступ
В данной статье представлен клинический случай пациента 81 года, поступившего в ФГБУ «НМИЦ кардиологии им. ак. Е.И. Чазова» МЗ РФ для проведения транскатетерной имплантации аортального клапана в связи с критическим аортальным стенозом (АС), провоцирующего такие симптомы, как одышка при небольшой физической нагрузке, головокружение и синкопальные состояния. Также в анамнезе у данного пациента пароксизмы фибрилляции предсердий. Особенностью клинической картины АС является длительный бессимптомный период, продолжительность которого существенно различается. После возникновения первых клинических проявлений заболевания резко возрастает риск внезапной смерти, а средняя продолжительность жизни составляет 2-3 года. Развитие фибрилляции предсердий приводит к серьезному клиническому ухудшению за счет исчезновения вклада систолы предсердий в наполнение левого желудочка(ЛЖ). Концентрическая гипертрофия ЛЖ, являющаяся на начальном этапе важным адаптационным механизмом, компенсирующим высокое внутриполостное давление, в дальнейшем приводит к относительному снижению коронарного кровотока и ограничению коронарного вазодилатационного резерва. В ходе подготовки к хирургическому лечению стеноза пациенту выполнена транслюминальная баллонная ангиопластика со стентированием правой коронарной артерии. Учитывая проведение чрескожного коронарного вмешательства и наличие нарушения ритма пациенту была назначена тройная антитромбоцитарная терапия, включающая клопидогрел, ацетилсалициловую кислоту и апиксабан. На фоне терапии данными препаратами у пациента развилось желудочно-кишечное кровотечение (синдром Маллори-Вейсса), что потребовало установку окклюдера в ушко левого предсердия, как альтернативы антикоагулянтной терапии при высоких рисках возникновения нежелательных побочных реакций.
Аортальный стеноз, синдром маллори-вейсса, окклюзия ушка левого предсердия, клинический случай
Короткий адрес: https://sciup.org/143179494
IDR: 143179494 | DOI: 10.38109/2225-1685-2022-4-68-73
Case report of transcatheter aortic valve implantation to the patient with severe aortic stenosis, atrial fibrillation, endovascular occlusion of the left atrial appendage and Mallory-Weiss syndrome
The case of a 81-year-old male with atrial fibrillation, associated with severe aortic stenosis (AS) is outlined. A peculiarity of the clinical portrait of AS is a long asymptomatic period with a significantly varying duration. After the appearance of the first clinical manifestations of the disease (shortness of breath on exercise, fainting) the risk of sudden death rises sharply, and the average life expectancy is 2-3 years. The development of atrial fibrillation (AF) leads to a serious impairment of the clinical condition due to loss of the contribution of atrial systole to the filling of the left ventricle (LV). Concentric hypertrophy of the LV, which at the first stage is an important adaptation mechanism compensatingfor a high intracavitary pressure, later leads to a relative reduction of the coronary blood flow and to limitation of the coronary vasodilatation reserve. So patient was referred for transcatheter aortic valve implantation. He had also a history of coronary artery disease with earlier percutaneous coronary intervention. Then, he was started on a triple antithrombotic therapy therapy. The triple antithrombotic therapy caused gastrointestinal bleeding (Mallory-Weiss syndrome). Considering the difficulties in the rational choice of anticoagulant therapy and high risks of adverse reactions, the patient underwent endovascular occlusion of the left atrial appendage.
Текст научной статьи Клинический случай проведения транскатетерной имплантации аортального клапана пациенту с критическим аортальным стенозом, фибрилляцией предсердий, эндоваскулярной окклюзией ушка левого предсердия и синдромом Маллори-Вейсса
Данная статья распространяется на условиях «открытого доступа», в соответствии с лицензией CC BY-NC-SA 4.0 («Attribution-NonCommercial-ShareAlike» / «Атрибуция-Некоммерчески-Сохранение Условий» 4.0), которая разрешает неограниченное некоммерческое использование, распространение и воспроизведение на любом носителе при условии указания автора и источника. Чтобы ознакомиться с полными условиями данной лицензии на русском языке, посетите сайт:
*Corresponding author: Marianna K. Barkovskaya, resident doctor, Department of Pulmonary Hypertension and Heart Disease, E.I. Chazov National Medical Research Centre of Cardiology, street 3rd Cherepkovskaya, 15 a, Moscow 121552, Russian Federation, ,
Zarina S. Valieva, Cand. of Sci. (Med.), Researcher, Department of Pulmonary Hypertension and Heart Disease, E.I. Chazov National Medical Research Centre of Cardiology, street 3rd Cherepkovskaya, 15 a, Moscow 121552, Russian Federation,
Dmiriy I. Darensky, M.D., Cand. Of Sci. (Med.), E.I. Chazov National Medical Research Centre of Cardiology, street 3rd Cherepkovskaya, 15 a, Moscow 121552, Russian Federation,
Andrey S. Tereschenko, Cand. of Sci. (Med), Researcher of the X-ray Endovascular Diagnosis and Treatment Department, E.I. Chazov National Medical Research Centre of Cardiology, street 3rd Cherepkovskaya, 15 a, Moscow 121552, Russian Federation,
Tamila V. Martynyuk, Dr. of Sci. (Med.), Head of the Department, Professor of pulmonary hypertension and heart disease, E.I. Chazov National Medical Research Centre of Cardiology, street 3rd Cherepkovskaya, 15 a, Moscow 121552, Russian Federation,
This is an open access article distributed under the terms of the Creative Commons Attribution-NonCommercial-ShareAlike 4.0 International (CC BY-NC-SA 4.0) License , which permits unrestricted use, distribution, and reproduction in any medium, provided the original author and source are credited.
Аортальный стеноз – это сужение выносящего тракта левого желудочка в области аортального клапана, ведущее к затруднению оттока крови и резкому возрастанию градиента давления между левым желудочком и аортой.
С увеличением продолжительности жизни и старением населения стеноз устья аорты в настоящее время является одним из наиболее распространенных форм приобретенной клапанной патологии. Ранняя постановка диагноза и лечение стеноза аорты имеют первостепенное значение, потому что прогрессирование тяжести данного заболевания является смертельным.
Кардиальными симптомами тяжелого аортального стеноза являются стенокардия, связанная с нагрузками, застойная сердечная недостаточность. Снижение сердечного выброса и преходящая недостаточность мозгового кровообращения приводят к головокружению и синкопе.
У большинства пациентов симптомы появляются при нормальной фракции выброса левого желудочка, однако у некоторых пациентов наблюдается снижение систолической функции миокарда до появления симптомов [1].
Хирургическое протезирование аортального клапана насчитывает более чем полувековую историю, начиная с первой успешной операции D. Harken, который в 1960 г. установил шариковый протез в условиях искусственного кровообращения [2]. «Стандартная» операция предусматривала выполнение стернотомии, использование искусственного кровообращения, иссечение патологически измененного клапана и фиксацию протеза швами к фиброзному кольцу аорты. Уровень госпитальной летальности в старшей возрастной группе с различной сопутствующей патологией превышал аналогичный показатель среди лиц молодого и среднего возраста (16% и 3-5%, соответственно) и каждый третий пациент с критическим аортальным стенозом признавался неоперабельным из-за выраженного снижения сократимости левого желудочка и тяжелых сопутствующих заболеваний [3].
Появление технологий транскатетерной замены аортального клапана обеспечивает захватывающие возможности для лечения пациентов, при которых традиционные хирургические процедуры не могли быть выполнены или были связаны с высоким риском.
Представляем клинический случай пациента Ш. 81 года, который поступил в ФГБУ «НМИЦК им. ак. Е.И. Чазова» МЗ РФ с жалобами на общую слабость, одышку при небольшой физической нагрузке, головокружение.
Из анамнеза известно о наличии у пациента гипертонической болезни в течение тридцати лет и пароксизмальной формы фибрилляции предсердий с 2019 года.
В 2017 году пациент впервые потерял сознание. В связи с подозрением на неврологическую патологию наблюдался у врача-невролога, было исключено вестибулярное головокружение.
По результатам эхокардиографии (ЭхоКГ) в 2019 году впервые выявлен аортальный стеноз, пиковый градиент давления 102 мм рт. ст., фиброзное кольцо 2,3 см., аневризма восходящего отдела аорты.
На фоне приема ривароксабана 15 мг/сутки отмечены эпизоды длительных носовых кровотечений.
Поступил для обследования и решения вопроса о возможности проведения транскатетерной имплантации аортального клапана (TAVI).
В лабораторных анализах отмечается незначительное cнижение гемоглобина до 12,74 г/дл, в остальном без особенностей.
На снятой ЭКГ при поступлении регистрируется синусовая аритмия, ЧСС 67 ударов в минуту. Отклонение электрической оси сердца влево. Единичные желудочковые экстрасистолы. Признаки изменения миокарда вследствие гипертрофии левого желудочка (рис. 1).
По данным рентгенографии органов грудной клетки: выраженный (III ст.) кальциноз аортального клапана; венозный застой в легких 1-2 ст., признаки прекапиллярной ЛГ; двусторонний плевральный выпот, слева – большое количество; эктазия восходящей аорты; расширены верхняя, нижняя полая вены; двусторонний пневмофиброз.
Трансторакальная эхокардиография (ЭхоКГ): фракция выброса 30-32%, четких зон нарушения локальной сократимости нет, гипертрофия миокарда левогожелудочкас преимущественным утолщением базального отдела межжелудочковой перегородки, Vмакс 5,0 м/с, максимальный градиент на АК = 100 мм рт. ст., средний градиент Г на АК = 65 мм рт. ст., площадь открытия
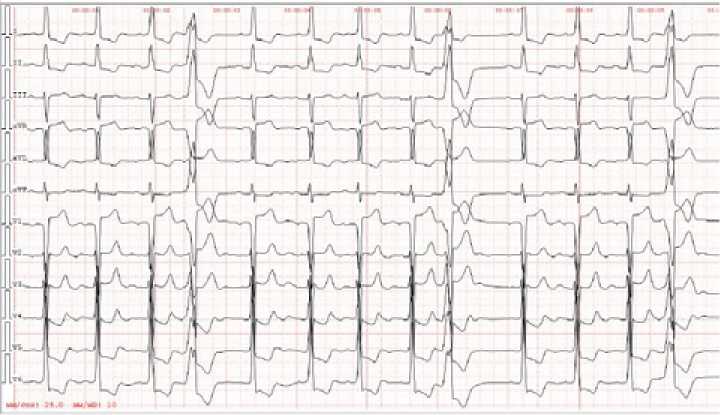
Рисунок 1. Электрокардиограмма при поступлении
Picture 1. Electrocardiogram on admission
70 ЕВРАЗИЙСКИЙ КАРДИОЛОГИЧЕСКИЙ ЖУРНАЛ, 4, 2022
Таблица 1. Классификация степени активности ЖКК по Forrest (1974)Table 1. The Forrest Classification (1974)
I — продолжающееся на момент осмотра кровотечение:
-
• IA — струйное кровотечение
-
• IB — диффузное кровотечение
II — остановившееся на момент осмотра
-
• IIA — видимый сосуд в дне язвы в виде столбика или бугорка
-
• IIB — плотно фиксированный к дну язвы тромб- сгусток (не смываемый струей воды)
-
• IIC — мелкоточечные сосуды в дне язвы в виде темных (красных) пятен
III — дефект слизистой оболочки без признаков кровотечени аортального клапана (по уравнению непрерывности) = ~0,5 см2, недостаточность аортального клапана I-II степени.
По данным эзофагодуоденоскопии (ЭГДС): недостаточность кардии, поверхностный антральный гастрит, катаральный бульбит.
В рамках подготовки к TAVI пациенту была выполнена ко-ронароангиография, по данным которой диагональная артерия в проксимальном отделе стенозирована на 70%, правая коронарная артерия в проксимальной сегменте стенозирована до 50%, на границе проксимального и среднего сегмента визуализируется спонтанная диссекция атеросклеротической бляшки с сужение просвета сосуда на 70%, с признаками пристеночного стеноза, отходящая в этом месте крупная правожелудочковая ветвь в устье стенозирована на 90%, далее с неровными контурами, в остальном без особенностей. Выполнена транслюминальная баллонная ангиопластика правой коронарной артерии (рис. 2).
Учитывая выполненную транслюминальную баллонную ангиопластику со стентированием правой коронарной артерии и наличие у пациента пароксизмальной формы фибрилляции предсердий, была назначена тройная антитромбоцитарная терапия клопидогрелем 75 мг, ацетилсалициловой кислоты 100 мг и апиксабаном 5 мг 2 р/сутки согласно клиническим рекомендация по фибрилляции предсердий от 2020 г.
На фоне приема данной комбинации через три дня после эндоваскулярного вмешательства у пациента появилось носовое, а после и желудочно-кишечное кровотечение, сопровождающееся рвотой и меленой.
По данным экстренно выполненной ЭГДС выявлен катаральный эзофагит, синдром Маллори-Вейсса (СМВ), признаки продолжающегося кровотечения, IB по Forrest (табл. 1), в связи с этим пациенту выполнена аргоноплазменная коагуляция дна дефекта. Гемостаз достигнут.
Назначена гастропротективная терапия, в виде пантопразола по 40 мг 2 р/сутки и комбинация магния гидроксида и алюминия гидроксида в виде суспензии по 10 мл 3 р/сутки, также были отменены апиксабан и ацетилсалициловая кислота.
В клиническом анализе крови отмечалось умеренное снижение уровня эритроцитов и гемоглобина (табл. 2).
Таблица 2 Динамика показателей клинического анализа крови Table 2. Dinamics of complete blood count
|
Показатель |
При поступлении |
После кровотечения |
|
Эритроциты |
5,45*1012/л |
4,42*1012/л |
|
Гемоглобин |
12,74 г/дл |
10,75 г/дл |
|
Гематокрит |
40,2% |
33,6% |
|
Лейкоциты |
8,5*109/л |
13,2*109/л |
|
Тромбоциты |
134*109/л |
143*109/л |
Для повышения уровня гемоглобина был назначен Сульфат железа 200 мг/сутки.
Учитывая пароксизмальную форму фибрилляции предсердий, CHA(2)DS(2)-VASc 5 баллов, наличие носового и желудочно-кишечного кровотечения на фоне приема антикоагулянтов была выполнена эндоваскулярная окклюзия ушла левого предсердия (окклюдер Watchman). Операция прошла без осложнений.
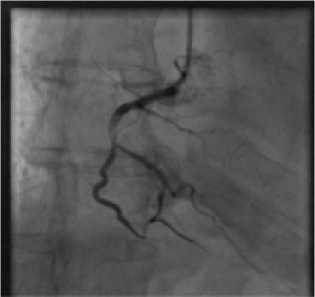
До стентирования (Before stenting)
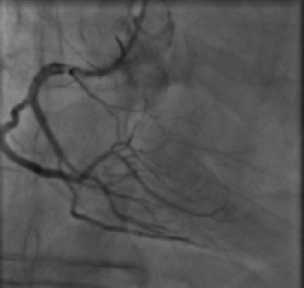
После (After)
Рисунок 2. Транслюминальная баллонная ангиопластика правой коронарной артерии
-
Figure 2. Transluminal balloon angioplasty of the right coronary artery
Пациент был выписан с целью амбулаторного лечения анемии и синдрома Маллори-Вейсса.
В апреле 2022 г. пациент поступил с улучшением самочувствия в виде уменьшения одышки и частоты эпизодов головокружений. На момент поступления принимает терапию клопи-догрел 75 мг/сутки, фуросемид 40 мг/сутки, спиронолактон 75 мг/сутки и сульфат железа 200 мг/сутки.
Однако по данным инструментальных методов обследова ния отмечается отрицательная динамика: по данным рентгенографии увеличился двусторонний плевральный выпот, справа небольшое количество (до 500 мл), слева количество жидкости больше (не менее 1 л), в остальном без динамики.
По результатам трансторакальной ЭхоКГ без достоверной динамики по сравнению с данными предыдущей госпитализации.
По данным лабораторных анализов крови выявлена тромбоцитопения (108*10*9/л), гемоглобин и эритроциты в пределах референсных значений.
Перед TAVI пациент был переведен с клопидогрела в дозе 75 мг/сутки на ацетилсалициловую кислоту в дозе 100 мг/сутки согласно рекомендациям американской коллегии кардиологов и американской ассоциации сердца от 2020 г. [4].
Учитывая отсутствие противопоказаний, принято решение о проведении пациенту транскатетерной имплантации аортального клапана (рис. 4).
В послеоперационном периоде состояние пациента оставалось стабильным, по данным ХМ-ЭКГ жизнеугрожающих нарушений ритма и проводимости не выявлено, по данным трансторакальной эхокардиографии: фракция выброса 45-50%; Vмакс 1,9 м/с; мГДcАК = 14 мм рт. ст.; срГДсАК = 7 мм рт. ст.
По результатам контрольных анализов крови тромбоцитопения не прогрессировала, гемоглобин, эритроциты и креатинин в пределах нормальных значений (эритроциты – 4,87*10*12/л; гемоглобин – 14,90 г/дл (N:13,00-18,00); тромбоциты – 116*10*9/л (N:130-400).
Пациент выписан с клиническим улучшением, в состоянии компенсации явлений хронической сердечной недостаточности.
ОБСУЖДЕНИЕ
Фибрилляция предсердий (ФП) является самой распространенной сердечной аритмией. Ишемический кардиоэмболический инсульт является самым грозным осложнением ФП, зачастую приводя к смерти и выраженной инвалидизации, его риск варьирует от 1,9 до 18,2% в год и определяется возрастом, полом и сопутствующими заболеваниями. Применение пероральных антикоагулянтных препаратов позволяет снизить риск инсульта и других тромбоэмболических осложнений, что подтверждено в ряде крупных рандомизированных исследований и лежит в основе традиционного подхода к лечению больных ФП. [5]. Основным ослож- нением антикоагулянтной терапии являются кровотечения, в том числе желудочно-кишечные, к данной категории относится и синдром Маллори-Вейсса.
Клинические проявления СМВ зависят от степени и глубины разрыва и, как правило, схожи с симптомами желудочнокишечных кровотечений иной этиологии. Это гематемезис (кровавая рвота), мелена, боли в эпигастральной области, за грудиной, дисфагия, затруднение дыхания, а также симптомы развития геморрагического шока при массивном кровотечении — артериальная гипотензия, тахипноэ, тахикардия, угнетение сознания. Гематемезис возникает в 40% случаев развития СМВ, мелена — в 30% случаев.
Различают три группы разрывов при СМВ:
Согласно рекомендациям Европейского общества кардиологов, вопрос об эндоваскулярном закрытии УЛП может быть рассмотрен при наличии у пациента противопоказаний к длительной антикоагулянтной терапии (класс IIb, уровень доказательности B) [5].
В 1996 г. J.L. Blackshear и соавт. было установлено, что источником до 90% всех тромбов при ФП является ушко левого предсердия (УЛП). В связи с этим на протяжении 20 лет разрабатываются методы, направленные на исключение УЛП из системного кровотока в качестве альтернативы длительной антикоагулянтной терапии. На сегодняшний день наибольшее распространение получили эндоваскулярные методы закрытия УЛП [5].
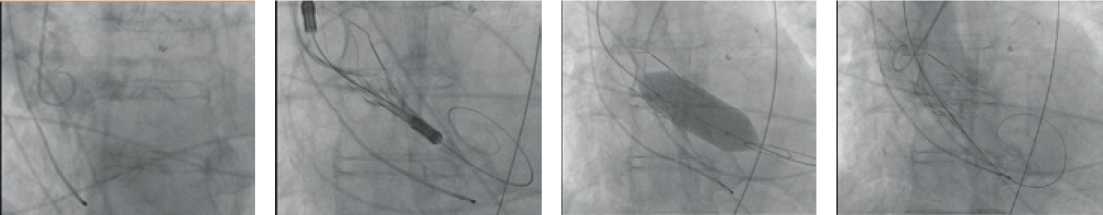
Рисунок 4. Транскатетерная имплантация аортального клапана пациенту с ранее установленным окклюдером Watchman
Figure 4. Transcatheter aortic valve implantation to the patient with Watchman occluder
72 ЕВРАЗИЙСКИЙ КАРДИОЛОГИЧЕСКИЙ ЖУРНАЛ, 4, 2022
ЗАКЛЮЧЕНИЕ
В данном клиническом случае транслюминальная баллонная ангиопластика со стентированием осложнилось желудочно-кишечным кровотечением, что потребовало установку окклюдера в ушко левого предсердия как альтернативы медикаментозной терапии при высоких рисках возникновения нежелательных побочных реакций. В свою очередь, проведение TAVI для нашего пациента является самым безопасным методом коррекции критического стеноза.
Таким образом, совершенствование существующих и разработка новых методов рентгеноэндоваскулярного лечения дает возможность пациентам с наличием множественной сопутствующей патологии продлить жизнь и улучшить её качество.
Список литературы Клинический случай проведения транскатетерной имплантации аортального клапана пациенту с критическим аортальным стенозом, фибрилляцией предсердий, эндоваскулярной окклюзией ушка левого предсердия и синдромом Маллори-Вейсса
- Kanwar A, Thaden J.J., Nkomo V.T. Management of Patients With Aortic Valve Stenosis. Mayo Clin Proc. 2018 Apr;93(4):488-508. PMID:29622096.https://doi.org/10.1016/j.mayocp.2018.01.020
- Имаев Т.Э., Комлев А.Е., Акчурин Р.С. Транскатетерная имплантация аортального клапана. Состояние проблемы, перспективы в России. Рациональная фармакотерапия в кардиологии. 2015;11(1):53-9.https:// https://doi.org/doi.org/10.20996/1819-6446-2015-11-1-53-59
- Смирнова Е.А., Терехина А.И., Филоненко С.П., Муранчик Е.Н. Кальцинированный клапанный аортальный стеноз: возможности и осложнения хирургического лечения. Российский медико-биологический вестник им. академика И.П. Павлова. 2021;29(1):147-160. https://doi.org/10.23888/PAVLOVJ2021291147-160
- Otto CM, Nishimura RA, Bonow RO et al. 2020 ACC/AHA guideline for the management of patients with valvular heart disease: a report of the American College of Cardiology/American Heart Association Joint Committee on Clinical Practice Guidelines. Circulation. 2021;143:e72-e227. https://doi.org/10.1161/CIR.0000000000000923
- Гучаев Р.В., Певзнер Д.В., Меркулов Е.В. и др. Клинический случай возобновления антикоагулянтной терапии после имплантации окклюдера ушка левого предсердия Amplatzer cardiac plug. Атеротромбоз. 2019;1:82-91. https://doi.org/10.21518/2307-1109-2019-1-82-91
- Баялиева А.Ж., Зефиров Р.А., Янкович Ю.Н. Особенности ведения пациентов с желудочно- кишечными кровотечениями в отделениях реанимации и интенсивной терапии. Казанский мед. ж. 2019; 100(6): 930-934. https://doi.org/10.17816/KMJ2019-930
- Rawla P, Devasahayam J. Mallory Weiss Syndrome. 2021 Dec 12. In: StatPearls [Internet]. Treasure Island (FL): StatPearls Publishing; 2022 Jan. PMID:30855778.
- Baumgartner H, De Backer J, Babu-Narayan S.V., et al., ESC Scientific Document Group, 2020 ESC Guidelines for the management of adult congenital heart disease: The Task Force for the management of adult congenital heart disease of the European Society of Cardiology (ESC). Endorsed by: Association for European Paediatric and Congenital Cardiology (AEPC), International Society for Adult Congenital Heart Disease (ISACHD). European Heart Journal. 2021;42(6):563-645. https://doi.org/10.15829/1560-4071-2021-4702
- Holmes D.R., Reddy V.Y., Turi Z.G., et al. PROTECT AF Investigators. Percutaneous closure of the left atrial appendage versus warfarin therapy for prevention of stroke in patients with atrial fibrillation: a randomised non-inferiority trial. Lancet. 2009;374(9689):534-542. https://doi.org/10.1016/S0140-6736(09)61343-X
- Holmes D.R. Jr., Kar S., Price M.J., et al. Prospective randomized evaluation of the Watchman Left Atrial Appendage Closure device in patients with atrial fibrillation versus long-term warfarin therapy: the PREVAIL trial. J Am Coll Cardiol. 2014;64(1): 1-12. https://doi.org/10.1016/j.jacc.2014.04.029
- Комлев А.Е., Саидова М.А., Имаев Т.Э. и др. Гемодинамические варианты тяжелого аортального стеноза. Рациональная Фармакотерапия в Кардиологии 2020;16(5):822-830. https://doi.org/10.20996/1819-6446-2020-10-06


