Клинический случай развития острого инфаркта миокарда при микрососудистой стенокардии
Автор: Минюк Ю. И., Салиева Е. В., Тамоян З. С., Урманова Ю. Р., Таипова Л. У., Хасанов А. Х.
Журнал: Евразийский кардиологический журнал @eurasian-cardiology-journal
Рубрика: Клинический случай
Статья в выпуске: 1, 2020 года.
Бесплатный доступ
Цель работы. Описать клинический случай коронарной отягощенности без стенозирующего поражения магистральных ветвей венечных артерий у больного микрососудистой стенокардией с последующим развитием инфаркта миокарда с формированием ишемического гипокинеза передневерхушечной области левого желудочка при отсутствии повышенных уровней сывороточных маркеров некроза миокарда.Материалы и методы. За основу исследования взят единичный клинический случай. Объектом исследования является пациент, у которого были жалобы на давящие боли с локализацией за грудиной и иррадиацией в левую руку, сопровождающиеся смешанной одышкой, возникшие в покое, слабо купирующиеся короткодействующими нитратами и наркотическими анальгетиками, общей резкой слабостью. При первичном осмотре состояние больного средней степени тяжести, сознание ясное, положение активное, кожные покровы и видимые слизистые чистые, обычной окраски. Больному была проведена оценка лабораторных показателей, ЭКГ, эхо-кардиография (ЭХО-КГ), рентгенография органов грудной клетки (ОГК), коронароангиография (КАГ) с последующим переводом в отделение неотложной кардиологии.Результаты...
Микрососудистая стенокардия, микрососудистая дисфункция, коронарный синдром, коронарная артерия, коагуляционная нестабильность системы гемостаза
Короткий адрес: https://sciup.org/143171847
IDR: 143171847 | DOI: 10.24411/2076-4766-2020-10006
Clinical case of acute myocardial infarction in patients with microvascular angina
Purpose. To describe a clinical case of coronary burden without stenosing lesions of the main branches of the coronary arteries in a patient with microvascular angina with subsequent development of myocardial infarction with the formation of ischemic hypokinesis of the anterior-apical region of the left ventricle in the absence of elevated levels of serum markers of myocardial necrosis.Materials and methods. The study is based on a single clinical case. The object of the study is the patient in whom there were complaints of pressing pain localized behind the sternum and radiating to the left arm, accompanied by a mixed shortness of breath that occurred at rest, poorly stoped short-range nitrates and narcotic analgesics, sharp General weakness. Under primary inspection state of ailing average extent of gravity, consciousness clear, position active, skin integuments and visible mucous of clean, conventional painting. The patient was evaluated laboratory parameters, ECG, echo-cardiography (ECHO-kg), chest x-ray (OGK), coronary angiography (CAG), followed by transfer to the emergency Department of cardiology...
Текст научной статьи Клинический случай развития острого инфаркта миокарда при микрососудистой стенокардии
Наиболее распространенной причиной развития ИБС и, соответственно, ишемии миокарда считается коронарный атеросклероз с различной степенью обструкции, вплоть до окклюзий, питающих миокард сосудов, имеющий грозные осложнения (коронарный тромбоз, сердечная недостаточность, внезапная смерть). Тем не менее, по разным данным, примерно у половины пациентов со стабильной стенокардией, которым проводится диагностическая коронарная ангиография (КАГ), и у 10–20% пациентов с острым коронарным синдромом выявляются неизмененные или малоизмененные (менее 50% сужения просвета сосуда) коронарные артерии [1-4].
В одном из исследований у 44,5% из 925 пациентов, направленных на плановую диагностическую КАГ, были выявлены неизмененные или малоизмененные коронарные артерии [1, 4]. Согласно данным W.L. Proudfit et al., у 20% пациентов, которым была выполнена КАГ при болях в груди, обнаруживались нормальные коронарные артерии [1, 5]. Еще в одном исследовании у 14,6% пациентов, которым была выполнена КАГ при наличии болевого синдрома в груди и подозрении на поражение коронарных артерий, также не было выявлено их изменений [1, 6]. Следует отметить, что у пациентов с болями в груди и без предварительного установления ишемии миокарда обнаруженные при КАГ неизмененные коронарные артерии исключают диагноз микрососудистой стенокардии (МСС), а само инвазивное обследование может оказаться малообоснованным в отсутствие других данных и факторов риска.
Указанное состояние впервые было описано примерно 40 лет назад H.G. Kemp et al. и получило название «кардиальный синдром Х» (КСХ) [1, 7]. Наряду с этим термином в последующем использовались и многие другие определения, такие как синдром Х, болезнь малых сосудов, стенокардия с поражением сосудов малого диаметра, синдром Джорлина–Лайкоффа, необструктивная болезнь коронарных артерий, а в последние годы наибольшее распространение получил термин МСС. Следует напомнить, что термин МСС был первоначально предложен R.O. Cannon, S.E. Epstein еще в 1988 г. для обозначения миокардиальной ишемии, возникшей не вследствие обструктивных изменений коронарного русла, а в связи с микрососудистыми аномалиями [1, 8]. В российских и европейских рекомендациях по стабильной ИБС предлагается в подобных случаях использовать термин МСС [1, 2, 9], который и употребляется наиболее часто в последнее время, в том числе в клинической практике. Его популяризация, возможно, связана еще и с тем, что у многих из таких пациентов клинические симптомы могут быть, как предполагают эксперты, следствием микрососудистой дисфункции (МСД) коронарного русла, которая чаще всего и описывается в указанных случаях [10-12].
Также предполагается, что МСС может возникать в результате функциональной или структурной дисфункции коронарной микроциркуляции при специфических заболеваниях сердца и сосудов, например, при кардиомиопатии, сочетаться с ИБС на фоне коронарного атеросклероза (рис.1) или при системных заболеваниях, например, в связи с аутоиммунными заболеваниями, коллагеновыми заболеваниями, артериальной гипертонией, и в таких случаях она определяется как вторичная МСС [13-15]. Однако в большинстве случаев MСС развивается вследствие изолированной коронарной МСД, которая является единственным или преобладающим механизмом, ответственным за возникновение эпизодов стенокардии или ишемии миокарда. Такая МСС определяется как первичная [13, 14].
Совсем недавно группа COVADIS предложила диагностические критерии для определения МСС в виде триады признаков [1, 10, 14]:
-
1) боль в груди (стенокардия), в основном при нагрузке (иногда также в состоянии покоя);
-
2) ишемические изменения на электрокардиограмме (ЭКГ) (депрессия сегмента ST) во время нагрузочного теста или других неинвазивных тестов на выявление ишемии миокарда;
-
3) нормальные или малоизмененные коронарные артерии при КАГ.
Не всегда МCС клинически представляет собой стабильную стенокардию, возникающую при напряжении. У некоторых пациентов заболевание может манифестировать в форме острого коронарного синдрома с выраженными и длительными болями в грудной клетке и изменениями реполяризации на ЭКГ, иногда также с повышенными уровнями сывороточных маркеров некроза миокарда, что обусловливает определение этого конкретного состояния как нестабильной (или острой) МCС с развитием инфаркта миокарда (ИМ) [1, 13, 14].
Таким образом, учитывая актуальность проблем, связанных с развитием инфаркта миокарда при микрососудистом поражении коронарных артерий и манифестации острого коронарного синдрома, мы в качестве клинического примера приводим историю болезни пациента 55 лет, проходивший обследование и лечение в отделении неотложной кардиологии Больницы скорой медицинской помощи г. Уфы.
МАТЕРИАЛЫ И МЕТОДЫ
Пациент Е., 55 лет, доставлен 8 февраля 2019 года в приемное отделение больницы скорой медицинской помощи (БСМП) г. Уфы экстренно бригадой СМП с жалобами на давящие боли с локализацией за грудиной и иррадиацией в левую руку, сопровождающиеся смешанной одышкой, возникшие в покое, слабо купирующиеся короткодействующими нитратами и наркотическими анальгетиками, общей резкой слабостью с диагнозом:
Основной: ИБС. Острый крупноочаговый инфаркт миокарда переднеперегородочной стенки левого желудочка от 03.02.2019 г. Рецидив от 08.02.2019 г. ТКАГ 08.02.2019 г.
Осложнения: ХСН I. ФК III.
Из анамнеза известно, что ИБС выявлена впервые, больным себя считает с 03.02.2019 г., когда на фоне относительного благополучия появились давящие загрудинные боли в ночные часы, сопровождавшиеся одышкой, усиливающиеся при физической нагрузке, за медицинской помощью не обращался, самостоятельно лекарства не принимал. Повторный приступ с более интенсивной загрудинной болью зафиксирован 08.02.2019 г., вызвал СМП, доставлен в БСМП с диагнозом: острый коронарный синдром.
Коронарная микроциркуляция
Эпикардиальные коронарные артерии
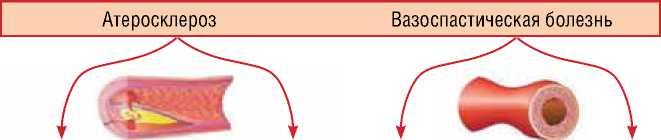
Микроваскулярная дисфункция
Стабильная бляшка
Нестабильная Фокальный / преходящий Стойкий бляшка вазоспазм вазоспазм

I
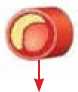
Отрыв бляшки
Восстановление резервного коронарного кровотока
Стенокардия Принцметала
Инфаркт миокарда
Влияние физиологии коронарного кровотока и кровотока миокарда на субъектов с факторами риска

Ишемия потребления ± стенокардия
Тромбоз
Острый коронарный синдром / ИМ
Способствует ишемии миокарда при ИБС и кардиомиопатии
Вызывает тяжелую острую ишемию такоцубо
Эти три механизма могут сочетаться
Коронарная МСД - современные представления
Из анамнеза жизни, пациент курит с 35 лет, индекс курения пациента 10 пачка/лет. Имеет место, отягощенный по сердечно-сосудистым заболеваниям семейный анамнез.
При первичном осмотре кардиолога состояние больного средней степени тяжести, сознание ясное, положение активное, кожные покровы и видимые слизистые физиологического окраски, чистые. Аускультативно над всей поверхностью легочной ткани везикулярное дыхание, хрипов нет. ЧД 18 в минуту. При исследовании сердечно-сосудистой системы тоны сердца ритмичные, приглушены. Перкуторно границы сердца расширены влево +1 см. АД 120/70 мм рт. ст. на обеих руках. ЧСС 70 в минуту, пульс 70 в минуту, удовлетворительных свойств.
Со стороны ЖКТ: живот обычной формы, в акте дыхания участвует, пальпаторно мягкий, безболезненный. Печень, селезенка не увеличена. Больному в экстренном порядке была проведена оценка лабораторных данных, коронароангиогра-фия (КАГ), электрокардиография (ЭКГ), ЭХО-кардиография (ЭХО-КГ) с последующим переводом в отделение неотложной кардиологии (ОНК).
В ОНК больному проводилась терапия антиангинальными препаратами (раствор изокета 0,1% – 10,0 на 200 мл 0,9% физиологического раствора внутривенно капельно под контролем АД), дезагрегантами (аспирин (0,5 гр.) внутрь по % таблетки 1 раз на ночь, брилинта (90 мг) – 2 таблетки 1 раз в сутки, гиполипидемическая терапия (аторвастатин 40 мг) 1 таблетку 1 раз в сутки), гипотензивными препаратами (лизиноприл 10 мг/сутки), антикоагулянтами прямого действия (клексан 0,4 подкожно 2 раза в сутки), бета-адреноблокаторами (метопролол 50 мг ^ таблетки 2 раза в сутки).
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
При обследовании в общем анализе крови выявлено повышение уровня лейкоцитов до 9,5 х 109/л, биохимический скрининг липидов, кардиоспецифических ферментов и общий анализ мочи не выявил отклонений от нормы. Коагулограмма выявила повышение уровня фибриногена до 4,3 г/л, АЧТВ до 35,8 сек., РФМК до 5,5 x 10 '2 г/л.
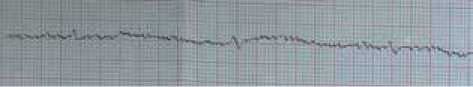
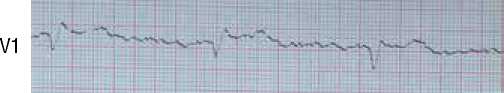
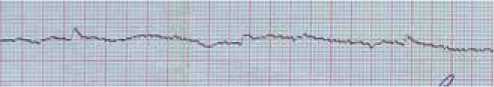
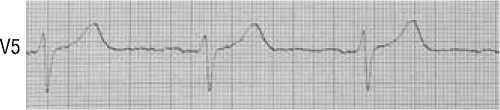
По данным ЭКГ – трансмуральные изменения (рис. 2) передневерхушечной области левого желудочка с подъемом сегмента ST во V1, V2, V5 отведениях и высоким остроконечным зубцом Т в отведениях V3, V4. Незначительное смещение сегмента ST во II, III, AVF отведениях свидетельствует о спазме заднебоковых сегментов коронарных артерии.
При ЭХО-КГ выявлено уплотнение стенок аорты (табл. 1), митральная недостаточность I-II степени с признаками диастолической дисфункции левого желудочка I типа на фоне гипокинеза передне-перегородочной области левого желудочка. В результате проведенной коронарной ангиографии (табл. 2) окклюзионной патологии и гемодинамически значимых стенозов в коронарных артериях не выявлено. Стеноз 11 сегмента левой коронарной артерии не более 10%. Умеренная извитость коронарных артерий.
За время наблюдения в ОНК состояние больного стабилизировалось, признаки коронарной недостаточности купированы, гемодинамика и дыхание стабильны (АД от 120/80 до 110/70 мм.рт.ст., ЧСС от 78 до 58 в мин., ЧД – от 17 до 19 в минуту). Сердечные тоны ритмичны, приглушены. Живот мягкий, безболезнен при пальпации. Диурез без особенностей. Активно жалоб не предъявлял, пациент был выписан с рекомендациями продолжить лечение брилинтой, аспирином, аторвастатином,
I
II

III
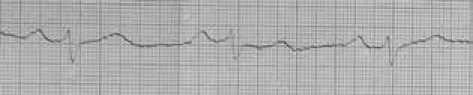
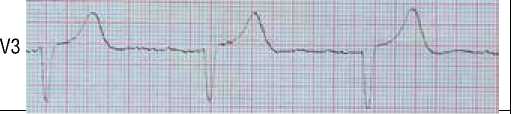
AVR
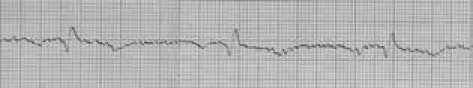
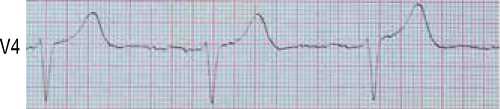
AVL
AVF

Таблица 1. Протокол эхокардиографии (А04.10.002)
|
Аорта основ.(мм) |
32 |
КДРЛЖ (см) |
4,5 |
||
|
Аорта восх. (мм) |
26 |
КСР ЛЖ (см) |
3,4 |
||
|
Раскрытие АК (мм) |
кдо (мл) |
92 |
|||
|
ЛП (мм) |
27 |
ксо (мл) |
49 |
||
|
МЖП (мм) |
10 |
УО (мл) |
43 |
||
|
ЗСЛЖ (мм) |
8 |
ФВ % |
46 |
||
|
ПЖ (мм) |
22 |
||||
|
ПП (мм) |
37 |
AS |
24 |
||
|
ЛА (мм) |
|||||
|
Сократительная функция миокарда ЛЖ: снижена. Сегментарная сократимость миокарда нарушена |
|||||
|
сегменты |
переднеперегородочный |
перегородочный |
передний боковой |
нижний |
задний |
|
базальные |
|||||
|
средние |
гипокинез |
гипокинез |
|||
|
апикальные |
акинез |
гипокинез гипокинез |
|||
|
Показатели |
АК |
МК |
ТК |
ЛК |
|
|
Створки |
|||||
|
Фиброзное кольцо |
|||||
|
S,CM2 |
|||||
|
Пиковый градиент, мм.рт.ст. |
3,8 |
||||
|
Средний градиент, мм.рт.ст. |
|||||
|
Регургитация Площадь ( % ) \ степень (+) |
1-2+ |
1+ |
|||
|
Нижняя полая вена не расширена 15мм, на вдохе спадается более 50%. Жидкость в полости перикарда не обнаружена. Жидкость в плевральной полости не обнаружена. Расчетное систолическое давление в правом желудочке: 21 мм.рт.ст. Признаки диастолической дисфункции ЛЖ выявлены I тип. Уплотнение стенок аорты. |
|||||
Таблица 2. Протокол коронароангиографии (А06.10.006)
После обработки операционного поля под местной анестезией Sol. Novocaini 0,25%-20,0 мл, произведена пункция правой бедренной артерии.
-
1) Коронароангиография:
Диагностическими коронарными катетерами JL 4.0 5F и JR 4.0 5F произведено канюлирование и контрастирование коронарных артерий.
На коронарографии: Тип кровоснабжения - правый.
Из устья ЛКА контрастируются ствол ЛКА, ПМЖА, ОА и их ветви.
Ствол ЛКА диаметром до 3,8 мм с четкими неровными контурами, просвет не изменен. ПМЖА диаметром до 3,0 мм, с четкими неровными контурами, просвет не изменен. Кровоток TIMI III. ОА до 1,8 мм с четкими неровными контурами, стеноз в 11 сегменте не более 10%. Кровоток TIMI III.
Из устья ПКА контрастируются собственно ПКА, СА, КА, ВОК, ЗБА и ЗМЖА. Диаметр артерии до 3,2 мм, с четкими неровными контурами, просвет не изменен. Кровоток TIMI III.
Заключение : Окклюзионной патологии и гемодинамически значимых стенозов в коронарных артериях не выявлено. Стенозы коронарных артерий не более 10%. Умеренная извитость коронарных артерий.
бета-блокаторами, ингибиторами АПФ по тем же схемам с дальнейшим наблюдением у кардиолога по месту жительства, с контролем лабораторно-инструментальных показателей, ограничением физической активности, соблюдением диеты.
Результаты представленного наблюдения за пациентом ИМ с МСС на фоне непораженных крупных коронарных артерий показали, что при рецидиве острого коронарного синдрома выраженными длительными загрудинными болями с иррадиацией в левую руку, сопровождающиеся смешанной одышкой, возникшие в покое, слабо купирующиеся короткодействующими нитратами и наркотическими анальгетиками, сопряжено с характерными крупноочаговыми изменениями на ЭКГ, но без повышенных уровней сывороточных маркеров некроза миокарда. Следует отметить, что, хотя коронарные артерии остаются «чистыми», с клинической точки зрения самочувствие пациентов из-за болевого синдрома является неудовлетворительным, а качество жизни низким [1].
По результатам 20-летнего наблюдения, проведенного в Дании и включавшего 17 435 больных с неизмененными коронарными артериями и с необструктивным диффузным поражением коронарных артерий со стенокардией, в этих группах было выявлено 52 и 85% повышение риска крупных сердечно-сосудистых событий (сердечно-сосудистая смертность, госпитализация по поводу ИМ, сердечной недостаточности, инсульта) соответственно и 29 и 52% повышение риска общей смертности соответственно без существенных различий по половому признаку [16]. Ухудшение сердечной функции в исследованиях описывалось довольно редко [17].
Вместе с тем в последнее время МСС уже не рассматривается как абсолютно доброкачественное состояние. Было установлено, что частота сердечно-сосудистых событий близка или даже сопоставима с прогнозом при обструктивных изменениях коронарного русла. В одном из исследований в группе пациентов с МСС и исходной ПЗВД плечевой артерии <4,7% был отмечен достоверно более высокий риск сердечно-сосудистых осложнений в сравнении с группой с ПЗВД >4,7% (p<0,05) на протяжении 9–18 лет наблюдения [18].
Учитывая актуальность этой проблемы, необходимо отметить, что в последние годы необструктивной ИБС уделяется всё больше внимания, и для практического кардиолога важно уметь распознать и правильно квалифицировать таких пациентов, даже в отсутствие стенозирующих просвет коронарных артерий атером, и проводить лечение на основе имеющихся симптомов [1].
ВЫВОДЫ
В представленном клиническом случае был описан пример развития ИМ при микрососудистом поражения коронарных артерий у больного манифестацией острого коронарного синдрома с выраженными длительными загрудинными болями и изменениями реполяризации на ЭКГ, а также без повышенных уровней сывороточных маркеров некроза миокарда, что, вероятно, обусловливает определение этого состояния как нестабильной (или острой) микрососудистой дисфункции с развитием инфаркта миокарда.
В развитии заболевания могут принимать участие самые разные патофизиологические механизмы. Новые данные способствовали улучшению понимания дисфункции коронарных сосудов и результирующей ишемии миокарда, которые характеризуют МСД у пациентов с МСС. Несмотря на то, что ряд препаратов, включая антиангинальные, могут облегчать симптомы, у многих пациентов сохраняется клиническая симптоматика, плохое качество жизни, и лечение остается сложной задачей. Прогноз у больных с МСС, по последним данным, не такой благоприятный, как считалось ранее, что делает актуальным поиск новых методов диагностики и лечения.
Список литературы Клинический случай развития острого инфаркта миокарда при микрососудистой стенокардии
- Карпов Ю.А., Соболева Г.Н., Ерпылова Е.А. 2018. Микрососудистая стенокардия: вопросы диагностики и лечения 2019 г.: научный обзор. Атмосфера. Новости кардиологии, 4(4), 16-27.
- Montalescot, G., Sechtem, U., Achenbach, S. 2013. 2013 ESC guidelines on the management of stable coronary artery disease: the task force on the management of stable coronary artery disease of the European Society of Cardiology. European Heart Journal, 34(38): 2949-3003.
- Humphries, K.H., Pu, A., Gao, M., Carere, R.G., Pilote, L. 2008. Angina with "normal" coronary arteries: sex differences in outcomes. American Heart Journal, 155(2): 375-381.
- Ouellette, M., Löffler, A.I., Beller, G.A., Workman, V.K., Holland, E., Bourque, J.M. 2018. Clinical characteristics, sex differences, and outcomes in patients with normal or near normal coronary arteries, non-obstructive or obstructive coronary artery disease. Journal of American Heart Association, 7(10): 1-13.
- Proudfit, W.L., Shirey, E.K., Sones, F.M.Jr. 1966. Selective cine coronary arteriography. Correlation with clinical findings in 1,000 patients. Circulation, 33(6): 901-910.
- Sandler, K.M., McNaughton, C.D., Presley, M.A., Williams, J.R. 2015. Incidence and management of mild coronary atherosclerotic disease diagnosed with coronary CTA in the emergency department. Emergency Medicine (Los Angeles), 5(6): 283.
- Kemp, H.G., Kronmal, R.A., Vliestra, R.E., Frye, R.L. 1986. Seven-year survival of patients with normal or near normal coronary arteriograms. A CASS registry study. Journal of the American College of Cardiology, 7: 479-483.
- Cannon, R.O., Epstein, S.E. 1988. ‘Microvascular angina' as a cause of chest pain with angiographically normal coronary arteries. The American Journal of Cardiology, 61(15): 1338-1343.
- Клинические рекомендации. Стабильная ишемическая болезнь сердца. 2016. http://cr.rosminzdrav.ru/#!/schema/.
- Lanza, G.A., De Vita, A., Kaski, J.C. 2018. "Primary" microvascular angina: clinical characteristics, pathogenesis and management. Journal of Interventional Cardiology, 13(3): 108-11.
- Crea, F., Camici, P.G., Bairey Merz, C.N. 2014. Coronary microvascular dysfunction: an update. European Heart Journal, 35(17): 1101-1111.
- Сергиенко В.Б., Саютина Е.В., Самойленко Л.Е., Самко А.Н., Першуков И.В., Левицкий И.В., Соболева Г.Н., Карпов Ю.А. 1999. Роль дисфункции эндотелия в развитии ишемии миокарда у больных ишемической болезнью сердца с неизмененными и малоизмененными коронарными артериями. Кардиология, 39(1): 25-30.
- Lanza, G.A., Crea, F. 2010. Primary coronary microvascular dysfunction clinical presentation, pathophysiology, and management. Circulation, 121(21): 2317-2325.
- Villano, A., Lanza, G.A., Crea, F. 2018. Microvascular angina: prevalence, pathophysiology and therapy. Journal of Cardiovascular Medicine (Hagerstown, Md), 19(Suppl 1): e36-9.
- Camici, P.G., Crea, F. 2007. Coronary microvascular dysfunction. The New England Journal of Medicine, 356(8): 830-840.
- Jespersen, L., Hvelplund, A., Abildstrøm, S.Z., Pedersen, F., Galatius, S., Madsen, J.K., Jørgensen, E., Kelbæk, H., Prescott, E. 2012. Stable angina pectoris with no obstructive coronary artery disease is associated with increased risks of major adverse cardiovascular events. European Heart Journal, 33(6): 734-744.
- Kaski, J.C., Elliott, P.M. 1995. Angina pectoris and normal coronary arteriograms: clinical presentation and hemodynamic characteristics. The American Journal of Cardiology, 76(13): 35D-42D.
- Соболева Г.Н., Федулов В.К., Самко А.Н., Левицкий И.В., Рогоза А.Н., Балахонова Т.В., Карпов Ю.А. 2017. Прогностическое значение дисфункции эндотелия коронарных и плечевой артерии, традиционных факторов риска в развитии сердечно-сосудистых осложнений у пациентов с микрососудистой стенокардией. Российский кардиологический журнал, 22(3):54-58.


