Клинический случай успешного одномоментного чрескожного коронарного вмешательства и эндоваскулярной пластики митрального клапана "край-в-край" устройством Mitraclip G4
Автор: Алекян Б.Г., Карапетян Н.Г., Саидова М.А., Кадырова М.В., Григорян М.В., Мелешенко Н.Н., Гелецян Л.Г., Титов Н.С.
Журнал: Сибирский журнал клинической и экспериментальной медицины @cardiotomsk
Рубрика: Клинические случаи
Статья в выпуске: 2 т.37, 2022 года.
Бесплатный доступ
Митральная регургитация (МР) занимает одно из лидирующих мест среди клапанных пороков у взрослого населения. Приблизительно у половины пациентов этиология данного порока напрямую связана с обструктивным поражением коронарных артерий. Как правило, высокий периоперационный риск у таких пациентов является основной причиной отказа в выполнении традиционных открытых вмешательств. На основании данных доступной литературы представлен первый опыт успешного одномоментного чрескожного коронарного вмешательства (ЧКВ) и транскатетерной пластики митрального клапана «край-в-край» устройством MitraClip G4 у 77-летнего пациента с тяжелой МР, который ранее перенес инфаркт миокарда и пароксизмальную форму фибрилляции предсердий. Продемонстрированы преимущества подобного подхода к лечению и актуализирована необходимость его дальнейшего изучения для системного внедрения.
Митральная регургитация, mitraclip, стентирование
Короткий адрес: https://sciup.org/149140490
IDR: 149140490 | УДК: 616.126-089 | DOI: 10.29001/2073-8552-2022-37-2-112-117
A clinical case of successful simultaneous percutaneous coronary intervention and endovascular mitral valve repair “edge-to-edge” with the Mitraclip G4 device
Mitral regurgitation is one of the prevalent entities among valvular defects in the adult population. In approximately half of the patients, the etiology of this defect is directly related to obstructive coronary artery disease. As a rule, the high perioperative risk in such patients is the main reason for the refusal to perform traditional open interventions. According to the available literature, the first experience of successful simultaneous percutaneous coronary intervention and transcatheter mitral valve repair “edge-to-edge” with the MitraClip G4 device is presented in a 77-year-old patient with severe mitral regurgitation who had previously suffered myocardial infarction and paroxysmal atrial fibrillation. The advantages of such an approach to treatment are demonstrated, and the need for its further study for systemic implementation is actualized.
Текст научной статьи Клинический случай успешного одномоментного чрескожного коронарного вмешательства и эндоваскулярной пластики митрального клапана "край-в-край" устройством Mitraclip G4
В зависимости от причины возникновения митральной регургитации (МР) выделяют две ее формы – первичную и вторичную. Первичная форма, также именуемая органической, обусловлена структурной патологией клапанного аппарата. Причиной возникновения вторичной, или функциональной, формы является дисфункция левого желудочка (ЛЖ), чаще всего развивающаяся при ишемической болезни сердца (ИБС) и ее осложнениях, а также различных формах кардиомиопатий и более редких состояниях, таких как, например, апикальный пейсинг правого желудочка [1].
МР является одним из самых распространенных приобретенных пороков сердца. Из 5219 пациентов, включенных в крупное проспективное мультицентровое исследование Valvular Heart Disease Survey II, изучавшее применение на практике рекомендаций по ведению пациентов с тяжелыми клапанными пороками, МР имела место у 1114 пациентов, что составило 21,3%. Таким образом, по частоте встречаемости в европейской популяции она занимает 2-е место после аортального стеноза. Вторичная форма МР обнаружена у 368 пациентов, среди которых ишемический генез был у 190 (51,6%), неишемический – у 178 (48,4%) пациентов [2].
На основании данных 63463 эхокардиографических (ЭхоКГ) исследований авторы европейского регистра EuMiClip выявили МР любой степени у 15 501 пациента. На долю умеренной и тяжелой степени МР пришлось 3309 пациентов, среди которых 1010 (30,1%) имели вторичную форму. Кроме того, в 51,4% случаев вторичной формы МР в качестве этиологии был выявлен именно ишемический фактор [3].
Хотя открытые операции остаются золотым стандартом в коррекции тяжелой МР, около половины кандидатов получали отказ из-за высокого хирургического риска [5]. По данным того же исследования Valvular Heart Disease Survey II, пациенты со вторичной формой МР по показателям индекса коморбидности Чарльсон сравнимы только с группой аортального стеноза и имеют наиболее высокие показатели шкалы риска хирургических вмешательств Euroscore II по сравнению с другими изолированными приобретенными пороками сердца [2].
Как было показано выше, ИБС нередко выступает в качестве этиологического фактора МР. Следовательно, данная категория пациентов требует коррекции как МР, так и ИБС.
Согласно рекомендациям Европейского общества кардиологов (ЕОК) по реваскуляризации миокарда (2018 г.), пациентам, у которых имеются показания к выполнению как коронарного шунтирования (КШ), так и открытой операции на митральном клапане, оба вмешательства должны быть выполнены одномоментно (класс рекомендаций I, уровень доказательности С). Данные рекомендации касаются пациентов с тяжелой степенью как первичной, так и вторичной МР [4].
Обращаясь к рекомендациям ЕОК по клапанным заболеваниями сердца (2021 г.), можно обнаружить, что для пациентов, которые признаны консилиумом «сердечной команды» не подходящими для выполнения симультанного КШ и открытого вмешательства на клапане, следует рассмотреть чрескожное коронарное вмешательство (ЧКВ) с последующим выполнением транскатетерной коррекции «край-в-край» в случае сохранения тяжелой степени вторичной МР (IIa класс рекомендаций и уровень доказательности B) [6].
Тем не менее, несмотря на большое количество выполняемых в мире ежегодно операций транскатетерной коррекции «край-в-край», при анализе доступной литературы мы обнаружили крайне малое количество исследований и клинических случаев одномоментного транскатетерного лечения ИБС и МР. Одним из наиболее крупных исследований является работа K. Giffit и соавт. Авторы данного ретроспективного исследования изучили более 2500 пациентов, которым была выполнена эндоваскулярная коррекция МР устройством MitraClip. Приблизительно две трети из них имели сопутствующую ИБС, что было ассоциировано с более высокой частотой внутрибольничного инфаркта миокарда. При субанализе подгруппы из 40 пациентов, которым в ту же госпитализацию выполнено ЧКВ, по сравнению с пациентами, подвергшимися только установке MitraClip, были выше внутрибольничная смертность от всех причин (2,5 против 2,0%, p < 0,01), срок госпитализации (21,5 против 5,1 койко-дней), острое почечное повреждение (55 против 13,7%, p < 0,01) и инсульт (10 против 0,6%, p < 0,01) [7].
Другое ретроспективное исследование J. Shamekhi и соавт., оценивавшее коронарный статус у 444 пациентов с запланированной эндоваскулярной коррекцией МР и, при необходимости, ЧКВ, показало, что тяжесть остаточного поражения коронарных артерий у пациентов, перенесших ЧКВ и имплантацию MitraClip, была независимым предиктором смертности от всех причин. Летальность в течение года после вмешательств у пациентов, чей резидуальный SYNTAX Score был больше 0, составила 31,4 против 9,9% в группе пациентов, у которых резидуальный SYNTAX Score был равен 0. Стоит отметить, что пациенты, получившие полную реваскуляризацию миокарда, имели наиболее благоприятные результаты независимо от этиологии МР [8].
Хотя к этим противоречивым данным и следует относиться с осторожностью, учитывая многочисленные ограничения ретроспективного подхода, они подтверждают распространенность ИБС у пациентов с МР и указывают на необходимость проспективных рандомизированных исследований для выработки надежного подхода к таким пациентам. Кроме того, в вышеперечисленных работах рассматривались пациенты только с этапными вмешательствами на митральном клапане и коронарных артериях.
На момент написания данной статьи в доступной нам литературе мы не обнаружили ни одного случая симультанного транскатетерного вмешательства на коронарных артериях и митральном клапане.
Клинический случай
Цель данной публикации: представить клинический случай успешного одномоментного ЧКВ и эндоваскулярной пластики митрального клапана «край-в-край» с помощью устройства MitraClip G4.
Пациент 77 лет, мужчина, некурящий, с длительным коронарным анамнезом: 21 год назад был выставлен диагноз «постинфарктный кардиосклероз». Коронарография впервые была проведена 19 лет назад, по данным которой уже было выявлено многососудистое поражение, однако реваскуляризация миокарда не была осуществлена. Была подобрана консервативная терапия с положительным эффектом. За 2 мес. до госпитализации в наш Центр пациент без клиники предшествующей стенокардии был госпитализирован с диагнозом «острый коронарный синдром без подъема сегмента ST» в одну из больниц г. Москвы, где выполнена коронарография. У пациента был выявлен правый тип кровоснабжения миокарда, стеноз 90% в средней трети промежуточной ветви (ПВ), окклюзия огибающей ветви (ОВ) в дистальной трети, стеноз 85% средней трети правой коронарной артерии (ПКА). Последняя расценена как инфаркт-связанная артерия, выполнено ее стентирование в той же клинике. Кроме того, при дообследовании выявлена МР тяжелой степени (площадь поперечного сечения струи (EROA) = 0,61 см2, объем МР (RVol) = 85 мл, фракция регургитации (RF) = 67%) и пароксизм фибрилляции предсердий неизвестной давности (рис. 1, 2).
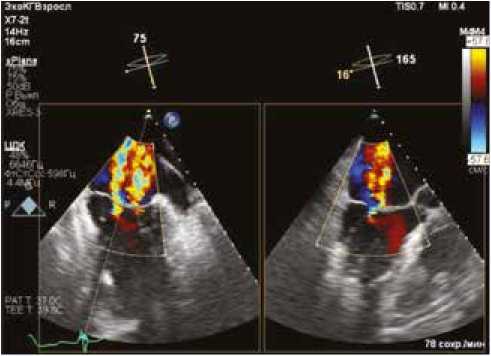
Рис. 1. Первичная чреспищеводная эхокардиография (ЧПЭхоКГ).
Определяется тяжелая МР (2 струи, центральные, ширина наибольшей – 4,8 мм)
Fig. 1. Primary transesophageal echocardiogram. Severe MR is detected (two jets, central, the width of the largest 4.8 mm)
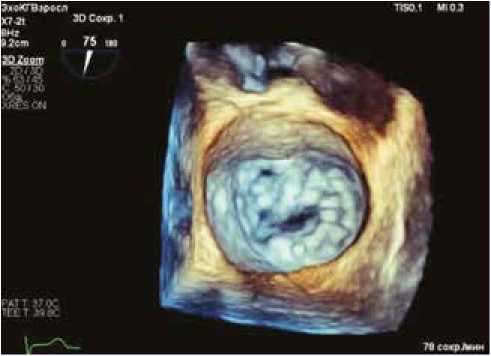
Рис. 2. 3D-реконструкция при первичной ЧПЭхоКГ. Отмечаются дегенеративные изменения створок митрального клапана с пролабированием сегмента А2
Fig. 2. 3D-reconstruction during primary transesophageal echocardiogram. Degenerative changes of the mitral valve flaps with prolapse of the A2 segment are detected
Для выполнения полной реваскуляризации миокарда и определения тактики лечения клапанного порока пациент был переведен в наш Центр, где обсужден на консилиуме «сердечной команды». Ввиду высокого риска сочетанного вмешательства в объеме КШ и пластики митрального клапана (7,18% по шкале Euroscore II) принято решение выполнить эндоваскулярное вмешательство: чрескожное вмешательство (ЧКВ) крупной промежуточной артерии и пластику митрального клапана по типу «край-в-край» устройством MitraClip G4. Учитывая техническую возможность проведения вмешательств в рамках одного анестезиологического пособия, а также потенциальные преимущества данного подхода в виде уменьшения срока госпитализации и, следовательно, снижения также и финансовых затрат, риска внутрибольничной инфекции, решено выполнить симультанную операцию.
Пациенту подобрана тройная антитромботическая терапия в соответствии с рекомендациями ЕОК по ведению пациентов с фибрилляций предсердий. Она включала в себя апиксабан (2,5 мг дважды в день), клопидогрел (75 мг один раз в день) и ацетилсалициловую кислоту (75 мг один раз в день).
Под эндотрахеальным наркозом трансрадиальным артериальным доступом справа пациенту первым этапом выполнено прямое стентирование средней трети промежуточной ветви. Имплантирован стент с лекарственным покрытием Xience Alpine 2,5 х 18 мм (Abbott Laboratories, Chicago, IL, USA) (рис. 3, 4).
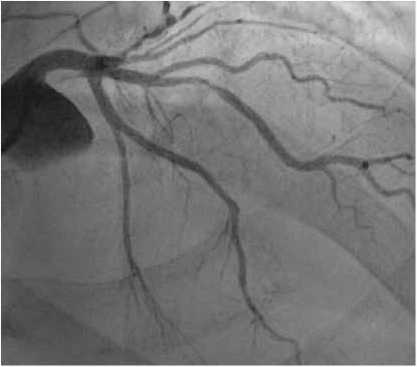
Рис. 3. Коронарограмма бассейна левой коронарной артерии. Визуализируется стеноз 90% в средней трети крупной промежуточной ветви (указано стрелками)
Fig. 3. Coronary angiogram of the left coronary artery. 90% stenosis is visualized in the middle third of a large intermediate branch (indicated by arrows)
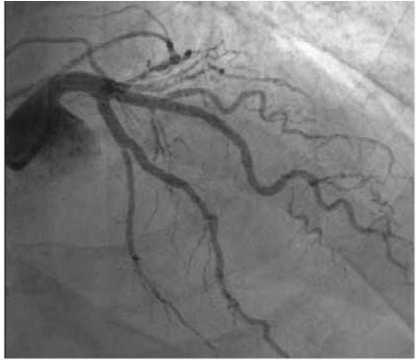
Рис. 4. После ЧКВ средней трети промежуточной ветви.
Проходимость артерии восстановлена (указано стрелками)
Fig. 4. Coronary angiogram obtained after PCI of the middle third of the intermediate branch. Patency of the artery has been restored (indicated by arrows)
Далее выполнена пункция правой общей бедренной вены, установлен интродьюсер 8F, введена система Perclose ProGlide (Abbott Vascular, Abbott Park, IL, USA), выполнен предварительный сосудистый шов. С помощью интродьюсера для пункции межпредсердной перегородки, проведенного в правое предсердие, в овальной ямке выполнена трансептальная пункция на расстоянии 4,5 см от фиброзного кольца митрального клапана под контролем ЧПЭхоКГ. Далее в полость левого предсердия через ранее установленный гайд-катетер Steerable Guide Catheter 24F проведена доставляющая система MitraClip G4 XTW (Abbott, Menlo Park, CA, USA), наложена клипса на сегменты A2 и P2 створок МК. Однако при контрольном ЧПЭхоКГ отмечается остаточная МР среднетяжелой степени, ввиду чего принято решение о проведении и имплантации дополнительной клипсы. Аналогичным образом доставляющая система клипсы MitraClip G4 NTW (Abbott, Menlo Park, CA, USA) проведена в проекции коаптации створок митрального клапана, выполнен захват и клипирование створок в центральных сегментах. При контрольной ЧПЭхоКГ – отмечается положительная динамика в виде уменьшения степени МР до 1-й степени. Операция завершена без осложнений.
Первые сутки пациент наблюдался в отделении реанимации и интенсивной терапии. На вторые сутки переведен в общую палату профильного отделения, послеоперационный период протекал без особенностей.
При контрольном ЧПЭхоКГ через 5 дней установлено, что положение клипс оптимальное, регургитация на митральном клапане умеренной степени. Данных за стенозирование левого атриовентрикулярного отверстия не получено. Регургитация на трикуспидальном клапане 1-2-й ст. Отмечается лево-правый сброс на межпредсердной перегородке 2-3 мм. Пациент выписан в удовлетворительном состоянии на 12-е сут после вмешательства (рис. 5, 6).
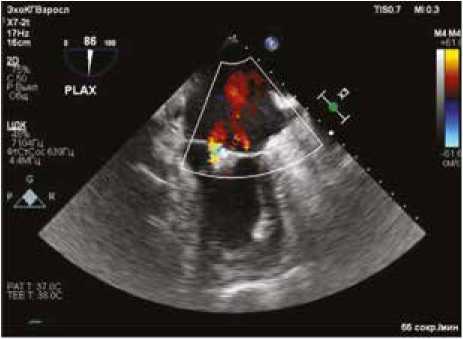
Рис. 5. Контрольная ЧПЭхоКГ. Определяется умеренная МР, две струи Fig. 5. Preforming transesophageal echocardiogram after the clipping. A moderate MR is determined, two jets
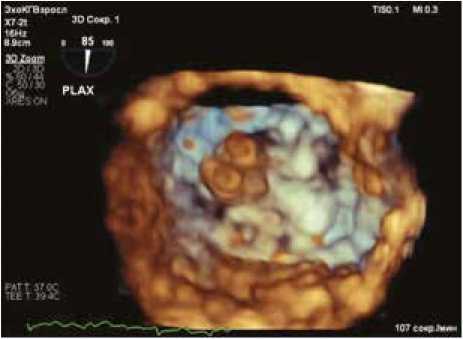
Рис. 6. 3D-реконструкция изображения при контрольной ЧПЭхоКГ.
Визуализируется 2 клипсы на уровне сегментов A2, P2
Fig. 6. 3D reconstruction of the transesophageal echocardiogram. Two clips are visualized at the level of segments A2, P2
Обсуждение
Необходимость реваскуляризации миокарда при ишемической форме МР имеет патогенетическое обоснование. Причина МР при ишемии миокарда кроется в дисбалансе между натяжением хорд и смыканием створок клапана из-за смещения папиллярных мышц. Это прямое следствие ремоделирования миокарда. В результате исходное положение створок и точка коаптации становится более апикальным, что ограничивает их движение в систолу, препятствуя полному смыканию. Наряду с этим присутствует и вносит вклад снижение сократимости и диссинхрония миокарда, дилатация фиброзного кольца, которая только усиливается по мере нарастания МР за счет дилатации ЛЖ [9, 10].
Существуют исследования, согласно которым коррекция МР при ее ишемической форме, совместно с реваскуляризацией миокарда, оправдана [11, 12].
Так, при субанализе результатов исследования STICH было показано преимущество в выживаемости у группы пациентов, которым была выполнена пластика митрального клапана с КШ по сравнению с группой, подвергшейся только реваскуляризации миокарда [11]. Исследование RIME показало, что даже пациентам со средней степенью МР аннулопластика, выполненная с КШ, может снизить уровни гормона BNP, улучшить функциональный класс хронической сердечной недостаточности и обратное ремоделирование ЛЖ, то есть ключевой аспект патогенеза ишемической МР, по сравнению с одним только КШ [12].
Заключение
Данный случай отражает возможность одномоментного эффективного проведения эндоваскулярной рева- скуляризации миокарда и пластики митрального клапана у пациента, которому в выполнении КШ и пластики митрального клапана отказано в силу высокого хирургического риска.
Транскатетерные технологии позволяют оказать помощь большому числу пациентов высокого хирургического риска по сравнению с традиционными открытыми операциями за счет своей малой травматичности. Это крайне важно в связи с мировой тенденцией к старению населения и, следовательно, росту числа коморбидных пациентов с высоким хирургическим риском, который является главной причиной отказа в проведении оперативных вмешательств.
Технология MitraClip была специально разработана для пациентов со вторичной МР и хотя одобрена FDA только в 2013 г., уже выдержала испытание крупными рандомизированными исследованиями [13]. Несмотря на то, что данная технология в Российской Федерации начала входить в клиническую практику только в 2021 г., уже есть результаты первого отечественного исследования [14].
Совмещение этих двух вмешательств потенциально может снизить риск осложнений каждой операции по отдельности, так как все происходит в рамках одного анестезиологического пособия, и, соответственно, уменьшить ожидаемый срок госпитализации для пациентов с ИБС и ишемической МР.
Для получения достоверных доказательств эффективности и включения такого подхода в рекомендации необходимы масштабные рандомизированные контролируемые исследования, однако единичные случаи будут первым шагом на пути к этому.
Список литературы Клинический случай успешного одномоментного чрескожного коронарного вмешательства и эндоваскулярной пластики митрального клапана "край-в-край" устройством Mitraclip G4
- Wong D.T., Leong D.P., Khurana S., Puri R., Tayeb H., Sanders P. Severe mitral regurgitation due to right ventricular apical pacing. BMJ Case Rep. 2010;2010:bcr1220092524. https://doi.org/10.1136/bcr.12.2009.2524.
- Iung B., Delgado V., Rosenhek R., Price S., Prendergast B., Wendler O. et al. Contemporary presentation and management of valvular heart disease: The EURObservational Research Programme Valvular Heart Disease II Survey. Circulation. 2019;140(14):1156-1169. https://doi.org/10.1161/CIRCULATIONAHA.119.041080.
- Monteagudo Ruiz J.M., Galderisi M., Buonauro A., Badano L., Aruta P., Swaans M.J. et al. Overview of mitral regurgitation in Europe: Results from the European Registry of mitral regurgitation (EuMiClip). Eur. Heart J. Cardiovasc. Imaging. 2018;19(5):503-507. https://doi.org/10.1093/ehjci/jey011.
- Neumann F.J., Sousa-Uva M., Ahlsson A., Alfonso F., Banning A.P., Benedetto U. et al. 2018 ESC/EACTS Guidelines on myocardial revascularization. Eur. Heart J. 2019;40(2):87-165. https://doi.org/10.1093/eurheartj/ehy394.
- Russo G., Maisano F., Massaro G., Terlizzese G., Mariano E., Bonanni M. et al. Challenges and open issues in transcatheter mitral valve implantation: Smooth seas do not make skillful sailors. Front. Cardiovasc. Med. 2022;8:738756. https://doi.org/10.3389/fcvm.2021.738756.
- Vahanian A., Beyersdorf F., Praz F., Milojevic M., Baldus S., Bauersachs J. et al. 2021 ESC/EACTS Guidelines for the management of valvular heart disease: Developed by the Task Force for the management of valvular heart disease of the European Society of Cardiology (ESC) and the European Association for Cardio-Thoracic Surgery (EACTS). Eur. Heart J. 2022;43(70):561-632. https://doi.org/10.1093/eurheartj/ehab395.
- Gifft K., Omran J., Ghrair F., Allaham H., Eniezat M., Abdullah O. et al. Impact of preexisting coronary arterial disease in patients undergoing percutaneous mitral valve repair (MitraClip). Catheter. Cardiovasc. Interv. 2021;97(5):919-924. https://doi.org/10.1002/ccd.29404.
- Shamekhi J., Weber M., Sugiura A., Öztürk C., Treede H., Grube E. et al. Impact of сoronary аrtery disease on outcomes in patients undergoing percutaneous edge-to-edge repair. JACC Cardiovasc. Interv. 2020;13(18):2137-2145. https://doi.org/10.1016/j.jcin.2020.05.031.
- Varma P.K., Krishna N., Jose R.L., Madkaiker A.N. Ischemic mitral regurgitation. Ann. Card. Anaesth. 2017;20(4):432-439. https://doi.org/10.4103/aca.ACA_58_17.
- Castleberry A.W., Williams J.B., Daneshmand M.A., Honeycutt E., Shaw L.K., Samad Z. et al. Surgical revascularization is associated with maximal survival in patients with ischemic mitral regurgitation: A 20-year experience. Circulation. 2014;129(24):2547-2556. https://doi.org/10.1161/CIRCULATIONAHA.113.005223.
- Deja M.A., Grayburn P.A., Sun B., Rao V., She L., Krejca M. et al. Influence of mitral regurgitation repair on survival in the surgical treatment for ischemic heart failure trial. Circulation. 2012;125(21):2639-2648. https://doi.org/10.1161/CIRCULATIONAHA.111.072256.
- Chan K.M., Punjabi P.P., Flather M., Wage R., Symmonds K., Roussin I. et al. Coronary artery bypass surgery with or without mitral valve annuloplasty in moderate functional ischemic mitral regurgitation: Final results of the Randomized Ischemic Mitral Evaluation (RIME) trial. Circulation. 2012;126(21):2502-2510. https://doi.org/10.1161/CIRCULATIONAHA.112.143818.
- Stone G.W., Lindenfeld J., Abraham W.T., Kar S., Lim D.S., Mishell J.M. et al. Transcatheter mitral-valve repair in patients with heart failure. N. Engl. J. Med. 2018;379(24):2307-2318. https://doi.org/10.1056/NEJMoa1806640.
- Имаев Т.Э., Комлев А.Е., Кучин И.В., Саидова М.А., Колегаев А.С., Макеев М.И. и др. Транскатетерная пластика митрального клапана по методу “край-в-край” у больных с митральной регургитацией тяжелой степени (результаты исследования “MitraClip Russia”). Российский кардиологический журнал. 2022;27(2):4689. https://doi.org/10.15829/1560-4071-2022-4689.


