Клиническое наблюдение лечения рака желудка с метастатическим поражением брюшины с применением внутрибрюшного введения доцетаксела под давлением
Автор: Климин С.А., Гамаюнов С.В., Петрякова Ю.А., Гагаев Р.А., Загайнов В.Е., Киселев Н.М.
Журнал: Ульяновский медико-биологический журнал @medbio-ulsu
Статья в выпуске: 4, 2025 года.
Бесплатный доступ
Перитонеальная диссеминация является одним из наиболее частых вариантов метастазирования при распространенном раке желудка, прогноз при котором в настоящее время остается плохим. Улучшение результатов лечения у тщательно отобранной группы больных возможно при использовании комбинации системной терапии и локальных методик. В публикации приведен клинический пример лечения диссеминированного по брюшине рака желудка комбинацией системной трехкомпонентной химиотерапии и внутрибрюшной аэрозольной химиотерапии под давлением с использованием доцетаксела. Цель. Изучение результатов лечения метастатического рака желудка с диссеминацией по брюшине с применением внутрибрюшного введения доцетаксела под давлением на примере клинического наблюдения. Материалы и методы. Проводилась оценка переносимости, эффективности и безопасности применяемого метода лечения, патоморфологического ответа очагов по брюшине, первичной опухоли, а также качества жизни в процессе лечения и период наблюдения после него. Примером послужил клинический случай лечения рака желудка IV стадии, cT4aN1M1 (Cy+, per+ PCI 5) по схеме FLOT 3 курса + (mFLOT 3 курса + dPIPAC). Результаты. Был продемонстрирован пример успешного применения доцетаксела методом внутрибрюшного аэрозольного введения под давлением в составе курсов системного лечения в первой линии химиотерапии. После достижения полного патоморфологического регресса перитонеальных метастазов рака желудка с помощью системной и внутрибрюшной химиотерапии под давлением оперативное лечение не привело к развитию хирургических осложнений и ухудшению качества жизни в течение 1 года наблюдения. Выводы. С учетом ограниченного арсенала лечения больных раком желудка с перитонеальной диссеминацией предлагаемый способ может стать одним из вариантов терапии.
Рак желудка, перитонеальные метастазы, внутрибрюшная химиотерапия, PIPAC, ВАХД, химиотерапия
Короткий адрес: https://sciup.org/14134211
IDR: 14134211 | УДК: 616.33-006.6:616.381-033.2-085 | DOI: 10.34014/2227-1848-2025-4-55-66
Clinical observation of treating gastric cancer with peritoneal metastases: Pressurized intraperitoneal docetaxel administration
Peritoneal dissemination is one of the most frequent metastatic pattern of advanced gastric cancer. Currently, its prognosis remains poor. It is possible to improve treatment outcomes in a carefully selected group of patients through a combination of systemic and local therapies. This publication presents a clinical case of peritoneal disseminated gastric cancer treatment using a combination of systemic triple chemotherapy and pressurized intraperitoneal aerosol chemotherapy with docetaxel. Objective. The aim of the article is to study the treatment outcomes for metastatic gastric cancer with peritoneal dissemination using pressurized intraperitoneal docetaxel injection (clinical case study). Materials and Methods. We assessed the tolerability, efficacy, and safety of the treatment method used, the pathological response of peritoneal lesions, the primary tumor, and quality of life during treatment and the follow-up period. The example was a clinical case of stage IV gastric cancer treatment, cT4aN1M1 (Cy+, per+ PCI 5) using the FLOT regimen (3 cycles) + (mFLOT (3 cycles) + dPIPAC) regimen. Results. The study demonstrates successful application of docetaxel via pressurized intraperitoneal aerosol administration as part of systemic treatment in first-line chemotherapy. After achieving complete pathomorphological regression of gastric cancer peritoneal metastases using systemic chemotherapy and pressurized intraperitoneal chemotherapy, surgical treatment resulted in no surgical complications or deterioration in quality of life during a 1-year follow-up period Conclusion. Given the limited treatment options for patients with gastric cancer and peritoneal dissemination, the proposed method may become a viable therapeutic option.
Текст научной статьи Клиническое наблюдение лечения рака желудка с метастатическим поражением брюшины с применением внутрибрюшного введения доцетаксела под давлением
Объективизацию результатов применения тех или иных методов лечения обеспечивает как цитологический, так и гистологический контроль. С целью оценки лечебного па-томорфоза опухоли в очагах по брюшине используется система Peritoneal Regression
Grading Score (PRGS), а в первичной опухоли – шкала Mandard с оценкой Tumor Regression Grade (TRG) [12, 13].
Материалы и методы. Проводилась оценка переносимости, эффективности и безопасности применяемого метода лечения, па-томорфологического ответа очагов по брюшине, первичной опухоли, а также качества жизни в процессе лечения и период наблюдения после него.
Примером послужил клинический случай.
Fig. 1. Pre-treatment computed tomography scan. Gastric body tumor with metastatic paragastric lymphadenopathy
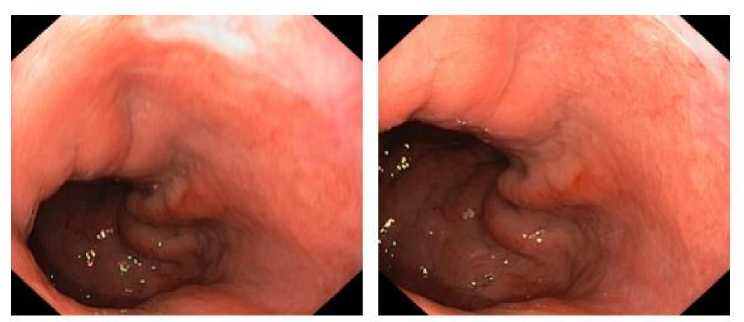
Рис. 2. ЭФГДС до начала лечения. Тип III по Borrmann
Fig. 2. Pre-treatment esophagogastroduodenoscopy (EGD). Borrmann Type III
Перед началом лечения был оценен объективный статус: шкала оценки тяжести состояния пациента по версии ВОЗ (ECOG) – 0, шкала Американского общества анестезиологов (ASA) – I, шкала Московского научного общества анестезиологов-реаниматологов (МНОАР) – I степень, шкала скрининга нутритивного риска (NRS-2002) – 1 балл. С учетом клинической стадии заболевания первым этапом пациенту проведена диагностическая лапароскопия, при выполнении которой выявлена и верифицирована перитонеальная диссеминация с индексом 5 по Sugarbaker (PCI 5), метастазы по брюшине подтверждены гистологически (per+), цитологически – положительный перитонеальный лаваж (Cy+) (рис. 3–5), в связи с чем произведена конверсия диагноза на T4aN1M1 (Cy+, per+, PCI 5), stage IV. Индекс спаечного процесса по Coccolini был равен 1 (PAI 1).
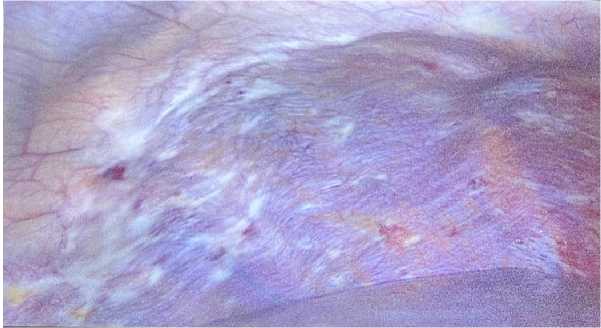
Рис. 3. Интраоперационно правый купол диафрагмы с перитонеальными метастазами до начала лечения. Множественные очаги от 5 до 15 мм
-
Fig. 3. Pre-treatment intraoperative finding: Peritoneal metastases on the right hemidiaphragm. Multiple lesions (5–15 mm)
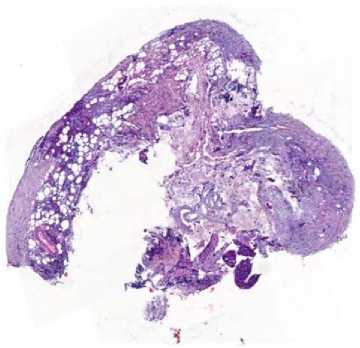
Рис. 4. Гистологические сканы перитонеальных метастазов до начала лечения (окрашивание гематоксилином и эозином, ув. ×50)
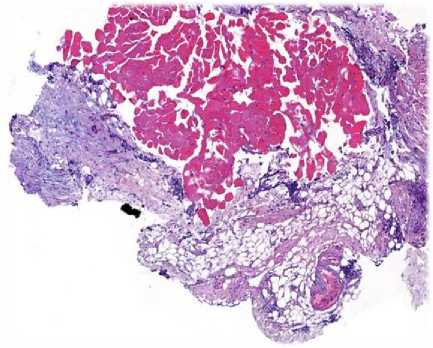
-
Fig. 4. Pre-treatment histopathological scans of peritoneal metastases (hematoxylin and eosin staining, ×50 magnification)
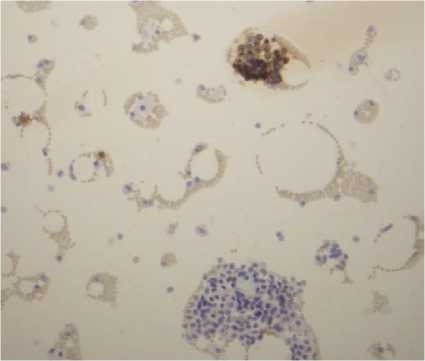
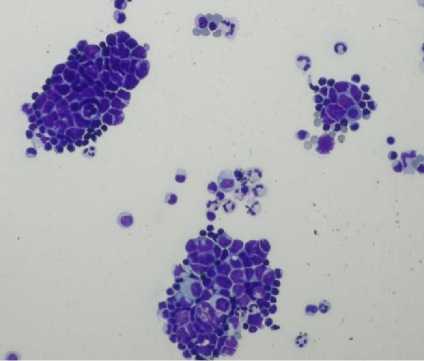
Рис. 5. Цитологические сканы положительного перитонеального лаважа с комплексами карциномы до начала лечения (окраска LD200, ув. ×20)
-
Fig. 5. Pre-treatment cytological scans of positive peritoneal lavage showing carcinoma cell clusters (LD200 staining, ×20 magnification)
На 1-м, 3-м, 5-м курсах лечение проводилось по схеме FLOT и включало в себя введение доцетаксела из расчета 50 мг/м2 внутривенно капельно в течение 1 ч, оксалиплатина из расчета 85 мг/м2 внутривенно капельно в течение 2 ч, лейковорина из расчета 200 мг/м2 внутривенно капельно в течение 2 ч, 5-фтору-рацила из расчета 2600 мг/м2 внутривенно капельно через помпу в течение 24 ч последовательно, что при площади поверхности тела 1,8 м2 (рост 171 см, вес 68 кг) составило 90, 153, 360 и 4680 мг соответственно.
Метод внутрибрюшной аэрозольной химиотерапии под давлением применялся на 2-м, 4-м, 6-м курсах лечения. Раствор доцетаксела изготавливался за 1 ч до начала сеанса терапии из расчета 50 мг/м2, что составляло 90 мг, и доводился до объема 200 мл физиологическим раствором хлорида натрия. Аэрозольное введение препарата осуществлялось в условиях операционной лапароскопическим доступом под наркозом с помощью ангиографического инжектора через магистраль высо- кого давления и форсунку в герметичном контуре созданного внутрибрюшного карбоксипе-ритонеума со стабильным давлением 12 мм рт. ст. Время введения составило 6,7 мин при скорости 30 мл/мин и давлении в системе инжектора 250 PSI с экспозицией от начала введения 30 мин и последующим удалением газа из брюшной полости. Сеанс в каждом случае завершен снятием карбоксиперитонеума, удалением портов, послойным ушиванием и хирургической обработкой операционных ран и поля. Хирургических осложнений не отмечено, продолжительность каждой операции составляла 60 мин, объем максимальной кровопотери – 5 мл. Через 24 ч после внутрибрюшного аэрозольного введения под давлением раствора доцетаксела выполнялась внутривенная инфузия химиопрепаратов в следующих дозировках и последовательности: оксалиплатин из расчета 85 мг/м2 внутривенно капельно в течение 2 ч, лейковорин из расчета 200 мг/м2 внутривенно капельно в течение 2 ч, 5-фторурацил из расчета 2600 мг/м2 внутривенно капельно через помпу в течение 24 ч, что составило 153, 360 и 4680 мг соответственно. Таким образом, на 2-м, 4-м, 6-м курсах раствор доцетаксела был исключен из системного внутривенного введения.
Максимальная степень токсичности, проявившейся в рвоте и диарее, определена как grade 2 по CTCAE v.5.0.
На сеансе внутрибрюшной аэрозольной химиотерапии под давлением, проводимом на 6-м курсе, дополнительно выполнены контрольный перитонеальный лаваж, полипози-ционная биопсия очагов по брюшине. Отмечены отсутствие свободных опухолевых клеток в перитонеальном лаваже – отрицательный перитонеальный лаваж (Су-), полный лечебный патоморфоз метастатических очагов по брюшине (PRGS 1) (рис. 6–8).
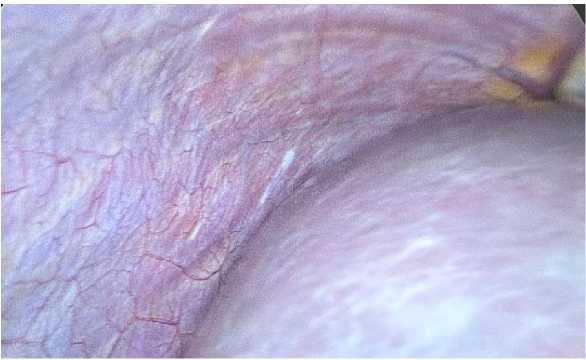
Рис. 6. Интраоперационно правый купол диафрагмы с перитонеальными метастазами после 6 курсов лечения
-
Fig. 6. Intraoperative finding: right hemidiaphragm with peritoneal metastases after 6 treatment cycles
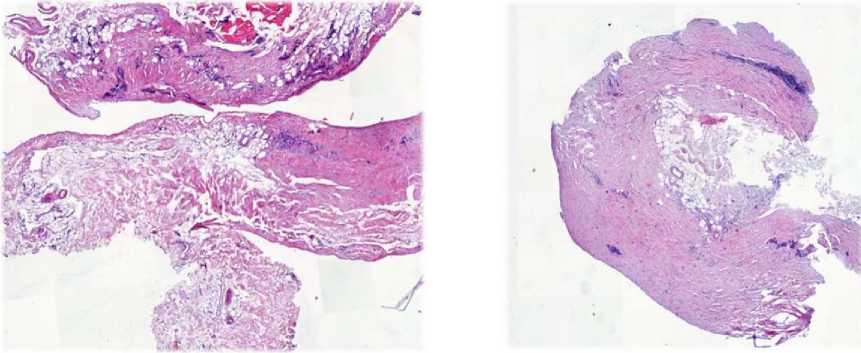
Рис. 7. Гистологические сканы перитонеальных метастазов после 6 курсов лечения (окрашивание гематоксилином и эозином, ув. ×50)
-
Fig. 7. Histopathological scans of peritoneal metastases after 6 treatment cycles (hematoxylin and eosin staining, ×50 magnification)
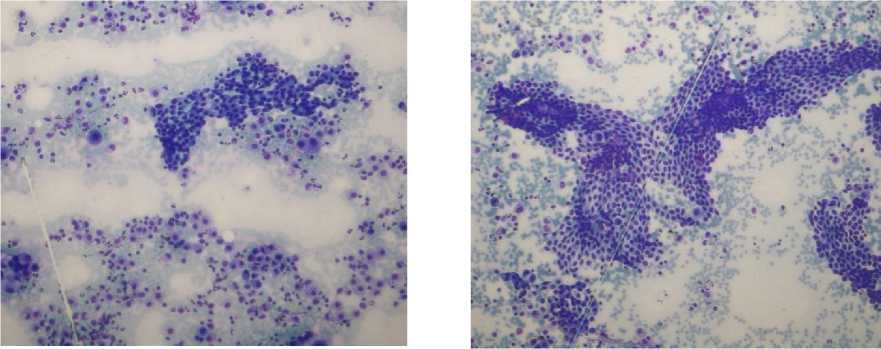
Рис. 8. Цитологические сканы реактивных изменений мезотелия после 6 курсов лечения (окраска LD200, ув. ×20)
-
Fig. 8. Cytological scans showing reactive mesothelial changes after 6 treatment cycles (LD200 staining, ×20 magnification)
Полученный от внутрибрюшной аэрозольной химиотерапии под давлением и системной химиотерапии эффект в виде отсутствия проявлений диссеминации позволил запланировать проведение пациенту операции через 6 нед. после их окончания.
Накануне хирургического вмешательства был ценен объективный статус: ECOG 0, ASA I, МНОАР I степень, NRS-2002 2 балла.
В раннем реабилитационном периоде (на амбулаторном этапе) выполнялись исследование электролитов (калий, натрий, хлор), общий (гемоглобин, эритроциты, нейтрофилы, ретикулоциты, тромбоциты) и биохимический (альбумин, мочевина, креатинин, глюкоза, АСТ, АЛТ, СРБ, общий билирубин, амилаза) анализы периферической крови (на 10-е, 20-е, 30-е сут). Значимых отклонений не определено. По данным контрольных исследований, включавших в себя КТ (рис. 9), ЭФГДС (рис. 10), УЗИ периферических лимфатических узлов, через 10, 20 и 40 нед. после хирургического лечения прогрессирования опухолевой патологии не отмечено.
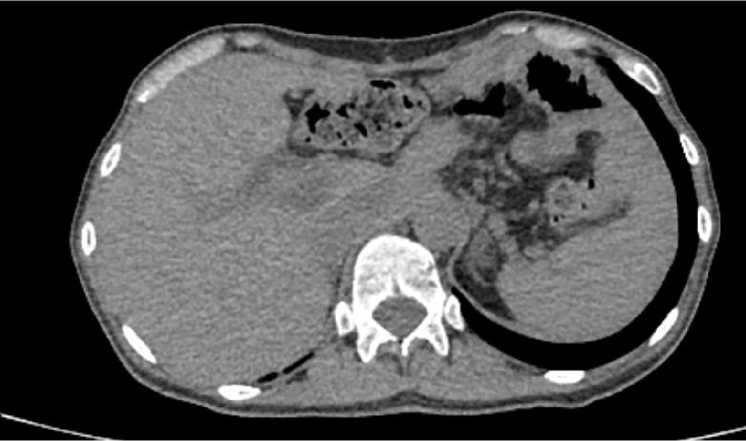
Рис. 9. Компьютерная томография после 6 курсов лечения и выполненной гастрэктомии: 40 недель динамического наблюдения
Fig. 9. Computed tomography scan after 6 treatment cycles and gastrectomy. 40 weeks of follow-up
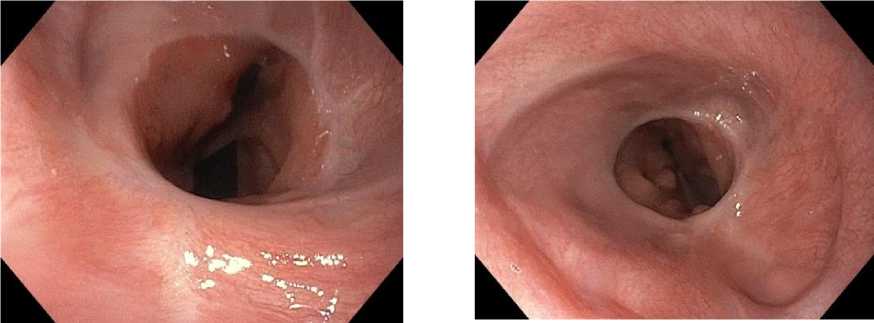
Рис. 10. ФГДС после 6 курсов лечения и выполненной гастрэктомии: 40 недель динамического наблюдения. Эзофагоэнтероанастомоз проходит свободно, слизистая без признаков воспаления
Fig. 10. EGD after 6 treatment cycles and gastrectomy. 40 weeks of follow-up. Patent esophagoenteroanastomosis, no signs of mucosal inflammation
Самочувствие пациента и его объективный статус спустя 1 год после лечения соответствовал 0 по шкале ECOG. Анализ качества жизни, проведенный на разных этапах лечения и наблюдения с использованием стандартизированных шкал Европейской организации по изучению и лечению рака (QLQ-C30), свидетельствовал о высоких оценках по функциональным, симптомным компонентам. Продолжено динамическое наблюдение за пациентом.
За период наблюдения продолжительностью 1 год не отмечено прогрессии заболевания, равно как и ухудшения качества жизни.


