Клиническое наблюдение успешного лечения псевдомембранозного колита в практике хирурга
Автор: Соловьев И.А., Першко А.М., Васильченко М.В., Гравшина Е.Н., Казимагомедов К.Н., Лычев А.Б., Гребеньков В.Г.
Журнал: Вестник Национального медико-хирургического центра им. Н.И. Пирогова @vestnik-pirogov-center
Рубрика: Клинические наблюдения
Статья в выпуске: 3 т.16, 2021 года.
Бесплатный доступ
В настоящее время антибиотикотерапия имеет ведущее значение в профилактике осложнений после операций на органах брюшной полости. При длительном их применении может развиться антибиотикоассоциированная диарея, которая у 80-90% носит идиопатический характер и самостоятельно разрешается после отмены антибиотиков. У 10-20% больных развивается псевдомембранозный колит, вызванный C. difficile и представляющий собой серьезную проблему для здоровья пациентов, вплоть до летального исхода у 13-38% больных. Представлено наблюдение успешного лечения псевдомембранозного колита у пациента 70 лет после лапароскопической брюшно-анальной резекции прямой кишки, выполненной по поводу рака нижне- и среднеампулярного отделов прямой кишки pT3N0M0G1.
Рак прямой кишки, псевдомембранозный колит, антибиотикоассоциированная диарея, брюшно-анальная резекция прямой кишки
Короткий адрес: https://sciup.org/140290427
IDR: 140290427 | DOI: 10.25881/20728255_2021_16_3_125
A clinical case of successful treatment of pseudomembranous colitis in the practice of a surgeon
Currently, antibiotic therapy is of leading importance in the prevention of complications after operations on the abdominal organs. With prolonged use, antibiotic-associated diarrhea may develop, which in 80-90% is idiopathic in nature and independently passes after the withdrawal of antibiotics. 10-20% of patients develop pseudomembranous colitis caused by C. difficile and present a serious problem for the health of patients, up to a fatal outcome 13-38%. The article presents a case of successful treatment of pseudomembranous colitis in a 70-year-old patient after laparoscopic abdominal-anal rectal resection, performed for cancer of the lower and middle ampullary rectum pT3N0M0G1.
Текст научной статьи Клиническое наблюдение успешного лечения псевдомембранозного колита в практике хирурга
Keyword: rectal cancer, pseudomembranous colitis, antibiotic-associated diarrhea, abdominal-anal resection of the rectum.
В настоящее время антибиотико-терапия имеет ведущее значение в профилактике осложнений после операций на органах брюшной полости. При длительном их применении у 5,0–25,0% развивается антибиотикоассоциированная диарея, которая проявляется наличием трех и более эпизодов неоформленного стула в течение двух и более суток. У 80,0–90,0% антибиотикоассоциированная диарея носит идиопатический характер и самостоятельно проходит после отмены антибиотиков. У 10,0–20,0% больных вследствие избыточного роста анаэробных спорообразующих бактерий — Clostridium difficile развивается псевдомембранозный колит [1–5].
Несмотря на то, что псевдомембранозный колит может быть спровоцирован практически любыми антимикробными препаратами, наиболее часто развивается на фоне приема цефалоспоринов и фторхинолонов [5–6].
Клиника псевдомембранозного колита проявляется диарейным синдромом (частый жидкий стул со слизью небольшими порциями от 3 до 20–30 раз/сут- ки), схваткообразной болью в животе различной локализации и лихорадкой [7]. Выделяют 3 степени тяжести течения псевдомембранозного колита [8–9]:
-
1. Лёгкая форма. Характеризуется диареей и незначительной болью в животе, что может приводить к нарушению водно-электролитного баланса, обезвоживанию, вплоть до развития судорог.
-
2. Среднетяжелая форма. Характеризуется диареей, повышением температуры тела до 38 °С и другими клиническими проявлениями (например, боли в животе) без дополнительных симптомов, которые требуют констатации тяжелого или осложненного псевдомембранозного колита.
-
3. Тяжелая форма. Проявляется диареей, спастическими болями в животе, лихорадкой, развитием гипоальбуми-немии и увеличением уровня лейкоцитов больше 15x10 9 кл/л [9-11].
Осложненная форма псевдомембранозного колита диагностируется при развитии одного из следующих симптомов: гипотония, гипертермия выше 38,5 °С, выраженное вздутие живота, изменения сознания, лейкоцитоз более 15х109/л или лейкопения менее 2х109/л, уровень сывороточного лактата более 2,2 ммоль/л, развитие синдрома полиорганной недостаточности [12–14].
Основными диагностическими критериями псевдомембранозного колита являются характерные изменения слизистой оболочки толстой кишки с наличием псевдомембран (фибринозных пленок, образующихся на участках некроза эпителия слизистой оболочки кишки), выявляемые при эндоскопическом осмотре, а также лабораторное подтверждение наличия токсинов А и В в кишечном отделяемом больного. При этом для постановки диагноза псевдомембранозного колита достаточно одного из указанных признаков [15–16].
Лечение псевдомембранозного колита преследует две основные цели: купировать воспалительный процесс в кишечнике и санировать его от спор C. difficile [4; 10; 12; 14]. Несмотря на то, что антибиотики чаще всего служат причиной развития псевдомембранозного

колита, именно антибакте- риальная терапия является неотъемлемой частью стандартной базисной терапии. Наиболее стабильная и высокая чувствительность C. difficile наблюдается к ванкомицину и метронидазолу. Обязательным условием проведения этиотропной терапии у больных псевдомембранозным колитом является энтеральное введение антибиотиков, поскольку при парентеральном их введении в кишечнике не создается достаточной концентрации и санация толстой кишки не наступает [1; 3; 6; 7; 9; 11; 14].
Пациентам с лёгкой и среднетяжёлой формой заболевания назначается метронидазол в дозе 500 мг внутрь три раза в день в течение 10 суток. При отсутствии клинического эффекта через 5–7 дней производят смену препарата на ванкомицин в дозе 125 мг 4 раза в день per os в течение 10 дней [6, 7, 10, 14].
Пациентам с тяжёлой формой псевдомембранозного колита изначально показано назначение ванкомицина в дозе 125 мг внутрь 4 раза в сутки в течение 10 суток. Несмотря на непосредственную эффективность ванкомицина и метронидазола, частота рецидивов очень высока и достигает 19,0%. При диагностике осложненной формы псевдомембранозного колита требует его перевода в отделение интенсивной терапии для дальнейшего лечения. Наряду с инфузионной терапией назначается ванкомицин внутрь в дозе 500 мг 4 раза в сутки в сочетании с метронидазолом в дозе 500 мг 3 раза в сутки внутривенно. При невозможности введения препарата per os ванкомицин назначается ректально. При этом препарат в дозе 500 мг разводится в 500 мл 0,9% раствора хлорида натрия и вводится в виде клизм четыре раза в день [4; 6; 10; 16].
В крайних случаях при неэффективности других методов лечения используют трансплантацию фекальной микрофлоры [3; 6].
У некоторых больных, несмотря на проводимое лечение, тяжелое течение псевдомембранозного колита может сопровождаться развитием осложнений, таких как токсическая дилатация толстой кишки, перфорация ободочной кишки и кровотечение, требующие срочного оперативного вмешательства. Вопрос об его объёме решается индивидуально, основываясь на результатах интраоперационной ревизии и выявленных патологических изменений толстой кишки [1–3; 6; 7; 10; 12].
Наиболее патогенетически обоснованным объемом операции является тотальная колэктомия с выведением концевой илеостомы [1–7; 11; 13]. Однако показатели летальности при данной операции достигают 30–50% [1; 3; 6; 7].
Резекция только пораженных участков толстой кишки не является приоритетной, так как оставляет после себя значительно большее количество воспаленных тканей, при этом 15,9% пациентов нуждаются в повторной операции. Культя прямой кишки, как правило, также поражается, но высокие риски летального исхода после выполнения проктоколэктомии нивелируют все ее преимущества [6; 11; 14].
В ряде случаев ограничиваются формированием илеостомы, с последующим введением в отключенные отделы кишечника внутрипросветных антибиотиков. При выраженной токсической дилатации с диастатическими разрывами или перфорации стенки кишки возникает необходимость выполнения срочной операции — колэктомии [1; 2; 4; 7; 9].
Таким образом, проблема лечения больных псевдомембранозным колитом является актуальной в настоящее время. Несмотря на проводимые в раннем послеоперационном периоде профилактические мероприятия, частота развития после операции псевдомембранозного колита остается прежней.
Больной А., 70 лет, поступил в клинику военно-морской хирургии Военномедицинской академии им. С.М. Кирова 01.12.2019 г. с диагнозом направления: «Рак нижне- и среднеампулярного отделов прямой кишки сT3N0M0G1. Состояние после курса химиолучевой терапии» для выполнения хирургического вмешательства.
При поступлении жаловался на боли в области заднего прохода, чувство неполного опорожнения кишечника и примесь крови в стуле при дефекации, периодические запоры.
Из анамнеза заболевания известно, что вышеперечисленные жалобы больного беспокоили с декабря 2018 г. В связи с этим пациенту выполнялось обследование: при ректальном исследовании на 4 см от ануса определялась плотная бугристая опухоль. Результат фиброколоноскопии: на 4 см от ануса определяется образование, циркулярно распространяющееся на 2/3 окружности прямой кишки, неравномерно приподнятое над окружающей слизистой, протяженностью около 5,0 см, ригидное при инструментальной пальпации, с участка- ми втяжения (биопсия). Гистологическая структура опухоли — высокодифференцированная аденокарцинома. Учитывая локализацию опухоли, в феврале 2019 г. была проведена неоадъювантная химио — (Капецитабин 800 мг/м2х2 р/сут.) и лучевая терапия (на область лимфатических узлов малого таза и ложе опухоли прямой кишки РОД = 2 Гр, СОД = 46 Гр, локально на опухоль прямой кишки РОД = 2 Гр, СОД = 50 Гр). По данным фиброколоноскопии от 13.09.2019 г. наблюдался регресс опухоли, результаты исследования биопсийного материала — отрицательные. Однако, на МРТ органов малого таза от 07.11.19 г. сохранялось новообразование нижне- и среднеампулярного отделов прямой кишки на фоне постлучевых изменений, постлучевые изменения жировой клетчатки таза и костного мозга костей таза. МР-при-знаки доброкачественной гиперплазии предстательной железы по смешанному типу. В нижне- и среднеампулярном отделах прямой кишки на расстоянии 38 мм от анодермальной линии определялось неравномерное утолщение стенки кишки (от 8 до 20 мм), в задних и боковых отделах (больше влево), за счет наличия неопластического процесса, протяженностью — 57 мм. Образование неоднородной МР-структуры, преимущественно изогиперинтенсивного МР-сигнала на Т2-ВИ. Просвет кишки неравномерно сужен. Наружный контур кишки на уровне образования относительно ровный, с признаками минимального лимфангита по левой боковой поверхности, слизистая оболочка кишки отечная — постлучевые изменения. Структурных изменений мезоректальной фасции не отмечалось. Выше образования стенки кишки не утолщены, структурно не изменены. Предстательная железа размерами 35x45x40 мм, визуализируются участки аденоматозных изменений до 13 мм. Капсула железы прослеживается на всем протяжении (Рис. 1).
Онкомаркеры (РЭА, Са 19-9) — в пределах нормы. Компьютерная томография органов грудной и брюшной полости: данных за вторичное поражение органов грудной клетки и брюшной полости нет.
Учитывая рецидив онкологического процесса после неоадъювантной химиолучевой терапии и «низкую» локализацию опухоли, пациенту была предложена операция в объеме брюшно-промежностной экстирпации. Однако от такого объема больной категорически отказался в связи с необходимостью
формирования постоянной стомы. Под эндотрахеальным наркозом 03 декабря 2019 г. выполнена операция в объеме лапароскопической брюшно-анальной резекции прямой кишки с низведением сигмовидной кишки в анальный канал, с формированием промежностной сиг-мостомы. Окончательный вид операции представлен на рисунках 2 и 3.
Результат патогистологического исследования макропрепарата: высокодифференцированная аденокарцинома прямой кишки на фоне тубулярно-ворсинчатой аденомы с интраэпителиальной неоплазией высокой степени, инвазия во внутренний слой мышечной оболочки. В лимфатических узлах опухолевые клетки не обнаружены.
Послеоперационный диагноз: «Рак нижне- и среднеампулярного отделов прямой кишки рT2N0M0G1. Состояние после курса химиолучевой терапии (Ка-пецитабин) на область лимфатических узлов малого таза и ложа опухоли прямой кишки РОД =2 Гр, СОД= 46 Гр, локально на опухоль прямой кишки РОД =2 Гр, СОД= 50 ГР от 02.2019 г. Регресс опухоли. Погрессирование. Рецидив опухоли нижнеампулярного отдела прямой кишки от декабря 2020 г.».
Послеоперационный период протекал без осложнений. С целью профилактики ранних послеоперационных осложнений в течение 5 суток внутримышечно получал цефтриаксон 1,0 — 2 раза в сутки. 19.12.2019 г. в плановом порядке выполнена реконструкция низведенного нисходящего отдела толстой кишки. Окончательный вид операции представлен на рисунке 4.
В послеоперационном периоде проводилась антибиотикопрофилак-тика офлоксацином 100,0 — 2 раза в сутки внутривенно, на фоне которой 24.12.2019 г. развилась антибиотикоассоциированная диарея, что потребовало отмены антибиотиков и назначения препаратов: линекс 1 капс. — 3 раза в сутки, смекта 1 пакетик — 4 раза в сутки. На фоне проводимой терапии антибиотикоассоциированной диареи течение послеоперационного периода осложнилось развитием 30.12.2019 г. псевдомембранозного колита. Консультрован гастроэнтерологом: «Псевдомембранозный колит тяжелой степени тяжести с экссудативной энтеропатией и гипопротеинемическим асцитом». Получал метро-дидазол 500 мг внутрь 3 раза в сутки, ванкомицин 500 мг 4 раза в сутки per os, салофальк 4 капс. 1 раз в сутки, энтерол внутрь 250 мг 1 раз в сутки, смекта 2 па-
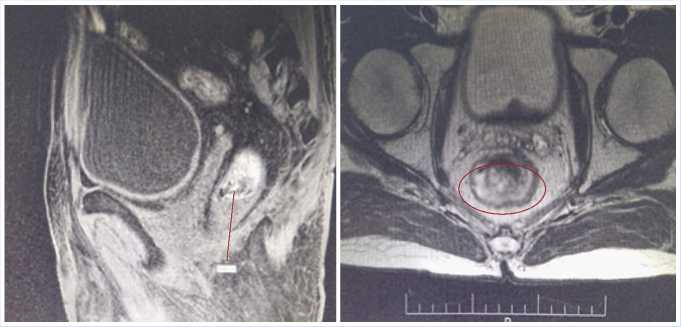
Рис. 1. МРТ малого таза. Нижний полюс опухоли расположен на расстоянии 38 мм от анодермальной линии.
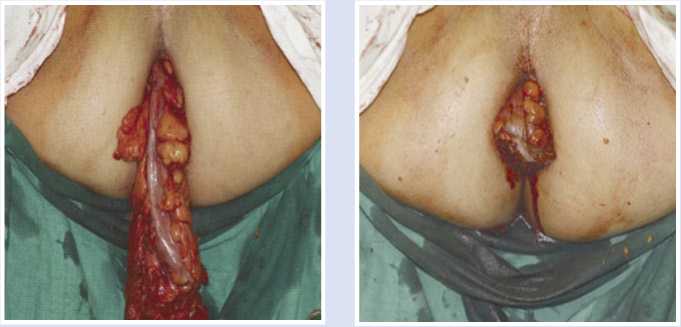
Рис. 2. Низведенный участок сигмовидной кишки через анальный канал.
кетика 3 раза в сутки и модулен 6 ложек в 200 мл воды 2 раза в сутки. Несмотря на начатое лечение, диарея сохранялась, на фоне которой 31.12.2019 г. диагностирована несостоятельность сигмо-анального анастомоза в виде диастаза между низведенной сигмовидной кишкой и слизистой анального канала протяженностью около 5 мм, без поступления кишечного содержимого за пределы зоны анастомоза. В связи с развитием несостоятельности сигмоанального анастомоза фиброколоноскопия не выполнялась. По срочным показаниям 31.12.2019 г. выполнена лапароскопическая трансвер-зостомия, в ходе операции из брюшной полости эвакуировано около 5 литров асцитической жидкости. Петли тонкой и толстой кишки умеренно увеличены в диаметре преимущественно за счет газового компонента, перистальтика ослаблена. На рисунке 5 представлен общий вид трансверзостомы с характерными для псевдомембранозного колита макроскопическими признаками: на воспаленной
Рис. 3. Сформированная промежностная сиг-мостома с «избытком».
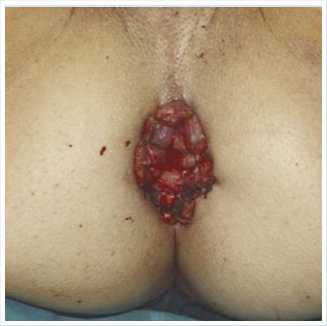
Рис. 4. Окончательный вид промежностной сигмостомы.
гиперемированной слизистой оболочке толстой кишки имеются массовые фибринозные наложения с некрозом слизистой оболочки.
Терапия дополнена ванкомицином (500 мг), который вводили в отводящий

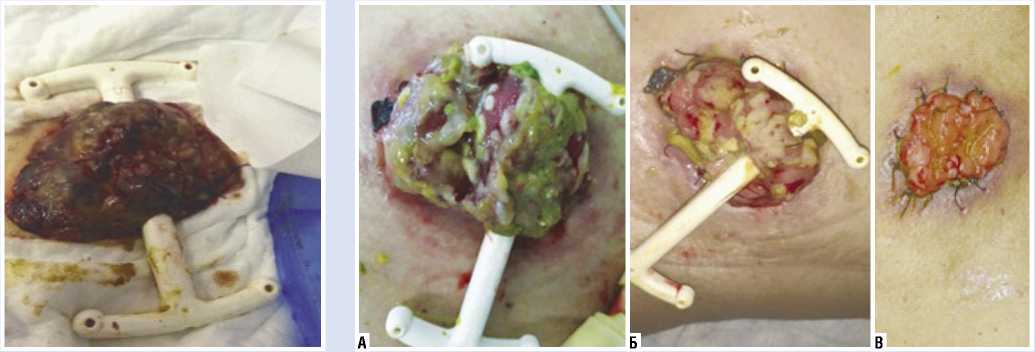
Рис. 5. Окончательный вид трансверзостомы.
Рис. 6. Общий вид трансверзостомы: А — на 8 сутки; Б — 14 сутки; В — 29 сутки после операции.
конец толстой кишки через трансвер-зостому 2 раза в сутки. По дренажу из малого таза отмечалось обильное выделение асцитической жидкости до 1,5 литров в сутки. На этом фоне отмечалось снижение количества общего белка максимально до 34 г/л, альбумина — до 21,6. Гипопротеинемию компенсировали введением 25% раствора альбумина (4 флакона ежедневно). На 7 сутки после операции у пациента клинически и рентгенологически диагностирован парез кишечника. В связи с наличием признаков нарушений тонкокишечной проходимости 07.01.2020 г. выполнялся пассаж бария, который позволил исключить его механический характер (через 45 часов достиг транс-верзостомы).
На фоне проводимого лечения отмечалась положительная динамика в виде улучшения общего состояния, уменьшения болевого синдрома, нормализации температуры тела, изменения консистенции стула от жидкого до кашицеобразного, нормализации лабораторных показателей. Отчетливую положительную динамику имели морфологические изменения со стороны слизистой оболочки толстой кишки в виде уменьшения воспалительных изменений и наложений фибрина. На рисунке 6 представлен общий вид трансверзостомы на 8, 14 и 29 сутки после операции.
Отмечалось прогрессивное снижение количества отделяемого по дренажу из малого таза, в связи с чем он был удален на 25 сутки после операции. Пациент был выписан из стационара в удовлетворительном состоянии 24 января 2019 г. За время динамического наблюдения рецидива псевдо-мембранозного колита не отличалось.
Заключение
Представленный клинический случай показал эффективность лечения псевдомембранозного колита в послеоперационном периоде у онкологического больного и демонстрирует необходимость комплексного подхода в диагностическом и лечебном процессах врачей различных специальностей (онколог, хирург, реаниматолог, гастроэнтеролог).
Авторы заявляют об отсутствии конфликта интересов (The authors declare no conflict of interest).
и др. Рекомендации Российской гастроэнтерологической ассоциации и Ассоциации колопроктологов России по диагностике и лечению взрослых больных язвенным колитом // Российский журнал гастроэнтерологии, гепатологии, колопроктологии. — 2015. — Т.25. — №1. — С. 48-65.
[Ivashkin VT, Shelygin UA, Halif IL, et al. Rek-omendacii Rossijskoj gastroenterologicheskoj associacii i Associacii koloproktologov Rossii po diagnostike i lecheniyu vzroslyh bol’nyh yazvennym kolitom. Rossijskij zhurnal gastro-enterologii, gepatologii, koloproktologii. 2015; 25(1): 48-65. (In Russ).]
Список литературы Клиническое наблюдение успешного лечения псевдомембранозного колита в практике хирурга
- Ивашкин В.Т., Шелыгин Ю.А., Халиф И.Л. и др. Рекомендации Российской гастроэнтерологической ассоциации и Ассоциации колопроктологов России по диагностике и лечению взрослых больных язвенным колитом // Российский журнал гастроэнтерологии, гепатологии, колопроктологии. — 2015. — Т.25. — №1. — С. 48-65. [Ivashkin VT, Shelygin UA, Halif IL, et al. Rek-omendacii Rossijskoj gastroenterologicheskoj associacii i Associacii koloproktologov Rossii po diagnostike i lecheniyu vzroslyh bol'nyh yazvennym kolitom. Rossijskij zhurnal gastroenterology gepatologii, koloproktologii. 2015; 25(1): 48-65. (In Russ).]
- Ивашкин В.Т., Шелыгин Ю.А., Абдулганиева Д.И. и др. Проект клинических рекомендаций по диагностике и лечению взрослых пациентов с болезнью Крона // Колопрокто-логия. — 2013. — №S3(45). — С. 4-21. [Ivashkin VT, Shelygin UA, Abdulganieva DI, et al. Proekt klinicheskih rekomendacij po diagnostike i lecheniyu vzroslyh pacientov s bolezn'yu Krona. Koloproktologiya. 2013; S3(45): 4-21. (In Russ).]
- Корнеева О.Н., Ивашкин В.Т. Антибиотико-ассоциированный колит: патоморфология, клиника, лечение // Российский журнал гастроэнтерологии, гепатологии, колопрокто-логии. — 2007. — Т. 17. — №3. — С. 65-71. [Korneeva ON, Ivashkin VT. Antibiotikoassociirovannyj kolit: patomorfologiya, klinika, lechenie. Rossijskij zhurnal gastroenterolog-ii, gepatologii, koloproktologii. 2007; 17(3): 65-71. (In Russ).]
- Lau CS, Chamberlain RS. Probiotics are effective at preventing Clostridium difficile-associated diarrhea: a systematic review and meta-analysis. Int J Gen Med. 2016; 9: 27-37. doi:10.2147/IJGM.S98280.
- Лобзин Ю.В., Захаренко С.М., Иванов Г.А. и др. Современные представления об инфекции Clostridium difficile // Клиническая микробиология и антимикробная химиотерапия. — 2002. — Т.4. — №3. — С.200-232. [Lobzin UV, Zaharenko SM, Ivanov GA, et al. Sovremennye predstavleniya ob infekcii Clos-tridium difficile. Klinicheskaya mikrobiologiya i antimikrobnaya himioterapiya. 2002; 4(3): 200-232. (In Russ).]
- Ивашкин В.Т., Ивашкина Н.Ю., Баранская Е.К. Рациональная фармакотерапия заболеваний органов пищеварения: руководство для практикующих врачей. — Москва: Лит-терра, 2007.
- Kostic AD, Xavier RJ, Gevers D. The microb-iome in inflammatory bowel disease: current status and the future ahead. Gastroenterology. 2014; 146(6): 1489-1499. doi:10.1053/j.gast-ro.2014.02.009.
- Сафин А.Л., Ачкасов С.И., Сухина М.А. Факторы риска развития диареи, ассоциированной с Clostridium difficile, у колопрок-тологических больных (обзор литературы) // Колопроктология. — 2017. — №1(59). — C.59-67. [Safin AL, Achkasov SI, Suhina MA. Faktory riska razvitiya diarei, associirovannoj s Slostridium difficile, u koloproktologicheskih bol'nyh (obzor literatury). Koloproktologiya. 2017; 1(59): 59-67. (In Russ).]
- Шептулин А.А. Рефрактерные и рецидивирующие формы колита, ассоциированного с Clostridium difficile // Российский журнал гастроэнтерологии, гепатологии и коло-проктологии. — 2011. — Т.2. — С.50-53. [Sheptulin AA. Refrakternye i recidiviruyushch-ie formy kolita, associirovannogo s Clostridium difficile. Rossijskij zhurnal gastroenterologii, gepatologii i koloproktologii. 2011; 2: 50-53. (In Russ).]
- Шелыгин Ю.А., Алешкин В.А., Сухина М.А. и др. Клинические рекомендации национальной ассоциации специалистов по контролю инфекций, связанных с оказанием медицинской помощи и общероссийской общественной некоммерческой организации «ассоциации колопроктологов россии» по диагностике, лечению и профилактике clostridium difficile-ассоциированной диареи // Колопроктология. — 2018. — Т.65. — №3. — С.7-21. [Shelygin UA, Aleshkin VA, Suhina MA, et al. Klinicheskie rekomen-dacii nacional'noj associacii specialistov po kontrolyu infekcij, svyazannyh s okazaniem medicinskoj pomoshchi i obshcherossijskoj obshchestvennoj nekommercheskoj organi-zacii «associacii koloproktologov rossii» po diagnostike, lecheniyu i profilaktike clostridium difficile-associirovannoj diarei (CDI). Koloprok-tologiya. 2018; 65(3): 7-21. (In Russ).]
- Collins DA, Elliott B, Riley TV. Molecular methods for detecting and typing of Clostridium difficile. Pathology. 2015; 47(3): 211-218. doi: 10.1097/PAT.0000000000000238.
- Knight DR, Elliott B, Chang BJ, Perkins TT, Riley TV. Diversity and Evolution in the Genome of Clostridium difficile. Clin Microbiol Rev. 2015; 28(3): 721-741. doi: 10.1128/CMR. 00127-14.
- Steindl G, Fiedler A, Huhulescu S, Wewalka G, Allerberger F. Effect of airborne hydrogen peroxide on spores of Clostridium difficile. Wien Klin Wochenschr. 2015; 127(11-12): 421-426. doi: 10.1007/s00508-014-0682-6.
- Surawicz CM, Brandt LJ, Binion DG, et al. Guidelines for diagnosis, treatment, and prevention of Clostridium difficile infections. Am J Gastroenterol. 2013; 108(4): 478-499. doi: 10.1038/ajg.2013.4.
- Wright Donna F.R. Largest ever European clinician consensus report on Clostridium difficile infection provides recommendations for improved management of CDI pressemitteilung astellas. EMEA. 2014.
- Yoon SS, Kim EK, Lee WJ. Functional genomic and metagenomic approaches to understanding gut microbiota-animal mutualism. Curr Opin Microbiol. 2015; 24: 38-46. doi:10.1016/ j.mib.2015.01.007.


